

解析高电压水系电解液最新研究进展
描述
一般情况下,可充电电池中电解液主要以无水有机溶液为主,具有较高的电化学窗口,因而可以发挥出远高于传统二次电池如铅酸电池、氢镍电池的能量密度,但是有机电解液易燃有毒及严格的操作条件等限制了其在大规模储能的应用,因而发展绿色环保的高比能新电池体系成为当前的研究热点之一。
自1994年报道了以VO2做负极,LiMn2O4做正极,LiNO3水溶液做电解液的水系锂离子电池后,具有高导电,高倍率性能的水系电池就受到人们广泛关注。
与有机电解液相比,水系电解液安全、绿色、高效且可以在更宽的温度范围工作(如传统的有机电池仅能在低于60℃的条件下工作),因而采用水系电解液取代有机电解液是解决有机电解液易燃、有毒、安全性低的有效方法之一。但是水系电池仍然存在固有缺陷,如较窄的电化学窗口(《1.23V),存在副反应,电极材料的分解等,这些因素限制了水系电池的发展。
一、水系电解液面临的问题与挑战
水系电解液作为电池(电容器)的重要组成部分,其中发生的化学/电化学过程远比有机电解液要复杂得多,会发生许多副反应,从而使得水系电池(电容器)循环稳定性很差,且输出电压低,电池比能量约为40-50Wh/kg,与镍铬电池相当。这些副反应主要包括:
(1)电极材料与水或氧反应。一般情况下,水系电解液无毒无害且稳定存在,在空气中组装即可。Li等在理论上证明了当电解液中有氧气或水存在时,会使得负极材料被O2和H2O氧化而非发生电化学氧化还原过程,通过除氧或调节电解液在适当的pH值可以保证电极材料的稳定性;
(2)质子共嵌反应。因为H+的半径比Li+小很多,因此Li+发生嵌入反应时,会伴随H+的嵌入。质子共嵌反应一般与电极材料的晶体结构与电解液的pH值有关。通常,尖晶石Li1-xMn2O4与橄榄石Li1-xFePO4不存在质子共嵌现象而层状材料如Li1-xCoO2 , Li1-xNi1/3Mn1/3Co1/3O2在较低的酸性电解液中会发生质子共嵌现象,可以通过碳包覆改性或调节电解液pH值来改善;
(3)析氢/析氧反应。为使电极材料发挥出最大容量,电池(电容器)的电化学窗口应该小于电解液的分解电压,而水的电化学稳定窗口仅为1.23V,在此区间内,电极材料无法发挥出最大容量,必然会发生水的分解,即导致析氢/析氧反应的发生,电极附近pH值发生变化,电极材料稳定性变差。解决此方法可以通过构建稳定的电极电解液界面或抑制水的活度来实现;
(4)电极材料的分解。通常低温条件下制备的材料具有较大的比表面积,或者含有多变价金属元素的材料(VO2 , LiV3O8 , LiV2O5)在水溶液中不稳定,易分解,因此适用于水系电解液的材料很少 。电极材料应尽量选择比表面积小的电极材料,可以通过掺杂、碳包覆等方式来提高材料的稳定性。
总之,基于水系电解液中反应的复杂性,水系储能装置电压普遍低于1.5V,且循环稳定性很差,无法实现大规模商业化应用。要改善水系储能装置的性能,除了电极材料的选择、优化组装条件等,提高电解液的电化学窗口是解决水系电池低压低能量密度的关键技术之一。
二、电解液电压改善方法及进展
2.1 构建稳定的电极电解液界面
稳定的电极-电解液界面是实现拓宽电化学窗口的有效方法之一,随着电解质的分解,在固体电极和电解液之间形成稳定的中间相,这些中间相通常是离子导电而电子不导电的。
2015年,Suo等报道了一种“Water-in-salt“ 体系,即采用有机盐双三氟甲基磺酰亚胺锂(LiTFSI)与水形成的超高浓度水溶液,在该体系中溶质的质量和体积远高于溶剂。此时,每个离子周围的水分子数远低于常规水系电解质中的“溶剂化数”,包含阴离子的锂离子溶剂化鞘,离子之间的相互作用增强,促进中间相的形成(如图1所示)。
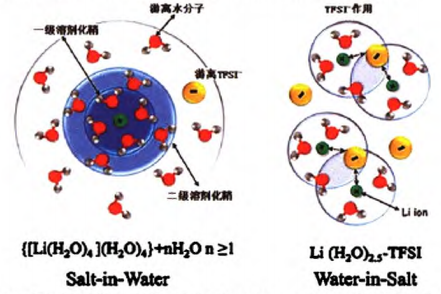
图1 Li+溶剂化鞘在稀溶液与”Water-in-salt”溶液中的演化
该水溶液室温时可达到21 mol/L。通过测试不锈钢集流体的循环伏安曲线确定该电解液的电化学窗口,如图2所示。从图中可以发现这种高浓度的电解液主要对析氢反应有抑制作用,且随TFSI浓度的增加,抑制作用增强,电位由2.63V降至1.9V,从而拓宽到3.0V。
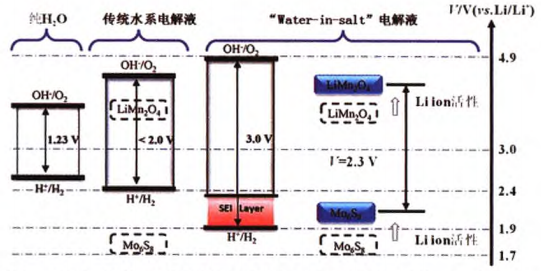
图2 高浓度水系电解液的电化学窗口及对LiMn2O4/Mo6O8电池的电压调节作用
为测试这种电解液的性能,Wang课题组采用LiMn2O4和Mo6O8电极组装全电池,其全电池电压高达2.3V , 比能量将近100Wh/kg,远高于铅酸蓄电池,且4.5C倍率下循环1000次,库仑效率为100% ,具有较高稳定性。
总之,高浓度LITFSI盐溶液会在负极表面形成一层氧化物薄膜,这是第一次在水系电解液中提出SEI膜的概念。该电解液体系的发现,打破了传统的通过牺牲电压来达到电池稳定性的观念,使电池的电压和稳定性有大幅度提升,这在水系储能装置领域是一个重大突破,同时中间相的形成和作用为我们研究水系电池打开了新思路。
在上述研究的基础上,Wang课题组又采用了一种新的阴极添加剂-三(三甲基硅基)硼酸(TMSB),添加剂的氧化形成了CEl(正极-电解液中间相),提高了LiCO2在水系电解液中的稳定性。理论计算表明,TMSB的最高分子占据轨道(HOMO)是检测氧化反应的关键因素,通过与“water-in-salt“ 体系中H2O和TFSI阴离子的HOMO对比,TMSB的HOMO远高于电解液中的水分子或TFSI阴离子(如图3所示)。
这表明,电解液氧化反应首先发生在TMSB上,且进一步模拟实验表明,添加剂的水解会在阴极表面形成不溶性的共沉淀物,抑制了Co的溶解和析氧反应,提高了LiCO2的循环稳定性。
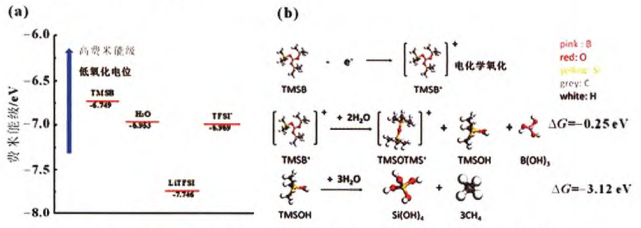
图3 (a) TMSO,H2O,LITFSI和TFSI的最高占据轨道;(b)TMSB电化学氧化分解机理
同时该课题组指出了添加剂的选择标准:
(1)添加剂的氧化电位比“water-in-salt”体系中水的氧化电位低;
(2)添加剂不可水解。
Wang课题组采用LiCO2和Mo6O8电极组装全电池,其全电池电压高达2.5V,且0.5C倍率下循环1000次,容量每次仅衰减0.013%,稳定性极高,这是第一次提出正极表面中间相的存在,这一新发现为研制高能量密度的稳定高电压水电池提供了一定的启示。
Wang等研究人员的研究表明,中间相的形成可以阻止电极与水直接接触,同时构建稳定的电极-电解液界面,在提高电池电压的同时提高电池的循环稳定性。
2.2 水合物熔融盐
除了形成稳固的界面,高浓度电解液本身也可以起到抑制水的活度及材料溶解的作用。2016年, R.S.Kuhnel等采用高浓度LiTFSl为电解液,成功地抑制了AI的溶解,有望采用轻质的铝做集流体,降低电池生产成本提高效益。
同年, Yumada课题组报道了水合物熔融盐电解质,即包含高浓度的金属锂盐及极少水的一类电解液。在这种电解液中,所有的水分子与金属阳离子配位,同时保持流动性。该课题组采用双三氟甲基磺酰亚胺锂(LITFSl)与双(五氟乙基磺酸)亚胺锂( LiBETI)的二元体系作为电解液,该电解液体系中,阴离子的存在促进了Li+的溶剂化,同时具有“增塑性”抑制锂盐与锂盐溶剂结晶的产生,保证了电解液的流动性。
相图研究表明【 如图4(a)】,LITFSl和LiBETI摩尔比为7:3比与H2O有更大的相容性(如图4),高比例下电解液的电化学窗口拓宽到3.8V。基于此水合物熔融盐体系,由 Li4Ti5O12电极与 LiCoO2/Li4Ti5O12组成的全电池电压为2.3-3.1V,平均比能量高达130Wh/kg,这一研究推动了水系电池的发展。

图4 (a) Li(TFSI)x(BETI)1-x混合物液相线;(b)室温水合物熔融盐的制备
2.3 电解液的pH值调节
理论上,由于析氢析氧反应的存在,使得水系电解液的电化学窗口限制在1.23V左右,通过调节电解液的pH值,可以有效抑制析氢/析氧反应,拓宽电化学稳定窗口。
早在2005年,V.Khomenko等指出析氢和析氧反应的过电势取决于电解液的pH值,并探究了α-MnO2和活性炭组装的水系非对称电容器,以KNO3(2 mmol/L , pH=6.4)电解液为基础,通过添加HNO3和KOH来调节电解液的pH值,测定α-MnO2和活性炭的电位与pH值关系。结果表明,pH为6.4的条件下α-MnO2可以达到更宽的电化学窗口0.47-1.19V,而活性炭的电化学窗口为-0.88-0.47V,因此组装的电容器电位高达2.1V。
2010年,M.P.Bichat等采用海藻碳组装的电容器在中性电解液(Na2SO4)中的工作电压达到1.6V,这是第一次证明在中性电解液中,如果材料表面具有足够的表面官能团,尤其是醌类基团,材料就可以与电解液发生赝电容反应。与有机电解液相比,中性电解液有望应用于环境友好的电容器领域。
2011 , Yang采用水合石墨烯薄膜作为电极制备高压超级电容器在中性 Li2SO4电解液中的最大电压高达1.6v,甚至1.8V。2013年,Chen等研究人员基于酸碱双电解质采用陶瓷超离子导体薄膜作为离子交换介质,正极采用酸性电解液提高析氧电位,负极采用碱性电解液降低析氢电位,使得电解液原来的电化学窗口由1.23V拓宽到3.0V(如图5所示),并在此电解液的基础上组装了Zn/KMnO4水系电池,其工作电压高达2.8V。
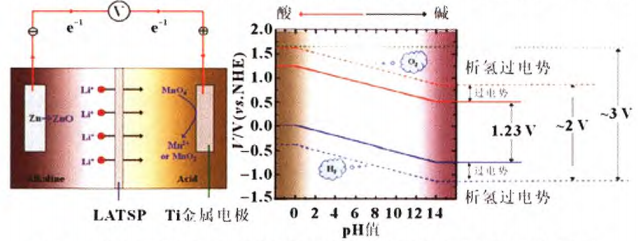
图5 (a) Zn/KMnO4电池的结构及工作原理;(b)电解液在不同pH值下的稳定窗口
2017年, Wang课题组采用LiTFSI做电解液,用HTFSI调节电解液pH=5,以 LiNi0.5Mn1.5O4/Mn6S8组装的电池电压为3.0V,比能量高达126Wh/kg,且5C倍率下每次容量衰减0.075%。目前为止,可以使水系储能装置实现高压的方法及进展如图6所示。
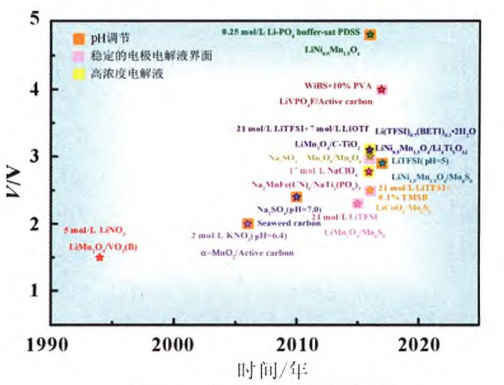
图6 电压改善方法及进展
三、结论与展望
水系电解液因其高安全性、高倍率性能,有望取代有机电解液成为新一代电化学储能装置,可以缓解环境污染及化石能源的消耗,但是水系固有的电化学窗口大大限制了其使用。近几十年来,人们对水电池进行了大量的研究,以提高电池的电压,目前有效提高水系电池电化学窗口的方法主要有pH值调节、中间相的形成和浓缩电解质,但对这些新的电池体系所涉及的机制仍然缺乏完整的理解。
总之,通过选择合适的电极材料、电解液、pH值控制和电池组装工艺的优化,可以构建出一种既具有稳定比能量又具有较高电压的水系储能装置。但是距离水系储能装置实现大规模的商业化应用还有很长一段路要走,必须指出的是,水系电解液的研究是一个新的领域,具有很高的学术价值,其实际应用需要在科学的指导下大胆假设,小心求证,合理判断。
编辑:jq
-
薄膜锂电池的研究进展2011-03-11 0
-
锂离子电池电解液有机溶剂的发展趋势2013-06-17 0
-
电解液电容器老化电压与电解液火花电压的关系2013-12-30 0
-
锂空气电池的研究进展和最新情况2016-01-13 0
-
锂离子电池电解液超全面介绍 有何神秘之处?2017-02-22 0
-
电解液——锂电池的‘血液’2018-08-07 0
-
卡尔费休滴定仪更换电解液步骤介绍2019-03-20 0
-
电解液干涸是铝电解电容器失效的原因是什么2021-02-24 0
-
2021年电解液行业相关资料分享2021-08-31 0
-
锂离子电池电解液的安全性研究进展2010-08-29 364
-
锂离子电池电解液研究进展2009-10-30 956
-
脑电信号伪迹去除的研究进展_杜晓燕2016-01-15 904
-
新宙邦电解液的研究新进展和成果2020-09-28 3064
-
电解液宽温性能的影响因素和宽温电解液研究进展2020-10-21 8042
-
深度解读钴酸锂体系电解液应用2021-04-17 5940
全部0条评论

快来发表一下你的评论吧 !

