

半导体封装散热材料——Low-α射线球形氧化铝
电子说
描述
技术前沿:半导体封装散热材料——Low-α射线球形氧化铝
氦是宇宙中含量居第二的元素,在全宇宙中质量占大约24%,但在地球的大气浓度中仅为5.2 ppm (0.00052%)。并且由于氦的密度很小,很容易就上升到大气层的上方,从而被太阳风等高能粒子给吹到宇宙里去,永远逃离地球(与此相比,天王星大气中氦气的体积和质量分数分别为15%和26%,非常接近银河的组成)。相反的是,在地壳深处,却由于大量镭、钍、铀等重元素的衰变,产生了大量的氦气体,这也意味着我们的地球深处,实际上是一个非常缓慢的氦气生产工厂。
氦的原子核又被称为α粒子。从核物理的开端,到当前的前沿核物理研究,遍布α粒子的身影。
氦本身除了是宇宙大爆炸的遗迹,还是恒星燃烧的产物,以及放射性核素衰变的产物。在恒星中,宇宙通过聚变的自然法则,将两个质子首先聚变生成氘,然后一个质子再与氘生成氦-3,两个氦-3聚变后生成氦-4。实现从氢到氦的不断转换,从而持续向外输入光和热——我们的太阳即是如此。
1896年,贝克勒尔发现铀射线及其贯穿辐射性,后来被称为贝克勒尔射线,这是人类第一次发现核现象。随后,施密特发现钍元素能够产生贯穿放射性。
1898年,居里夫妇在研究放射性金属的性质时,发现了钋元素,并在随后的研究中发现镭元素。以上所列铀、钍、钋、镭元素均具有贯穿辐射性。
1899年,28岁的E·卢瑟福发表论文,将已知的两种射线按照贯穿本领,分为α射线和β射线。1900年,维拉德发现γ射线。1902年,31岁的卢瑟福对放射性物质的类型按照贯穿能力和在磁场中的偏转性质,分为α射线、β射线和γ射线。
1903年,老布拉格(W.H.Bragg)和助手研究α射线贯穿本领时,发现了α粒子穿过物质时的“布喇格峰”现象。重带电粒子这种特殊的能量损失方式,后来被发展成为目前肿瘤质量的尖端技术——质子重离子肿瘤治疗技术。2020年,我国中国科学院近代物理研究所团队完成首台重离子治疗装置的建造,使我国成为国际上第四个拥有自主技术的国家。
1904年,卢瑟福用α放射性估算了地球的年龄(5亿年左右),大大提高了地球年龄的估算值。
1906年,尽管还不知道α射线是什么组成的,卢瑟福开始设计利用α射线探测原子的性质。
1909年,卢瑟福通过巧妙的实验证明了α射线就是氦的原子核。同年,马斯登在卢瑟福的建议下利用α射线轰击金属靶,发现了α的大角度散射现象。
1910年,林德通过研究α射线在气体中的离子对数目,首次研究辐射化学效应。
1911年,卢瑟福结合对α散射实验结果的理解,提出了原子的有核模型,并计算出原子核的大小。
1913年,K·法扬斯(K. Fajans)和F·索迪分别独立发现α衰变和β衰变过程中的化学元素变化规律,索迪引入同位素一词。同年,盖革发明了盖革计数管,用以α和β粒子计数。
1919年,卢瑟福通过α与氮-14碰撞,产生并发现质子,首次提出核反应的概念,并实现人工元素转变。1925年,布拉克特(P.M.S.Blackett)利用改进的云室证实卢瑟福的核反应假设,找到8个α粒子撞击氮分子的图像,并发现氮核蜕变和释放质子的证据。
1928年,伽莫夫(G.Gamov)利用量子隧道效应解释α衰变机制,这是量子力学在原子核物理中的第一次成功应用,证明了量子力学的正确性。
1930年,玻特(W.Bothe)率先发表用α轰击Be的实验结果,其中发现了一种传统能力极强的中性射线,但他错误解释了实验结果。这种中性射线实际上是中子。
1934年,小居里夫妇用α射线轰击铝,首次制造出了人工放射性核素磷-30.这也提供了人工产生正电子放射性核的方法。
1936年,罗克(Locher)提出硼中子俘获治疗方法,其主要原理是利用中子与硼-10反应生成硼-11,硼-11衰变中产生的高能α和锂-7,杀死肿瘤细胞。硼中子俘获治疗技术目前已经成为临床应用的肿瘤治疗技术。
1940年,赛格雷等人利用α轰击铋元素,生产出了不稳定的85号元素,并命名为砹。
2011年,我国科学家从相对论金-金原子核碰撞中发现了氦的反物质粒子反氦-4,这是迄今为止最重的反物质原子。与此巧合的是,在100年前的1911年,卢瑟福用α散射的结果发现了原子核的存在。
2015年,国际纯粹与应用化学联合会(IUPAC)确认人工合成113、115、117和118号元素,使现有化学元素周期表的空缺全部填满。事实上,超铀人工合成元素的确认,需要利用它们的α等粒子衰变性质来证实。
α 射线 (α-ray)
又称 α 粒子束。指核衰变时释放出的高速运动的α 粒子束流。1898 年,卢瑟福发现铀和铀的化合物所发出的射线有两种不同的类型,他把带正电的射线命名为 α 射线,带负电的射线命名为β 射线。许多不稳定核素发生 α 衰变时会产生 α 射线,这些核素一般为原子序数大于 82 的重核(如氡、锕、钍、镭等),也有少数几种核素原子序数小于 82。
α 粒子即氦原子核,其质量近似等于质子质量的 4倍,带有两个正电荷,常用 4He 表示。α 衰变放出的 α 粒子能量大多 为 4~9 MeV。
α 粒子是重带电粒子,它通过物质时,主要与轨道电子发生库仑作用。由于重带电粒子的能量显著大于电子在原子内的结合能,很容易使电子电离。
α 粒子在物质中行进时,方向不会发生太大偏转,而其自身能量不断减小,运动速度减慢,最后完全失去能量,与外界电子相结合,形成氦原子。因此α 射线的电离能力很强而贯穿本领较弱。它在空气中的射程一般只有几厘米。所以从防护上来看,α 射线的外照射对人体危害不大,容易防护,一般纸张就能阻挡它,但α 射线一旦进入人体,其内照射就会引起明显的组织损伤。此外,对于低能的 α 粒子而言,它与原子核的弹性碰撞也是一种重要的能量损失过程,该过程会改变 α 粒子的运动方向,使原子核反冲,带走 α 粒子的一部分能量,该过程被称为卢瑟福散射。原子核的反冲可使晶格原子发生位移,形成缺陷,造成靶物质的辐射损伤。
α 射线的应用十分广泛。可用于放射性同位素火灾自动报警装置、静电消除器及放射性同位素电池等;也可用作“核弹”轰击其他元素原子核作为同位素源或中子源,或者用于研究原子内部结构。
生活中的氦,应用广泛。从我们的日常家居、呼吸饮食、生产生活、火灾报警,到医学放射治疗等等,都有氦和α粒子的身影。
Low-α 射线球形氧化铝主要应用于高端芯片封装材料。在这一领域,日本公司凭借 长期的技术积累和成熟的下游应用,占领了全球市场大部分份额,国内应用主要依赖进 口。在全球范围内,目前能达到 Low-α 射线控制及磁性异物控制,同时在形貌控制上 可以实现纳米级产品的生产企业仍然较少。
α粒子(也称为α射线或α辐射)的动能可达4-9MeV。由于α粒子带有正电荷,通过物质时极易使其中的原子电离,因此它有很强的电离作用。在阿尔法粒子入射至微电子器件的灵敏区时,会引起半导体器件发生单粒子效应(单粒子翻转、单粒子锁定、单粒子烧毁、单粒子栅击穿等),导致在CPU的指令缓存中引起软错误。由于它对电路的损害不是永久性的,所以这种现象称为软失效,同类名词软错误,软误差(软错误通常通过系统重新启动来解决,因此电子产品软件崩溃或者数据异常,重启它会变正常,是有科学根据的!)。在一些重要的应用场合,芯片任何一次软失效问题都有可能会给系统带来致命的灾难,所以如何应对软失效问题已经成为各大半导体厂商和芯片应用商共同关心的问题。
α粒子主要来源于在导体器件的各种制造和封装材料中存在天然放射性元素:主要是痕量的铀(U)、钍(Th)等杂质,这些材料发射的α粒子可使集成电路发生软误差,是造成芯片发生软失效的主要来源。
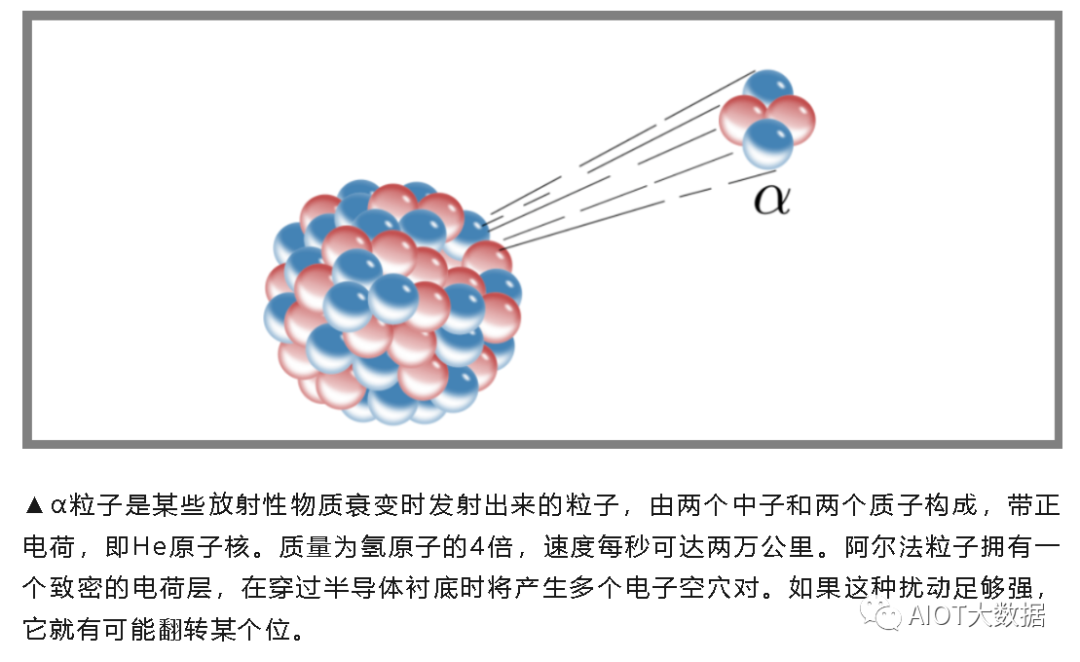
α粒子只能通过特定的放射性核素衰变,自然发出。
属于直接电离辐射,电离本领最强。
通常具有放射性而原子量较大的化学元素,会透过α衰变放射出α粒子,从而变成较轻的元素,直至该元素稳定为止。由于α粒子的体积比较大,又带两个正电荷,很容易就可以电离其他物质。因此,它的能量亦散失得较快,穿透能力在众多电离辐射中是最弱的,人类的皮肤或一张纸已能隔阻α粒子。
α粒子是某些放射性物质衰变时放射出来的粒子,由两个中子和两个质子构成(氦-4),质量为氢原子的4倍,速度每秒可达两万公里,带正电荷。穿透力不大,能伤害动物的皮肤。
α粒子是带正电的高能粒子(He-4原子核),它在穿过介质后迅速失去能量。它们通常由一些重原子(例如:铀,镭)或一些人造核素衰变时产生。
α粒子在介质中运行,迅速失去能量,不能穿透很远。但是,在穿入组织(即使是不能深入)也能引起组织的损伤。α粒子通常被人体外层坏死肌肤完全吸收,α粒子释放出的放射性同位素在人体外部不构成危险。然而,它们一旦被吸入或注入,那将是十分危险。α粒子能被一张薄纸阻挡。
如果人类吸入或进食具有α粒子放射性的物质,譬如吸入了辐射烟雨,α粒子就能直接破坏内脏细胞。它的穿透能力虽然弱,但由于它的电离能力很强,它对生物所造成的危害并不亚于其他辐射。
α粒子就是氦原子核,电子全部剥离,也就是He2+,相对原子质量为4,速度为光速的1/10。
β粒子就是电子,也就是e-,质量非常小,速度可达光速9/10。
γ粒子就是光子,全称光量子,传递电磁相互作用的基本粒子,静止质量为0,速度为光速。
穿透力:γ粒子>β粒子>α粒子
因α粒子比电离值高,所以能形成高密度的离子云,当它靠近带静电荷的物体时,就能中和掉物体表面静电荷。这种装置特别适用于易燃、易爆、不准用明火的环境。在胶片、塑料、印刷、纺织、印染、电子等静电危害严重的行业中使用,可改善工人劳动条件,减少事故,提高质量,增加产量,获得显著的经济效益和社会效益。
球形氧化铝的前世今生
起源:铝土矿
自然界中含铝矿物和岩石种类丰富,如铝土矿、页岩、明矾石、霞石正长岩、黏土、煤矸石、粉煤灰等,这些矿物及岩石都可以作为提取铝的原料,然而截至目前,唯一具有商业开采价值的原料只有铝土矿。铝土矿通常是指以一水软铝石、一水硬铝石、三水铝石为主要成分的矿物。
铝土矿主要分布在几内亚(储量74亿吨)、澳大利亚(储量62亿吨)和巴西(储量26亿吨)、牙买加(20亿吨),四国已探明铝土矿储量约占全球铝土矿总储量280亿吨的65%。从全球铝土矿储量角度来看,我国不属于铝土矿资源丰富的国家,铝土矿储量为9.8亿吨,主要分布在山西、贵州、广西和河南四省(山西41.6%、贵州17.1%、河南16.7%、广西15.5%)。
转化:氧化铝
铝土矿提炼氧化铝是一个经典的化工产业。目前,世界上95%的铝业公司都在使用拜耳法生产氧化铝,该方法由奥地利工程师卡尔·约瑟夫·拜耳初创于1887年。拜耳法工艺原理:用浓氢氧化钠溶液将铝土矿中的氧化铝水合物转化为铝酸钠,通过稀释和添加氢氧化铝晶种使氢氧化铝重新析出,剩余的铝酸钠溶液也叫母液重新用于处理下一批铝土矿。
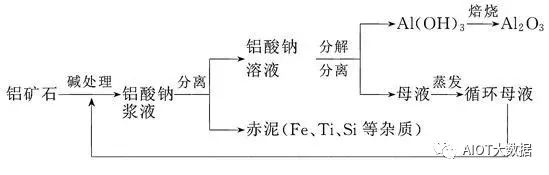
图1 拜耳法经典工艺流程
氧化铝中主要杂质为硅、铁、钠,一部分是铝土矿中自身含有,一部分则是提炼工艺中引入的,特别是钠杂质。
后来根据铝土矿品位差异,衍生出烧结法、和拜耳法-烧结法联合法等多种工艺方法。
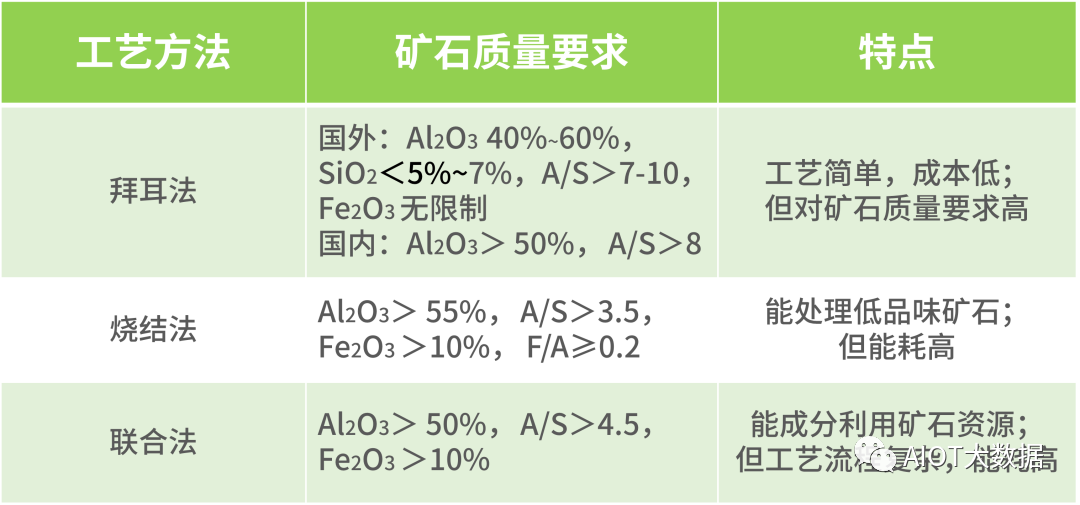
图2 铝土矿主流提炼工艺对比
氧化铝是现代工业中极为重要的基础原料。90%以上氧化铝被用作电解铝原料,通过冰晶石-氧化铝融盐电解法冶炼出金属铝,广泛应用到工业体系。
剩下10%氧化铝因为氧化铝多变的特性,被用到各种细分行业。例如:陶瓷、高温耐材、吸附催化、导热、光学等行业。
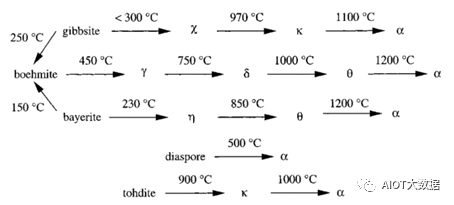
图3 氧化铝的相变过程
进阶:球形氧化铝
致密的晶体构型赋予α氧化铝优良的导热绝缘性能,特别是球形化后的氧化铝,成为了导热散热材料的主力军。
不同于氧化铝的电解应用,导热用氧化铝对钠杂质要求更高,因此适宜选用经煅烧加工的低钠氧化铝,其中钠含量低至300ppm以下。经火焰法高温熔融,氧化铝颗粒快速熔化收缩成球形微粒,再经分级、清洗、干燥等一系列精细处理工艺,最终制备出电子行业适用的球形氧化铝产品。
球形氧化铝工艺核心在于粉末的球形化及粒度、离子杂质的控制。球化效果直接影响到应用粘度,粒度波动也会影响导热配方导热性能的稳定性,离子杂质会干扰配方粘度,反应效果等。
球形氧化铝到底好在哪里?
球铝的形貌结构
先从形貌结构上让大家直观感受下角铝(不规则形貌氧化铝)和球铝的差异。
基于形貌结构的差异,在制胶和实际应用的过程中角铝因棱角锋利,更易磨蚀制胶设备和点胶设备;而球铝球形度好可以延长相关设备的使用寿命。
Low-α射线球形氧化铝-高端芯片封装材料
因为球形Al2O3粉体的独特形貌,使其具有耐腐蚀、耐高温、高硬度、高强度、抗磨损、抗氧化、流动性大、热导率高、绝缘性高和表面积大等优异特性,极大地提高制品的应用性能,广泛应用于电子、化工、国防及航天等高科技领域。
随着科学技术的不断进步,电子、航天航空,特别是通讯技术的飞速发展,电子元器件由分立元件不断向大功率、集成化和模块化发展,因此运行过程中必然会产生更多的热量同时由于使用场合和工况的更加复杂化,对材料的导热性能要求也越来越高。传统的金属导热虽然导热率高,但有其致命的缺点即绝缘性差,高分子复合材料可以克服上述缺点并在各种工业导热场合得到广泛应用。
导热复合材料是由有机、高分子材料(本体导热材料)添加高导热填料制备而成,由于有机高分子材料导热率较低且改进提高非常困难,因此选择高导热率的填料对有机高分子材料进行填充制备复合导热材料。氧化铝是一种常用的复合导热材料的填料,主要是因为氧化铝具有较高的导热率、较好的绝缘性能、稳定的物理化学性能等。
但半导体器件具有高密度化和高容量化,因此,受到来自于半导体芯片附近的材料的α射线的影响而发生软错误的危险增多。使用Low-α射线作为封装材料也显得非常重要。球形氧化铝具有优良导热性,已经成为散热垫片,固定半导体和半导体装置部件的绝缘密封材料的基底材料等的侯选填料,在高集成化集成电路、大规模集成电路和超大规模集成电路的树脂密封材料中使用低α射线指标球形氧化铝颗粒作为填料(铀含量为10ppb以下,可以防止半导体元件的故障),特别适于预防由α射线所引起的记忆装置的操作故障。
据悉Low-α射线球形氧化铝其技术门槛高,生产难度大,单位售价极高,因此主要应用于特殊用途和高端性能需求的电子封装材料中,例如国家安全部门的存储服务器。
如何获得Low-α射线球形氧化铝?
由于球形氧化铝粉末中的铀含量取决于原料中的铀含量,因此重要的是使用铀/钍含量尽可能低以制备具有低铀含量的球形氧化铝粉末,或者通过特殊手段除去氧化铝中的铀/钍杂质。
无机酸溶液洗涤
专利文件JPS56164013A中提到了使用无机酸溶解氧化铝粉体中的放射性元素并除去放射性元素的方法。为了获得适用于半导体存储设备的氧化铝,对煅烧α-氧化铝进行精细粉碎,并用稀无机酸溶液洗涤粉碎的晶体,以洗脱铀和钍在无机酸溶液中,随后氧化铝通过固液分离从无机酸溶液中分离出来。硝酸作为无机酸最有效,其次是硫酸。然后用纯水充分洗涤所得分离的氧化铝并干燥。类似的,其他工艺路线得到的氧化铝理论上也可以采用酸洗的方式除去放射性元素。
高纯金属燃烧法
专利文件JPH1192136A中提出了一种使用高纯金属铝制备Low-α射线球形氧化铝的方法,将高纯铝在高纯石墨坩埚中熔化并雾化生产含铀(U)和钍(Th)低于1ppb的铝粉,将铝粉通入含氧气流燃烧,得到平均粒径为0.4μm~30μm、α射线剂量可低至0.001C/cm2hr的氧化铝粉。改工艺的关键材料是高纯金属、高纯石墨坩埚、高纯雾化气体,以及无污染氧化气体。
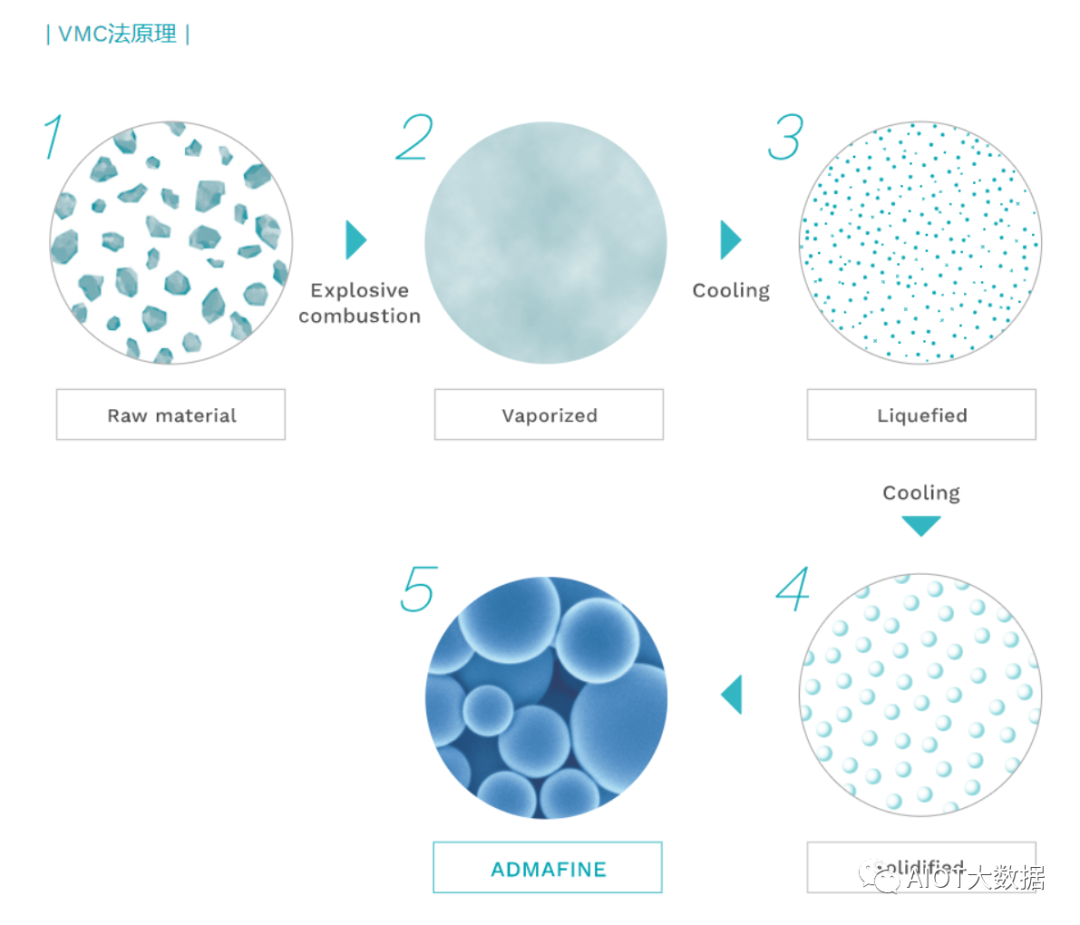
VMC(汽化金属燃烧法)法最初由Admatechs开发,是一种利用金属粉末的爆燃来产生球形氧化物颗粒的方法,冷却后,生成细小的氧化物颗粒,即“ADMAFINE球形颗粒”。球形颗粒也可以用复合氧化物和单一氧化物生产。金属在高温下汽化氧化,产生的氧化热用于汽化后续金属,过程节能、不产生有害副产物。
审核编辑:黄飞
-
陶瓷隔膜氧化铝-提高电池安全性能2014-04-23 0
-
氧化铝的用途有哪些?2016-10-21 0
-
先进陶瓷材料应用——氧化铝陶瓷基板2021-03-29 0
-
氧化铝填充球在某些方面的作用2020-03-05 1897
-
氧化锆增韧氧化铝基板的特点及应用2022-07-12 2206
-
煅烧氧化铝粉末和氧化铝粉体不同区别在哪里?2022-11-03 1368
-
导热氧化铝填料如何搭配才能获得高导热硅胶?2023-05-12 460
-
案例分享第三期:氧化铝陶瓷基板切割2022-03-25 1062
-
氧化铝和特种球形氧化铝粉末的介绍2022-02-20 1758
-
陆芯半导体精密划片机案例分享氧化铝陶瓷基板切割2022-03-30 515
-
氧化铝基板为何要黑色2023-07-04 1038
-
氧化铝陶瓷基板你了解吗?2023-08-02 961
-
氧化铝陶瓷基板:5G时代的材料革命2023-09-06 437
-
捷多邦氧化铝陶瓷基板:电子封装材料的新选择2023-09-06 367
-
半导体划片机助力氧化铝陶瓷片切割:科技与工艺的完美结合2023-12-06 252
全部0条评论

快来发表一下你的评论吧 !

