

可穿戴柔性电子设备在糖尿病治疗方面的应用
描述
糖尿病是生活中常见的一种慢性病,其特征是血液中存在高浓度的葡萄糖。血糖浓度过高会导致代谢紊乱,并衍生一系列的并发症,严重降低了患者的生活质量,病情发展严重还会导致残疾甚至死亡。随着智能终端和移动互联网的普及,柔性电子产品因为具有质量轻、可拉伸和延展性好等独特的优势,近年来逐渐进入人们的日常生活,并被应用在医疗设施中,尤其是在对慢性疾病如糖尿病的诊断、治疗和护理等方面展现出极大的应用潜力。
糖尿病患者需要定期检测血液中的葡萄糖水平,长期使用相关药物进行治疗与控制,由糖尿病引起的各种并发症也需要长期进行监控和护理。传统的糖尿病诊断方法形式单一,不能连续、实时地检测血液中的葡萄糖水平,会对患者造成创伤或延误患者最佳治疗时间。此外,对糖尿病患者的后期护理机制不健全,加上目前的护理设备相对落后,导致患者病情迅速发展。
柔性电子通过结合传感器技术集成为可穿戴柔性电子设备,能够连续、实时地以无创或微创的形式来检测体内葡萄糖水平。可穿戴柔性电子设备通过集成给药装置和无线通信设备,可以智能化地控制药物剂量以及给药治疗,并对糖尿病患者进行健康监测和运动辅助。因此,可穿戴柔性电子设备的出现为糖尿病的诊断、治疗和护理提供了新的途径,成为糖尿病个体化管理最理想的平台。
本文综述了近几年来可穿戴柔性电子设备在糖尿病诊断、治疗和护理中的应用和进展,分析了可穿戴柔性电子设备发展过程中所面临的挑战以及潜在的应用前景。
糖尿病(Diabetes mellitus,DM)是以高血糖为主要特征的慢性代谢性疾病。在过去的几十年中,糖尿病患病率一直呈上升趋势。国际糖尿病联盟(International diabetes federation,IDF)调查结果显示,2017年全球糖尿病患者人数约为4.51亿,预计到2045年患者人数将增加至6.93亿。糖尿病典型的代谢紊乱症状,如多饮、多食、多尿、体重降低,给患者生活质量带来严重的影响。此外,糖尿病还会衍生一系列的并发症,如糖尿病肾病、糖尿病眼、糖尿病足、糖尿病心血管病和糖尿病神经病等,是目前已知并发症最多的一种疾病。糖尿病并发症一旦发生,很难用药物治疗来恢复患者身体健康,病情发展严重最终还会导致患者残疾甚至死亡,给患者带来严重的生理和心理负担。在我国,以淀粉为主食的饮食习惯是导致人们患糖尿病的重要原因之一。同时,经济的快速增长推动了人们的生活方式尤其是饮食习惯的急剧变化,导致人们在日常生活中患糖尿病的概率大大增加。随着我国人口老龄化问题日趋严重,中老年糖尿病患者人数日益增多,由于中老年人对糖尿病缺乏充分的认知与防范意识,给社会的经济发展带来沉重负担。此外,传统的糖尿病治疗方法由于形式单一、治疗时间周期较长、易造成身体创伤等因素,给患者带来了巨大的生理和心理负担。贫困地区医疗设施相对缺乏,医疗设备较为落后,对糖尿病患者的后期护理机制不健全,加上贫困地区患者会因经济落后等产生就医惰性,最终导致糖尿病的迅速发展。
随着科学技术的进步,柔性电子引发了医疗设备产业新一轮的技术革命。近年来,随着个体化健康管理观念日益普及,柔性电子技术逐渐被应用于医疗器件的开发中,成为运动健康管理,疾病的诊断、治疗和监护等变革性的新型设备。首先,柔性电子通过结合传感器和柔性材料,集成为可直接穿戴在使用者身上的柔性电子设备。这些设备具有独特的优势,如质量轻、柔韧性好、可拉伸等,在解决糖尿病等慢性病方面具有极大的应用潜力。同时,可穿戴柔性电子设备能够连续、实时地进行无创或微创的葡萄糖检测来诊断体内葡萄糖水平,为糖尿病的诊断方式提供了新的途径。其次,柔性电子设备可通过集成传感器和给药设备,智能化地对所检测的葡萄糖水平进行分析,方便糖尿病患者进行个性化治疗。最后,柔性电子设备通过与传感技术、短程通信技术和无线技术的结合,集成为微型化、智能化的身体监控设备,能够对糖尿病患者进行健康监测和运动辅助,为患者提供了更加便捷的移动医疗方式。本文综述了近几年来柔性电子在糖尿病的诊断、治疗、护理方面的应用和进展,以期对开发新型糖尿病相关医疗设备的研究人员有所启发。
1 柔性电子与糖尿病的诊断
传统的糖尿病诊断以刺尖采血和静脉采血检测为主,通过刺穿皮肤采集血液来检测体内葡萄糖水平。便携式血糖仪是葡萄糖检测医疗仪器中使用最普遍的仪器之一,根据换能器的不同一般分为电极型和光电型血糖仪。血糖仪由血糖仪主机、试纸条、采血针等组成,使用时先用采血针将血液采集到试纸条上,再由血糖仪主机检测试纸条上的血液样品,通过分析获得葡萄糖浓度数据。血糖仪虽然可以随身携带,能够精确地检测体内葡萄糖浓度,但是需要使用采血针进行反复性的刺痛采血,给使用者身体带来创伤,采血后留下的伤口也可能引起细菌感染并最终造成疾病。
柔性电子的出现为糖尿病的快速诊断提供了更为先进的检测方法。柔性电子通过与其他电子设备集成为可穿戴柔性电子器件,可以随身佩戴并对体内的葡萄糖水平进行连续、实时地检测,避免了传统设备长期进行采血检测所带来的繁琐。其次,柔性电子设备通过采用无创或微创的检测方式减轻了对人体造成的创伤和引起的副作用。Chen等报道了一种柔性贴片传感器,并将其用于检测血液中的葡萄糖浓度。该传感器是由柔性的纸质电池贴片和超薄的生物传感器贴片组成。首先纸质电池(图1b)贴在皮肤上会在皮下产生电化学双通道(Electrochemical twin channels,ETC)(图1a),ETC由透明质酸(Hyaluronic acid,HA)一直连通到组织液(Interstitial fluid,ISF)。纸质电池阳极端带负电的HA会沿着该通道渗透到阴极端,导致在阴极端的HA浓度增加,使ISF的渗透压升高打破了原始的浓度平衡,促进动脉末端血管内的葡萄糖重吸收,因此血管内的葡萄糖往皮外渗透最后输送到皮肤表面。图1c是贴片生物传感器结构示意图,从下往上依次是聚甲基丙烯酸甲酯(Polymethylmethacrylate,PMMA)层、聚酰亚胺(Polyimide,PI)层、金电极层(Au)、普鲁士蓝(Prussian plue,PB)换能器层和葡萄糖氧化酶(Glucoseoxidase,GOx)固定层。在金电极层上通过电化学沉积PB层可以形成更容易弯曲的薄膜,设计双电极系统(工作电极和对电极)可以在反应电流较小时提高检测的精确度(图1d)。在使用过程中,人们先将纸质电池贴附在皮肤上等待约20 min取出,然后将超薄的贴片传感器贴附在阴极接触区域进行葡萄糖浓度测量。图1e展示了分别用血糖仪进行指尖采血检测血液中葡萄糖含量和该贴片传感器进行汗液中葡萄糖检测得到的电流随时间的变化情况,两条曲线的变化情况一致,因此用该传感器可以对体内葡萄糖水平进行实时监控。除了通过检测血液中的葡萄糖水平来诊断糖尿病外,还可以通过检测身体产生的体液和气体来诊断糖尿病。汗液、泪液、唾液、尿液以及呼出的气体中都存在特殊的生理标记物,通过检测这些生理标记物可以获取人体的一些生理信息。
图1 (a)ETC原理示意图;(b)纸质电池贴附在皮肤表面;(c)生物传感器多层结构示意图;(d)生物传感器贴在皮肤表面;(e)使用血糖仪(红色)和该生物传感器(蓝色)进行每小时检测葡萄糖的结果
人体汗腺周围血管高度发达,因此汗液中葡萄糖浓度能够反映人体内的血糖水平。Pott等研究了汗液葡萄糖浓度和血液葡萄糖浓度的关系,发现二者存在显著的相关性,汗液中葡萄糖浓度约为血液中对应浓度的1%~2%,且汗液对血液葡萄糖水平的反映存在约8 min的滞后。糖尿病患者体内的葡萄糖水平比正常人高,出汗时较健康人群会有更多的葡萄糖随着汗液排出皮肤外,通过分析汗液的微量葡萄糖,可以诊断患者体内葡萄糖水平。Lin等报道了一种汗液检测传感器来诊断糖尿病,该传感器通过附有葡萄糖氧化酶(Glucose oxidase,GOD)的多孔膜和纳米结构金属电极结合作为传感检测装置,其中GOD会将葡萄糖氧化为葡萄糖酸内酯和过氧化氢,具有氧化性的过氧化氢进行氧化反应时会释放自由电子,纳米结构的金属电极接收释放的电子会产生电流响应,利用传感器检测电流响应大小可以分析体内的葡萄糖浓度进而诊断糖尿病。
糖尿病患者体内胰岛素不足会引起糖代谢紊乱,因此细胞会优先代谢体内的脂肪,造成了患者体重的急剧下降。脂肪在肝脏分解时会产生丙酮并随呼出的气体排出体外,而糖尿病患者呼出的气体中丙酮含量比健康人群高,因此可以通过检测呼出气体中的丙酮含量对糖尿病进行诊断。Liu等报道了用石墨烯和铁酸锌的复合材料制成的呼吸传感器对糖尿病进行诊断。采用溶剂热法制备石墨烯和铁酸锌的混合物作为传感器的敏感材料,当丙酮气体接触到铁酸锌金属氧化物表面时,会被氧化成二氧化碳和水,并释放出自由电子。通过混合石墨烯材料可以促进丙酮分子的吸收,增大氧化反应的转化率。患者呼出的丙酮气体浓度高,氧化反应所释放出的电子数增多,电子在传感器金属电极上产生电流响应,通过传感器检测响应电流的大小获取丙酮气体浓度,从而判断体内葡萄糖浓度是否高于正常水平。用该材料检测时发现其对丙酮气体有良好的气敏特性,可以实现对糖尿病的诊断。
高血糖也会导致血液中的血糖渗透进入到泪液中。研究表明,人体角膜中存在葡萄糖转运蛋白,在延髓和睑结膜中存在钠和葡萄糖的共转运蛋白,这些转运蛋白通过渗透作用可将葡萄糖转运到泪液中。Sarin等研究了正常人和糖尿病患者眼泪中葡萄糖水平的相关性,结果表明正常受试者眼泪中的葡萄糖平均水平为0.2 mmol/L,而糖尿病患者为0.92 mmol/L。March等研究发现,正常人服用葡萄糖后,眼泪中葡萄糖水平的变化与血液中的相比大约延迟5 min。根据正常人和糖尿病患者泪液中葡萄糖的关系,可以通过分析泪液中的葡萄糖含量来检测糖尿病患者体内的葡萄糖水平。Yao等报道了一种嵌入式隐形眼镜传感器,并将其用于泪液中葡萄糖水平的检测。采用聚对苯二甲酸乙二醇酯(Polyethylene terephthalate,PET)聚合物制备隐形眼镜的主体,然后在隐形眼镜上通过微加工集成传感器。传感器由工作电极(Ti)、对电极(Pd)和参比电极(Pt)组成,在电极附近的传感区域固定一层葡萄糖氧化酶膜,形成一种简单的泪液检测传感器。传感器上的GOD将葡萄糖氧化为葡萄糖酸内酯和过氧化氢,同时释放一定数量的电子,金属电极接收到电子并产生电流响应,测量时用导线将三个电极连接外部电流检测设备进行响应电流测量,通过分析响应电流的大小可以诊断糖尿病。
2 柔性电子与糖尿病的治疗
通常糖尿病治疗主要是以胰岛素注射和口服降糖药为主。胰岛素是最为常用和有效的血糖控制药物,通过与降糖药如磺酰脲类、双胍类、胰岛素增敏剂和葡萄糖苷酶抑制类等药物的配合使用,对体内葡萄糖水平的控制能够产生显著效果。然而,无论是口服还是注射方式给药,都要求患者长期准备药物并定期按时给药,给患者生活带来不便。胰岛素泵是常用的透皮给药治疗设备,通过内部集成传感器,可以根据机体需求持续向患者皮下输注胰岛素,有效控制体内葡萄糖水平,但使用胰岛素泵递药会对身体造成创伤,甚至引起细菌感染。
微针透皮递药是治疗糖尿病的一种先进技术,通过采用微针阵列作用在皮肤表面形成微米级的小孔作为递送药物的通道为体内输送药物。由于微针的结构尺寸很小,对患者皮肤层几乎不会产生创伤。微针贴片通过内部集成传感器,可以检测糖尿病患者体内的葡萄糖浓度,并通过反馈系统自动调节药物的释放量,进行精确的药物递送治疗。Kim等报道了一种集成血糖浓度传感器的智能微针贴片用于糖尿病的治疗。图2a是微针贴片系统示意图,集成系统由汗液控制模块、传感器模块和治疗模块构成。汗液控制组件由汗液吸收层和防水层组成。传感器组件由温度传感器、湿度传感器、微震传感器、pH传感器和葡萄糖传感器组成。治疗组件由微针和加热器组成(图2b)。加热器是由金和石墨烯混合材料通过化学气相沉积制成的蛇形网状结构,提高了可弯曲的力学性能以及热传导效率。图2c是微针结构示意图,微针由生物可降解的聚合物(聚乙烯吡咯烷酮(Polyvinyl pyrrolidone,PVP))与二甲双胍药制剂组成,微针表面涂有一层温度相变材料(Phase-change material,PCM),可以对药物进行保护。当器件温度高于临界值时,相变材料就会融化,从而释放出降糖药物。湿度传感器被用于检测皮肤表面的相对湿度,以确保工作过程中有足够汗液存在。葡萄糖传感器用于检测汗液中葡萄糖水平,pH传感器通过测量汗液pH值的实时变化来校正葡萄糖传感器的pH依赖性偏差。在使用过程中,人们首先将便携式微针贴片贴附在皮肤表面,在一定时间内允许汗液吸收层收集汗液,湿度传感器监测湿度的变化判断收集汗液量,随后开始汗液中葡萄糖和pH值的测量。当葡萄糖传感器检测到高浓度的葡萄糖时,加热器对微针进行加热,当微针的温度超过阈值温度时(图2e),外层PCM融化并将包含的药物释放到血液中,集成的温度传感器对皮肤温度进行监控,防止过热对皮肤造成损伤。图2d是监控体内葡萄糖所得到的数据,发现分别用血糖仪检测血液和用微针贴片检测汗液得到的葡萄糖浓度能够匹配。将微针贴附在患有糖尿病的老鼠腹部(图2f)进行治疗,随后检测老鼠血液中的葡萄糖发现葡萄糖浓度逐渐降低(图2g)。
图2 (a)微针贴片集成模块示意图,由控汗(i,ii)、传感(iii-vii)和治疗(viii-x)组件组成;(b)微针贴片传感阵列(左)和治疗阵列(右)光学相机图像:(i)汗液吸收层;(ii)防水膜;(iii)湿度传感器;(iv)葡萄糖传感器;(v)pH传感器;(vi)Ag/AgCl电极;(vii)微震传感器;(viii)含药物的微针;(ix)加热器;(x)温度传感器;(c)生物可吸收微针的结构示意图;(d)一日检测人体汗液和血液中的葡萄糖浓度曲线图;(e)不同温度下微针进行药物释放;(f)将微针贴在老鼠腹部进行治疗;(g)治疗组(含药物)和对照组(无贴剂和无药物)的小鼠体内葡萄糖含量
糖尿病足(Diabetic foot,DF)是糖尿病最常见的慢性并发症之一。糖尿病患者由于机体内长期高血糖水平导致了周围神经系统损伤和血管病变造成感觉丧失及血液循环不畅,而脚部不敏感往往会使患者行走方式异常,造成足部畸形及足底异常的力学负荷,以上多种病理学因素最终造成糖尿病足溃疡的形成。更为严重的是,糖尿病足溃疡大都伴随着病原体感染,这使伤口更加难以愈合,糖尿病足部感染的发生显著增加了患者截肢的风险。目前对糖尿病足的感染主要实施抗生素治疗,由于糖尿病患者免疫功能低下,糖尿病足病程往往较长,而病原菌的耐药性问题极大限制了抗生素类药物的长期应用。水凝胶是由亲水性聚合物通过物理或化学交联作用形成的三维网状材料,具有优异的生物相容性、柔韧性、药物负载及释放能力,成为制备伤口敷料的理想材料,具有抗菌功能的水凝胶也成为生物医学研究的焦点。以抗菌水凝胶为基底制备的柔性电子器件可以实现智能化的糖尿病足治疗。Lin等使用聚多巴胺包覆的银纳米粒子、聚苯胺(Polyaniline,PANI)以及聚乙烯醇(Polyvinyl alcohol,PVA)制备了一种多功能导电聚合物基水凝胶PDA@AgNPs/CPHs用于糖尿病足的治疗(图3a)。通过低温诱导PVA的结晶形成物理交联,为该水凝胶赋予良好的力学性能。PDA@AgNPs/CPHs还具有良好的成型加工性、可调控的弹性模量以及优异的自愈合特性,同时还具有良好的生物相容性和抗菌性能。当水凝胶附着在潮湿且溃烂的伤口表面后,可以通过促进血管生成、加速胶原蛋白沉积、抑制细菌生长和控制伤口感染来有效地加速伤口愈合,展现出对糖尿病足感染治疗的巨大应用潜力(图3c)。该水凝胶还可以直接粘附在皮肤表面,作为表皮应力传感器实时监测糖尿病足患者的运动行为(图3b)。
图3 (a)PDA@AgNPs/CPHs水凝胶的制备过程及其作为表皮传感器和糖尿病足敷料的应用示意图;(b)PDA@AgNPs/CPHs应变传感器,用于检测人体的运动;(c)在 20 d中分别用PBS和PDA@AgNPs/CPHs 处理鼠糖尿病足伤口照片,显示了PDA@AgNPs/CPHs糖尿病足伤口愈合的作用
3 柔性电子与糖尿病的护理
与急性的传染病或高致死率的肿瘤疾病不同,长期的护理以及精确的血糖控制是解决糖尿病及并发症引发的健康问题的关键手段。柔性电子技术的发展为糖尿病的长期智能护理提供了新的可能,结合了传感器技术集成的可穿戴生物电子设备具有微型化、智能化和携带方便的特点,能够在不影响患者生活的同时进行有效护理。
日常生活中隐形眼镜常用于视力矫正治疗和美容,同时也可以用于眼科疾病的监测。让患者佩戴具有血糖监测功能的隐形眼镜,可以允许护理人员远程监控糖尿病患的血糖情况。Chu等报道了一种基于电化学的隐形眼镜生物传感器,并将其用于监测泪液中的葡萄糖浓度。图4a中(Ⅰ)展示了传感器柔性电极的制备过程,即以硅片为模板,在柔性聚合物基底上分别镀上Pt电极膜和Ag/AgCl电极膜,进一步负载了葡萄糖氧化酶聚合物柔性电极集成到隐形眼镜表面,从而获得具有高度生物相容性的隐形眼镜传感器。随后,Chu等通过动物实验测试了隐形眼镜连续监测泪液葡萄糖的性能。图4b为用隐形眼镜测量兔子泪液得到血糖浓度的实验过程。通过隐形眼镜返回信号与商业血糖检测仪得到的结果进行对比,可以看出用两种方法测得的葡萄糖浓度在随时间的变化趋势上能够匹配一致(图4c)。这证明用该隐形眼镜能够通过分析泪液中的葡萄糖含量,对血液中的葡萄糖水平进行实时的监控。尽管Chu等的研究中隐形眼镜的设计已经初步满足了持续性检测血糖的要求,但是仍不能满足生物电子器件在日常护理中的便携性要求。相信随着柔性电子技术发展的逐步成熟,可实现隐形眼镜与透明电化学储能器件和无线传输器件的进一步集成,最终实现泪液血糖检测设备的便携性要求。
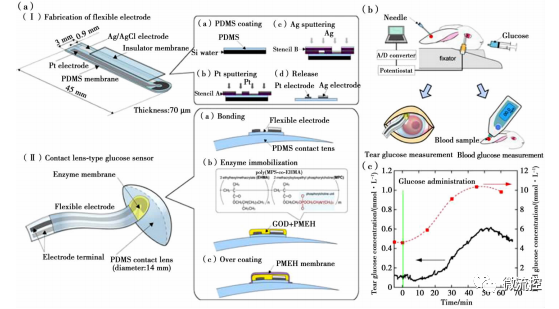
图4 (a)隐形眼镜生物传感器的制备方法:(Ⅰ)在PDMS膜上形成柔性电极,(Ⅱ)将柔性电极粘合到隐形眼镜表面;(b)用隐形眼镜生物传感器和商业血糖监测试剂盒测量泪液中的葡萄糖;(c)泪液和血液中的葡萄糖水平随时间的变化
Kim等集成了一种可穿戴汗液检测手环,该手环可实现高效的汗液收集,进行精确的汗液化学分析。手环由汗液分析条和传感器组成,汗液分析条设计为多层结构,由葡萄糖传感带、隔离层、防水层、汗液条和氢致变色层组成(图5a)。其中隔离层和防水层可以控制汗液吸收量。葡萄糖传感带放置在隔离层的中心,有助于汗液在底部有效积聚。葡萄糖传感器由三个碳工作电极(Working electrodes,WE)和两个Ag/AgCl参比电极(Reference electrodes,RE)组成,使用多个电极可确保传感器的精确度。传感器和氢致变色(Hydrochromic,HC)层之间的缝隙形成流体通道可允许汗液通过(图5b),氢致变色层与汗液接触后会变透明,可以作为汗液收集的视觉指示器。收集到汗液时,WE和RE之间会产生电位差。引入分析物葡萄糖时,WE和RE之间的电位差会发生改变。汗液条收集好汗液之后,将其插入配备的智能手环中进行测量。图5c为手环内部电子组件的简化示意图,三个工作电极(W1—W3)连接到复用器,两个参比电极分别接地和波分复用器,用于葡萄糖传感器连续寻址。阻抗放大器将传感器测得的电流进行放大便于采集,低通滤波器用于消除测量时产生的噪音以便得到稳定的信号,微控制器单元中的数模转换器将模拟信号转换为数字信号。温度传感器通过分压电路连接到控制单元,实时监测人体温度。光电探测器和LED连接到模拟前置芯片作为监测的指示器。最后,微控制器单元配备加速器,将采集到的原始数据通过蓝牙发送到外部移动设备。图5d是进行汗液测量的方法示意图,首先,使用者将汗液条贴在额头皮肤上,并佩戴智能手环传感器,当汗液条收集到聚集的汗液后,将其插入到智能手环的连接端口以进行汗液测量。图5e展示了温度传感器电阻响应和葡萄糖传感器的电流响应,曲线显示三个独立传感器能对汗液中的葡萄糖进行快速响应,并且经过一定时间后测得的电流响应大小趋于稳定值。这种智能手环具备轻薄、耐用和配戴舒适的特点,手环可长期佩戴在患者手腕上,操作简单并且可以随时监测患者体内的葡萄糖浓度。
图5 5(a)一次性汗液分析条的结构示意图;(b)一次性汗液分析条的光学相机图像(左),葡萄糖传感器放大图(右上方)以及汗液条的侧视图(右下方);(c)内部电极组件的集成连接示意图;(d)光学相机图像的测量步骤:ⅰ,将汗液条贴在额头皮肤上;ⅱ,佩戴智能手环;ⅲ,汗液产生;ⅳ,将汗液条插入智能手环测量汗液葡萄糖;(e)温度传感器的电阻响应(顶部)和葡萄糖传感器的电流响应(底部)
糖尿病足患者因末端运动神经发生病变而引发足底压力负荷分布不良,导致在日常行走时,足底一些骨突出部位如拇指、跖骨头和脚跟等产生压力峰值的部位容易受到伤害。同时,糖尿病患者伤口愈合速度较慢,而且容易造成细菌感染,使没有得到长久护理的糖尿病足患者的病情日益严重,并最终导致截肢。因此,开发能够实时测量足底应力分布的柔性电子器件可以实现对糖尿病足患者的有效护理。Rajala等报道了一种基于压电聚合物聚偏二氟乙烯(Polyvinylidene fluoride,PVDF)薄膜的鞋内传感器,并将其用于足底压力分布测量。如图6a所示,Rajala等在PVDF制备的鞋垫基板上选取了拇指(HALLUX)、跖骨头(MTH1A、MTH1B、MTH2-5)和脚跟(HEEL)这几个产生压力峰值的部位作为独立传感器放置的位置,然后使用模板(图6b)在基底上沉积了一层聚对苯二甲酸乙二酯(Polyethylene terephthalate,PET)保护的铜电极层,最后用导线将感应位置与外部检测装置连接。外部检测装置集成了放大器和模数转换器,可对压力变化产生的电信号进行放大和采集(图6c)。实验使用产生动态激励力的振动器对八个独立传感器施加压力来检测和校准传感器的灵敏度,通过标准曲线的绘制计算足底压力的大小。如图6d所示,实验测试了步行时八个独立传感器所测得的压力数据,在各个测量点分别测得的压力随时间变化的趋势不同,证明了八个传感器能够独立地对各个测量点进行压力检测。图6e展示了五次实验所得的压力随时间变化的曲线,可以看出各个测量点每次检测到的压力随时间的变化趋势一致,产生的压力峰值大小几乎一样,说明传感器进行多次测量具有良好的稳定性。用PVDF作为传感器的基底材料,具有易形变和轻薄的特点,根据患者的足底生理结构进行鞋垫定制,可提高穿戴舒适性。通过无线技术将传感器集成到鞋垫内,可对患者进行实时足底压力监测并使足底压力得到均匀分配,使足部末梢循环畅通。
图6 6(a)鞋内传感器由八个测量点组成;(b)金属膜板;(c)PVDF鞋内传感器的测量装置;(d)八个独立传感器测量实验结果;(e)用八个独立的传感器进行五次测量得到的实验结果
4 结语与展望
对于糖尿病这种伴随患者终身的慢性疾病,传统的诊断、治疗和护理方法已经不能满足现代个性化医疗体系的要求,柔性电子的出现为这种疾病提供了新的医疗方法和途径。近几年来柔性电子技术发展迅速,通过结合传感器技术集成可穿戴柔性电子设备,在医疗领域已经逐渐从实验室研究走向临床应用。可穿戴柔性电子设备作为极具前景的医疗手段,正在向着数字化、智能化和精细化方向发展,被逐渐应用于糖尿病的诊断、治疗和护理中,其发展前景非常乐观。特别是对糖尿病患者的护理方面,可穿戴柔性电子设备可突破时间、空间和地域等限制,满足个性化护理服务的需求。作为新型医疗设备,目前柔性电子设备还存在一些不足之处,比如动态测量条件下的信号可靠性,设备长期使用的舒适性等问题。因此需要寻求一条真正适合我国先进医疗方式的道路,推动柔性电子设备进一步深入发展,更有效地提高个人的健康水平。
-
医学创新:提高糖尿病患者的生活质量2018-10-15 1699
-
泪液葡萄糖传感器有望让可穿戴无创血糖监测仪成为现实2018-11-21 2441
-
ML之Sklearn:利用八种ML算法对根据糖尿病数据集预测新个体是否患糖尿病2018-12-20 4164
-
rFGF212—2型糖尿病的新治疗靶点2019-09-25 1926
-
糖尿病治疗设备市场、技术和知识产权的格局和发展趋势2012-06-19 1157
-
糖尿病医疗设备的技术创新之路2012-06-26 1601
-
新的设备将使移植后的胰岛细胞存活更久改善糖尿病的治疗方法2018-06-18 6200
-
物联网IoT装置如何帮助人们管控糖尿病2018-12-23 2133
-
糖尿病机器学习算法获得临床测试2020-04-25 2827
-
集成糖尿病管理系统解析2020-07-03 1351
-
Apple Watch 就能预测糖尿病2020-07-13 2115
-
将人工智能和鞋类相结合,改善糖尿病治疗2022-06-09 3597
-
如何利用科技发展治愈糖尿病2023-07-03 1565
-
利用荧光成像技术动态监测糖尿病发展和治疗进程2023-07-07 2954
-
用于糖尿病创面的防疤痕愈合的自供电酶联微针贴片2023-07-30 3907
全部0条评论

快来发表一下你的评论吧 !

