

器官芯片助力开发COVID-19并发症治疗新方案
描述
据麦姆斯咨询报道,近日,多伦多大学(University of Toronto,U of T)的一个工程研究小组通过新型器官芯片(organ-on-a-chip)平台发现了一种分子,具有治疗由COVID-19(新型冠状病毒肺炎)感染引起的严重的免疫反应的潜力。
该分子是一种名为QHREDGS新型抗炎衍生肽。它不会直接作用于病毒,但会防止发生潜在的危及生命的免疫反应——细胞因子风暴。
据了解,细胞因子风暴出现在部分COVID-19和一些其它疾病的患者中。当人体在血液中释放大量被称为细胞因子的信号蛋白时,就会引起细胞因子风暴。过多的细胞因子会使免疫系统超负荷运转,进而引发血管并发症、多器官衰竭,甚至死亡。
COVID-19大流行期间,临床医生面临的最大挑战之一是了解为什么一些感染了SARS-CoV-2 (新型冠状病毒)的人会经历细胞因子风暴,而另一些感染者则不会。
由Milica Radisic教授(生物工程专业(BME)和化学工程专业(ChemE))领导的多伦多大学流体技术研究与应用工程中心(Engineering’s Centre for Research and Applications in Fluidic Technologies,CRAFT)的研究人员,凭借他们在器官芯片技术方面的专业知识,正在进行上述问题的研究工作。
“基于人体细胞的器官芯片系统具有独特的优势,它使我们能够通过简化系统和有策略地引入各种类型的免疫细胞来更好地了解生物反应,从而剖析其复杂的过程。”Radisic表示。
Radisic和她的团队是体外培养功能性心脏组织的专家。这类可实验室培养的组织使研究人员能够对疾病进行建模,并了解心脏组织中的基因突变导致心力衰竭的过程。
“在COVID-19大流行期间,我们再次利用了心脏组织平台,以了解SARS-CoV-2如何导致血管功能障碍。”Rick Lu(生物工程博士候选人)说道。
近期,该项研究成果发表在《芯片实验室》(Lab on a Chip)杂志上,Rick Lu和他的研究伙伴在论文中展示了他们是如何使用“评估动态事件的集成脉管系统(InVADE)”的特定组织模型平台进行SARS-CoV-2的感染研究,这项研究得到了多伦多大学康诺特基金(Connaught Fund)、多伦多创新加速合作伙伴(Toronto Innovation Acceleration Partners)和多伦多大学捐助者的支持。
利用InVADE平台,研究人员利用SARS-CoV-2感染了一个基于微纳制造技术的可灌注血管芯片,以了解该病毒如何引发炎症和血管功能障碍。
他们还筛选了5种此前已被临床医生测试过的具有抗炎特性的化合物,来确定其中是否有预防细胞因子风暴潜力的化合物。
QHREDGS是一种先前已被发现可改善心肌细胞代谢和增强内皮细胞存活率的衍生肽。在这项研究中,Rick Lu发现它可以增强血管功能,并修复SARS-CoV-2对人体造成的不良影响。例如,与没有QHREDGS的内皮细胞相比,含有QHREDGS的被称为内皮屏障的内皮细胞,其血管结构功能提高了62%,而引起细胞因子风暴的分子分泌却极大地减少了。
“血管功能障碍会导致SARS-CoV-2扩散到人体器官,如心脏、肝脏和肠道等。”Rick Lu说,“我们希望通过改善血管功能和减少体内炎症,预防COVID-19患者出现器官衰竭。”
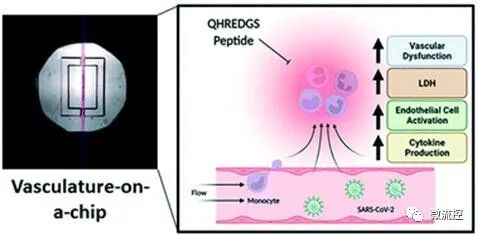
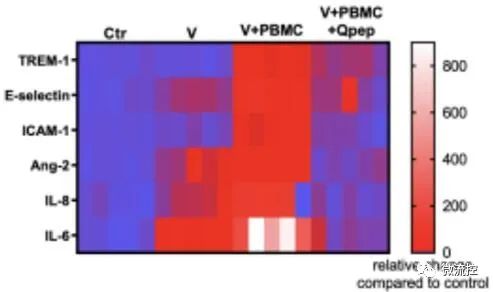
血管芯片模型用于研究冠状病毒引起的血管功能障碍,找到针对SARS-CoV-2感染的潜在治疗方案(来源:CRAFT)
在Radisic的实验室,InVADE平台被用于许多其它研究,包括研究“为什么在心脏中很少发现癌症”。Rick Lu和他的同事们还通过血管芯片系统,来更好地了解COVID-19患者以及一些接种了COVID-19疫苗的群体出现心肌炎的原因。
该科研团队目前正在与多伦多的临床医生和研究人员合作,寻找与心肌炎相关的独特的生物分子标志物。
“目前,我们正在利用一些先天免疫系统,如外周血单核细胞(PBMC)和中性粒细胞,来观察这些免疫细胞如何与心脏组织相互作用,以了解它们如何影响心脏组织功能。”Rick Lu说,“我们对此感到非常激动,因为我们不仅能够识别与心肌炎相关的一些分子的来源途径,而且还希望找到潜在的治疗方案来逆转心脏中的这种炎症造成的损伤。”
Radisic希望这类器官芯片系统可使研究人员能够预测并更好地应对未来的公共卫生事件。
“除了消除利用活体动物的研究,以及保证临床研究参与者的安全之外,器官芯片的小尺寸还使我们能够高效地使用试剂,并通过将实验所需的病毒数量降至最低来保证安全性。”Radisic说,“这项器官芯片技术可以快速、高效地研究新出现的病原体,以及其感染和损害人体各器官功能的风险程度。”
论文链接:
https://pubs.rsc.org/en/content/articlelanding/2022/lc/d1lc00817j
审核编辑 :李倩
-
制作Covid-19探测器2023-07-04 667
-
COVID-19危机-发烧警报系统开源分享2023-07-03 584
-
COVID-19:手部消毒机2023-06-30 779
-
用于术后血管并发症监测的植入式传感器2023-05-23 1594
-
COVID-19非接触式洗手定时器2022-12-16 715
-
COVID-19短信警报2022-12-15 864
-
COVID-19额温枪开源分享2022-11-30 1945
-
使用交互式地图协调对COVID-19的响应2022-11-28 773
-
COVID-19预防警报系统2022-11-25 704
-
谷歌搜索添加COVID-19测试相关选项 将提供COVID-19检测中心信息及联系方式2020-04-18 5107
-
产后抑郁症的治疗好方法2012-10-13 1904
-
MP3不恰当使用带来并发症2010-02-02 610
全部0条评论

快来发表一下你的评论吧 !

