

基于LAMP-CRISPR耦合滑动芯片和智能手机的miRNA检测系统:“灵捕”
描述
近期,北京理工大学研究人员开发了基于LAMP-CRISPR耦合滑动芯片和智能手机的miRNA检测系统:“灵捕”。该系统在生物传感器的基础上,通过滑动芯片对检测的各个环节进行集成,同时利用智能手机微信小程序实现了可视化交互,以及现场快速即时检测(point-of-care testing,POCT),可应用于癌症早筛。
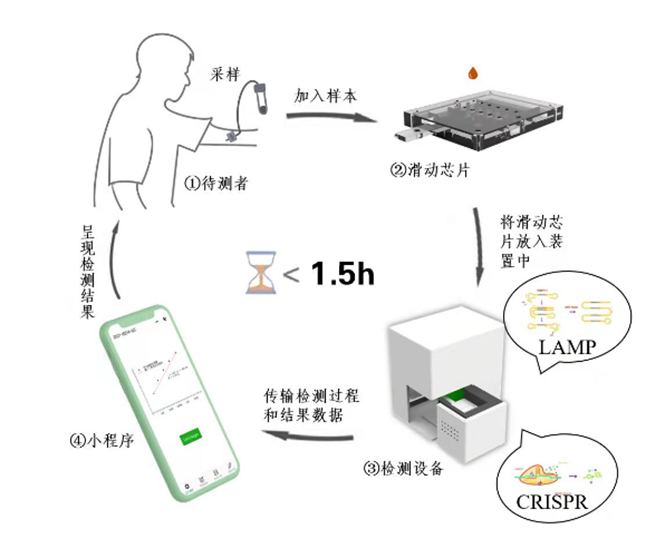
“灵捕”系统示意图
结直肠癌作为一种常见的消化道恶性肿瘤,具有较高的发病率和死亡率。随着社会经济水平的提高及生活和饮食结构的改变,我国结直肠癌总体发病率与死亡率呈现明显上升趋势。结直肠癌患者Ⅳ期5年生存率为8%,而Ⅰ期5年生存率可以达到87.9%,在患者早期完成结直肠癌的筛查具有十分重要的意义。
目前临床采用的筛查方法有胃肠镜检查、低剂量CT筛查及粪便隐血试验等,但仍存在临床检测成本较高,以及各类并发症或机体损伤的问题,目前临床普及性较高的癌症早期筛查手段均具有一定的局限性,迫切需要一种高效、安全的筛查方法。
微小核糖核酸(miRNA)是在进化上保守的、由19~22个成熟核苷酸组成的小分子非编码调节单链RNA序列。miRNA的功能涉及到各种生理病理过程,在癌症及相关癌前病变的不同疾病阶段以及不同的发病部位之间都存在较为显著的表达差异,并且已有多种miRNA被证实是有效的癌症早筛标志物,实现其检测意义重大。
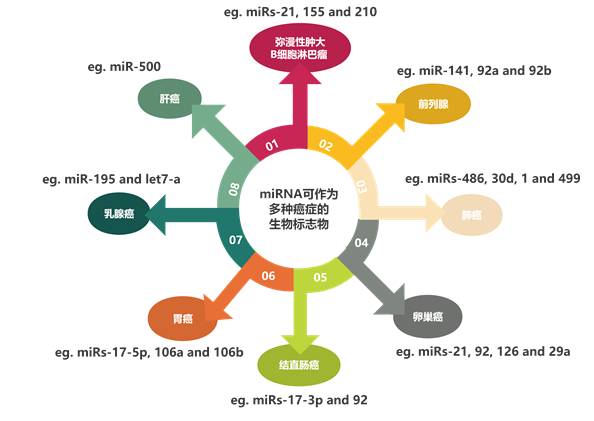
miRNA可作为多种癌症的生物标志物 RT-qPCR核酸扩增技术,可以通过复杂的探针设计将较短的miRNA序列变成较长的靶标,但作为变温扩增方法,需要大型且较为昂贵的热循环仪,其在资源有限的环境中的应用受限。在此基础上,研究人员提出环介导等温扩增法(LAMP)以提高序列特异性、简化扩增系统、降低检测设备的开发成本。此外,基于滑动芯片的微流控芯片,具有操作简便、对操作人员要求不高、所需样本量少和检测成本低、微型化、 高效快捷以及容易与其他装置集成等特点,因此,研究人员构建了与LAMP结合的全集成滑动芯片。
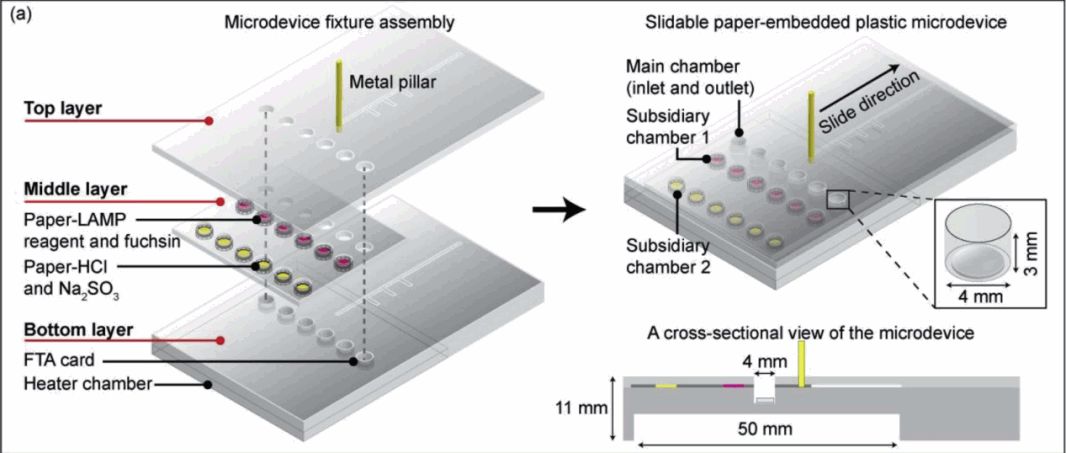
与LAMP结合的全集成滑动芯片示意图
目前,miRNA检测存在用时较长、检测成本较高、需要设备较多等问题。miRNA即时检测(POCT,point-of-care testing)系统,则是一类能够在采样现场即刻进行分析、省去标本在实验室检测时的复杂处理程序、快速得到检测结果的新方法。基于此,研究人员由滑动芯片以及智能手机共同构建了更具环境部署性与信息关联性的POCT系统,来实现方便、快捷的miRNA检测。
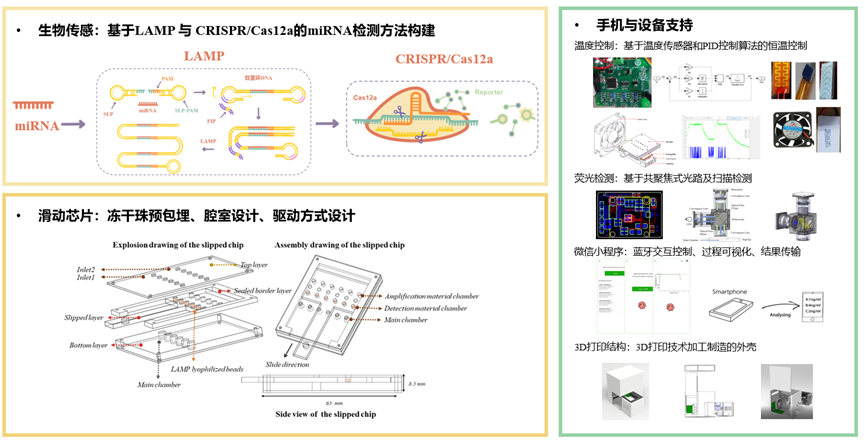
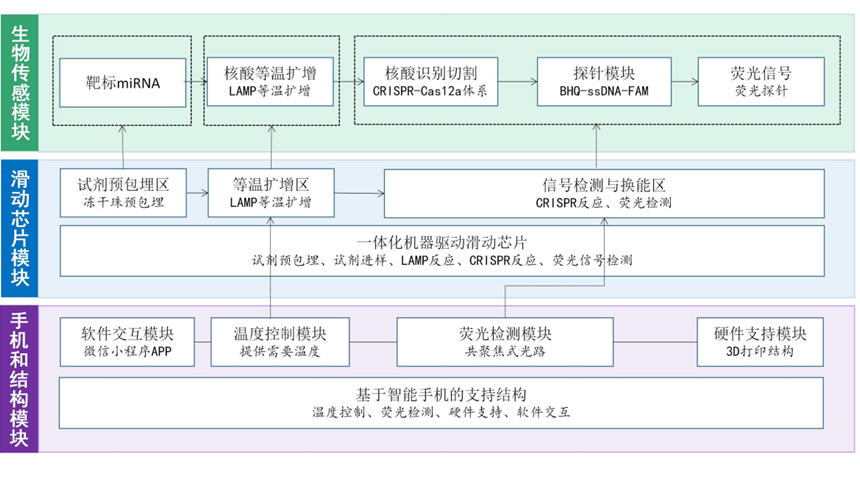
“灵捕”系统设计总方案
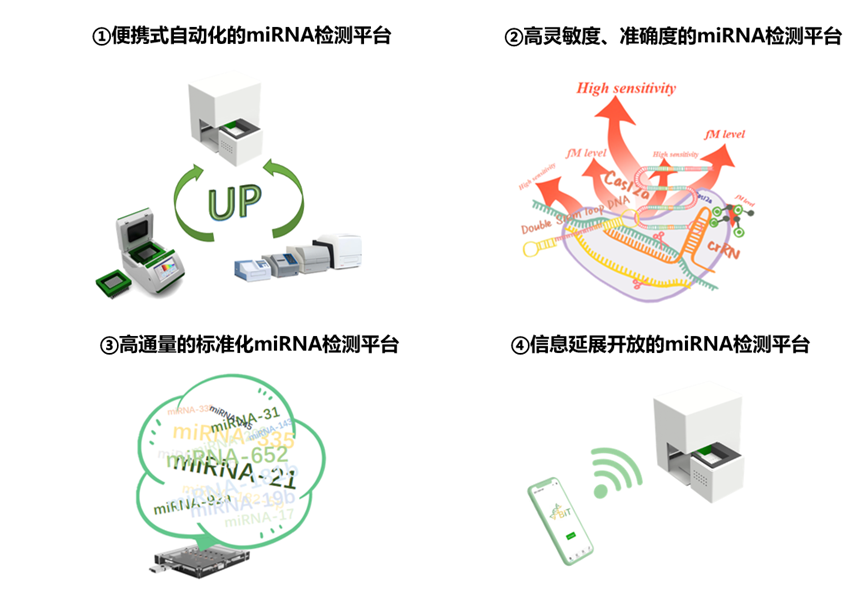
“灵捕”系统的优势 生物传感器的设计 “灵捕”系统充分整合LAMP等温扩增技术、CRISPR/Cas检测技术、荧光共振能量转移(FRET)等诊断学的新技术、新方法,通过LAMP实现miRNA的等温扩增,采用CRISPR/Cas12a系统特异性识别扩增产物并输出荧光信号,建立荧光强度与miRNA浓度的关系以实现定量检测。
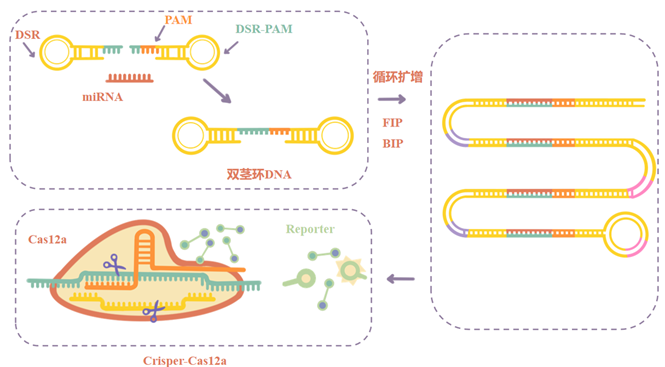
“灵捕”系统生物传感器设计
基于生物检测的硬件设计
研究人员设计了滑动芯片用以整合复杂的实验室操作,既可以保持LAMP简便、快捷、高效等优点,又能以较少的试剂消耗实现检测,在此基础上构建相应的小型化设备以提供反应温度、检测荧光结果。 软件设计 “灵捕”系统还搭建了基于智能手机的小程序平台,以实现对设备的控制及结果的可视化。使用者在使用时仅需按照微信小程序的操作提示进行加样操作即可完成仪器的使用,可以将反应主体部分拉出以进行反应试剂加样。
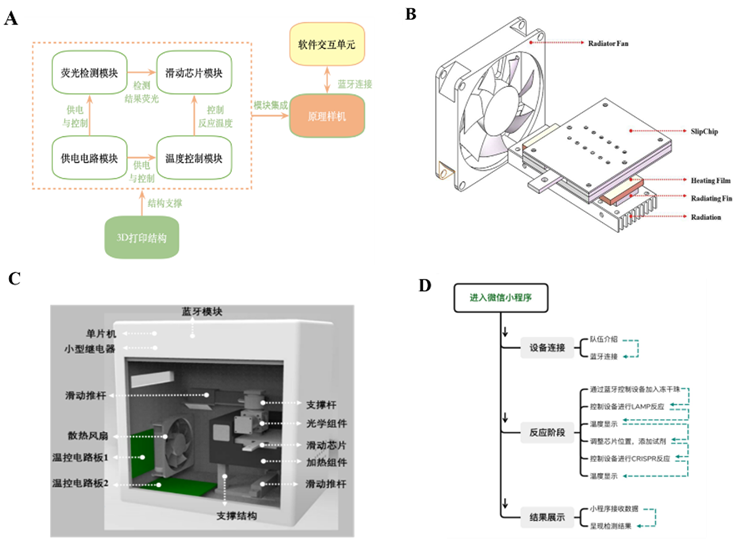
硬件和软件设计
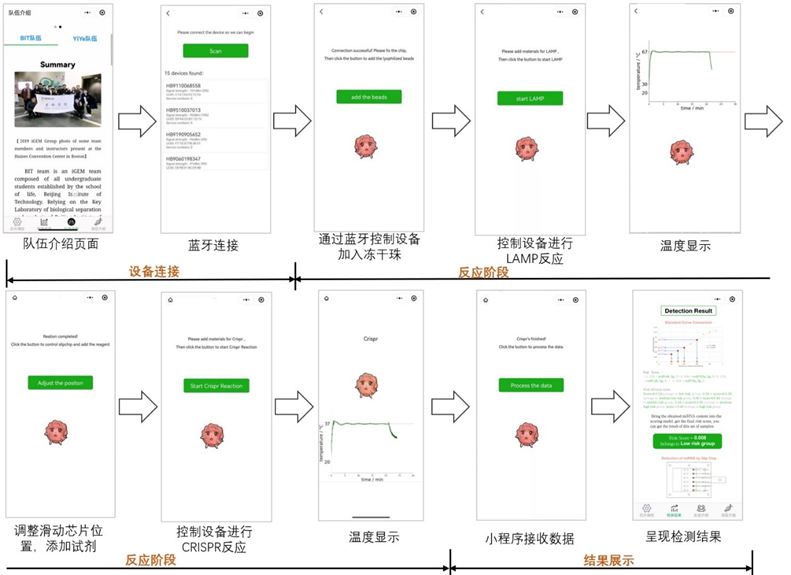
微信小程序示例图 建模流程设计 建模部分以结直肠癌为癌症代表,通过生物信息学方法,筛选结直肠癌相关miRNAs用于检测方法开发中检测对象的确定;并建立综合风险评分模型,基于检测到的用户样本中多种miRNA的含量,综合评价其患癌风险。
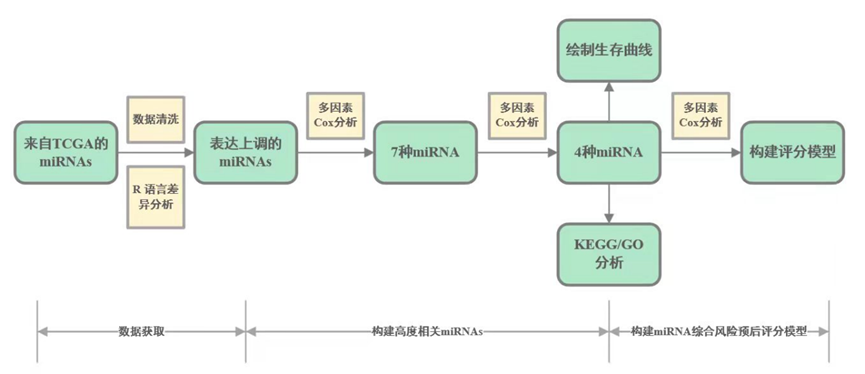
建模流程设计
LAMP-CRISPR反应的表征 研究人员首先验证LAMP-CRISPR检测miRNA的可行性,采用体系终浓度为5pM的miRNA-21进行LAMP引物连接反应、LAMP扩增及CRISPR/Cas12a三步实验,以证实这一检测原理的可行性。无LAMP扩增反应证明了LAMP扩增反应的必要性:将miRNA转换为CRISPR/Cas12体系可识别的双链结构,并对miRNA信号进行放大。
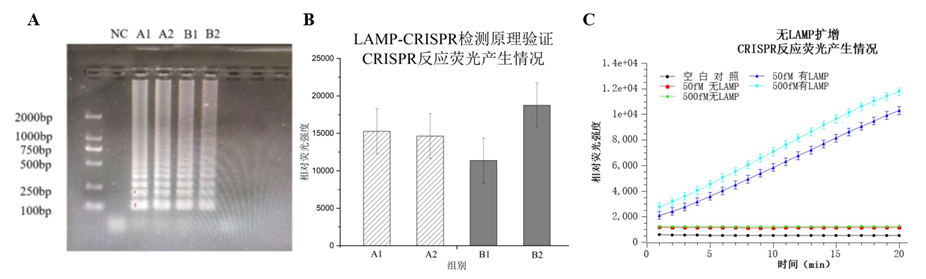
LAMP-CRISPR反应的表征 LAMP-CRISPR/Cas体系用于miRNA的定量检测 为了测试生物传感系统对miRNA的检出限,研究人员设置miRNA浓度梯度为500fM、50fM、5fM、0.5fM、0.05fM,构建检测标准曲线,结果表明miRNA的浓度与荧光强度具有线性关系,相关系数达93.13%,得出检测的标准曲线LOD为0.069fM。
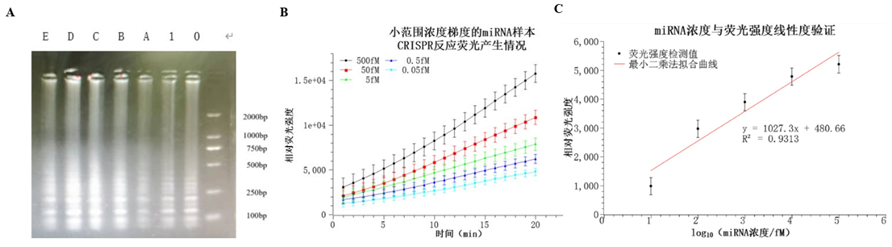
miRNA检出限测定 硬件基础及配套试剂优化 为在滑动芯片上实现miRNA检测试剂的预包埋,研究人员设计采用冻干珠替代LAMP试剂、CRISPR试剂,并实验验证可行性。在滑动芯片中进行单独LAMP反应和LAMP+CRISPR反应,通过荧光显微镜观测结果,发现滑动芯片和温度控制模块可以有效实现LAMP与CRISPR步骤,荧光检测模块经测试可以正常使用。
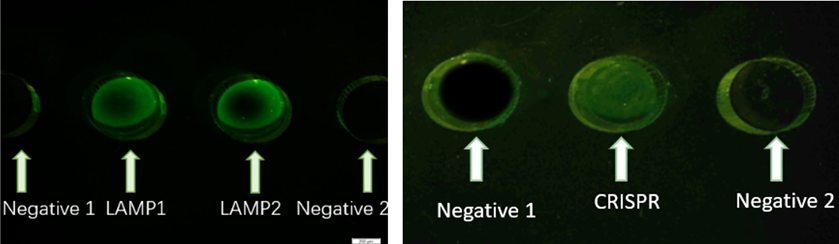
荧光显微镜下LAMP和LAMP+CRISPR反应结果观察图

温度控制模块和荧光检测模块 总体而言,研究人员构建了LAMP-CRISPR技术耦合滑动芯片及智能手机的miRNA检测系统:“灵捕”。检测系统以miRNA作为癌症早筛的生物检测标志物,将LAMP等温扩增与CRISPR/Cas12切割技术二者相结合,实现了对miRNA信号的高灵敏度扩增与识别。同时,研究人员通过滑动芯片实现了生物检测体系的集成,并以此为基础构建了相应的小型化设备以提供反应温度、检测荧光结果。此外,研究人员建立了可支持生物传感模块与滑动芯片模块的智能手机即时检测操作系统,保证以可视化的形式呈现检测结果、实现对设备的控制。
审核编辑 :李倩
-
议智能手机+平板电脑,商机?!2012-01-06 3498
-
智能手机电源管理注意事项2012-02-03 5056
-
基于IMS的双模智能手机系统的设计2012-08-20 2249
-
智能手机芯片之争一触即发2012-10-25 3378
-
君正100美金低成本3G智能手机解决方案详解2012-12-19 4252
-
智能手机2013-06-23 5685
-
智能手机如何判断人脸的贴近2013-09-30 5173
-
模拟智能手机2016-09-26 3688
-
你怎么定义智能手机壳,觉得高科技+手机壳=智能手机壳吗?!2018-01-05 5917
-
基于NFC技术的智能手机设计2019-06-19 3899
-
自动对焦在智能手机的应用2019-07-16 4088
-
智能手机怎么才能更加智能?2019-08-20 4098
-
pSouthPu外光设备怎么连接到智能手机?2019-09-20 2173
-
如何设计智能手机省电系统?2019-11-05 2735
-
请问如何去设计一种智能手机系统?2021-04-25 2458
全部0条评论

快来发表一下你的评论吧 !

