

SPR和LSPR传感器的最新研究成果
描述
高传染性病毒对生命安全和社会运行有重大的威胁,快速灵敏的病毒检测是防止病毒爆发的首要手段。基于表面等离子体共振(SPR)和局域表面等离子体共振(LSPR)技术的生物传感器具有快速、高灵敏等特点,在临床病毒检测上有巨大的应用潜力。
据麦姆斯咨询报道,来自南京理工大学电子工程与光电技术学院的研究人员从抗体、抗原、核酸和病毒颗粒这四类传感器捕获物入手,基于四种病毒检测方法,综述了SPR和LSPR传感器的最新研究成果,并以综述论文形式发表于《中国激光》期刊。
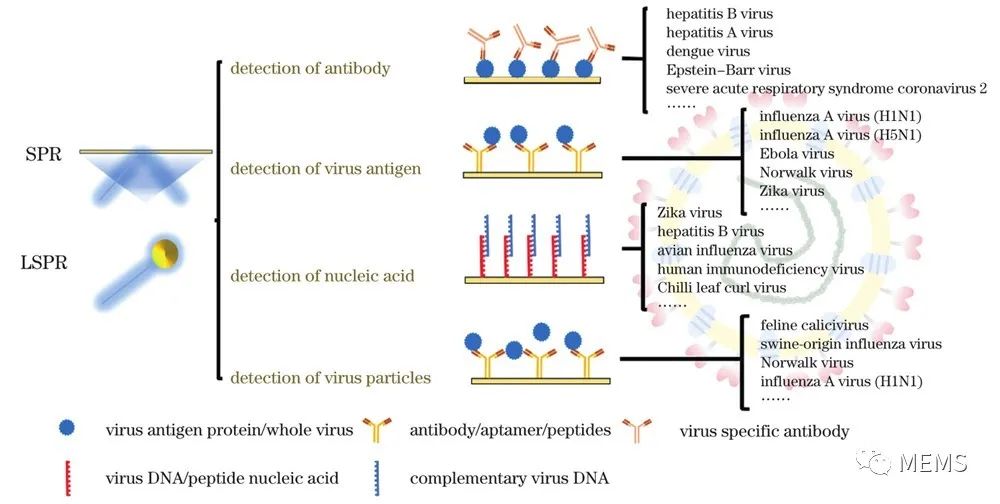
图1 基于SPR或LSPR技术的病毒检测方法
就目前的研究进展来看,基于抗原-抗体特异性结合原理的SPR或LSPR传感器的研究重心在抗原或抗体修饰物的筛选、抗原和抗体结合能力的评估以及抗体修饰物的替代等方面。在大量研究中,研究人员意图寻找针对某种病毒检测的最优识别元件,以提高传感器的检测性能、降低成本、增加可重复性等。
金纳米棒(AuNRs)常作为等离子体纳米换能器在LSPR病毒抗体检测中得到应用,AuNRs相对于球形AuNPs,其额外的纵向等离子体带对周围环境的介电特性变化高度敏感,且灵敏度随着纳米棒纵横比的增加而增加。
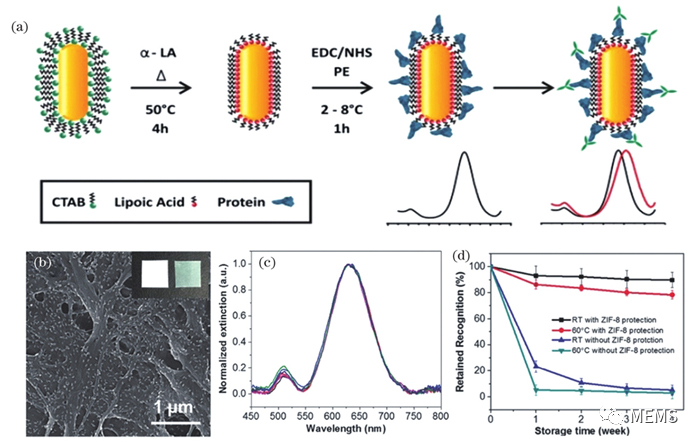
图2 利用AuNRs检测病毒
此外,有研究人员通过将AuNPs异质组装在载玻片表面上,制造了传感芯片,AuNPs单层和单一AuNP构成免疫夹心结构,芯片和AuNP之间的近场电子耦合可放大SPR响应信号,该夹心结构对乙肝病毒表面抗原(HBsAg)的检测限比单一异质组装AuNPs芯片高100倍,在临床人血清样品中展示了10pg/mL~10ng/mL的检测范围,该传感器工作示意图如图3所示。

图3 LSPR生物传感器芯片工作示意图
传统SPR或LSPR传感器对临床病毒核酸样本的检测效果并不理想,需要结合DNA扩增、荧光物质等增益手段才能实现低浓度核酸样本的检测。对于优化策略,SPR传感器主要聚焦于膜层材料增敏和金属粒子耦合增敏;LSPR传感器的优化策略的重心则是AuNPs、AuNRs等纳米粒子或纳米结构的设计和优化,常结合量子点(QDs)等荧光物质形成探针,通过光吸收峰偏移或荧光光强变化检测病毒。此外,聚合物刷和可替换磁珠能够有效解决传感器生物介质污染和重复性差等问题。
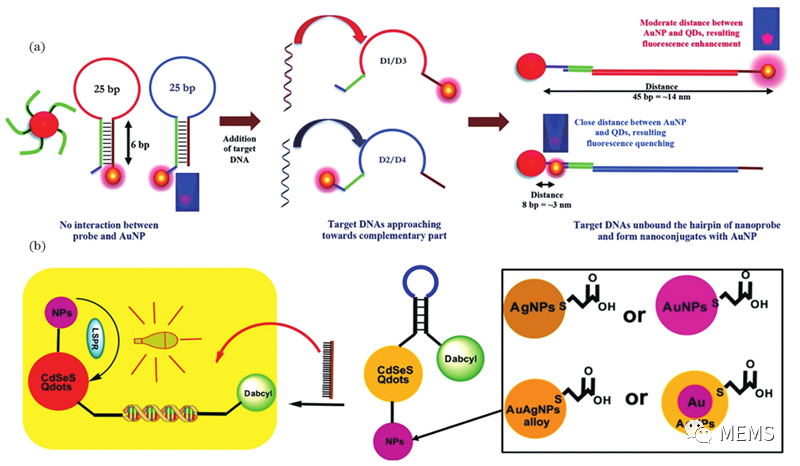
图4 LSPR结合QDs增强灵敏度
病毒蛋白抗原和病毒核酸的检测都需要从病毒中分离目标物或者在血清中对目标物进行纯化处理,而病毒颗粒的直接检测可以缩短样品的前处理时间。利用LSPR对荧光半导体QDs的荧光增强或淬灭效应来提高病毒传感器的灵敏度已有较多应用。
近年来,日本研究团队通过结合AuNPs与QDs来检测病毒颗粒,通过在AuNPs和CdSeTeS合金核量子点粒子表面分别修饰抗神经氨酸酶(NA)抗体和抗血凝素(HA)抗体,实现了两种粒子在病毒表面的偶联,病毒表面AuNPs诱导的LSPR效应增强了相邻QDs的荧光强度,荧光强度与目标病毒浓度变化成正比,从而实现了质量浓度低至0.03pg/mL的H1N1病毒的检测,并在H3N2和诺如病毒检测中也取得了较好效果。
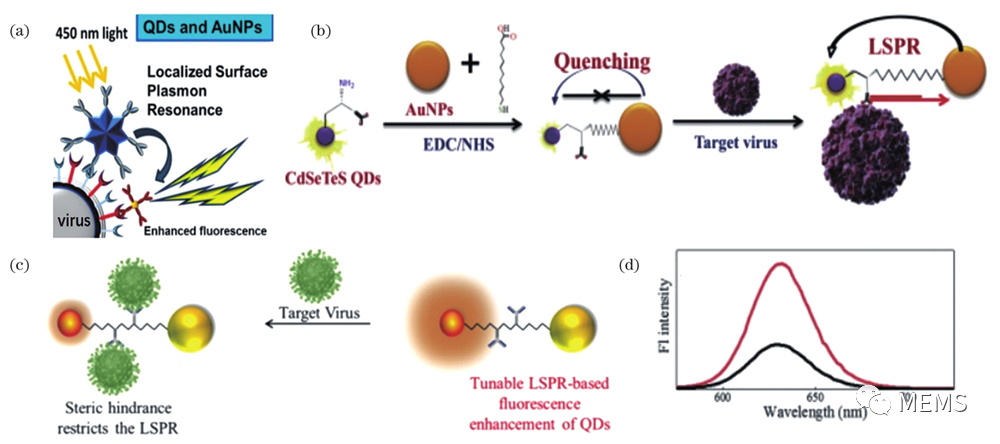
图5 金纳米颗粒-荧光量子点传感探针
总体来说,SPR和LSPR传感器在目标选择灵活性、检测时间及检测限方面较ELISA和PCR存在一定优势。但是SPR和LSPR技术的临床化和产业化仍面临一些挑战。首先需要考虑传感器整体的小型化和便携化;其次,要解决传感器芯片的保存问题;最后,需要降低传感器芯片的成本。可以预见,由于SPR和LSPR病毒传感器修饰物的多样性,未来或许可以通过传感器识别元件的集成化同时针对多种目标分析物进行特定病毒检测,在短时间内多维度评估病毒的感染情况,避免假阴性和假阳性案例的出现。
论文信息:
DOI:10.3788/CJL202249.1507401
审核编辑 :李倩
-
无线传感器及执行器网络2012-05-23 3351
-
最新数字图像传感器技术应用2013-09-23 2406
-
日本FDK用于生物物质及工业流体测定的SPR传感器2018-11-20 1939
-
动态范围可调的波导型SPR传感器模型2009-06-30 599
-
二氧化锡膜气敏传感器最新研究成果2009-07-03 640
-
光纤电参量传感器的研究2009-07-13 613
-
二氧化锡膜气敏传感器的最新研究成果2009-11-23 550
-
基于强度调制的光纤SPR系统的研究2010-08-25 718
-
传感器检测精度再度提高,检测精度和分辨率提升了2个数量级2017-10-27 3383
-
佳能展示最新研究成果_1.2亿像素传感器与400万ISO传感器2018-04-05 6546
-
深入了解最新的深度学习研究成果2019-04-03 5220
-
研究人员发现量产低成本纳米传感器的技术2019-05-20 2025
-
华东理工:自供电可穿戴传感器领域的最新研究成果2023-02-21 1778
-
一种基于横向位移检测机制的MXene增强SPR生物传感技术2023-10-29 1604
-
NVIDIA在ICRA 2025展示多项最新研究成果2025-06-06 1707
全部0条评论

快来发表一下你的评论吧 !

