

基于细胞外囊泡(EV)的液体活检技术
描述
液体活检是确定癌症发生发展的关键性技术,有助于提前预防癌症的发生或转移。基于细胞外囊泡(EV)的液体活检已经成为癌症检测中的新兴技术。然而,其应用存在众多障碍,如无法有效收集足够EV用于分析生物学功能的变化,无法有效定性其源组织。此外,由于缺乏有效的生物标记物,EV的分离技术也有所受限。如果能够提升基于EV的肿瘤检测性能,将有效解决临床中肿瘤的早期筛查等困难。
基于此,来自加拿大瑞尔森大学(Ryerson University)的谭波教授团队开发了一种纳米工程化的3D传感器,由纳米尺度探针实现自功能化的表面增强拉曼散射(SERS)技术,对三种难以检测的癌症——乳腺癌、肺癌和结直肠癌具有100%的敏感性和100%的特异性,能够准确的将癌症与非癌症样本区分开来。相关工作以“Cancer Stem Cell Derived Extracellular Vesicles with Self-Functionalized 3D Nanosensor for Real-Time Cancer Diagnosis: Eliminating the Roadblocks in Liquid Biopsy”为题于近期发表在ACS Nano期刊。
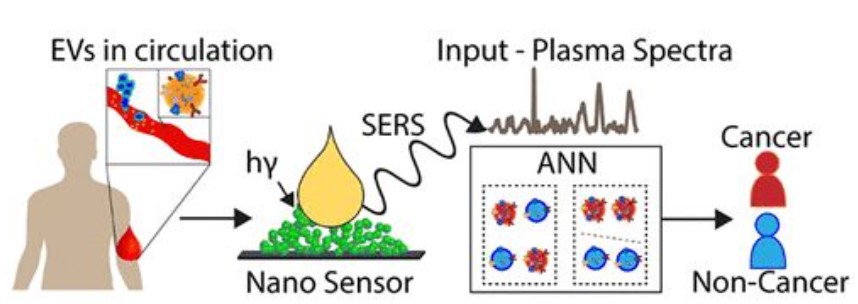
图1 3D纳米传感器的构造及其用于癌症的检测
研究人员利用超快飞秒激光的多光子电离机制制备了纳米传感器。通过将钛样品暴露在离子辐射下,生成自组装的纳米探针网络,制备了三种类型的纳米传感器。通过控制激光刻蚀深度和激光脉冲的峰值功率来控制纳米传感器的特性,并进一步用分析物(罗丹明6G;R6G)测试纳米传感器的SERS信号放大效率。R6G的SERS光谱显示了显著增强的特征峰。相比没有纳米传感器的R6G,纳米传感器1上的R6G的增强程度最高(约1000倍)。使用FDTD模拟求解麦克斯韦方程在钛基纳米探针周围的区域。散射光强度的增强与电场增强的四次幂成正比,场增强的存在产生了局域表面等离子体。此外,研究人员使用了三个激发波长分析了电荷转移机制的影响及其对波长的依赖。R6G的非完全对称模式在三个激发波长上的选择性放大证实了电荷转移的存在。钛的折射率为~2.61,TiO₂的折射率为~2.1,空气的折射率为1.61。三种材料折射率的对比可以产生全内反射,除了在多层功能化纳米探针中捕获光子外,这还大大增强了拉曼信号随着氧空位的存在,整体SERS水平显著提高。与低氧空位的传感器(纳米传感器2和3)相比,具有最高氧空位的纳米传感器(纳米传感器1)有效提高了约1000倍的SERS。此外,氧空位可以丰富表面态,放大分析物和表面相互作用,一定程度诱导癌症纳米传感器的拉曼信号显著改善。
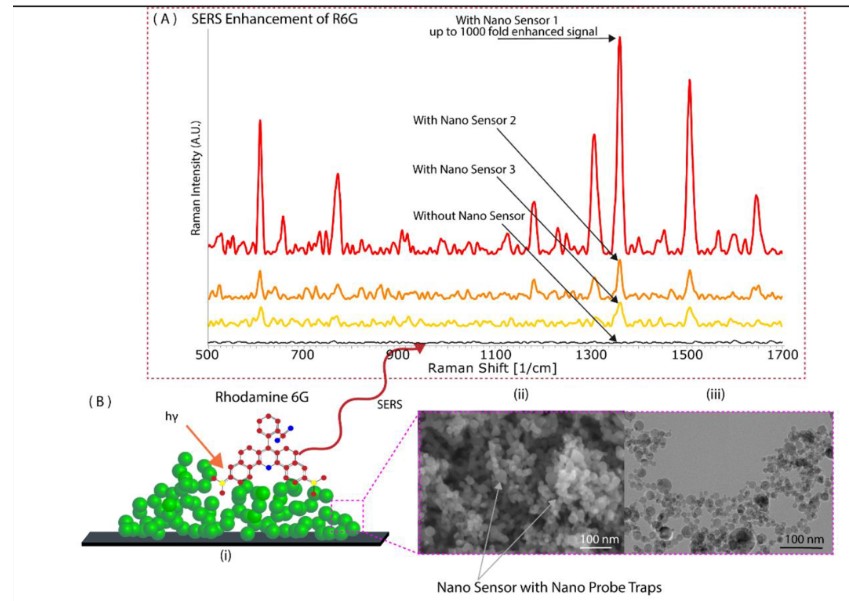
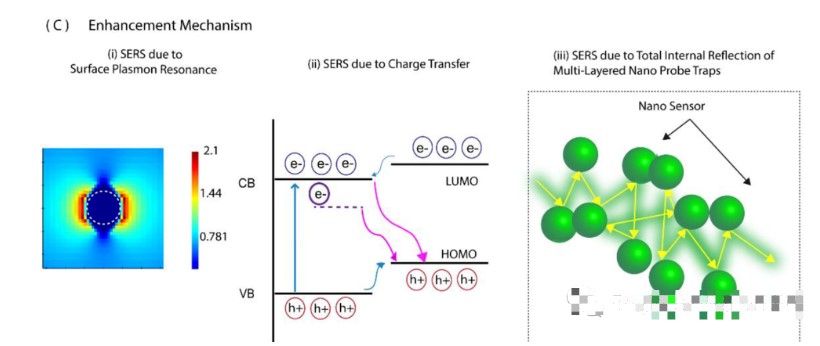
图2 基于肿瘤纳米探针的SERS技术。
(A)纳米传感器对罗丹明6G的SERS光谱显示,其拉曼信号增强高达1000倍。与其他传感器相比,最小尺寸和最高氧空位的纳米传感器(纳米传感器1)表现出最高的信号增强。(B)纳米传感器平台上罗丹明6G的示意图。(C)显著增强信号归因于多种现象的激活:(i)FDTD模拟表明存在SPR;(ii)极小尺寸相关的电荷转移机制和氧空位的存在是纳米传感器显著SERS响应的原因;(iii)由于纳米传感器三维网络的存在而产生的内部全反射。
研究人员对来自三种乳腺、肺和结肠CSC的EV进行纳米传感器辅助SERS谱分析。PCA结果显示PC评分存在显著差异。PC1、PC2和PC3演示了三个单独的簇。特征峰强度被绘制在热图中,以可视化观察EVs内容物的差异。然后将PCA得到的特征(拉曼峰)应用于未经处理的患者等离子体光谱,进行了两种类型的分析。
首先,将一个组织起源与所有其他起源进行分类。基于ANN的分类具有100%的敏感性、100%的特异性、100%的准确性和100%的精度。同时,对乳腺癌达到了100%的敏感性和68%的特异性;结直肠癌的敏感性为36%,特异性为100%;肺癌的敏感性为99%,特异性为100%。观察到大肠癌患者的血浆与乳腺癌有非常高的相似性。
因此,对于大肠癌,二分分类会更合适。这些结果表明,纳米传感器的能力可以准确识别组织来源。为了证实CSC EV对起源组织检测的适用性,研究人员利用PLSDA建立的训练模型进行补充分析,实现了73%的乳腺癌敏感性,42%的大肠癌敏感性和100%的肺癌诊断敏感性。乳腺癌的特异性为88%,大肠癌的特异性为100%,肺癌的特异性为70%。
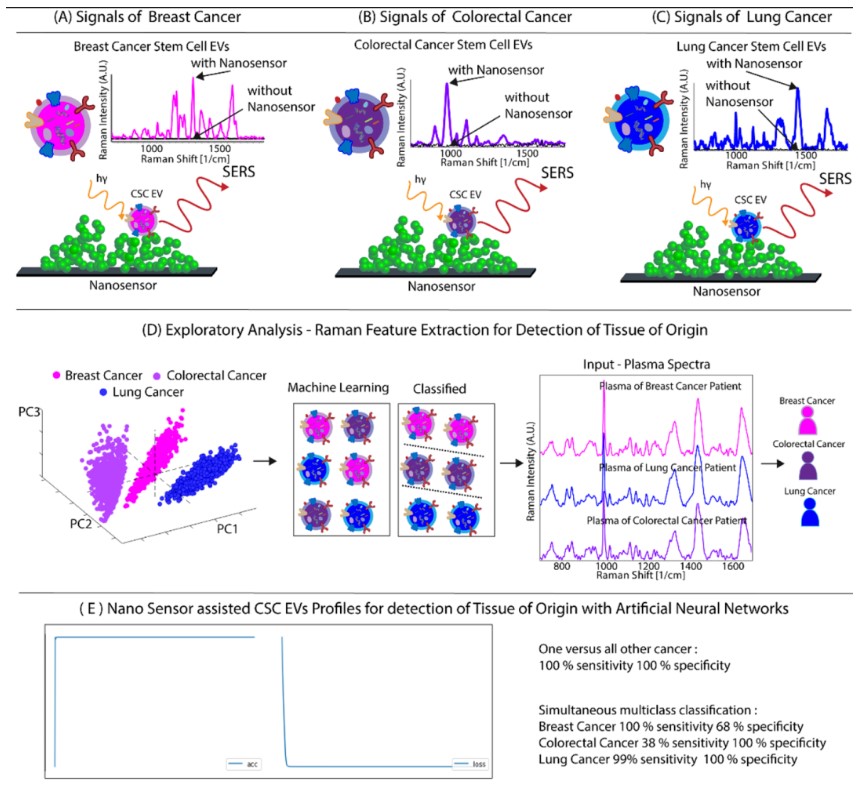
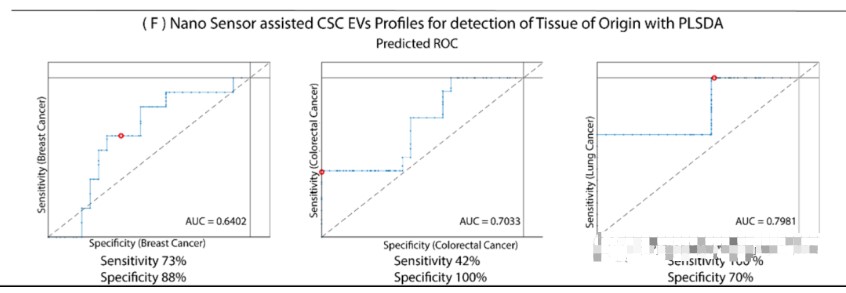
图3 CSC EV鉴定源组织。
(A)乳腺癌信号来自于乳腺CSC EV的拉曼谱。(B)从结直肠癌CSC EV的拉曼谱获得的结直肠癌信号。(C)肺癌的信号来自肺CSC的EV的拉曼谱。(D)乳腺癌、肺癌和结直肠癌的CSC EVs PCA显示CSC EVs聚类,源组织鉴定示意图。(E)将PCA特征应用于患者血浆样本。起源组织与所有其他组织的二元分类达到了100%的准确性。同时多类分类准确率达79%。(F)采用PLSDA分析对方法学进行验证,证明诊断具有很高的敏感性和特异性。
总而言之,由于一些生物学和技术上的挑战,例如无法同时获得EV内多个分子的分子信息,现有的基于EV的液体活检临床可用性非常有限。
此外,现有的EV液体活检不能识别组织的起源。研究人员通过对CSC EV的分子和功能信息的研究,消除了现有液体活检的局限性。采用这种液体活检工具,可以提高EV传感器相互作用效率,可同时检测多个EV的信号,通过实验证明了CSC EV信号的利用对液体活检是至关重要的。
对于三种难以检测的癌症(乳腺癌、肺癌和结直肠癌),人工神经网络以100%的敏感性和100%的特异性区分癌症和非癌症。基于ANN的二元分类将一个组织的起源与所有其他组织区分准确率100%,同时对所有三种不同类型的组织来源进行鉴定,患者血浆样本的准确率达到79%。证明了技术的临床可用性。如果在未来得到大量临床样本的验证,这种模式可能会作为一种无创工具来补充现有的诊断工作流程以及纵向治疗监测。
审核编辑:刘清
-
人工智能可助辨识细胞结构2018-10-15 2705
-
微流控技术的应用分析液体活检背景介绍2018-04-29 5899
-
液体活检将如何改变癌症诊疗?微流控技术推动技术突破2018-06-13 5156
-
英国研究人员使用人工智能检测卵巢癌患者活检样本中的微小异常细胞簇2019-01-21 740
-
中科院大连化学物理研究所在单细胞外囊泡多参数分析方面取得新进展2019-04-08 4634
-
血液活检:新型微流控技术可以对癌细胞进行详细的遗传分析2019-05-20 6471
-
脑神经化学活体原位电化学分析新技术2020-05-11 4474
-
浅析基于微流控芯片的异质性细胞外囊泡精准分离和定量方法2023-01-17 2165
-
基于微纳流控平台的细胞外囊泡荧光标记新策略2023-05-25 1821
-
利用DNA计算介导的串联微流控平台,实现细胞外囊泡亚群的有效分离2023-06-11 2040
-
微流控芯片在液体活检中的应用2023-07-25 1252
-
利用粘弹性微流控系统,直接从人体血液中分离小细胞外囊泡2023-10-19 2617
-
一种用于富集循环肿瘤细胞的螺旋微流控芯片设计2023-11-10 2387
-
基于磁珠的液滴微流控平台,用于细胞外囊泡的高效分离2024-03-12 2638
全部0条评论

快来发表一下你的评论吧 !

