

一种有效的开发高性能电解液的解决方案
电子说
描述
【研究背景】
能够在电极上形成富含阴离子的无机固体电解液界面(SEI)并具有广泛的电化学稳定性的电解液创新对于金属锂电池(LMB)的商业化至关重要。含氟电解液、高浓缩电解液(HCE)和局部高浓缩电解液(LHCE)是应对高压金属锂电池诸多问题的有效手段。然而,高浓度盐或氟化溶剂/稀释剂的高氟含量导致生产成本大大增加,环境负担加重。此外,还原含氟有机溶剂会导致副反应产生有机成分。因此,设计新型的低氟电解液,既环保又低成本,同时还具有与LMA和高压阴极的良好兼容性,对于推进实用LMB的商业化是非常可取的。
【工作简介】
近日,浙江大学范修林、中科院物理所王雪峰等人报告了一系列硅氧烷溶剂,其中的Si-O键确保了与锂金属阳极的高兼容性和与阴极的高氧化稳定性。该工作代表了在金属锂电池中电解液选择中高氟化以外的独特道路,不仅有利于LMBs的实用性和可持续性,而且还表明:通过化学键设计是一种有效的开发高性能电解液的解决方案。独特的1.5M LiFSI/二甲基二甲氧基硅烷电解液不含任何添加剂/协同溶剂,使金属锂实现了约99.8%的高沉积/剥离库仑效率(CE),在高压LiNi0.8Co0.1Mn0.1O2(NCM811)和LiCoO2(LCO)电池实现了>99.9%的高CE。在4.5V的LiCoO2(3 mAh cm-2)||Li(20 μm)电池中200次循环后保持仍可保持95%的容量,在贫电解液条件下(2.5g Ah-1)的1.4Ah的NCM811(3.6 mAh cm-2)||Li(20 μm)的软包电池中,140次循环后仍有高达96%的容量保持率。该成果以《Eco-friendly electrolytes via robust bond design for high-energy Li-metal batteries》为题发表在国际顶级期刊《Energy & Environmental Science》( IF 39.714 )上。第一作者为浙江大学Huang Yiqiang、Li Ruhong、中科院所理所Weng Suting。
【具体内容】
硅和碳都是元素周期表第IVA族的成员。在空的三维轨道上,硅可以通过共轭接受邻近原子(O、N和S等)的孤对电子,这导致Si-O键的键能高于C-O键(452 kJ mol-1 vs 352 kJ mol-1)。此外,鉴于硅醚保护基在有机合成中对一系列氧化和还原试剂的抵抗力,用Si-O键取代C-O键应改善溶剂的氧化还原稳定性,为锂电池电解液提供新的机会。
通过计算还原和氧化电位的指导,开发了一系列的硅氧烷分子,正硅酸四乙酯(TEOS)、甲基三乙氧基硅烷(MTES)、二甲基二乙氧基硅烷(DMES)和二甲基二甲氧基硅烷(DMMS)与低浓度的双(氟磺酰)亚胺锂(LiFSI)盐配对的电解液。
为了形成富含LiF的无机SEI,溶剂应该具有低的还原电位和高的氧化电位,牢固的键和低的去溶剂化能。酯类、磷酸盐、砜类和腈类以其出色的抗氧化性而闻名,但有很强的还原倾向。所有这些溶剂在电子供体或Li+受体域附近都有共轭结构。醚类是少数具有锂兼容性的例子,但它们不能忍受高压阴极(图1a)。这些现象可以用近似的分子轨道理论来解释。一旦与相邻的原子结合,碳酸盐中乙氧基的孤对电子将进一步与π*C=O反键轨道共轭,形成一个能量较低的填充轨道,意味着更难失去电子(图1 b)。醚容易被氧化,因为没有相位匹配和能量相当的空轨道可以稳定氧的非键合电子。新的轨道表现出原来轨道的混合特征,这为设计更好的溶剂提供了指导。与能量较高的Si(电负性比C低)三维轨道共轭,产生了能量较高的空轨道,以提高抗还原性,同时保留了低能量的填充轨道(图1b)。为了验证这一推论,计算了溶剂的分子轨道并进行了分布处理。硅氧烷本质上拥有比醚低得多的最高占有分子轨道(HOMO)能级,表明其具有更好的抗氧化性。如图1c的插图所示,局部的醚类电子轨道聚集在-O-基团周围,而在硅氧烷溶剂(DMMS、DMES和MTES等)和碳酸盐中,由于共轭效应,电子云分别向中心Si原子和C=O基团偏移。
根据量子化学计算,键的弹性力常数(FFC)可以作为描述符来定性地确定键的强度。一般来说,醚类和酯类中Si-O键的柔性力常数比C-O键高,说明溶剂的化学稳定性更高。此外,静电势最小值(EPM)按EC < DME < DMC < DOL < DMMS ≈ TEOS ≈ MTES < DMES的顺序增加,这表明Li+去溶剂化能下降,界面动力学改善,分解概率从左到右降低的趋势。因此,通过在醚类中用Si取代中心C,形成Si-O分子成为更稳定的线性分子,设计了新型硅氧烷溶剂,预计其综合电化学性能将优于醚类和酯类。
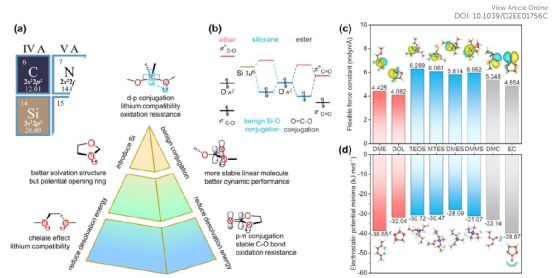
图1 分子设计原则。(a)、1,2-二甲氧基乙烷(DME)和碳酸乙烯酯(EC)分别是醚类和酯类溶剂的典型代表。它们都与Li+强烈结合,但方式不同。二甲醚的特殊构型,即两个O同时与Li+配位,导致了高去溶剂化能。缩短或延长-O-基团之间的烷基链可以打破螯合效应并降低能垒,另一种流行的醚类溶剂1,3-二氧戊环(DOL)就表明了这一点。至于EC具有的高去溶剂化能源于刚性环状结构的高极性。线性碳酸盐的开放结构,如碳酸二甲酯(DMC),导致了分子偶极子的相互抵消,从而减少了去溶剂化能,改善了电-电解液界面的动态性能。此外,线性结构消除了开环反应的风险,使溶剂更加稳定。正如在上下文中讨论的那样,良性共轭的Si-O分子具有像C=O基那样的低填充电子轨道和像C-O基那样的高空轨道。因此,通过模仿二甲醚的结构,用Si取代中心的烷基链,设计了具有更宽的电化学窗口和更好的化学稳定性的新型硅氧烷溶剂。(b), 醚、硅氧烷和酯的近似分子轨道的示意图。其中硅氧烷和酯具有共轭效应。(c), 8种溶剂中指定的C-O和Si-O键的计算弹性力常数(虚线标记)。(d), 8种溶剂的计算静电势最小值。
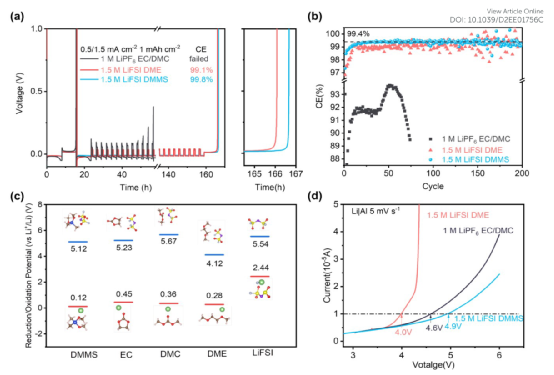
图2 电极和硅氧烷电解液之间的电化学兼容性。
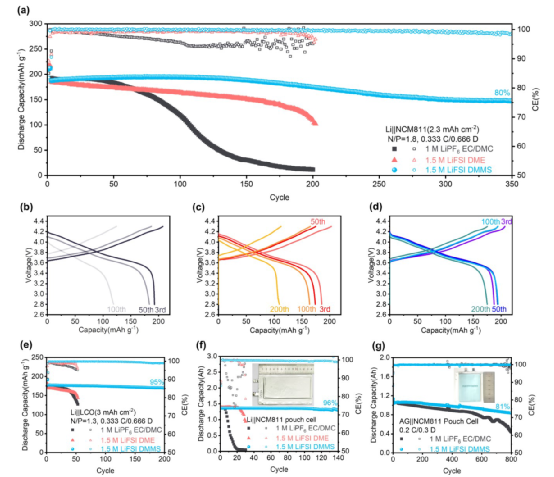
图3 金属锂全电池的性能。(a), 金属锂阳极全电池在0.333 C充电和0.666 C放电(1 C=200 mAh g-1)时的性能(20 μm锂阳极,2.3 mAh cm-2 NCM811阴极)。(b-d), 使用1 M LiPF6 EC/DMC (1:1, v/v) (b), 1.5 M LiFSI DME (c), 和 1.5 M LiFSI DMMS (d)的全锂电池的充电和放电曲线。(e) 20-μm-Li||3 mAh cm-2 LCO全电池在0.333 C充电和0.666 C放电(1 C = 180 mAh g-1)下的长期循环性能。(f), Li||NCM811软包电池的循环性能(>1.4 Ah大容量,<2.5 g Ah-1贫电解液,20μm超薄Li||和>3.6 mAh cm-2超高阴极负载)。(g), 工业人造石墨(AG)||NCM811电池与1 M LiPF6 EC/DMC电解液和1.5 M LiFSI DMMS电解液的长期循环性能。
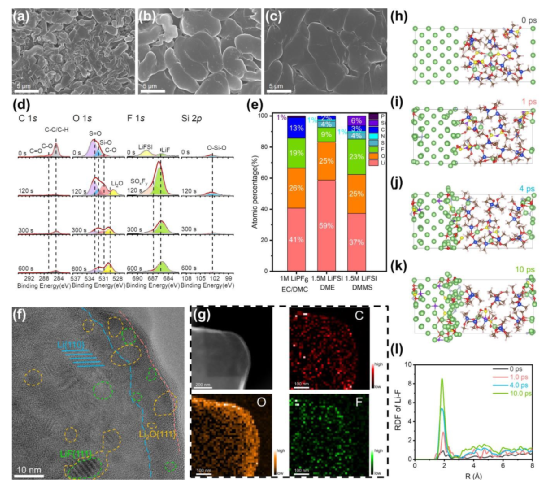
图4 阳极-电解液界面的特征和AIMD模拟结果。(a-c), 在1 M LiPF6 EC/DMC (1:1, v/v) 电解液(a)、1.5 M LiFSI DME 电解液(b)和1.5 M LiFSI DMMS 电解液(c)中金属锂的沉积形态。(d), 在1.5 M LiFSI DMMS中,经过10个循环后,金属锂表面的XPS深度图。(e),循环后的金属锂表面检测元素的原子百分比。(f), (g), 在1.5 M LiFSI DMMS电解液中新鲜沉积的锂的低温TEM(f)和EELS-mapping(g)图像。(h-k), 锂-电解液(1.5M LiFSI DMMS)界面的AIMD模拟快照。
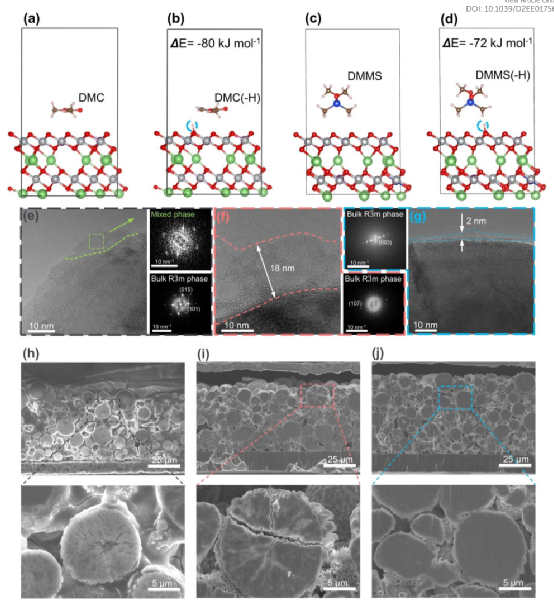
图5 阴极-电解液界面的特征和计算模拟结果。(a-d), DMC(a, b)和DMMS(c, d)的H-转移计算。(a), (c), H-转移前的快照。(b), (d), H-转移后的快照。 (e-g), 100个循环后,NCM811阴极的HR-TEM图像,通过拆卸使用1 M LiPF6 EC/DMC(1:1, v/v)(e)、1.5 M LiFSI DME(f)和1.5 M LiFSI DMMS(g)电解液的全电池收集。(h-j), NCM811电极在1M LiPF6 EC/DMC电解液(h)、1.5M LiFSI DME电解液(i)和1.5M LiFSI DMMS电解液(j)中循环100次后的SEM横截面图像。
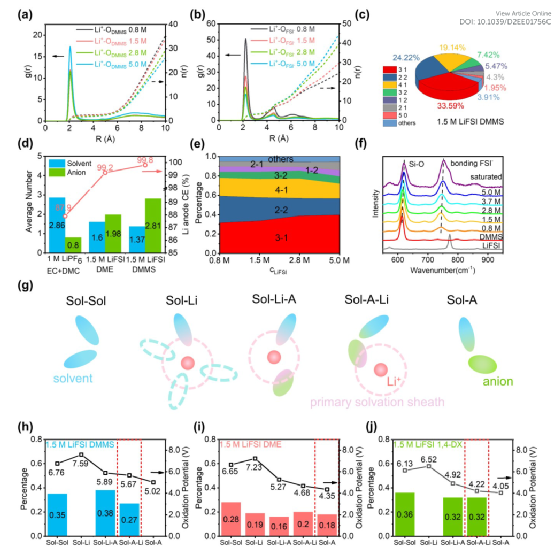
图6 硅氧烷基电解液中锂离子的溶剂化结构。(a), (b), 溶剂的O原子(a)和阴离子的O原子(b)围绕Li+的RDF。(c), 在1.5M LiFSI DMMS电解液中Li+的第一个溶剂化鞘中阴离子-溶剂数量的统计结果。(d), 1.5M LiFSI DMMS溶液的独特溶剂结构和锂阳极CE与传统的碳酸盐电解液和醚类电解液的比较。(e), 增加LiFSI浓度时电解液中Li+第一溶剂化鞘的演变。(f), LiFSI, DMMS, 和它们不同浓度溶液的拉曼光谱。(g), 五个以溶剂为中心的团簇的示意图:ⅰ)自由溶剂域中的溶剂二聚体,ⅱ)分离的溶剂中只有溶剂溶解Li+,ⅲ)Li+鞘中的溶剂部分被阴离子溶解,ⅳ)Li+鞘中靠近阴离子的溶剂,ⅴ)溶剂与自由阴离子接触。(h-j), 在1.5 M LiFSI DMMS (h), 1.5 M LiFSI DME (i), 和1.5 M LiFSI 1,4-DX (j)中五个溶剂团的比例和氧化电位。在电解液中存在的团簇的最小氧化电位被红色的虚线框住。
尽管溶剂的电化学稳定性可以通过键的设计来实现,但电池中的强化效果将受到实际电解液环境的高度影响。由于Li+离子和阴离子的极化作用,电解液的电位窗口在还原和氧化极限上都被缩小了。更确切地说,当与Li+配位时,溶剂的还原电位会增加,而溶剂的氧化反应则通过附近的阴离子而得到促进。有必要研究典型的以Li为中心和以溶剂为中心的团簇结构,并评估它们在电解液中的氧化还原行为。Li+-溶剂(图6a)和Li+-阴离子(图6b)的RDF表明,即使在低浓度下,阴离子也比硅氧烷更容易进入Li+主溶剂化鞘,RDF的整体结果证明了这一点。在1.5M LiFSI DMMS中,Li+溶剂化结构从高到低依次为3-1(即三个FSI-和一个DMMS)(33.59%)、2-2(24.22%)和4-1(19.14%)(图6c)。这种富含阴离子的Li+溶剂化鞘有利于形成有利的富含F、O的界面,防止溶剂分解。
如图6d所示,LMA的CE随着初级Li+溶剂化鞘中阴离子配位数的增加而增加。随着盐浓度的增加,LiFSI/DMMS电解液中的主要溶剂化构型比例没有明显变化(图6e)。拉曼光谱进一步证实了这一观察(图6f)。750 cm-1左右的峰被分配给紧密配位的FSI-,高于普通低浓度酯/醚基电解液中松散配位的FSI-。Si-O(~625 cm-1)和FSI-峰位置的变化随着盐浓度的增加而相对较小,这表现在很少的蓝移(小于10 cm-1)。与HCE/LHCE不同的是,由于溶剂分子数量不足,阴离子被动地进入Li+第一溶剂化鞘,在本工作的电解液中,最好的Li+溶剂化结构是由SiO键调节的。
总的来说,受益于Si-O键的设计,溶剂的稳定性得到提高,电解质结构得到优化。以阴离子为中心的锂簇在电解液中占优势,即使在氟化程度较低的条件下也能产生稳定的富锂SEI,同时Si-O键降低了溶剂的HOMO,并进一步巧妙地消除了最脆弱的Sol-A簇的氧化,最大限度地提高了与高电压阴极的兼容性。上述因素的这种紧密协同作用促进了整个电池性能的提高。
【要点总结】
通过合理设计溶剂的功能键,证明了一种可能性,即提高有限的氟源(低盐浓度和无氟溶剂)的氟输送效率,使电池性能更好。Si-O键策略同时有效地解决了C-O键的氧化挑战和C=O键的还原挑战。在分子间相互作用的尺度上,硅氧烷消除了最容易被氧化的Sol-A簇,但产生了大量以阴离子为中心的Li簇。因此,通过阴离子分解和溶剂强化形成了稳定的富含F、O的界面,进一步改善了电解液与活性LMA和高压阴极的兼容性。
通过对所有这三个方面的全面优化,硅氧烷电解液即使在最严酷的条件下也能提高LMB的性能。展示了积极的薄型Li||NCM811(3.5 mAh cm-2, N/P=1.1)和薄Li||LCO(4.5 V, 3 mAh cm-2, N/P=1.3)全电池出色的长循环寿命。1.4 Ah的Li||NCM811软包电池(< 2.5 g Ah-1贫电解液,20 μm超薄Li和> 3.6 mAh cm-2超高阴极负载)已获得成功。
此外,证明了这类电解液在商业石墨||NCM811软包电池中的普遍适用性。这项工作中的键合设计概念为开发可持续和实用的LMB的电解液开辟了一个新的前沿领域。
Eco-friendly electrolytes via robust bond design for high-energy Li-metal batteries
Energy & Environmental Science ( IF 39.714 ) Pub Date : 2022-09-02 , DOI: 10.1039/d2ee01756c
Yiqiang Huang, Ruhong Li, Suting Weng, Haikuo Zhang, Chunnan Zhu, Di Lu, Chuangchao Sun, Xiaoteng Huang, Tao Deng, Liwu Fan, Lixin Chen, Xuefeng Wang, Xiulin Fan
审核编辑 :李倩
-
自研电解液背后的技术逻辑——为什么电解液决定铝电解电容器的寿命与可靠性2026-05-14 399
-
攻克锂电池研发痛点-电解液浸润量化表征2025-07-14 1182
-
锂电池电解液如何影响电池质量?锂电池电解液成分优势是什么?2024-01-11 3042
-
电解液与SEI的关系?电解液对SEI的影响?2023-11-10 1890
-
电解液量对电池性能有什么影响2023-07-13 5252
-
分享一种高性能的FM内置天线解决方案2021-05-26 4102
-
电解液宽温性能的影响因素和宽温电解液研究进展2020-10-21 12965
-
电池电解液和电解质的区别_电池电解液和电解质的两种形态2020-04-16 25720
-
锂电池电解液是什么_锂电池电解液主要成分2020-03-30 50990
-
不易燃电解液在高性能钾电池的应用2020-02-21 3048
-
电解液——锂电池的‘血液’2018-08-07 6097
-
“防燃电解液”推动锂离子电池步入高性能化阶段2017-11-13 1494
-
电解液电容器老化电压与电解液火花电压的关系2013-12-30 4387
-
电解液比重2009-11-16 9488
全部0条评论

快来发表一下你的评论吧 !

