

对电池系统进行可靠阻抗测量的流程总结
电子说
描述
背景介绍
电化学阻抗谱提供了有关电化学氧化还原反应的稳态及其动力学的信息。比如,阻抗是研究电池动力学的一种非常有用的技术,深化对于电池运行期间的扩散过程或电荷转移反应动力学的理解。
二、正文部分
1、成果简介
威斯康星大学密尔沃基分校Qu Deyang等人总结了对电池系统进行可靠阻抗测量的流程,包括电池配置、阻抗测试系统的准备情况、阻抗谱中数据的验证、基于弛豫时间分布的电化学过程的反卷积和阻抗谱的等效电路拟合。该研究以题目为“Probing process kinetics in batteries with electrochemical impedance spectroscopy”的论文发表在国际顶级期刊《Communications Materials》。
2、研究亮点
本文讨论了准确和可重复的电池阻抗测量的关键参数。
3、图文导读
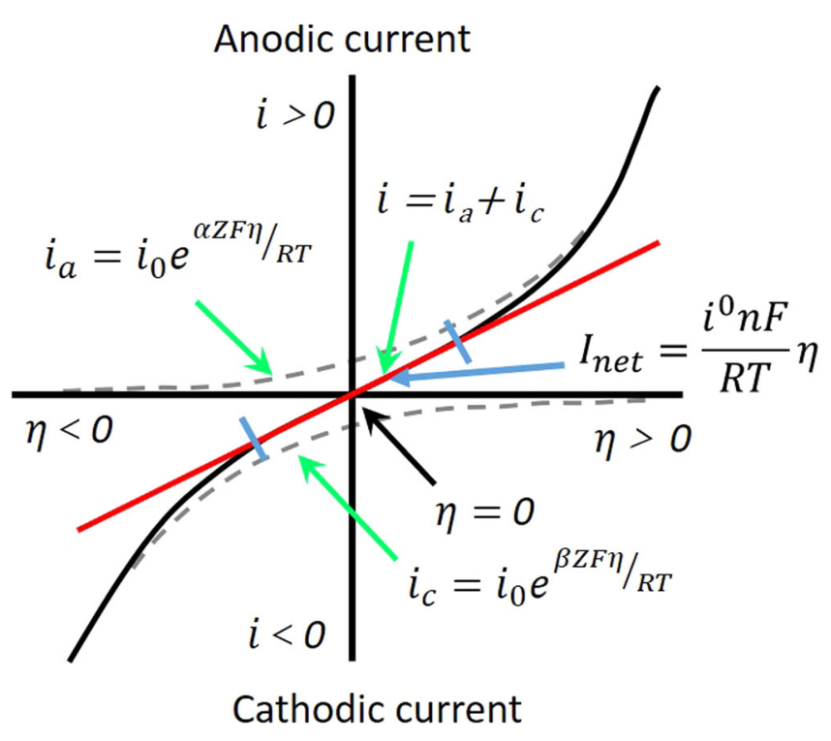
【图1】电化学极化曲线。电化学极化曲线显示了电池电压如何偏离其 OCV,可以将其视为其热力学平衡电压。充电或放电期间电池电压与其OCV的差异是过电位。ia 和 ic 分别是负极和正极电流密度;α 和 β (= 1−α) 分别是负极和正极的电荷转移系数; η 为电荷转移过电位;R 是气体常数,F 是法拉第常数。
对 EIS 的误解之一是它被错误地认为是一种非稳态技术。非稳态实验中的扰动信号大到足以使电化学系统远离其初始稳态。例如,当电池以大电流放电时,电化学系统被极化到远离平衡态的Tafel区。然而,EIS 实验是在稳态下进行的,其中小幅度激发信号叠加在稳态电位上。
由于激发信号的幅度很小,因此电极从未离开过稳态附近。与极化信号将不可避免地对电化学系统造成不可逆变化的非稳态实验不同,在稳态实验中可以避免这种不可逆的改变。电池通常需要很长时间才能达到稳定状态。在进行 EIS 之前,确保弛豫电流(直流电流)远小于激发电流是至关重要的。偶尔向系统施加 10 mV 脉冲(假设激发幅度为 10 mV),记录峰值电流。
当开路电压 (OCV) 下的电流衰减到小于峰值电流的 10% 时,可以对电池进行 EIS。当施加宽频率范围的激发信号时,可以在不偏离初始稳态的情况下获得大范围时间常数的界面过程。因此,EIS 非常适合研究电极稳态附近的动力学参数,因为它桥接了各种时间常数的稳态和瞬态。
因此,在进行阻抗测量之前,应确保电化学系统接近其平衡状态。大多数交流阻抗仪器和相关的数学处理仅适用于线性系统。如图1所示,电化学系统是非线性系统;例如,电极/电解质界面处的电流与电位成指数关系(Tafel 关系)。非线性可以显着地扭曲响应信号,因为它们可以通过在电池响应中产生激发信号的谐波来表现出来。
这种失真可能导致在阻抗结果建模期间对结果的错误表示或误解。接近平衡或稳态(i = 0 mA/cm2)的区域可以被认为是一个线性系统。
如果激发信号不足以将电化学系统极化到 Tafel 区域,则可以安全地假设电化学系统并将其视为线性系统。通常,大多数情况下使用 10 mV 的峰间幅值。 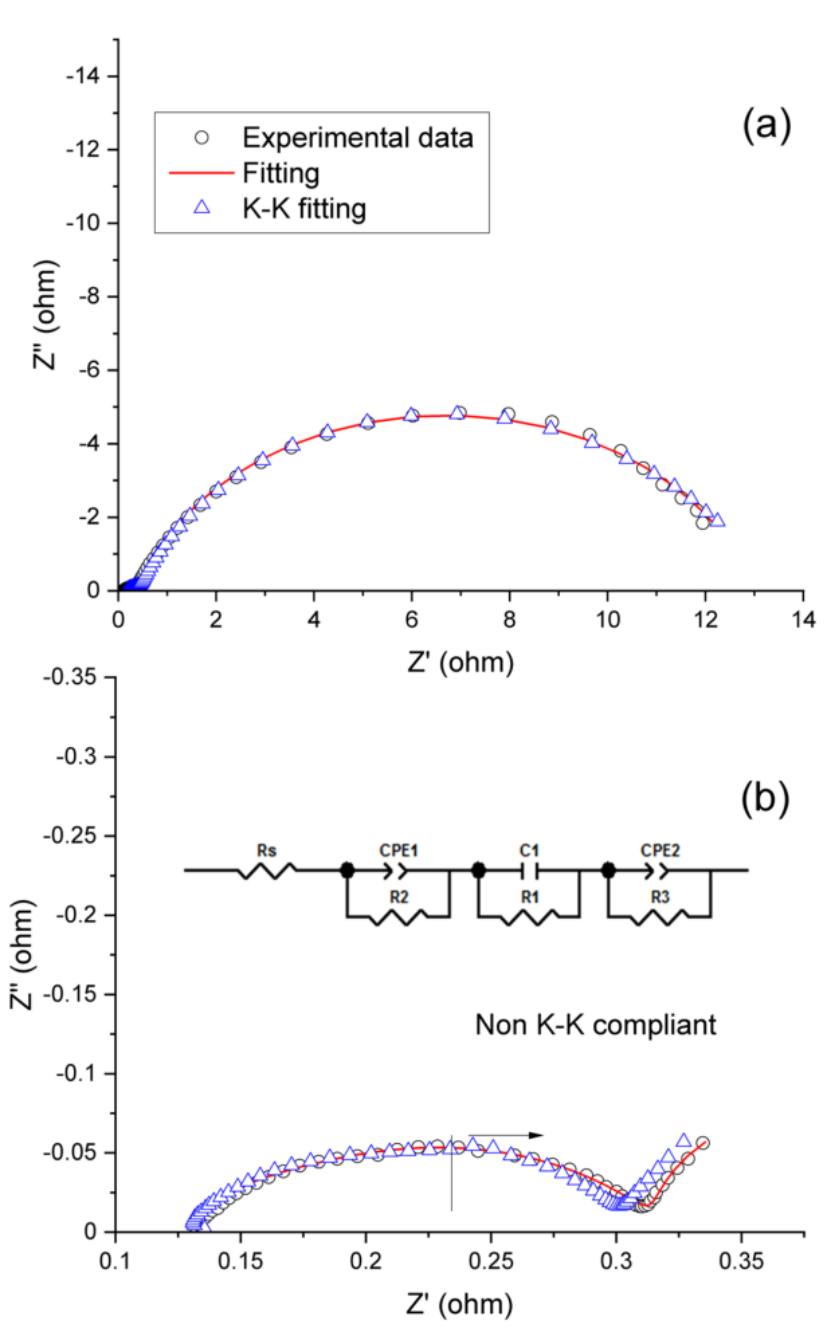
【图2】典型阻抗谱的数值拟合和K-K拟合。需要 K-K (Kramers-Kronig) 合规性来确保电化学系统的线性度。a 符合 K-K 标准;b 不符合 K-K 标准;等效模型用于计算测量频率范围之外的阻抗点。
阻抗谱的测量、解释和模拟是基于电化学系统的线性假设。即使是很小的测量噪声也可能导致不合规性,从而导致对电化学过程的误解和不准确的电化学参数。因果关系、线性、稳定性和有限性用于保证合规性。
Kramers-Kronig (K-K) 关系通常用于证明阻抗数据的合规性。K-K 关系由 Kramers 和 Kronig 提出用于光学分析,然后由 Bode 在电子电路分析中引入。
可以识别不符合要求的数据点并将其从阻抗谱中移除。 图 2 显示了两组阻抗数据的 K-K 验证。用于 K-K 验证的软件是 BioLogic EC-Lab 。图 2a 显示了整个频率范围内符合 K-K 标准的阻抗谱,而图 2b 显示了只有频谱的高频部分符合 K-K标准。图 2b 中低频的不符合 K-K标准的数据点需要从后续的数据建模和计算中排除。
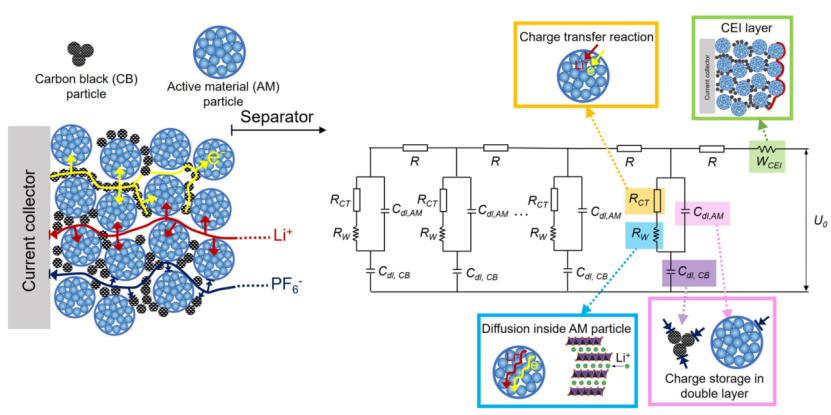
【图3】LIB 正极和传输线等效电路中所有可能的物理和电化学过程以及相应的电化学过程的图示。该图显示了如何在传输线模型中表示物理和电化学过程。例如,活性材料颗粒界面处的电荷转移过程可以用电阻器 (RCT) 表示,Li 在活性材料内部和通过 CEI 的扩散过程可以用 Warburg 电阻器 Rw 和 RCEI 表示。CEI 代表正极上可能的表面界面;Rs为电阻;Cdls 为双层电容,U0 为外加电压。
理想情况下,人们会根据从真实电化学过程(例如 Fick 定律、电化学吸收、Butler-Volmer 关系等)派生的数学分析阻抗数据。然后可以使用理论阻抗函数来提取动力学参数。由于正确分析所需的数学水平,几乎所有的阻抗分析都是使用基于等效电路的硬元件进行的。尽管该方法忽略了 EIS 解释电化学机制和动力学的能力,但它仍然产生了许多有用的信息,特别是对于电极、电池和电池组的实际设计。
即使使用降级或简化的等效电路建模,研究人员有时也打算轻而易举地使用它而没有仔细考虑。等效电路中的等效一词代表电化学过程的等效。没有一种万能的或通用的等效电路。与搭建乐高玩具类似,您需要熟悉每一件乐高积木。构建等效电路,需要对整个电化学过程、这些过程之间的关系(串联或并联)以及每个组件(电阻器、电容器,尤其是 CPE(恒相元件))的物理和电化学意义进行假设。
人们可能会阅读文献,其中在Nyquist图中显示了半圆和斜线。在讨论中,得出的结论是该过程与平行扩散过程具有界面反应。如果没有仔细分析,结论可能会产生误导或根本不充分。让我们研究锂离子电池 (LIB) 正极中的电化学过程以及如何将它们组装到等效电路中。图 3 说明了 LIB 多孔正极中所有可能的电化学过程。与任何电化学电极一样,包括四个基本电化学过程中的三个——电荷转移、双电层和扩散,而电吸附不应用或至少可以忽略不计。
电荷转移过程发生在正极活性材料颗粒和电解质之间的界面处。只要电化学反应保持在平衡状态附近,电荷转移过程就是线性的,如图1所示。因此,该过程可以用电阻器表示,并遵循欧姆定律。
在LIB的多孔正极中,双电层可以在活性材料颗粒和导电碳颗粒的表面上。对于单个活性材料颗粒,电荷转移电阻 RCT 与其双电层电容器并联,而附加碳颗粒上的双层电容器与 R/C 单元并联,如图 3 所示。正极中使用的导电碳是一种微量成分,其表面积较低(<100 m2 g-1),通常忽略导电碳的双电层贡献。
值得强调的是,在发生电化学反应的所有表面上都建立了双电层,因此,双电层电容可用于估计动态电化学可及表面积。 传质可以说是所有电化学过程中最重要和最复杂的。扩散速率决定了活性材料的利用率,在高倍率操作中尤其如此。扩散就像一个信使,在整个多孔电极的基质中传输质量,并将离子移入和移出电极和电解质界面。
在等效电路中使用 Warburg 阻抗来表示扩散过程。Warburg 阻抗可以直接通过求解 Fick 第二定律的偏微分方程得到。
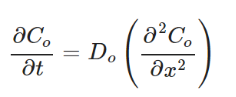
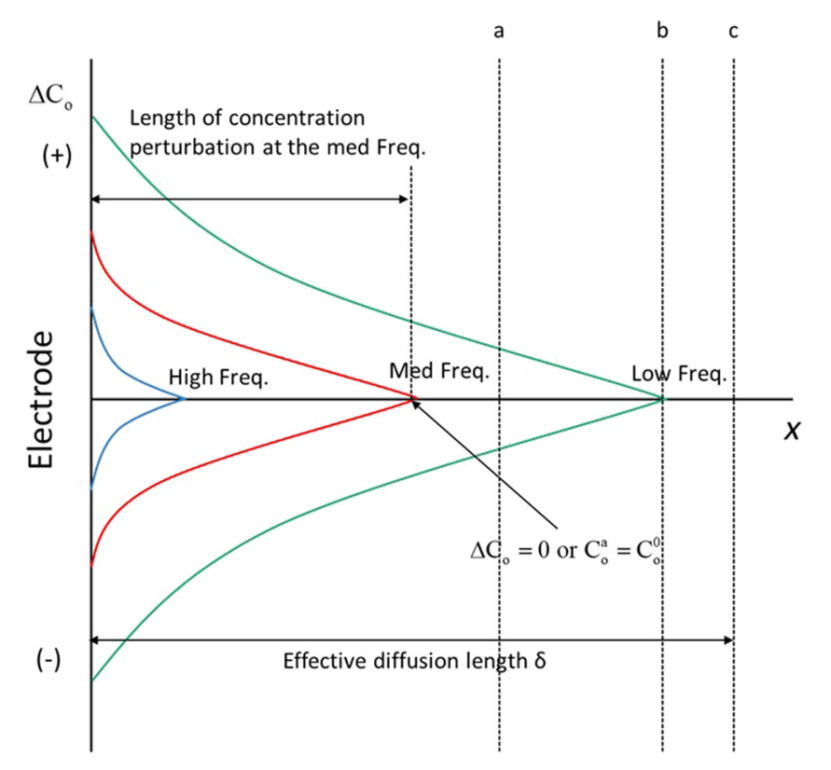
【图4】浓度扰动长度与激发频率。随着激发频率变低,扩散长度变长。由于在低频下,离子在一个方向上扩散的时间更长。ΔC 浓度变化。
在经典的电化学中,包含固体扁平电极的系统浸入充满的电解质中。使用半无限边界条件 (Co(∞,t)=C00) 来求解 Fick 的偏微分方程。半无限假设总是正确的,因为扁平电极上的扩散层长度总是比充满电解液的电化学电池的尺寸小几个数量级。
然而,锂离子正极可能无法满足半无限边界条件,尤其是在低频激发或扰动条件下。图 4 显示了不同频率激发下浓度微扰长度的变化。有效扩散长度 (δ) 代表可用于发生扩散的物理空间。显然,激发频率越高,浓度扰动长度越短。与大量溢流电解质中的扁平电极不同,其中 δ 可以是烧杯电池的大小,多孔正极中的锂离子扩散发生在活性材料的初级粒子中,在薄的 SEI(固体电解质界面)层和多孔电极内的孔隙中。
根据初级粒子的大小、细孔的直径和 SEI 层的厚度,可能不适用半无限条件。假设,如果 SEI 层的厚度约为图 4 所示的“a”长度,则半无限 Warburg 阻抗不应该用于低频区域,但适合用于高频区域。根据我们的经验,“a”情况是电池系统中最常见的情况。
这种情况下的边界条件是在x = δ,ΔC0 = 0。 Warburg 阻抗,无论是半无限的还是无限的,都不能很好地代表分布式多孔扩散矩阵中的扩散,即使没有发生电荷转移或法拉第反应,例如在理想的双层电容器中。Warburg 阻抗仅适用于边界条件用于求解 Fick 第二定律的连续介质。如图 3 所示,由于离子在不同尺寸的孔隙内扩散,在非连续介质中,物理孔隙表面的可及性并不均匀。只有一小部分可用表面,即大孔的表面,可以在高频调制下变得可及。
由于这些细孔中的传质比极化速率慢,因此细孔表面没有发生电化学反应或双电层。同样的问题也适用于厚电极。只有靠近隔膜的电极部分以高速率参与反应,而最靠近集流体的电极部分保持未反应。 Levie 提出的图 5 所示的传输线通常用于模拟非连续和多孔介质的分布现象。
传输线的数学方程与扩散方程具有相似的形式,因为发生在 RC 电路中的过程可以被视为电子扩散到半无限介质中。如图 5b 所示,每个RC 单元包含RCT。RW 和 CDL 代表多孔电极基质中的活性正极表面。
理想情况下,传输线模型中的 RC 单元的数量(n)(模拟发生在总孔表面的 1/n 上的电化学反应)应该是无限的,以代表多孔电极的全貌。每个 RC 单元,即孔隙表面的 1/n,具有不同的时间常数。
换句话说,并不是所有的表面都可以同时被电化学可及。使用图 5 所示的传输线模型,可以估计多孔电极的电化学可及表面积或电化学可及深度。图 5 显示了具有孔隙率梯度设计的厚电极的电化学可及性的模拟。
图 5d 清楚地表明,100% 的电极表面可以在非常低的频率(0.01 Hz)下参与电化学反应。
随着频率的增加,电化学反应所占据的物理表面积(例如,通过N2吸收等温线测量)的百分比会大幅下降。根据作者的经验,只有不到 50% 的电极表面可用于中等频率下厚度约为 200 μm 的电极。 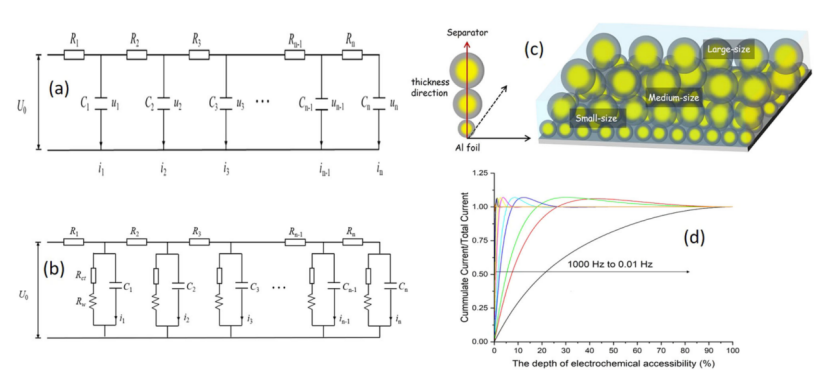
【图5】多孔电极的传输线模型。a 没有电荷转移,b 有电荷转移过程。c 厚电极的孔隙率梯度设计说明和 d 不同频率下的穿透深度估计。该图演示了如何使用传输线等效电路来表示具有不同孔结构和相关电化学可及性深度的多孔电极。
作者在经典电化学中研究了一个特定电极上的电化学过程。正在研究的电极称为工作电极 (WE)。为了确保电化学电池中的所有变化都归因于 WE,通常使用带有参比电极 (RE) 的三电极设置。RE 的组成是恒定的,并且电极在整个实验过程中保持在电化学平衡状态。
不允许有明显的电流通过 RE,否则会发生极化,导致电位偏移。因此,在三电极系统中,人们观察或控制 WE 相对于 RE 的电位。如图 6 所示,极化电流在 WE 和称为对电极(CE)的辅助电极之间流动。在三电极系统中,CE 的电化学特性不会影响工作电极的行为,其唯一目的是促进电流流动。
然而,在电池研究中越来越多地报道了双电极电池。在双电极电池中,两个电极的极化都包含在电化学数据中,例如阻抗谱。除非另有证明,否则不能假设双电极系统的电化学结果可归因于正极或负极。 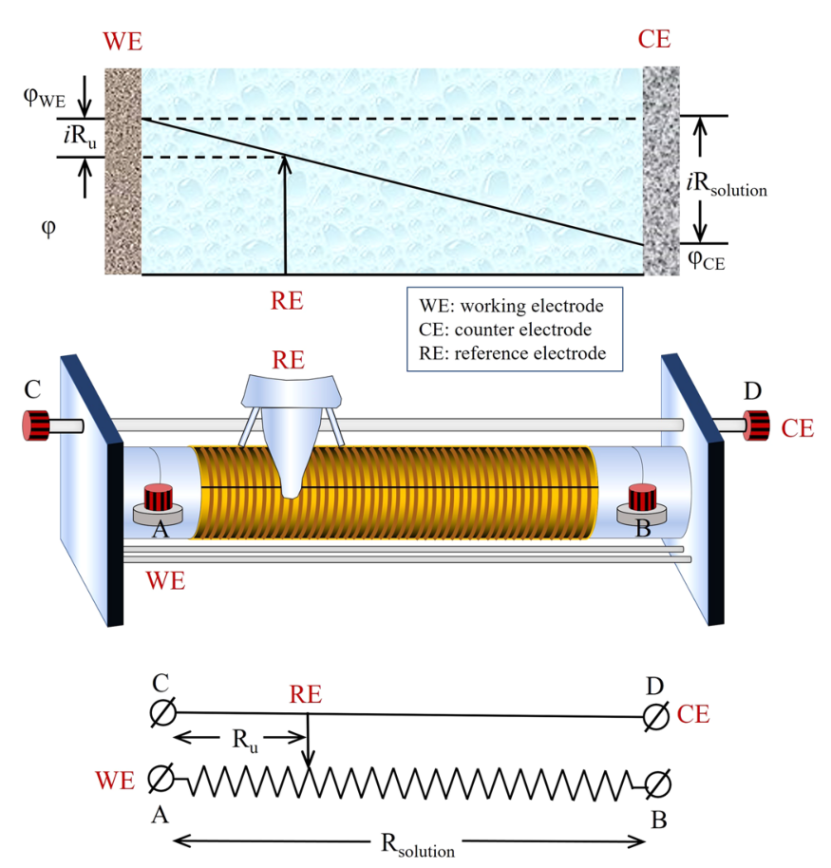
【图6】三电极系统的图示。可变电阻器用于演示工作电极 (WE) 和参考电极 (RE) 之间的 IR 压降。CE为对电极;φWE 和φCE 分别是工作电极和对电极的电位。
尽管参比的使用是一种非常有用的诊断工具,但它是一种破坏性的方法。有时,RE 的使用在技术上具有挑战性,例如,将参比插入到卷筒状电池中。
从理论上讲,RC 单元在时间弛豫空间中连续分布的广义电路可用于表示任何电化学阻抗,而与电化学性质无关。弛豫时间是系统在扰动后恢复到稳定状态所需的时间。因此,弛豫时间越短,反应动力学越好。例如,对于具有较高交换电流的电化学反应,弛豫时间很短。
为了解卷积频域中重叠的极化效应(阻抗谱),可以通过傅里叶变换或拟合到广义电路中,将阻抗谱转换为时域中的时间弛豫分布。在 DRT 分析中,在没有预先假设物理和电化学过程的情况下拟合阻抗。因此,每个过程可以沿着代表相应过程的速率常数的弛豫时间的变化分布。
图 7 显示了相应频域和时域中的物理和电化学过程。DRT 方法在电化学储能研究领域引起了越来越多的关注,因为它能够解开和解卷积在阻抗谱中相互重叠的各种过程的极化。
如果结合参比探针的使用,可以详细研究正极和负极的动力学。图 8 显示了具有宽温电解质的 LIB 与对照电解质的阻抗研究结果。Li 参比电极在面对面的单层软包电池中使用。实现正极vs.参比;负极vs.参比。在形成后、50 次循环后和 100 次循环后测量电池(正极与负极)。
如图 8 所示,阻抗谱中每个物理和电化学过程的速率常数(弛豫时间)和极化电阻(弛豫幅度,相应峰的积分)沿弛豫时间去卷积。图 3 显示了锂离子阴极的完整等效电路。将阻抗谱拟合到完整的等效电路既费时又麻烦。实际上,人们基于有根据的推测构建了一个简化的等效电路;这种方法适用于简单的电化学系统。由于电池系统中使用的多孔电极的分布式特性,重要的电化学过程可能在不同的频率范围内变化。
DRT 可用于识别不同频率范围内的主要电化学过程,方法是对它们进行去卷积以及时间的弛豫。然后可以相应地构建等效电路。 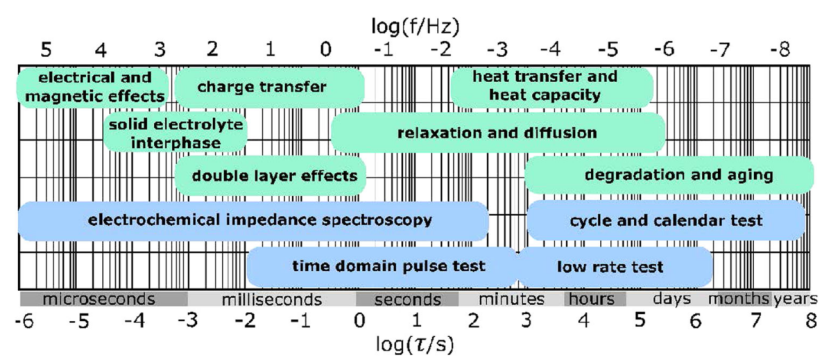
【图7】具有典型特征时间常数范围的电化学系统(绿色)和电池测试方法(蓝色)的动态、频率相关过程。该图显示了电池中各种电化学和物理过程的动力学及其时间常数。电化学技术的种类也被推荐用于不同过程的研究。 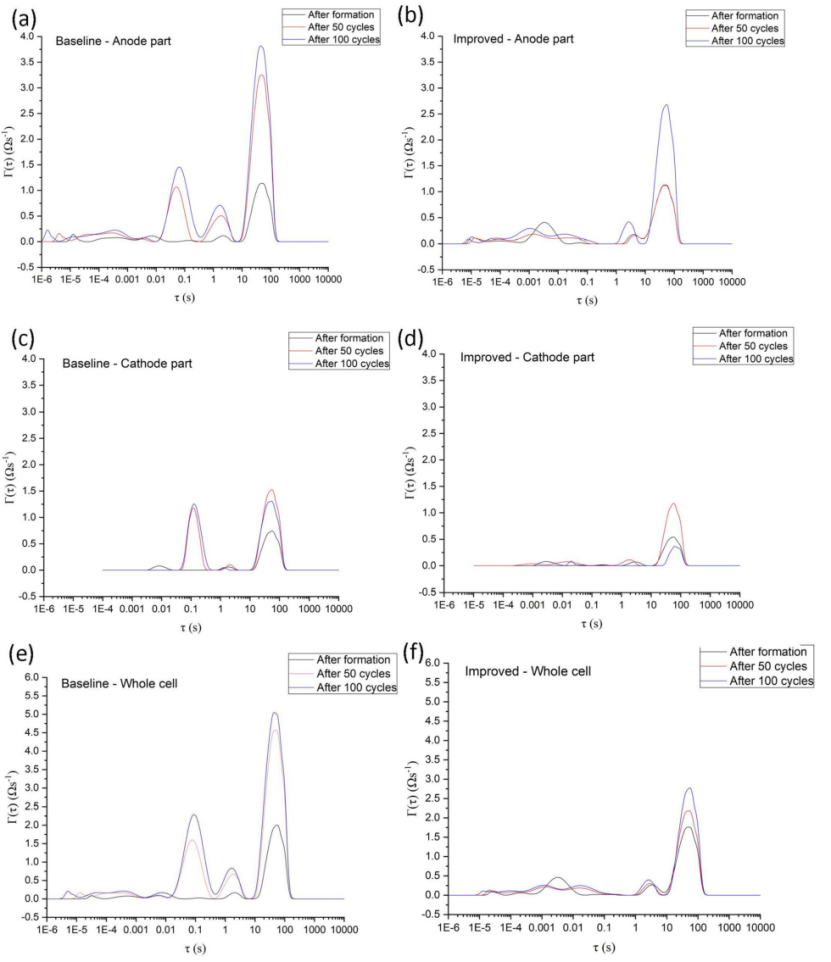
【图8】DRT 在不同的老化状态。a 基准负极,b 改进的负极,c 基准正极,d 改进的正极,e 基准全电池,f 改进的全电池。
固态电池最近引起了很多关注。EIS 的基本原理也适用于所有固态电池。全固态电池的一个独特特征是固态电解质的本质是固态电解质的电荷载流子。
与电极之间的电流由离子物质承载的液体电解质不同,固态电解质中可能存在电子传导性。虽然它很小,但电子导电性会造成潜在的漏电流,这相当于在正极和负极之间连接了一个大电阻。
理论上,电子电导率和离子电导率可以很容易地使用 DC 和 AC 分开。但实验上很难获得可重复的测量结果。
使用精心设计的电化学电池进行简单的交流阻抗测量和拟合可能是有利的。在阻抗测量期间,可以使用离子阻挡或电子阻挡或氧化还原电极。
离子阻挡电极可以是金属,例如 Pt 和 Au 或热解石墨,离子阻挡电极是惰性的,不利于界面处的电荷转移。电子阻挡电极是高离子电导率材料,其电子电导率可忽略不计。
因此,仅测量离子电导率。如果使用氧化还原电极,例如锂金属,则离子电导率和电子电导率都包含在阻抗测量中。
4、总结与展望
EIS 是一种强大的电化学研究技术。它连接了稳态和瞬态,因此可以在放电或充电的不同阶段研究电极的动力学。作者希望它可以正确地最大限度地发挥其潜力,希望本次讨论能为储能领域的研究人员,尤其是非专业电化学工作者提供一个有用的起点。
审核编辑:刘清
-
如何使用Moku进行阻抗测量?2025-01-23 926
-
使用ADC FFT数据进行输入阻抗测量2024-10-18 507
-
电池测试流程和测试方法有哪些2024-09-23 4394
-
如何测量系统的输入输出阻抗2023-01-30 8211
-
共射放大电路输入输出阻抗的测量方法2023-01-10 7838
-
鱼体复阻抗测量系统的设计过程2019-05-16 2169
-
锂电池的等效阻抗及测量方法2018-01-29 12157
-
基于LTC6804的锂离子电池阻抗测量系统设计2017-12-21 11965
-
MAX400 简单电路测量电池阻抗2016-08-18 799
-
电池研发流程总结2012-11-23 10120
-
基于交流阻抗法的蓄电池内阻测量2011-08-25 2111
-
MAX471 简单电路测量电池阻抗2010-07-26 1246
-
开路电压及交流阻抗测量系统2009-06-06 1428
全部0条评论

快来发表一下你的评论吧 !

