

乳腺癌微环境的时间分析揭示胶原蛋白XII是肿瘤转移的驱动因素
描述
肿瘤基质,特别是细胞外基质(ECM),是实体肿瘤的一个显著特征,在肿瘤发展中起着至关重要的作用。许多促结缔组织增生性肿瘤,包括乳腺癌,都涉及I型胶原的显著积聚,并且I型胶原分子的分布和结构与其丰度在肿瘤中同等重要。此外,癌相关成纤维细胞(CAF)存在于乳腺癌组织中,通过重塑ECM发挥促肿瘤和抗肿瘤作用。
本文中,为了研究上述三者与乳腺癌发展的关系,研究者利用质谱技术检测ECM中的蛋白质组,发现了在肿瘤中显著上调的胶原蛋白XII,可调节I型胶原纤维,促进癌细胞侵袭和转移,并结合单细胞转录组测序确认CAF是胶原蛋白XII的主要来源。
研究路线
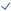
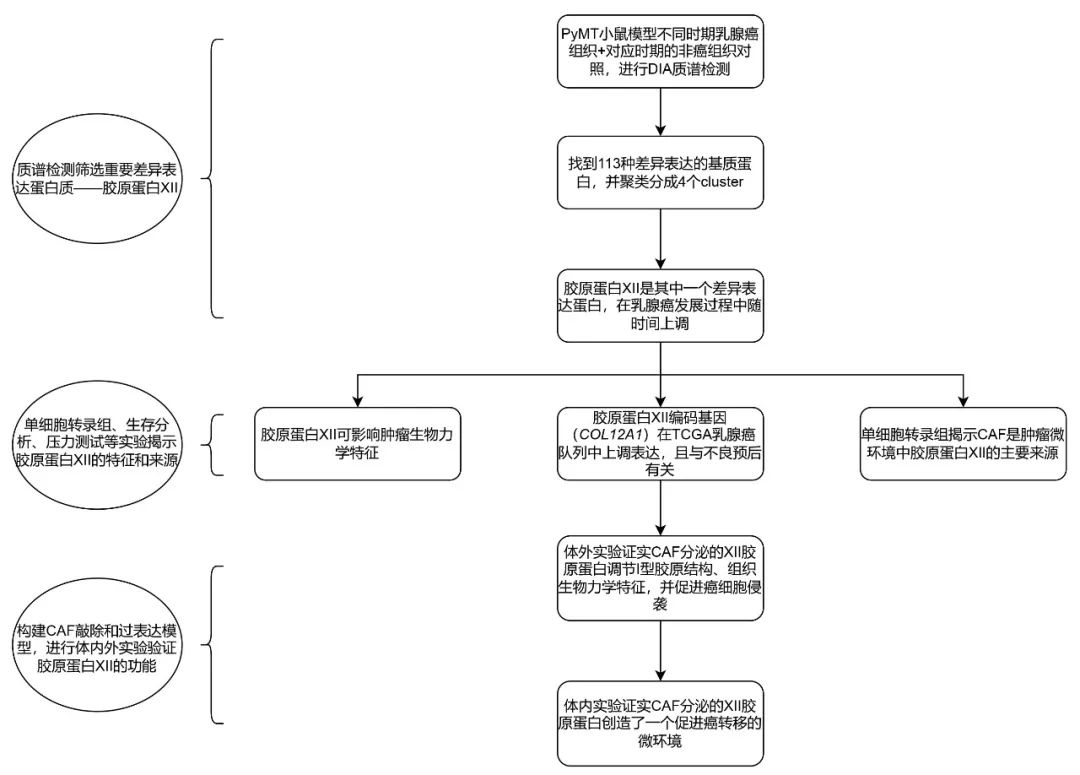
研究内容
肿瘤基质蛋白质组的动态变化
随着实体肿瘤生长,ECM的持续重塑导致正常组织基质被肿瘤基质取代,这种重塑在肿瘤进展中起着重要作用。研究者使用自发且多发性肿瘤中期(PyMT)基因工程小鼠模型(GEMM),收集早期(增生期)、中期(腺瘤)和晚期(转移性腺癌)的乳腺癌组织和相同年龄健康小鼠的乳腺脂肪垫组织,来研究乳腺癌发生过程中ECM随时间的变化。
对组织进行脱细胞操作以富集ECM蛋白质,然后进行DIA质谱检测蛋白质组,在脂肪垫和肿瘤中定量到150种基质蛋白,其中113种在肿瘤和健康脂肪垫中差异表达。这里面有71种属于核心基质蛋白,42种与基质相关,包括分泌因子、ECM相关蛋白和ECM调节剂。
通过聚类分析发现了四个具有不同时间表达特征的离散clusters。C1中的蛋白质在健康组织中随时间逐渐上调,但在肿瘤中表达更高,并随肿瘤发展进一步增加。C2中的蛋白质在肿瘤三个阶段与健康脂肪垫相比均上调,C3中蛋白质则随着疾病发展逐渐下调,C4则在早期中期下调而晚期上调。
C2中的SPP1可将乳腺成纤维细胞激活成促肿瘤的癌相关成纤维细胞(CAF),C3中的DCN在晚期肿瘤中下调且具有抗增殖和抗转移的特性,TNXB在三个阶段均下调且有报道称该蛋白在多种实体瘤中下调且与较差的生存率相关。C4中具有肿瘤抑制作用的TINAGL1下调。这些结果强调了关键的ECM分子是如何在原发性乳腺癌进展中发挥重要作用,从促进肿瘤细胞增殖和侵入基质、向脉管系统迁移、血管内和血管中的传播并导致转移性疾病。
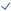
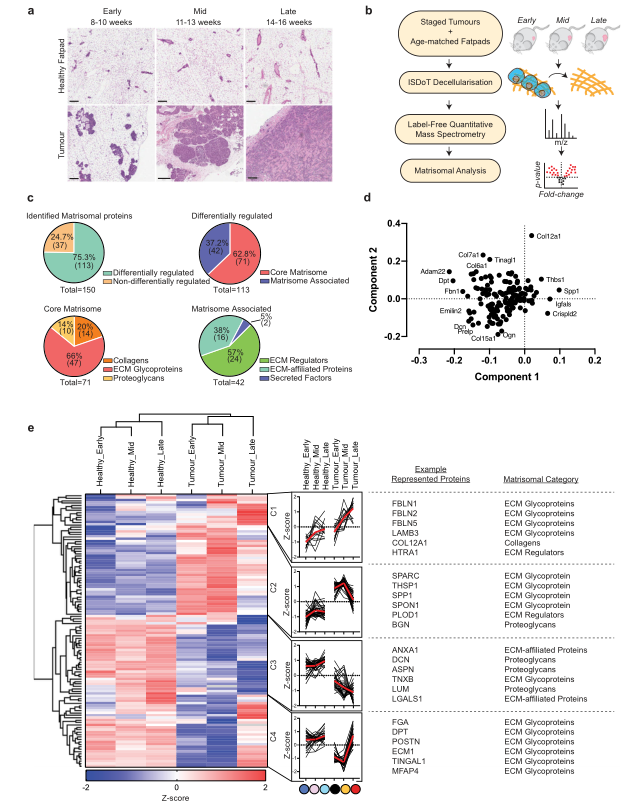
Fig.1 脱细胞乳腺癌蛋白质组图谱揭示基质体的动态变化
胶原蛋白 XII 在乳腺癌发展过程中随时间上调
比较健康脂肪垫和肿瘤的基质蛋白质组结果后发现了很多差异表达的ECM蛋白。其中,胶原蛋白XII(COL12A1)在所有时期的肿瘤基质中,与健康脂肪垫相比,均显著上调表达,且随着肿瘤发展,其表达逐渐上调。免疫组化(IHC)验证发现胶原蛋白XII主要定位于基质区,表达变化趋势与蛋白质组结果一致,证实了该蛋白作为关键基质支架蛋白的作用。已有报道表明胶原蛋白XII是正常组织中纤维状胶原结构的调节剂,并且与肿瘤侵袭性相关。
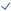
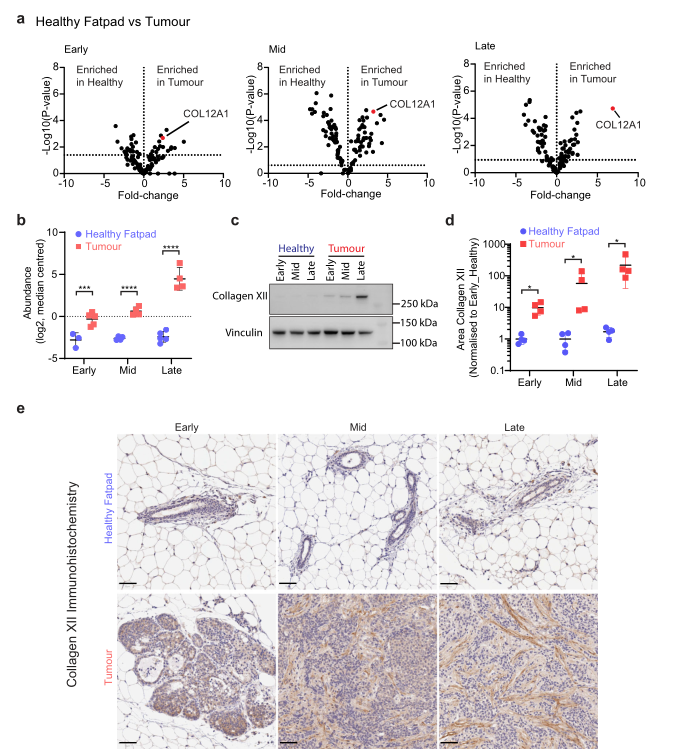
Fig.2 随着疾病的进展,XII胶原蛋白在乳腺癌中表达上调
胶原蛋白 XII 表达与肿瘤生物力学特性改变有关
为了评估胶原蛋白XII在原发性肿瘤进展中的潜在作用,研究者对胶原蛋白I/XII的空间组织和肿瘤生物力学进行了研究(胶原蛋白XII可与I结合发挥调节功能)。利用天狼星红对组织中的纤维状胶原蛋白染色和IHC切片分析发现在肿瘤进展过程中,总胶原蛋白与 XII 胶原蛋白一起增加。
无测限压力测试分析测量肿瘤的生物力学特性发现肿瘤硬度(体积弹性模量)在疾病的晚期显著增加,与质谱测得的XII胶原蛋白丰度增加相关。基于I型胶原纤维的非中心对称性质,使用二次谐波发生(SHG)多光子成像技术对I型胶原进行无标记成像和量化。结果表明,I型胶原纤维密度在肿瘤发展的晚期上调,I型胶原纤维束尺寸的量化显示,随着肿瘤的进展,I型胶原束宽度增加。
随着肿瘤从早期进展到中期和晚期,I型胶原纤维的线性度增加。这些数据证实了原发肿瘤进展过程中I型胶原纤维组织的广泛重构。
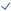
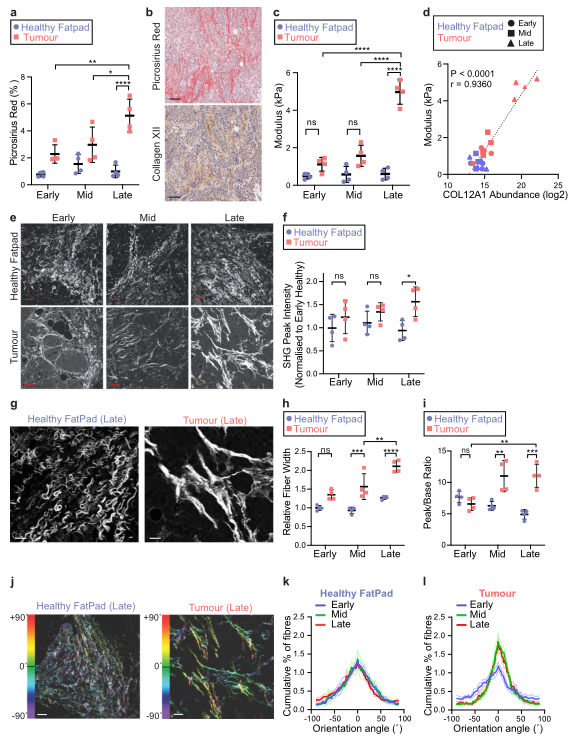
Fig.3 XII胶原蛋白丰度与纤维状胶原结构改变和肿瘤硬度相关
XII胶原蛋白在乳腺癌中表达上调,与不良预后有关
研究者使用TCGA数据库乳腺癌队列(BRCA)的RNA测序结果中XII胶原蛋白基因(COL12A1)表达数据进行预后研究,发现与非肿瘤组织相比,该基因在包括TNBC在内的所有原发乳腺癌组织中显著上调。XII型胶原的高表达与总体存活率低(OS)和不良的无进展生存期(PFS)显著相关。
多变量分析表明胶原蛋白XII的表达与肿瘤早期的进展更密切相关。为了证实上述发现,研究者对150名患者组织的胶原蛋白XII进行IHC分析,证实该蛋白高水平与疾病特异的存活率差显著相关,并且患者的远端复发率也更高。上述结果表明,XII胶原蛋白的表达与早期患者预后和复发密切相关,值得进一步研究以确定其作为侵袭性转移疾病生物标志物的潜力。
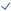
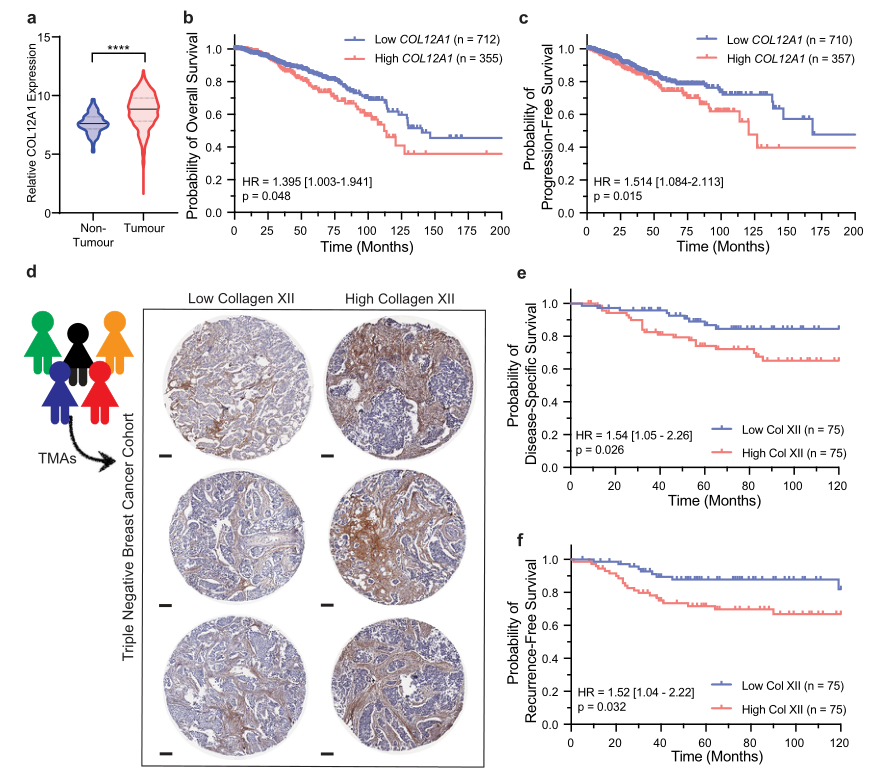
Fig.4 XII胶原蛋白表达与乳腺癌预后不良相关
单细胞转录组揭示CAF提供了肿瘤微环境中的胶原蛋白XII
为了确认原发肿瘤微环境(TME)中胶原蛋白XII的来源,研究者从体内模型中收集5个原发晚期肿瘤组织进行单细胞RNA测序,证实了XII胶原蛋白编码基因Col12a1在CAF的分泌基质亚型高表达,在另一个26名乳腺癌患者队列的单细胞转录组结果中也发现XII胶原蛋白的主要来源是CAF。
接下来,研究者利用该患者队列单细胞测序结果中CAF marker基因,对TCGA队列每个乳腺癌数据集计算了CAF分数,发现COL12A1的表达与CAF分数呈显著正相关,进一步证实了CAF是乳腺肿瘤中COL12A1的主要来源。但是分析还发现,胶原蛋白XII表达但没有CAF分数也与总体和无进展的存活率显著相关,将CAF分数添加到XII胶原蛋白生存模型中并不能显著改善该模型,说明XII胶原蛋白的表达是这些患者预后的预测指标,与CAF分数无关。
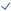
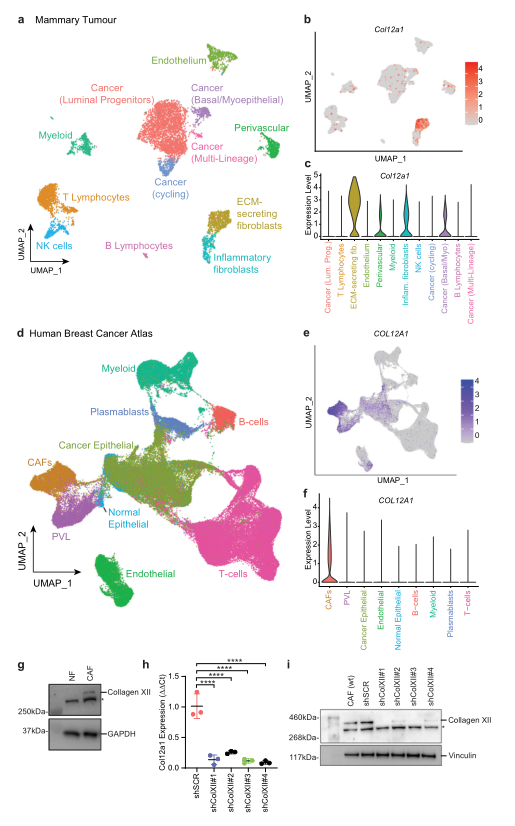
Fig.5 小鼠和人乳腺癌中的CAF产生XII胶原蛋白
CAF分泌的XII胶原蛋白调节I型胶原结构、组织生物力学和癌细胞侵袭
研究者分析了从原发PyMT肿瘤中分离出的CAF和肿瘤细胞后发现,与正常小鼠乳腺成纤维细胞相比,这些CAF中的XII胶原蛋白表达上调,与单细胞转录组结果一致。从CAF细胞中敲除COL12A1并做了大量实验发现,下调XII胶原蛋白的表达不会改变纤维胶原的总丰度,但会改变纤维胶原的超微结构,XII胶原蛋白在决定I型胶原纤维的空间组织结构中发挥了作用,并且CAF中XII胶原蛋白的枯竭可能起到了使基质正常化的作用。
此外,XII胶原蛋白敲除没有改变CAF收缩I型胶原器官型基质的能力,而无限制压力分析器官型基质的生物力学特征,揭示CAF中XII胶原蛋白的耗竭导致整体基质的硬度下降。XII胶原蛋白的敲除导致较薄的胶原束丰富程度较高,由于XII型胶原支架支撑着I型胶原的结合,这与XII型胶原已知的功能(即调节健康组织中I型胶原构型)是一致的。
最后,在CAF重塑的器官型基质里,先去除CAF后将PyMT癌细胞接种进去。结果表明癌细胞很容易侵袭到shScr-CAF(敲除模型的对照)重塑的基质中,但这种能力在敲除的CAF重塑基质中显著降低,证实胶原蛋白 XII 对胶原蛋白 I 的调节,在原发性乳腺癌中产生促侵袭性微环境的重要作用。
利用Crisper激活构建胶原蛋白XII过表达的CAF细胞系,研究者发现CAF过表达XII胶原蛋白并不影响胶原重塑的速度,但确实显著增加了CAF重塑的器官型基质的硬度和成熟的束状胶原纤维的比例,并且显著增加了PyMT癌细胞的侵袭性。这些结果表明,在CAF中增加XII胶原蛋白的表达与XII胶原蛋白的敲除具有相反的作用,并证实了XII胶原蛋白在调节肿瘤微环境中的纤维胶原结构和基质生物力学以及随后的乳腺癌细胞侵袭中具有重要的作用。
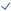
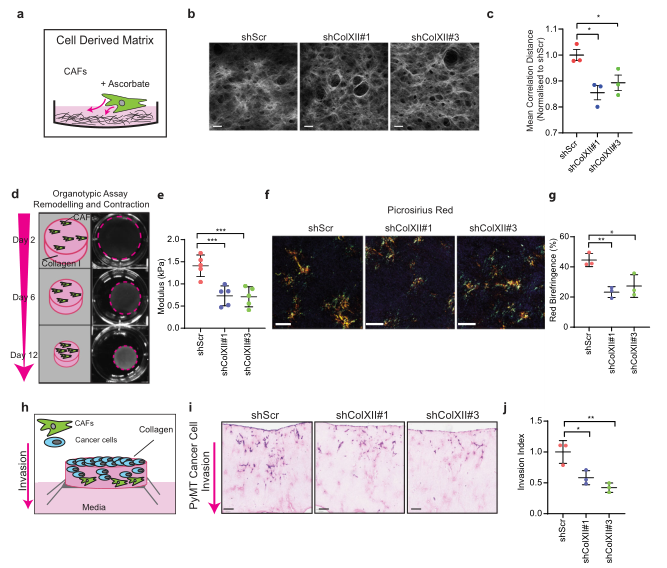
Fig.6 XII胶原蛋白基因敲除调控原纤维胶原结构并抑制癌细胞侵袭
Fig.7 XII胶原蛋白过表达增强肿瘤硬度和癌细胞侵袭
CAF分泌的XII胶原蛋白创造了一个促进癌转移的微环境
为了研究CAF分泌的XII胶原蛋白的作用,研究者将癌细胞与shScr、敲除后的CAF(癌细胞与CAF的比例为1:3)原位共植入第四乳房脂肪垫,并让肿瘤最大成长到520mm3。研究发现对照和敲除组的肿瘤到达最大体积的时间和肿瘤重量没有显著差异,但肿瘤硬度在敲除组里显著下降。肺组织切片观察癌转移发现对照组100%转移,而敲除组约50%左右转移,说明XII胶原蛋白在调节基质组织(可促进肿瘤细胞转移扩散)中起着关键作用。
研究者还证实在敲除组肿瘤中较低的XII胶原蛋白水平降低,但两组的CAF细胞量没有差异。此外,I型胶原束厚度显著减少,这与观察到的肿瘤硬度降低相关。敲除组肿瘤中pMLC2(有研究指出pMLC2可激活肿瘤成纤维细胞并放大基质重塑,导致肿瘤硬度增加和促进肿瘤细胞侵袭的微环境产生)水平显著低于对照组,癌细胞的转移潜力也降低。
这些结果表明,CAF中的XII胶原蛋白缺失会导致正在发展的肿瘤内I型胶原束和肿瘤硬度改变,这可能导致基质总体激活水平较低,并破坏允许癌细胞侵袭的微环境。利用XII胶原蛋白过表达CAF进行与上述敲除组类似的实验进一步证实XII胶原蛋白表达在转移扩散中的重要作用。
总之,在体外和体内,这些互补的敲除和过表达模型实验结果支持这样的假设,即CAF在原发部位分泌的胶原蛋白XII调节I型胶原的结构和肿瘤的生物力学特性,从而创造了允许癌转移的肿瘤微环境。
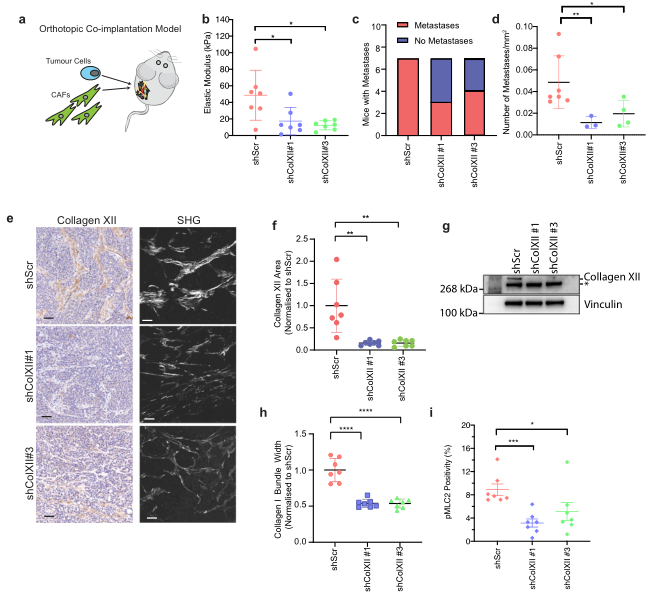
Fig.8 XII胶原蛋白基因敲除在体内减少癌转移
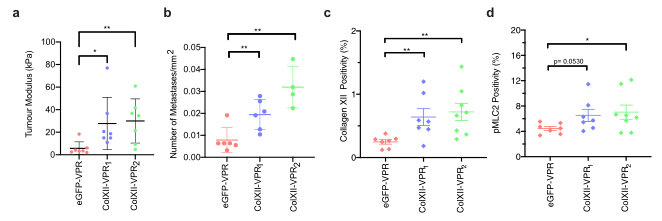
Fig.9 XII胶原蛋白过表达在体内促进癌转移
结果总结
本研究利用质谱技术描绘了脱细胞肿瘤随时间变化的蛋白质组图谱,揭示了乳腺癌发展过程中基质体的演变情况。研究者确定了四个关键的基质蛋白clusters,并明确指出XII胶原蛋白是调节I形胶原组织的关键成分。
通过将蛋白质组学和单细胞转录组数据联合分析,并使用遗传操作模型,研究者展示了由CAF分泌的XII胶原蛋白是如何改变I型胶原组织,以创造支持转移扩散的促侵袭微环境。此外,在TCGA的患者队列中,研究者发现XII胶原蛋白可能代表了乳腺癌患者转移复发的高风险指标。
审核编辑:刘清
-
基于逻辑回归算法的乳腺癌肿瘤二分类预测2019-06-18 3491
-
基于kNN算法可以诊断乳腺癌2019-06-21 2121
-
基于AMC7150的乳腺癌诊断系统设计_张云2017-03-19 985
-
HE染色乳腺癌组织病理图像分析2017-11-22 3883
-
英特尔携手汇医慧影,利用AI技术检查乳腺癌2018-09-30 1834
-
乳腺钼靶AI落地临床,乳腺癌患者的福音2018-10-19 3652
-
AI新闻:训练AI检测乳腺癌2018-11-05 2911
-
MIT研究员最新AI模型可提前5年预测乳腺癌风险!2019-05-11 5305
-
谷歌人工智能模型乳腺癌识别还存在什么没有完善的2020-01-03 1190
-
人工智能乳腺癌诊断能力精确 在防控乳腺癌的长期战斗中取得突破2020-01-07 1028
-
复旦肿瘤医院与华米联手研究:可穿戴设备可促进乳腺癌康复2020-11-03 2154
-
乳腺癌-冠心病标志物的生物信息筛选技术2021-04-30 926
-
使用Movidius和UP2进行乳腺癌分类2023-06-13 815
-
利用微流控技术模拟骨仿生微环境促进乳腺癌进展机理研究2023-07-11 1830
-
MedCognetics利用AMD平台优化乳腺癌检测2025-11-02 881
全部0条评论

快来发表一下你的评论吧 !

