

CRISPR诊断技术在不同领域的优势
描述
近日,来自西南大学前沿交叉学科研究院生物学研究中心的夏庆友教授、林平研究员与陆军军医大学陆军特色医学中心蒋建新院士、吴敏研究员合作在期刊Trends in Biotechnology上发表了题为“CRISPR-Cas-mediated diagnostics”的前瞻性综述论文,全面系统总结了基于CRISPR-Cas技术的体外分子诊断研究取得的最新进展,详细归纳了CRISPR诊断技术在不同领域的优势,讨论了CRISPR-Cas技术在未来临床诊断中面临的重大挑战和问题及解决措施,并提出了“以实现CRISPR诊断技术自动化和一体化为纽带联系病患和医院构建诊疗网络”这一前瞻性策略。
CRISPR-Cas系统是细菌和古细菌内类人体免疫防御系统,靶向切割外源遗传物质(DNA或RNA),实现抵抗外源病毒入侵。利用这一特点,将CRISPR-Cas系统开发为一种简单、快速、经济有效和精确的基因编辑技术,使基因诊断、病原防御和疾病治疗发生了革命性的变化。
传统诊断技术难以满足需求
传统PCR检测技术是诊断各种传染性疾病的主要手段。然而,以新型冠状病毒(SARS-CoV-2)引发的新冠肺炎为例,基于PCR检测技术的花费的时间为4-6小时,且检测成本昂贵,依赖大型设备,使得在偏远地区的医疗点难以开展检测工作,同时存在感染早期呈现假阴性的等问题。基于抗原-抗体反应的检测方法,如免疫荧光法、ELISA、免疫组化等技术,检测呼吸道分泌物中的SARS-CoV-2抗原或血清抗体,同样是SARS-CoV-2感染诊断或治疗监测的辅助手段。但是免疫学检测抗原或抗体存在交叉反应、检测窗口期较长、假阳性率高等许多缺陷。在新冠疫情仍然全球大流行的背景下,如何有效快速诊断新型冠状病毒感染者,降低传染率和死亡率是目前亟待解决的问题。基于CRISPR-Cas系统的新一代基因编辑技术以其快速、便携、经济、高效的特点,为SARS-CoV-2的快速分子诊断提供了解决方案,可实现及早地追踪和隔离被感染者,快速阻断病毒传播。论文对基于以CRISPR-Cas为基础的新兴诊断技术为病原微生物感染、癌症等早期预防、分子诊断与治疗监测的研究及其最新成果进行简述。
CRISPR诊断技术的独特优势和不足
CRISPR-Cas系统由gRNA和Cas蛋白组成,现已经建立了基于Cas效应器(Cas9、Cas12、Cas13)的分子诊断体系(图1)。主要通过采用等温扩增技术扩增病原体的核酸序列,从而使CRISPR诊断方法的检测速度超过传统PCR,而且不依赖于样本转运、人员和大型PCR设备。CRISPR蛋白复合物对目标序列的准确识别确保了CRISPR系统的高灵敏度;随后通过工具酶(例如Csm6)放大检测信号、串联使用gRNA以及引入微流控系统,将CRISPR系统的灵敏度提升至与PCR相似的水平。此外,CRISPR检测方法本质上是试剂和样品在一般条件下的混合反应,使得CRISPR诊断技术具备快速、灵敏、廉价、便携、易操作的五大优势。
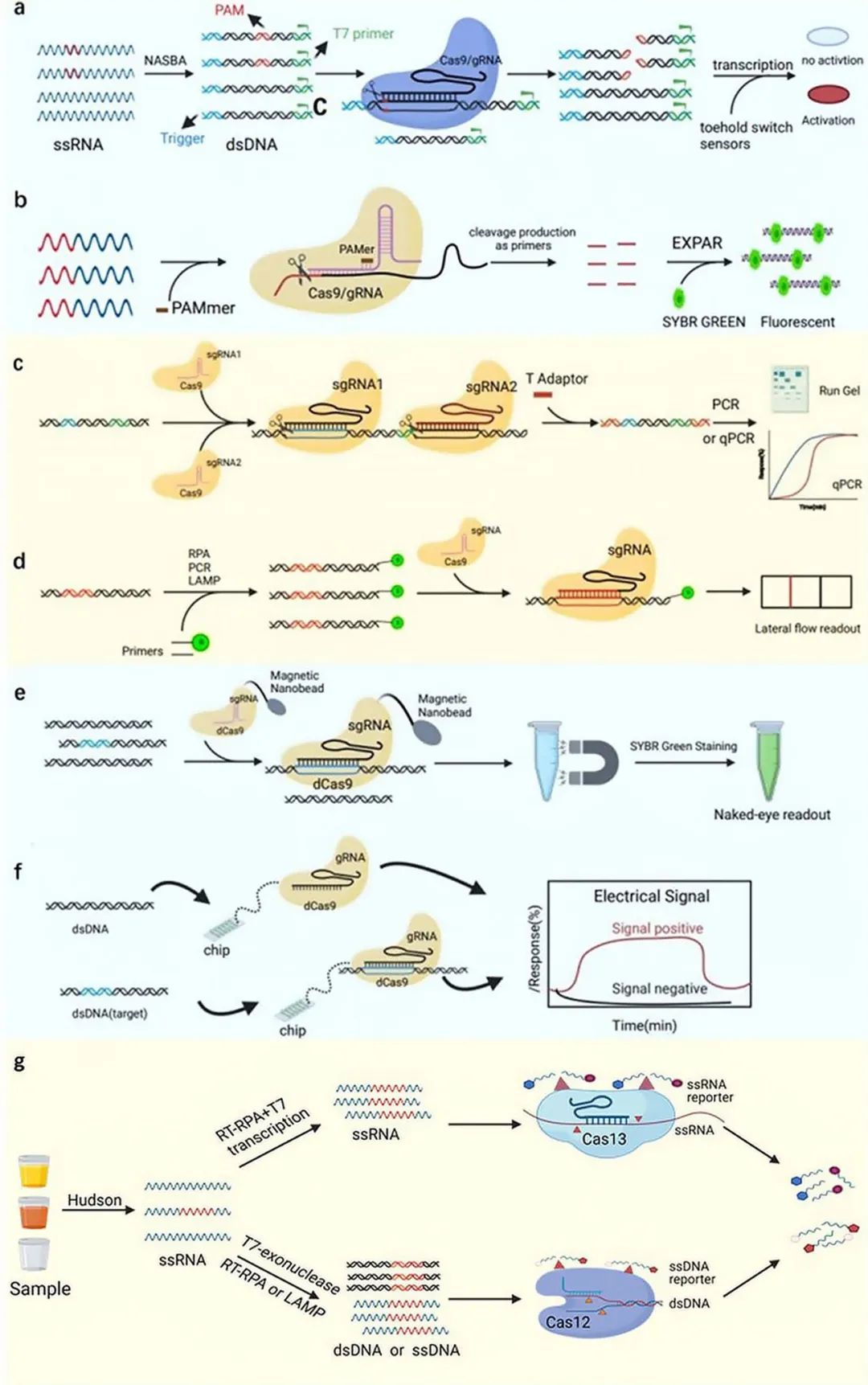
图1 CRISPR诊断技术的流程图:主要由样本处理、预扩增、CRISPR检测和结果读数四部分组成
目前,Cas9蛋白介导的基因编辑技术研究最为成熟,容易与其他技术进行结合。Cas9介导的诊断体系主要是将Cas9蛋白作为一个检测探头与其他新兴技术结合来提高检测灵敏度或者衍生出检测速度更快、成本更低的新方法,包括CAS-EXPAR技术、NASBACC技术、Cas9nAR、CASLFA等。而Cas12和Cas13蛋白利用靶向结合切割目标核酸的活性,同时附带激活旁切活性(即非特异性切割DNA或RNA的酶切活性)。旁切活性能切割引入的核酸报告分子产生检测信号,使CRISPR蛋白作为检测体系的核心组件。论文总结了三种主要诊断体系的优势、局限以及适用范围(表1)。
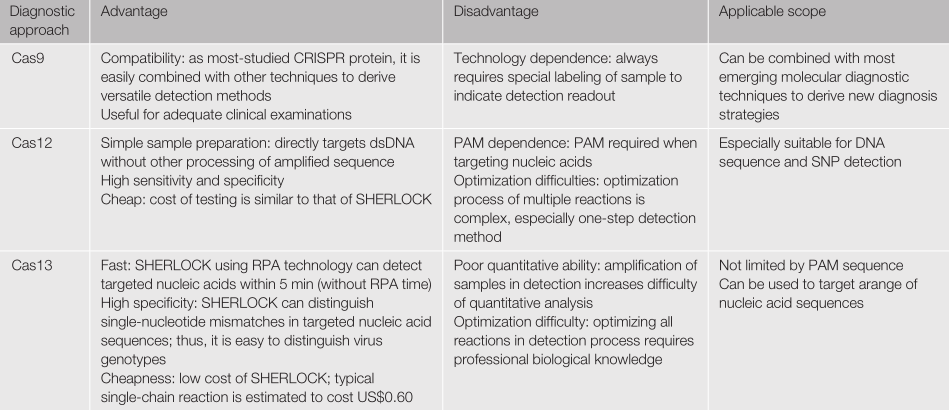
表1 CRISPR-Cas系统介导的分子诊断技术的优势与不足
CRISPR系统给分子诊断带来的革新
(1)核酸检测
论文具体论述了各种CRISPR核酸技术(图1)、阐述了基于CRISPR-Cas9系统的特异靶向DNA序列介导的检测技术和基于CRISPR-Cas12/Cas13系统介导的旁切活性的检测技术的原理、检测性能、临床应用情况。并且将针对特定病原体的CRISPR核酸检测技术与PCR技术进行比较,从检测周期、检测性能、检测成本、应用前景等方面对CRISPR技术进行综合评估。基于Cas12、Cas13的核酸检测技术更是将检测时间缩短到1h以内,检测成本最低可达到0.6美元/次。
同时,检测体系的预扩增策略和读数方式在近几年不断得到改进。扩增方式从RPA转变为效率更高、特异性更强的LAMP方法。读数方式由单一的显微镜读取荧光信号到测流层析试纸读数、比色法读数、智能反应材料读数等(图2)。除此之外,微流控技术的引入也使多路复用的诊断策略得以实现。CARMEN-Cas13凭借微流控技术实现了在同一样本中同时检测169种病毒(图3A)。这些新技术的引入使得CRIPSR技术的优势能在核酸诊断领域更好的发挥。
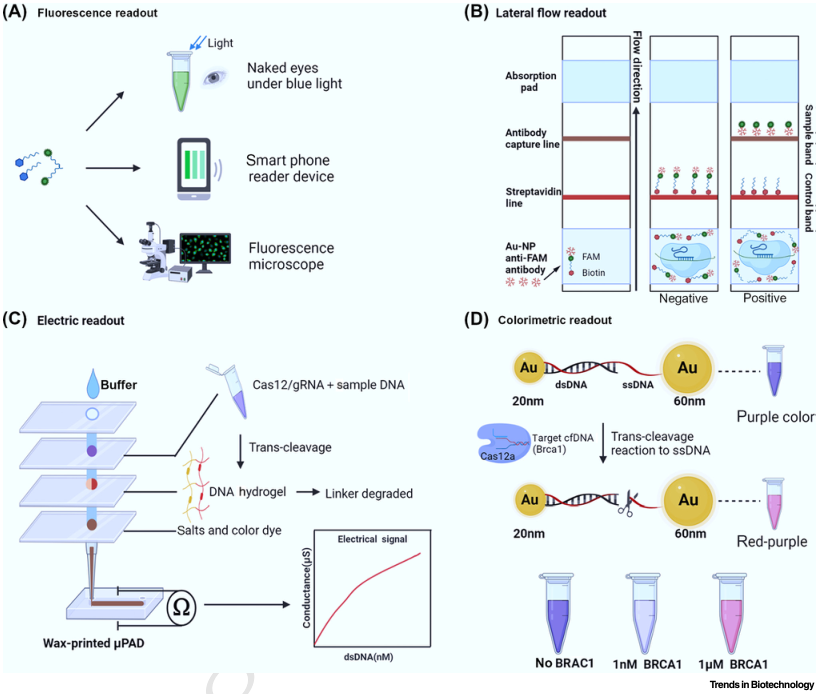
图2 新兴的读数方法
(2)抗体诊断试验
最近通过Cas9介导的自动组织技术(Cas9-mediated self-organization technology,PICASSO)开发了新的蛋白质微阵列构建方法。PICASSO将定制的多肽库与dCas9蛋白融合表达,然后用单引导(Sg)RNA标记融合蛋白。融合蛋白可以自动组装在包含数千个目标DNA的DNA微阵列上,以此构建蛋白质微阵列(图3B)。这意味着特定的位置对应于特定的DNA和融合蛋白,这使研究人员能够快速识别临床样本中的抗体或大规模研究各种感兴趣的蛋白质。与传统的蛋白质筛选工具相比,如噬菌体和核糖体展示,PICASSO可以实现蛋白质表达水平标准化以及蛋白结合可视化,这可以提高文库筛选的代表性并且避免扩增偏差。
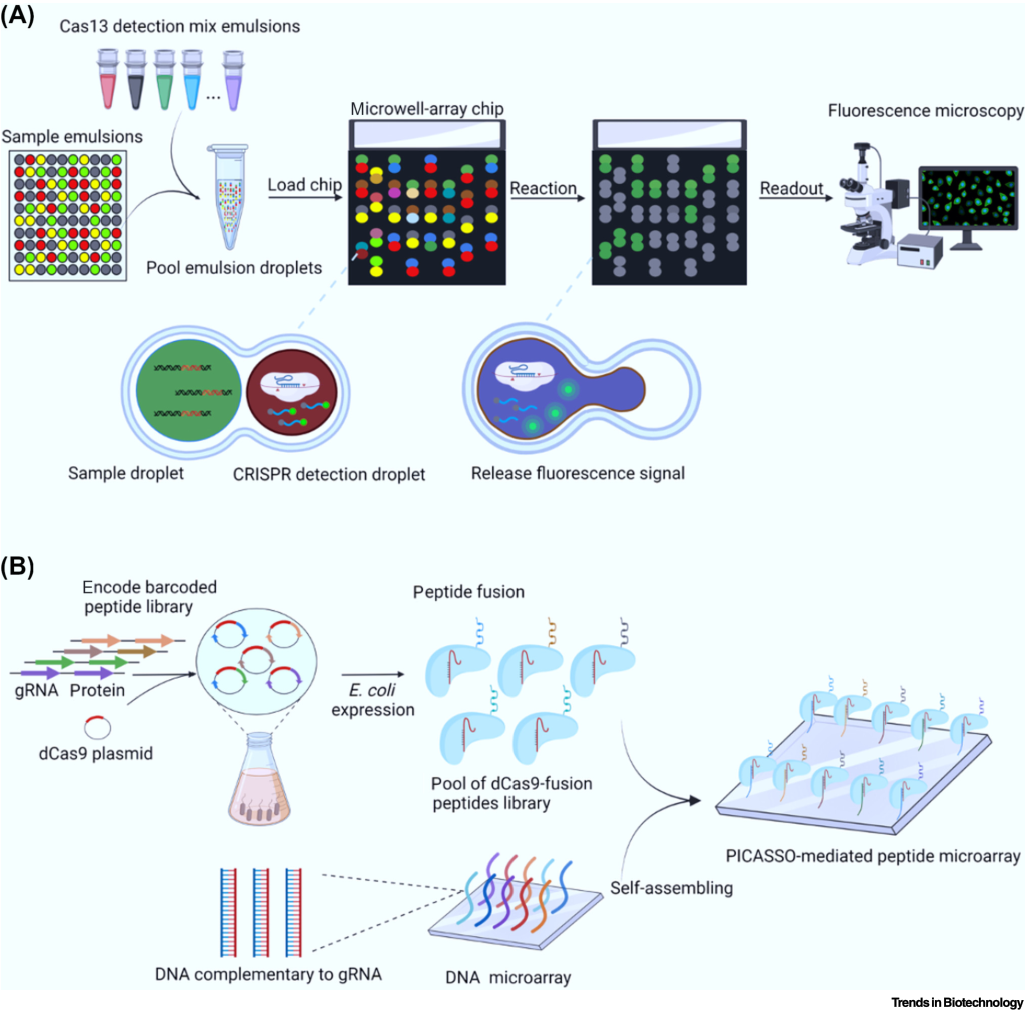
图3 (A)CARMEN-Cas13微流控检测方法原理图; (B)PICASSO蛋白微阵列的组装过程
(3)癌症生物标志物检测
癌症相关生物标志物的检测有助于癌症患者的预后。CRISPR检测技术可以检测不同类型的癌症生物标志物。与传统的检测方法如聚合酶链式反应和酶联免疫吸附试验相比,CRISPR检测技术不需要昂贵的仪器和经验丰富的操作员。例如,CRISPR技术可以检测循环中的肿瘤DNA(ctDNA)和人体循环中的miRNA。Cas12a检测系统可以在3小时内检测到EGFR858和EGFR790,检测限为0.005%。而蛋白质类型的生物标志物的检测需要引入适配子。依据蛋白质的特殊结构设计相应适配子来靶向蛋白质,并且适配子结合目标蛋白后能被CRISPR系统检测到,从而实现对蛋白质的检测。目前基于CRISPR的蛋白质检测方法有较高的灵敏度,但是由于适配子难以设计,该技术并没有实现广泛应用。
(4)CRISPR技术的发展前景
论文最后论述了“实现CRISPR诊断技术的自动化和一体化,并且以CRISPR诊断技术为纽带联系病患和医院构建诊疗网络”这一前瞻性策略(图4)。目前通过优化和整合CRISPR诊断体系中的样品处理、预扩增、CRISPR检测和读取过程,完全可能开发一体化CRIPSR检测仪。而检测自动化意味着降低检测成本、加快检测速度、统一诊断标准,这一举措能够扩大CRISPR诊断技术固有的优势。诊疗网络的构建不仅有利于对阳性人员进行及时处理,上传的诊断数据还能够指导CRIPSR检测体系的进一步优化。
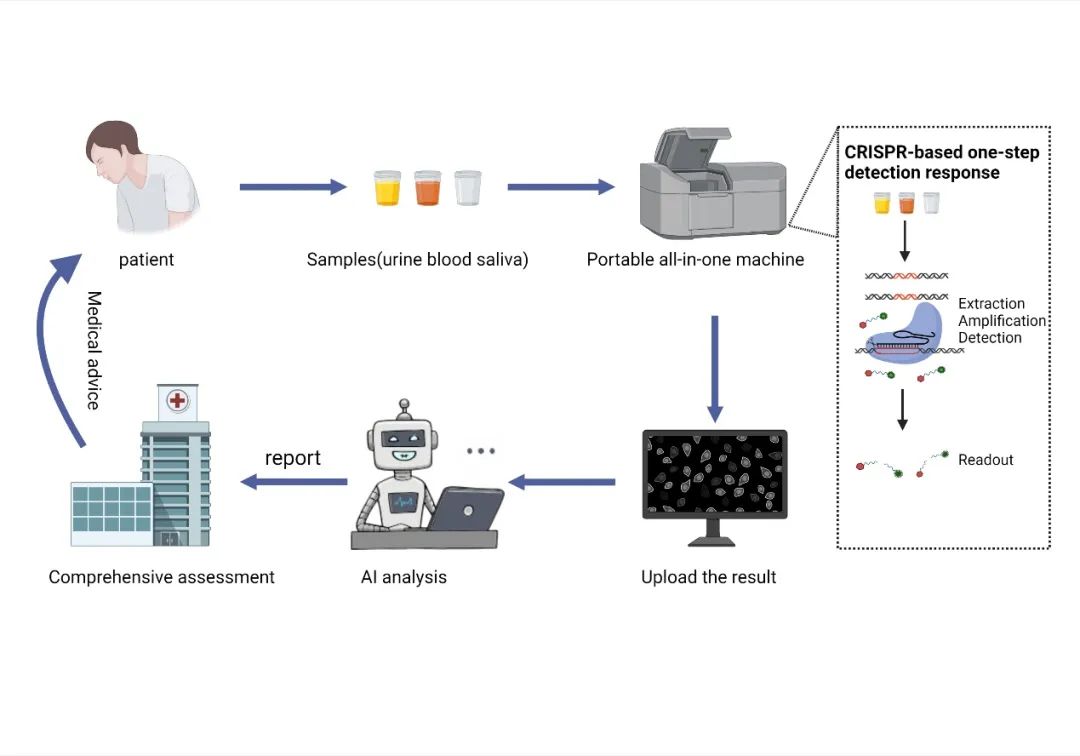
图4 CRISPR诊断体系的前瞻性设想
-
FPGA在自动驾驶领域有哪些优势?2024-07-29 8188
-
FPGA在图像处理领域的优势有哪些?2024-10-09 9529
-
麦科信汽车诊断示波器在机车维修领域中的应用实例2025-04-18 1503
-
大家说在控制领域DSP和FPGA那个有优势2013-07-28 3535
-
RFID技术在航空领域应用有什么优势?2019-08-05 2616
-
无线通信在应用中的优势2020-05-27 1729
-
武器装备测试诊断技术发展和综合诊断2009-07-16 946
-
DSP技术怎么样_DSP技术的应用领域及优势2018-01-03 20323
-
振动诊断技术在钻井泵故障诊断中有怎么样的作用和应用2020-01-06 1417
-
机器学习在故障检测与诊断领域中的应用综述2021-06-24 1148
-
基于CRISPR技术的高特异和高灵敏分子诊断方法CRISPR-Dx2022-12-01 2169
-
数字孪生技术在农业领域的应用优势2023-05-06 1429
-
面部表情识别技术在医疗领域的应用2023-08-29 1714
-
卷积神经网络在图像和医学诊断中的优势2024-07-01 3034
-
图像识别技术在医疗领域的应用2024-07-16 2992
全部0条评论

快来发表一下你的评论吧 !

