

使全固态钠离子或钠电池(ASNB)有望用于ESS中
电池
描述
【工作背景】
锂离子电池(LIB)已扩大到大规模储能系统(ESS)等应用领域。然而,锂的价格在过去十年中上涨了10倍以上。锂矿分布不均匀也引起了政治和经济问题。此外,从与使用易燃有机液体电解质相关的频繁火灾事故中可以看出,LIB存在安全问题。这些因素阻碍了LIB在ESS中的广泛使用。然而,使用不易燃的无机Na+超离子导体固态电解质(SEs)可以提高安全性并降低成本,使全固态钠离子或钠电池(ASNB)有望用于ESS中。
硫化物SEs因其高离子电导率和机械可变形性而被广泛研究,同时这允许基于冷压制造全固态电池。第一个硫化物Na+超离子导体立方Na3PS4的Na+电导率为0.2 mS cm-1。然而,硫化物SEs的电化学氧化稳定性低至∼2 V(vs Na/Na+)。
最近,卤化物SEs逐渐成为游戏规则的改变者,因为它们与硫化物SEs类似,可机械烧结并表现出优异的电化学氧化稳定性和与LiMOx(M=Ni、Co、Mn和Al混合物)正极活性材料(CAMs)的界面相容性。然而,自从关于Li3YCl6(0.5 mS cm-1)的开创性报道以来,目前仅通过实验鉴定了三种Na+类似物:Na2ZrCl6、Na3-xEr1-xZrxCl6,和Na3-xY1-xZrxCl6。
对卤化物SEs实际应用的批判是使用稀有和昂贵的中心金属,如Y、In和Sc。这对于Na+卤化物SEs更为关键,因为使用昂贵的元素严重抵消了Na化学的成本效益。这促使人们探索使用廉价和含量丰富的元素(如铝)组分。
长期以来,NaCl-AlCl3二元体系一直是各种研究领域的关键,包括可充电钠电池。NaAlCl4在约160 °C时熔化,因此可用作高温运行的Na-NiCl2和用于ESS的Na-Al电池的熔盐电解质。此外,NaAlCl4−nSO2在室温(RT)下是一种不易燃的无机液体电解质。因此,NaAlCl4的性质和相应的电池性能已经在高温下的熔融状态或无机液态(NaAlCl4-nSO2)下进行了研究,但迄今为止没有任何关于ASNB的固态Na+传导的报道。
【工作介绍】
基于上述问题,近日,韩国延世大学Yoon Seok Jung课题组首次验证了NaAlCl4用于室温ASNB的可行性。该研究工作中,与高温退火样品相比,新型机械化学法制备的斜方晶系NaAlCl4的Na+电导率(3.9×10-6 S cm-1,30 °C)显示出10倍的提升。电化学测量和理论计算证实了NaAlCl4的高氧化稳定性极限至少为∼4.0 V(vs Na/Na+)。尽管Na+电导率相对较低,但使用BM-NaAlCl4的NaCrO2/Na3Sn ASNB在30和60 °C下均表现出优异的循环性能。该工作以“NaAlCl4: New Halide Solid Electrolyte for 3 V Stable Cost-Effective All-Solid-State Na-Ion Batteries”为题发表在国际顶级期刊《ACS Energy Letters》上。
【核心内容】
三个NaAlCl4样品是通过对等摩尔NaCl-AlCl3混合物机械化学研磨制备而成,无需或随后在100或200 °C下进行热处理(HT),分别称为BM-、HT100-和HT200-NaAlCl4。使用Ti/SE/Ti对称电池,通过交流阻抗法测量所得冷压片的Na+电导率。Na+电导率的Arrhenius图如图1a所示。BM-NaAlCl4的奈奎斯特图显示其在30 °C下的Na+电导率为3.9×10-6 S cm-1,活化能为0.42 eV。通过计时电流法测量的BM-NaAlCl4的电子电导率为1.2×10-10 S cm-1,这转化为接近1的迁移数。
此外,该值远低于硫化物SEs(~10-9 S cm-1),这对于抑制副反应非常有利。在370 MPa下制备的冷压片的平整表面也证实了BM-NaAlCl4具有优异的变形能力。随着BM-NaAlCl4的热处理温度升高到100和200 °C,Na+电导率逐渐降低到2.4×10-6和3.3×10-7 S cm-1。后者比没有退火的要低10倍。与退火样品相比,BM-NaAlCl4的Na+电导率显著提高,与各种卤化物SE(如LiAlCl4、Li3YCl6和Li2ZrCl6)相当,这可以通过阳离子无序和/或堆垛层错呈现的离子传导通道和能量图来解释。
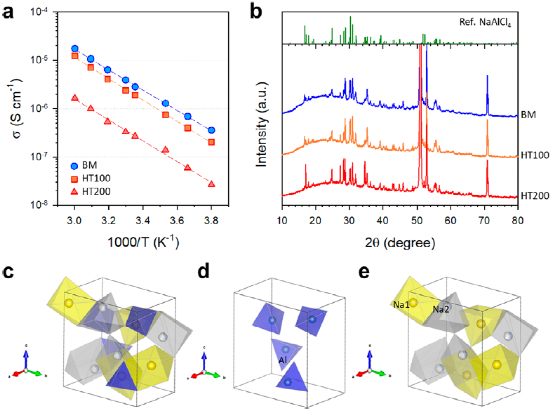
图1. BM-、HT100-和HT200-NaAlCl4的表征。
图1b中显示的所有三个样品的XRD图均与具有P212121空间群的正交NaAlCl4的布拉格峰相匹配。尽管BM-和HT100-NaAlCl4的XRD结晶度相似,但HT200-NaAlCl4的XRD结晶度显著增加。考虑到NaAlCl4的低熔点(约为160 °C),HT200-NaAlCl4的高结晶度源于NaAlCl4熔体的再结晶。BM-和HT100-NaAlCl4样品为粉末状,而HT200-NaAlCl4样品以块体形式存在。差示扫描量热法的结果证实了NaAlCl4的低熔点为152 °C。
BM-NaAlCl4的粉末XRD Rietveld精修曲线拟合结果显示其密度为2.02 g cm-3(a=6.17302 Å,b=9.88428 Å,c=10.33293 Å,V=630.5 Å3)。值得注意的是,该值显著低于其他Na+卤化物SE(Na2ZrCl6,2.43 g cm-3;Na2.8Er0.8Zr0.2Cl6,2.84 g cm-3),略低于硫化物SE Na3PS4(2.19 g cm-3),这表明使用NaAlCl4的ASNB在比能量密度方面具有优势。
NaAlCl4的晶体结构如图1c-e所示,其中Al3+位于四面体位置,形成相互隔离的AlCl4-四面体(图1d)。在Li3MCl6(M=Y,Er,In,Sc,Zr)中,MCl63−八面体形成结构框架。NaAlCl4中AlCl4-四面体的出现是由于Al3+的离子半径(晶体离子半径为53 pm)比Li3MCl6(86-103 pm)中其他离子的离子半径更小。
在BM-NaAlCl4中,Na+位于两个不同的棱柱形位置,表示为“Na1”和“Na2”位点(图1e)。另一方面,对于HT200-NaAlCl4,没有Na2位点的模型获得了可靠水平的最佳精修结果(χ=6.95)。当加入Na2位点时,χ值增加到7-8,表明没有Na2位点占据的结构模型更适合高结晶的HT200-NaAlCl4。
BM-NaAlCl4中分散的Na+占据类似于其他机械化学法制备的卤化物SEs,如Na2ZrCl6、Li2ZrCl6、Li3YCl6和Li3ErCl6。第一性原理计算表明,Na+全部分布在Na1位的结构比Na+同时分布在Na1和Na2位的结构在能量上更有利。然而,它们的能量差异仅为5-53 meV/原子,这支持了机械化学法制备的BM-NaAlCl4样品中Na+在Na2位点上的占据。
通过拉曼光谱进一步获得了结构信息。前驱体AlCl3在310 cm-1处有一个峰,对应于三向交叉AlCl63-八面体与其相邻八面体共用三个边。BM-和HT-NaAlCl4展示了位于350 cm-1处的峰且没有任何AlCl3信号。350cm-1处的特征峰对应于AlCl4-四面体的振动(A1模式)。
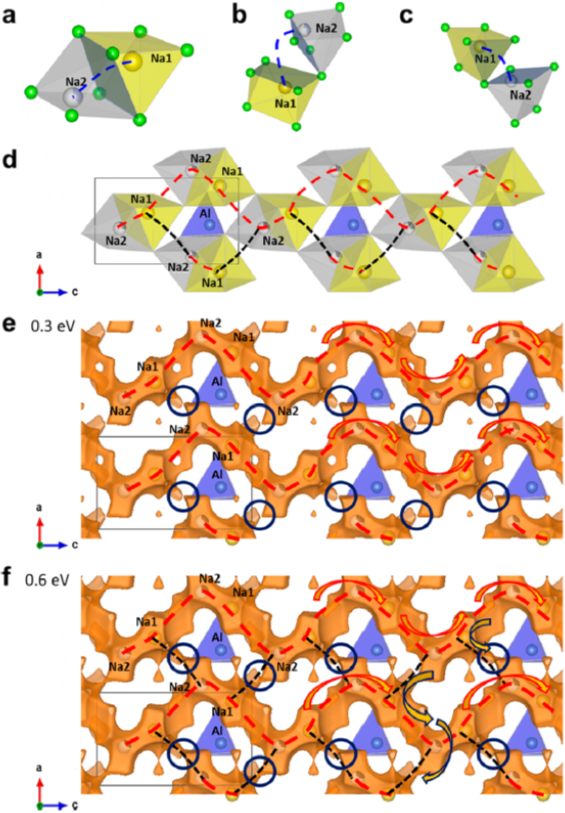
图2. BM-NaAlCl4的BVEL计算结果。
然后,研究人员进行了BVEL分析以评估BM-NaAlCl4中的Na+迁移途径(图2)。尽管不精确,但软BV对障碍的相对高度和离子迁移路径提供了合适的近似值。确定了Na1和Na2位点之间的三种不同Na+迁移机制:(i)通过共面三棱柱之间的共享矩形面(传输I,图2a),(ii)通过角共顶点三棱柱之间的矩形面(传输II,图2b),以及(iii)通过共顶点三棱柱中Na1位点的三角形面和Na2位点的矩形面(传输III,图2c)。
BV等值面映射图和BVEL计算结果表明,迁移模式传输I>传输II≫传输III,这可以通过传输III的三角形迁移区面积(6.7 Å2)比矩形迁移区面积(14.7 Å2)小得多来理解。这三种类型的迁移机制结合起来形成了ac平面中的二维Na+迁移途径(图2d)。图2e、f显示了等值面值分别为0.3和0.6 eV时在[010]方向上观察的键价等值面图。对于0.3 eV的图,沿[001]方向的1D锯齿形路径通过传输I和II形成(红色虚线,图2e)。
对于0.6 eV的图,上述1D路径通过传输I-III(深蓝色虚线)相互连接,形成扩展的2D网络路径(图2f)。与此形成鲜明对比的是,ab平面中的BV等值面图显示了沿[010]方向的断开,证实了BM-NaAlCl4中2D Na+迁移路径的1D倾向性。Na2位点是在机械化学法制备的NaAlCl4中新发现的,占据Na2位点会增强Na+通路的连通性。这表明与退火后的高结晶样品相比,在机械化学制备的NaAlCl4中Na2位点发生Na+占据可能是其Na+电导率显著提升的关键。
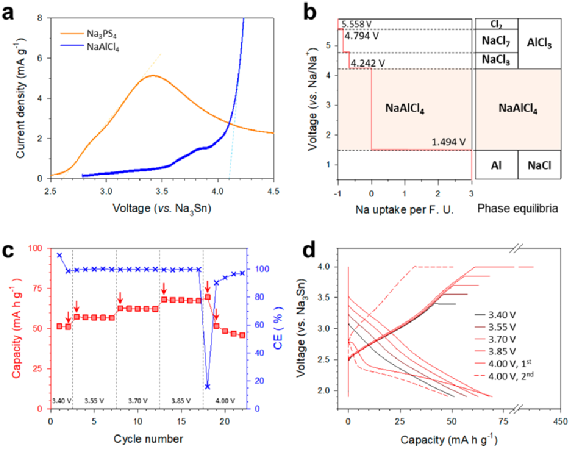
图3. BM-NaAlCl4的电化学稳定性。
在30 °C下,通过对SE-C混合电极(重量比为7:3)进行循环伏安法(CV)测量来评估BM-NaAlCl4的电化学稳定性。图3a显示了BM-NaAlCl4和Na3PS4的第一个正扫描曲线。BM-NaAlCl4发生严重氧化的起始电位为~4.1 V(vs Na3Sn≈4.0 V vs Na/Na+),这与Na3PS4的~2.6 V(vs Na3Sn≈2.5 V vs Na/Na+)形成鲜明对比。
此外,BM-NaAlCl4高达4.0 V(vs Na/Na+)的综合氧化电流(0.83 mA V g-1)远低于Na3PS4(4.72 mA V g-1),与硫化物变体相比,卤化物SE NaAlCl4在氧化稳定性方面展现出独特的优势。与其他卤化物SE一样,BM-NaAlCl4表现出较差的还原稳定性,起始还原电流约为2.1 V(vs Na3Sn≈2.0 V vs Na/Na+)。
此外,还进行了第一性原理计算以揭示NaAlCl4的内在电化学稳定性和分解产物。NaAlCl4的计算电化学窗口和相平衡如图3b所示。NaAlCl4显示出从1.494到4.242 V(vs Na/Na+)的宽电化学窗口,并且在氧化上限处的分解产物预计为NaCl3和AlCl3相。阳极(氧化)反应的起始电压与图3a中的CV结果一致。实验和计算结果表明,这种高氧化稳定性的NaAlCl4是一种有前景的SE,可用于高压ASNB。
为了评估使用NaMO2 CAM的NaAlCl4的实际电化学稳定性,选择Na0.67Ni0.1Co0.1Mn0.8O2(NaNCM118)作为模型CAM,因为它的可逆性高达∼4.5 V(vs Na/Na+)或更高,这与使用传统液体电解质的NaNCM118正极的电池测试结果一致。
使用BM-NaAlCl4作为电解质的NaNCM118/Na3Sn全固态电池在更高的截止电压下进行循环即从3.50 V逐步增加0.15 V到4.10 V(vs Na/Na+),而较低的截止电压固定为2.0 V(vs Na/Na+)。放电容量和库仑效率随循环次数的变化如图3c所示。使用BM-NaAlCl4的NaNCM118保持稳定的循环和接近100%的库仑效率(CE),直到截止电压达到3.95 V(vs Na/Na+)。
然而,一旦以4.10 V(vs Na/Na+)的截止电压(第18次循环)开始充电,充电容量增加了∼6倍(440 vs 70 mAh g-1),CE却从99.7%下降到15.9%,表明NaAlCl4有严重的副反应。图3d中相应的充放电电压曲线也显示出较大的过电势,特别是在截止电压为4.10 V(vs Na/Na+)循环的第一次放电期间。随后循环的容量突然下降。这些结果表明,NaAlCl4的实际截止电压极限为~3.95 V(vs Na/Na+),这与CV和第一性原理计算结果非常吻合(图3a,b)。
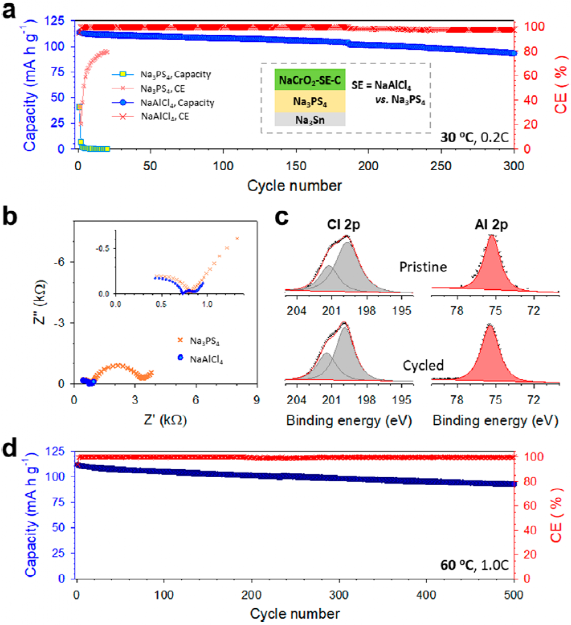
图4. 使用BM-NaAlCl4正极电解质的NaCrO2/Na3Sn ASNBs的电化学性能。
最后,本文评估了BM-NaAlCl4作为3 V级NaCrO2/Na3Sn ASNBs电解质的可行性,并与Na3PS4进行了比较(图4)。Na3PS4的Na+电导率为1.0×10-4 S cm-1,用作SE隔膜。图4a显示了不同固态电池在恒定电流-恒定电压(CCCV)充电模式下(限制电流密度为0.02 C)在30 °C和0.2 C下2.0和3.5 V之间的循环性能。使用Na3PS4的NaCrO2表现出35.2%的低ICE和41 mAh g-1的低放电容量。其初始容量在随后的循环中大幅下降。与以前的研究相比,性能较差的原因是苛刻的CCCV充电模式和导电碳添加剂的存在,加速了副反应发生。
相比之下,使用BM-NaAlCl4的NaCrO2电极表现出114 mAh g-1的高首次放电容量和95.2%的高ICE,在300次循环后容量保持率高达82.0%。通过电化学阻抗谱(EIS)分析了不同循环次数的ASNB电池中的电阻成分(图4b)。奈奎斯特图显示了一个不完整的高频半圆和一个完整的中频半圆,这分别归因于分隔SE层和正极界面的阻抗。
对于具有BM-NaAlCl4和Na3PS4(约700-800 Ω)的ASNB电池,R1+R2的类似振幅是因为它们使用了相同的Na3PS4作为SE隔膜。相比之下,使用BM-NaAlCl4时的界面电阻远低于使用Na3PS4时的界面电阻(例如,在第一个循环时为116与2405 Ω)。
此外,Na3PS4的振幅超过了SE层的振幅,并且在循环时显著增加(在第五圈循环时达到6334 Ω)。与Na3PS4(1.0×10-4 S cm-1)相比,BM-NaAlCl4(3.9×10-6 S cm-1)的Na+电导率较低;但与Na3PS4相比,使用BM-NaAlCl4的界面电阻却小得多。
通过在30 °C下20次循环前后对使用BM-NaAlCl4和Na3PS4的NaCrO2电极进行X射线光电子能谱(XPS)测试来探究潜在的界面演变机制(图4c)。对于使用Na3PS4的电极,S 2p和P 2p XPS光谱均揭示了氧化物质SO42-、PO43-、桥接硫(P-[S]n-P)和P2S5的演变。
相反,对于使用BM-NaAlCl4的电极,在20圈循环后观察到Cl 2p和Al 2p光谱的边缘变化(图4c),证明NaAlCl4保持完好。因此,决定ASNB电池性能的因素是电化学和界面稳定性,而不是离子电导率。BM-NaAlCl4(1.2×10-10 S cm-1)的低电子电导率导致的动力学过电势也有助于获得优异的稳定性。然而,当电极质量负载从11.3翻倍至22.6 mg cm-2,观察到过电势大幅增加,这需要提高电解质的Na+电导率。
BM-NaAlCl4在30和60 °C下的倍率性能结果显示,0.5C时的放电容量在30 °C时≤70 mAh g-1,这归因于BM-NaAlCl4电解质的低Na+电导率。通过将温度升高到60 °C,Na+电导率提高到1.7×10-5 S cm-1,放电容量增加,在1C时达到∼100 mAh g-1。
基于此结果,采用BM-NaAlCl4电解质的NaCrO2/Na3Sn ASNB在60°C和1C下循环(图4d)。该电池的ICE为94.0%,其初始放电容量为112 mAh g-1,后续循环的平均CE高达99.93%;在500次循环后,该电池还表现出极高的长循环容量保持率,达到82.0%。与之前报道使用NaCrO2的ASNB相比,该工作中的ASNB显示了优异的性能。
【结论】
该工作首次证明了正交NaAlCl4在室温ASNB中的适用性。机械化学法制备的NaAlCl4在30 °C时的Na+电导率为3.9×10-6 S cm-1,比具有低电子电导率(1.2×10-10 S cm-1)的退火NaAlCl4高1个数量级以上。BVEL计算结果显示,Na+在ac平面上通过新发现的Na+间隙位点优先进行1D扩散。
NaAlCl4的高电化学氧化电压极限高达∼4 V(vs Na/Na+),并且使用NaNCM118正极通过第一性原理计算、CV和逐步增加电压测试得到了补充。在NaCrO2/Na3Sn ASNB中使用BM-NaAlCl4相比使用Na3PS4表现出更好的性能,强调了电化学和界面稳定性的决定性作用。
最后,使用BM-NaAlCl4电解质的NaCrO2/Na3Sn ASNB在30和60 °C下都显示出优异的循环稳定性:在30 °C下循环300次和在60 °C下循环500次后容量保持率分别为82.0%和82.9%。该电化学性能优异的ASNB电池使用高性价比的的Al和Na元素,突出了其在ESS应用中的广阔前景。
然而,BM-NaAlCl6的低Na+电导率应该得到提高,以提升其在使用更高的面容量电极下的室温倍率性能。未来研究工作中可使用Na+硫化物和Li+卤化物的类似物Na3PS4和Li3YCl6等来进一步提高Na+电导率。
审核编辑:刘清
-
首台钠离子电池试验车亮相,有望打破电车价格底线2023-02-26 4809
-
钠离子电池研究现状2023-12-03 4157
-
界面层创新:全固态钠电池稳定性实现突破性提升2025-11-28 3045
-
苹果的新专利--全固态电池2015-12-23 4764
-
相比锂离子电池,碳基钠离子电池负极未来发展难点?2018-10-30 2976
-
全固态电池是什么2021-07-12 2713
-
国外研究发现锂金属有望成为全固态电池的最终阳极材料2019-03-27 2569
-
钠离子电池应用_钠离子电池机遇与挑战2020-08-03 9819
-
钠离子电池与锂离子电池的比较2022-04-24 43785
-
宁德时代钠离子电池产业化布局 钠离子电池续航扩展至500公里2022-11-29 2980
-
全固态电池的工作原理是什么2023-02-21 12444
-
新能源钠离子电池预钠化技术进展2023-05-30 6566
-
圆柱钠离子电池的优缺点和应用领域2023-07-12 3437
-
隔膜容量补偿策略应用于钠离子电池2023-08-07 1855
-
锰系钠离子电池厂商安钠能源完成数千万元天使轮融资2024-02-05 1616
全部0条评论

快来发表一下你的评论吧 !

