

利用中空微针实现高效皮内递送治疗非黑色素瘤皮肤癌
描述
根据世界卫生组织(WHO)的数据显示,非黑色素瘤皮肤癌在过去几十年内发病率显著增加,全球每年报告病例超过100万例,且死亡率极高。现有常规治疗方案如手术切除、化疗、放疗、冷冻治疗等预后不佳,且多会引起全身毒性。光动力疗法(PDT)因其系统毒性低、可降低疾病复发率、联合治疗可及性高等优势在皮肤癌等恶性肿瘤治疗中获得了广泛关注。
其中,对于非黑色素瘤皮肤癌而言,局部光动力疗法更具优势。然而,现有的策略通常结合磁场或电场等外在媒介,较为复杂且需要训练有素的操作人员,不利于实际应用。
在该研究中,Donnelly教授团队采用脂质纳米胶囊包载光敏剂金丝桃素(Hypericin,Hy),进而利用中空微针实现高效皮内递送,通过局部PDT治疗非黑色素瘤皮肤癌(图1)。
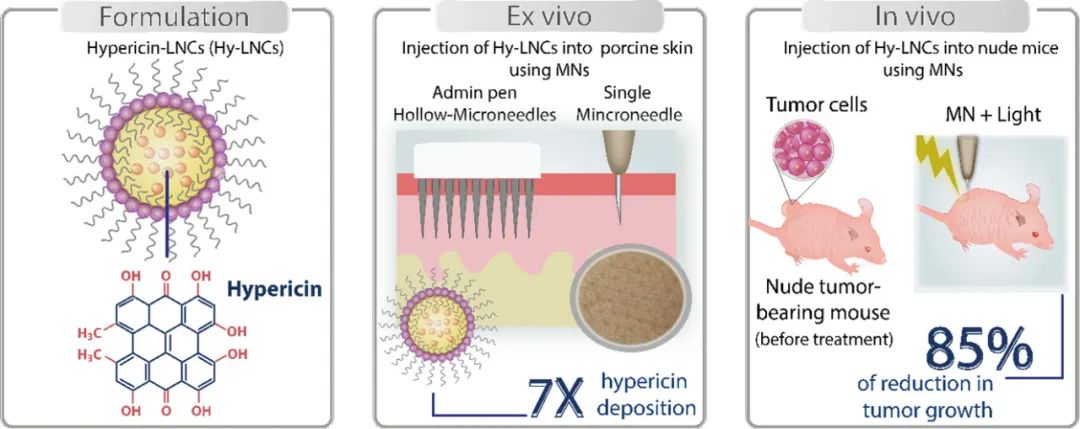
图1 中空微针辅助皮内递送脂质纳米光敏剂,实现肿瘤局部光动力治疗的示意图
光敏剂在脂质纳米胶囊中的装载
Hy是一种有效的脂溶性光敏剂,具有良好的抗癌活性。但其水溶性较差、易在生物系统中聚集,且在皮肤中难以渗透,严重阻碍其应用。研究人员以Labrafac、KolliphorHS 15和LipoidS 100为主要脂质成分,通过相转换和温度循环制备脂质纳米胶囊并高效包载Hy,得到Hy-LNCs。当Hy浓度为100μM时,所得Hy-LNCs粒径为47.76±0.49nm,聚合物分散性指数(PDI)为0.12±0.02,且Hy的封装效率高达99.67%。
此外,Hy-LNCs可有效抑制Hy的聚集,相比游离Hy,光活性提高396倍,光稳定性也有显著提高,其中游离Hy于20分钟内全部降解,而Hy-LNCs在40分钟内仅降解18%。此外,Hy-LNCs的细胞摄取与细胞毒性也得到明显提升。
中空微针的应用
胶体粒子和大分子治疗剂等难以克服皮肤屏障,大多停留于表层皮肤,无法跨越角质层渗透至更为深层的表皮和真皮层,阻碍了其有效使用。微针(MNs)拥有微米级针尖,可透皮递送治疗性分子而不会引起明显的疼痛。其中,中空微针(Ho-MN)设计有水溶性微通道,能够刺穿上层皮肤有效注入不同的药物制剂,使药物直接沉积于表皮和真皮层中。
许多商品化中空微针(例如MicronJet、AdminPen Ho-MNs等)可与标准注射器适配,用于各类制剂的高效皮内递送。
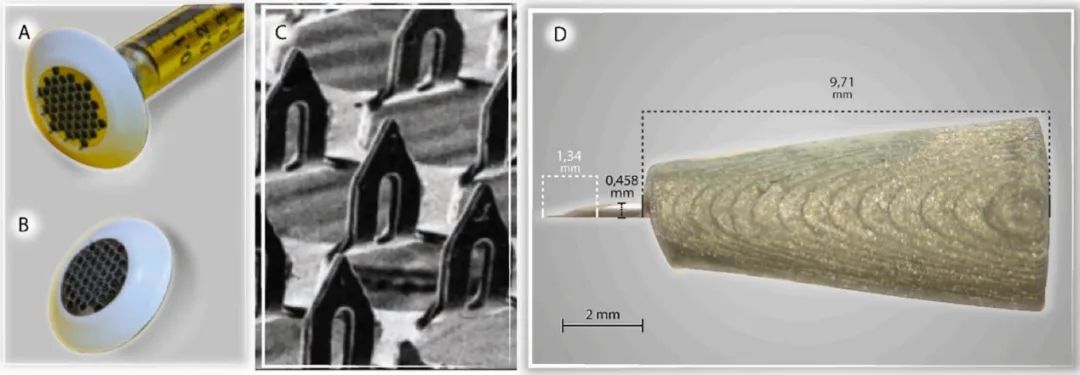
图2 两种不同类型的中空微针装置:AdminPen(A-C)和S-Ho-MN(D)
研究人员比较了两种类型的Ho-MNs(AdminPen和S-Ho-MN)。其中,AdminPen Ho-MN阵列面积为1平方厘米,由43个非常锋利的不锈钢针尖组成(图2A-C),其特点是每个针尖侧面都有偏心管轴,确保药物可以有效递送而不会堵塞针尖。选取的针尖高度为1200μm,可经皮创建深约1100-1200μm的微孔,将药物有效递送至真皮而不触及疼痛受体。
去除微针阵列后,形成的水性微孔可坍塌,皮肤屏障快速修复以避免感染。单根中空微针(S-Ho-MN)由Donnelly教授团队设计,他们以26G × ½英寸的不锈钢Terumo针为基础,制造了这款高约1300μm的中空微针,并使用3D打印,获得了由PLA组成的微针底座,组装后得到同样能够适配注射器的S-Ho-MN(图2D)。
两种微针均具有很高的机械强度,可有效穿透皮肤屏障。OCT图像显示,AdminPen 1200μM Ho-MN在新生猪皮肤中的穿透深度为1045.5±22.8μm,约为实际针长的95%(图3a、b)。另外,闭孔动力学研究显示(图3c),去除微针阵列后,皮肤在2-4分钟内迅速开始愈合,10分钟内皮肤屏障即可完全恢复。
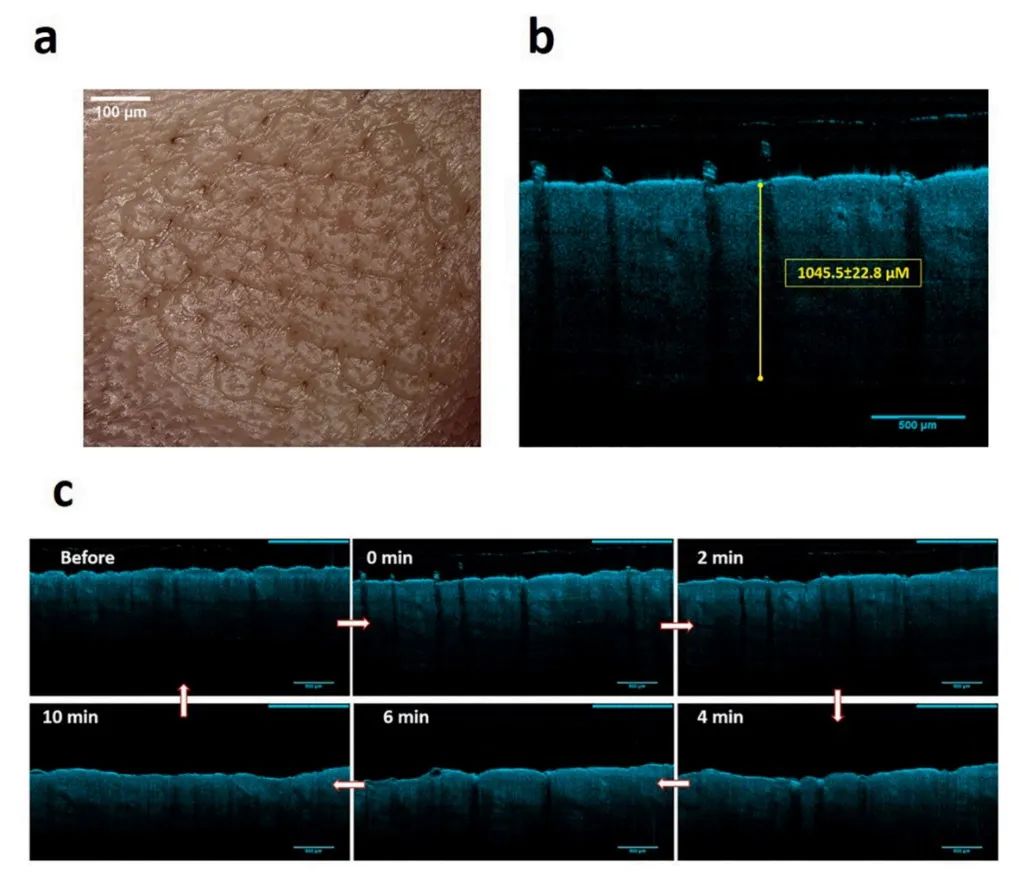
图3 AdminPen 1200μM中空微针对于新生猪皮肤的穿透(a)、OCT图像(b)和闭孔动力学图像(c)
当微针阵列应用于皮肤时,其创建的水性微通道能够一直保持打开,因此,可持续递送Hy-LNCs至深层皮肤中。Hy在离体猪皮肤的渗透研究显示,在每个深度水平,Hy-LNCs的药物浓度都显著高于游离Hy,其最深可扩散至2900μm,而游离Hy最深仅可扩散至900μm,表明LNCs封装Hy可辅助Hy在皮肤中的渗透。此外,三维重建的共聚焦图像显示,Ho-MN可将Hy-LNCs有效递送至目标深度。
通过S-Ho-MN注射Hy-LNCs和游离Hy的离体研究显示,Hy-LNCs显著提高了Hy的皮内沉积量,约为游离Hy的7倍之高,二者的皮肤药物沉积分别为总给药剂量的92.5%和14%。类似地,通过AdminPen 1200μM Ho-MN给药时,Hy-LNCs的皮肤沉积量达到了给药剂量的75%,也显著高于Hy溶液的12%。总体而言,通过中空微针注射Hy-LNCs可显著改善Hy在不同皮肤层内的皮内分布和药物沉积。
体内抗肿瘤效果研究
研究人员采用荷皮下CT-26(CRL-2638)小鼠结肠癌的裸鼠模型评估了中空微针辅助皮内递送Hy-LNCs的光动力治疗效果。体内生物分布显示,Hy-LNCs会在皮下组织中保留1h,其后会逐步扩散至身体其它组织,所以选择微针给药45分钟后开始进行LED光照(595±10nm)。
在应对具一定曲度的病灶部位时,AdminPen Ho-MN因其扁平的阵列样式造成了制剂的大量泄漏,而研究人员设计制造的S-Ho-MN可有效将制剂垂直递送至肿瘤中而不会泄漏。体内治疗结果显示(图4),由S-Ho-MN递送的Hy-LNCs在LED光照射后(45±2mW/cm²)表现出显著的抗肿瘤效果,肿瘤体积从103±5.16mm³减少至15±2.30mm³,抑瘤率达85.84%。
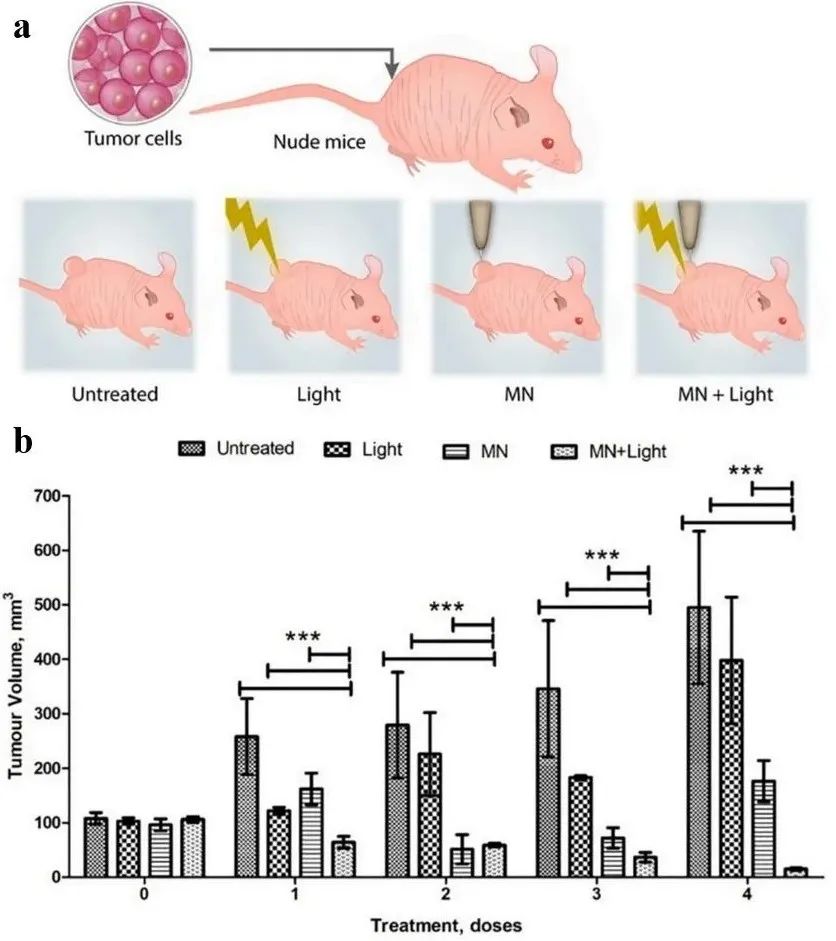
图4 S-Ho-MN递送Hy-LNCs在小鼠皮下肿瘤模型中的光动力治疗效果
综上所述,该研究使用中空微针作为局部光动力癌症治疗的潜在药物递送平台。两种类型的Ho-MNs均可高效将Hy-LNCs透皮递送至皮肤深层。然而在体内应用于荷瘤小鼠的简便性和可行性方面,S-Ho-MN优于AdminPen Ho-MN。该研究表明采用中空微针递送Hy-LNCs联合光照为非黑色素瘤皮肤癌提供了一种创伤小、高效的局部治疗方法。
论文链接:
https://doi.org/10.1016/j.jconrel.2022.06.027
审核编辑:刘清
-
求助:请问一下皮肤黑色素怎么测量啊?2012-11-17 2993
-
具备机器学习能力的黑色素瘤自动侦测工具来袭 可提前发现2017-01-01 801
-
能快速准确检测皮肤癌的温度传感器2018-06-15 2775
-
一种新的基于电穿孔的皮肤高效核酸递送方法2018-05-10 6551
-
Skan皮肤癌检测仪便携设备,帮助患者及早发现病症2018-10-14 1664
-
AI新闻:利用人工智能进行皮肤癌筛查2018-11-05 3243
-
新型激光扫描仪可在极短时间内检测到皮肤癌2019-10-29 1233
-
粘性纳米颗粒可帮助治疗皮肤癌2021-02-02 2654
-
科学家通过深度学习算法检测黑色素瘤2021-02-19 2752
-
利用微流控平台探究剪切应力在黑色素瘤转移中的功能2022-08-19 1515
-
Ultra96皮肤癌AI构建2022-10-21 855
-
实现高效肿瘤局部给药的智能水热反应微针设计2023-08-23 2170
-
新型微针可实现药物递送和生物标志物检测2023-08-28 3068
全部0条评论

快来发表一下你的评论吧 !

