

一种简便的微流控电阻抗检测系统
描述
基于电阻抗的细胞分析是一种无标记、非侵入性技术,已广泛用于分析和识别各种应用中的细胞特征,如组织培养、细胞生长及活力检测等。微流控技术能够将涉及样品制备、操作和基于阻抗检测的分析过程集成到单片芯片上,最大限度地减少系统尺寸、重量。
据麦姆斯咨询报道,近期,中国科学院上海微系统与信息技术研究所的研究人员于《功能材料与器件学报》发表论文,搭建了一种简便的微流控电阻抗检测系统,可根据电学差异对体积相近的不同微粒进行区分,具有成本低、易集成、非标记等优势,未来可进一步用于现场细胞即时检测。
微流控芯片的设计与制作
采用的微流控阻抗检测芯片主要分为三层:微通道层、电极层和引线层(图1(a))。微通道层主要提供细胞流动通道,电极层用来感测阻抗变化,引线层用于连接信号的输入与输出。此外,检测电极采用剥离工艺,在玻璃上形成金电极(Au/Cr,厚度200nm/50nm),检测电极宽度为30μm,间隔为15μm,检测口流道宽度为30μm,高度为30μm。微通道模具为SU-8结构,由匀胶、前烘、曝光、显影、硬烘等步骤制成。将PDMS预聚物与固化剂(10:1)混合后浇筑在模具上,80℃烘箱烘烤90min后脱模,然后将微通道层和电极层通过氧等离子对准键合(图1(c)),最后焊接电极和PCB引线层,完成微流控阻抗检测芯片的制作,如图1(b)。
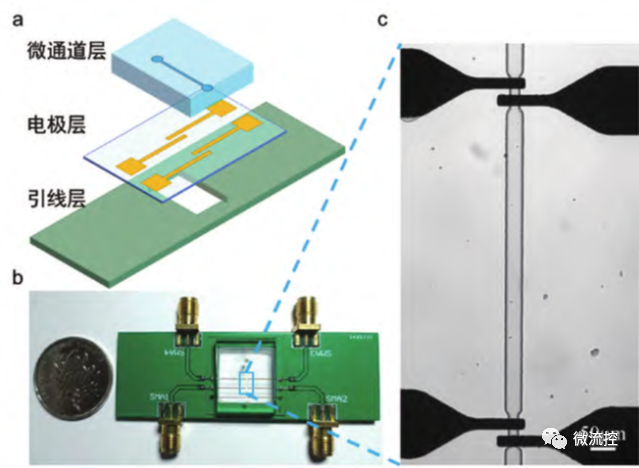
图1 细胞阻抗检测芯片设计:(a)芯片结构;(b)最终制作出的检测芯片;(c)微通道层和电极层的键合
阻抗测试平台的搭建
锁相放大器能够将微弱的阻抗脉冲信号从噪声中提取出来,原理如图2,锁相放大器首先将输入信号经过运算放大器OPA657实现跨阻放大后,采用高速乘法器AD835与参考信号混频,然后通过低通滤波器进行滤波,将期望频率的信号从其他频率信号中分离出来。
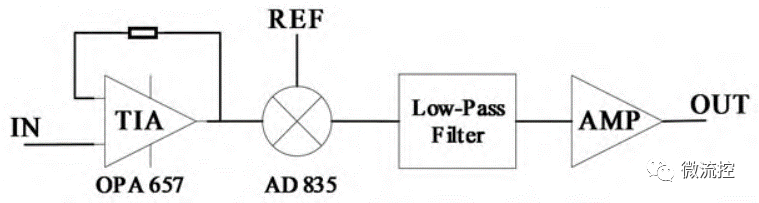
图2 锁相放大电路原理
目前用于微流控阻抗检测的锁相放大器主要有苏黎世系列和美国斯坦福SR系列,但是商用仪器体积较大,不易集成。本实验采用运算放大器和乘法器自行设计出模拟锁相放大器,并基于此搭建流式阻抗检测系统,如图3所示。芯片放置在显微镜上观察,由注射泵进样,信号源施加激励信号,锁相电路放大感应信号,然后数据通过采集卡传输到电脑进行显示、储存和分析。
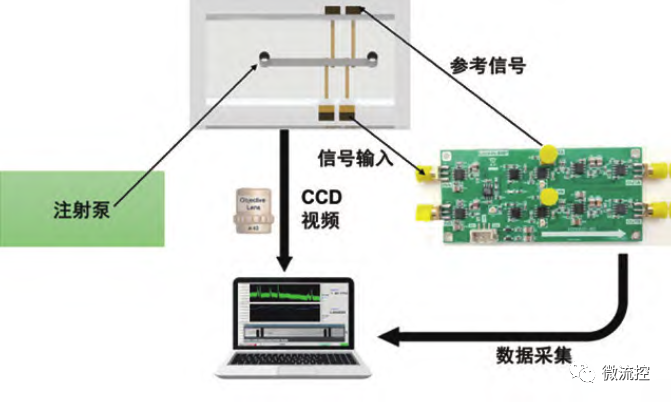
图3 流式阻抗检测系统
不同粒径微球的区分
采用直径分别为5μm和10μm的聚苯乙烯微球进行实验,分别取728和797个点进行统计,得到电不透明度-低频幅值散点图及电不透明度和低频幅值直方图(图4(a))、幅值的均值及标准差(图4(b))。两种粒子低频幅值差异明显、重叠较少,可进行有效区分,验证了该系统具有根据电学特征区分粒子体积的功能。电不透明度反映样品内容物的信息,两者均为同等材质的微球,故通过电不透明度无法区分。
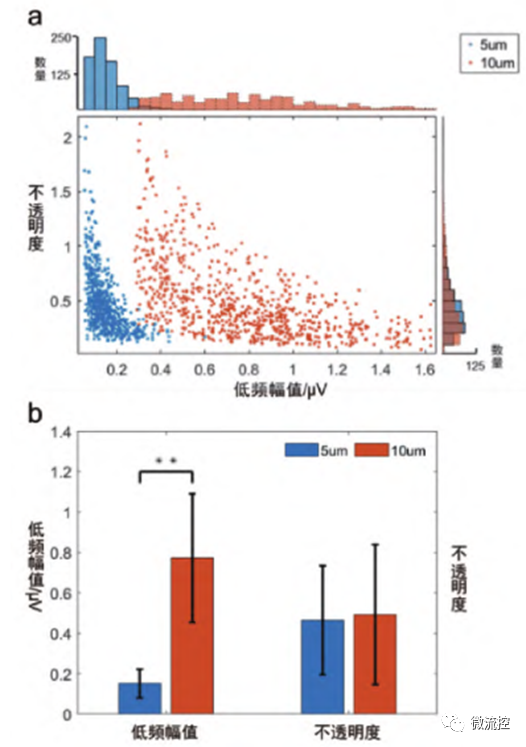
图4 不同粒径聚苯乙烯微球检测:(a)电不透明度-低频幅值散点图及电不透明度和低频幅值直方图;(b)幅值的均值及标准差
相似粒径微球和细胞的区分
为验证系统对相似粒径不同粒子的区分能力,采用HEPG2肝癌细胞和10μm的聚苯乙烯微球进行实验。HEPG2肝癌细胞的尺寸约12μm。分别取755和797个点进行数据处理,获得电不透明度-低频幅值散点图及电不透明度和低频幅值直方图(图5(a))。结果显示,在粒径上区分不开的两种微粒,可以通过电不透明度区分,电不透明度反映了颗粒内容物的信息,细胞与微球内容物的确不一样,两者电学差异较大,实验结果与实际相符。
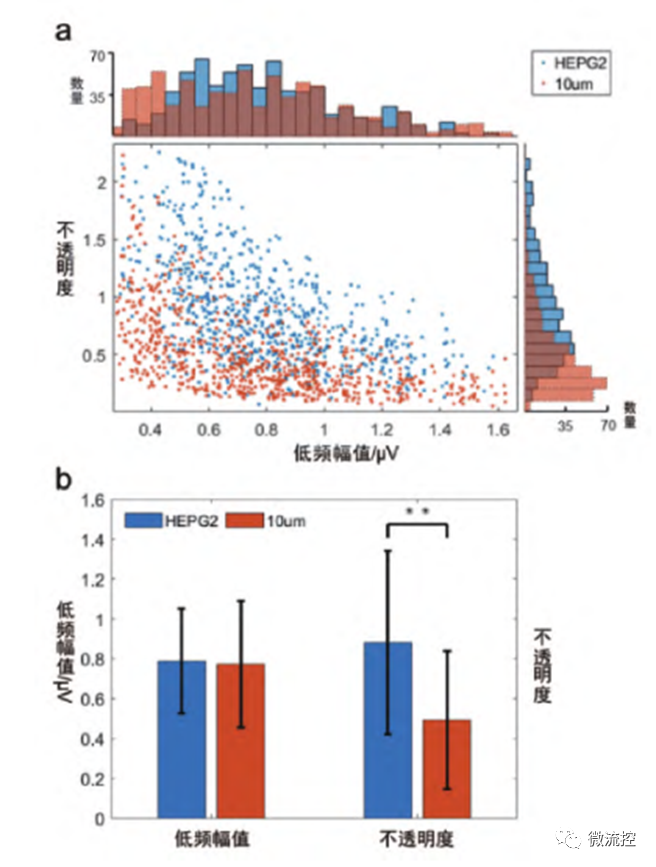
图5 相似粒径聚苯乙烯微球和细胞检测:(a)电不透明度-低频幅值散点图及电不透明度和低频幅值直方图;(b)幅值的均值及标准差
综上所述,该研究通过自行搭建的微流控阻抗流式系统,实现了对不同粒径的聚苯乙烯微球和细胞的无标记检测。锁相放大电路可以实现微粒信号的放大并通过算法提取。通过聚苯乙烯微球和细胞验证了系统的性能。5μm微球低频幅值与10μm微球差异明显,HEPG2肝癌细胞电不透明度与10μm微球比较具有一定差异,表明该系统具有根据电学特征区分粒子体积和内容物的功能,为微流控阻抗流式研究开辟了一个有应用前景的平台。
论文链接:
https://doi.org/10.20027/j.gncq.2022.0052
审核编辑 :李倩
-
一种简便的GPS车辆跟踪系统,不看肯定后悔2021-05-18 1026
-
一种用于胸腔监测的电阻抗成像系统2009-08-14 953
-
适用于家庭健康检测的生物电阻抗测量系统2010-07-13 610
-
一种简便的基于ARM的嵌入式应用开发模式2017-09-22 849
-
一种新型的便携微流控空气取水设备2018-03-07 1223
-
探讨微流控技术在生物传感检测领域的广泛应用2018-08-12 3864
-
一种用于外泌体分离富集和检测的微流控芯片2018-12-31 5536
-
一种新型的微流控-电化学检测系统2021-05-30 4183
-
一种基于微流控的血管芯片模型设计2023-03-09 2543
-
一种多层纸基微流控芯片设计2023-04-21 4076
-
介绍一种高通量多重比色离心微流控芯片2023-06-29 2356
-
介绍一种高灵敏度多靶标核酸检测微流控芯片2023-08-16 2830
-
介绍一种用于绝对定量的微腔式数字PCR微流控芯片2024-03-04 2401
-
基于一种AI辅助可穿戴微流控比色传感器系统2024-06-29 12454
-
基于细胞微流控的阻抗测试解决方案2025-07-02 1499
全部0条评论

快来发表一下你的评论吧 !

