

电极电位影响锂金属负极可逆性
描述
01
导 读
锂金属电池是一种很有前途的储能技术,可以满足高能量密度的需求。然而,由于电解液不断分解,它们的循环库仑效率(CE)较低。提高固体电解质间相(SEI)的稳定性,能够抑制电解质分解,提高库仑效率。然而,仅凭SEI形貌和化学组成不能解释库仑效率的不一致性。
02
成果简介
近日,Nature Energy上发表了一篇题为“Electrode potential influences the reversibility of lithium-metal anodes”的文章,该文章证明在不同电解质中,锂电极电位的移动(>0.6 V)与Li+配位结构高度相关,从而影响锂电镀/剥离的库仑效率。机器学习回归分析和振动光谱分析表明,离子对的形成是提高锂电极电位的关键,即削弱锂的还原能力,从而导致电解液分解减弱,获得高的库仑效率。因此,设计了各种具有增强离子配对结构的电解质,来显著提高库仑效率(>99%)。
03
关键创新
(1)本研究证明,Li+与反阴离子的配位状态与ELi高度相关;
(2)较高的ELi导致Li金属负极获得较高的库仑效率;
(3)Li+配位态的光谱特征可以一定程度上反映ELi,这将有助于设计高库仑效率的锂金属负极电解质。
04
核心内容解读
1. 电极电位与锂金属稳定性
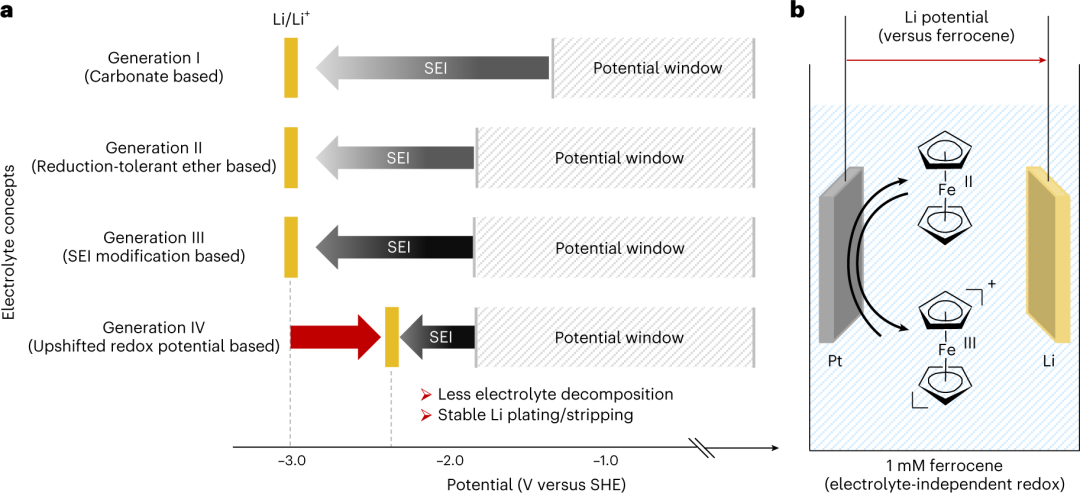
图1. (a)锂金属电池电解液概念的历史。锂金属负极的电极电位远离非水电解质的电位窗口,导致低的库仑效率,伴随电解质严重的还原分解。本文的目的是提高锂的电极电位,从而削弱锂的还原能力,抑制电解质分解;(b)测量各种电解质中锂电极电位的电化学电池示意图。@Springer Nature
金属锂是高能量密度可充电电池的理想负极,因为它具有较高的理论容量(3860mAh g-1)和较低的电极电位(-3.04 V相比标准氢电极)。但其低的库仑效率(CE)是其实际应用的最大障碍。低库伦效率归因于Li/有机电解质界面的热力学不稳定性,因为Li的还原能力强。
锂的电极电位远低于有机电解质的电位窗口(图1a),这导致了电解质的还原分解。在某些情况下,还原产物沉积在Li表面,作为一个导Li+但隔绝电子的界面层,称为固体电解质间相(SEI),它可以有效地延迟电解液的进一步分解。
SEI通常被认为是影响库仑效率的主要因素。为了使SEI的效果最大化,在过去的几十年里,人们设计了多种电解质。首先,有机碳酸盐(例如碳酸丙烯(PC)和碳酸乙烯(EC))被用作溶剂来形成SEI,但得到的库伦效率(<90%)远远低于要求(>99.9%)。其次,开发了醚基电解质(例如四氢呋喃(THF)和1,2-二甲氧基乙烷(DME)),它们表现出较高的还原稳定性,减少了它们的电位窗口和Li电位之间的差距,导致较高的库仑效率。
最先进的电解质设计更多地关注SEI的稳定性,例如浓缩电解质、带有非极性溶剂的局部浓缩电解质和弱溶剂化电解质,它们通常采用LiN(SO2F)2(LiFSI)盐,通过LiFSI的优先还原分解形成富含LiF的无机SEIs,从而获得高的电化学/机械稳定性和≥99%的高库仑效率。
然而,即使存在富含LiF的SEI, 库伦效率(90-99%)也有相当大的变化,这取决于体相电解质。因此,需要探索可能影响库仑效率的其他关键因素。
本工作报道了锂电极电位(ELi)对锂负极库仑效率的影响。电极电位随电解质的不同而显著变化。ELi与电解质中Li+(μLi+)的化学势直接相关。因此,可以通过调节μLi+来控制反映锂还原能力的ELi。如果提高ELi,以减小距离电位窗口的间隙,就可以减少电解液分解,这将大大提高Li负极的库仑效率(图1a)。例如,具有0.3 V高电极电位的Na金属负极获得了超高的库伦效率(≥99.9%)。Li4Ti5O12通过将电极电位提高到浓缩水系电解质的电位窗口中,实现了高度可逆的Li+插层。
2. 精确测量ELi
本工作测量了74种不同电解质中的ELi(图1)。作为国际化学联合会(IUPAC)推荐的电极电位内部标准,二茂铁(Fc,~1 mM)被引入到所有电解质中。假设Fc/Fc+的电极电位恒定且与电解质无关,那么就可以使用Fc/Fc+作为参比电极电对测量ELi(图1b)。
接下来,将74种不同的电解质(不含Fc)应用于Cu|Li电池中,测试铜上电镀/剥离锂反应的库仑效率(图2和图3)。在0.5 mA cm−2下镀锂1 h,然后在相同电流密度下脱锂至截止电压0.5 V。每种电解质选择三个电池来计算第2到第20个循环的平均库仑效率。为了与锂金属电极的标准电解质数据进行比较,ELi(V vs Fc/Fc+)被转换为ELi(V vs Li/Li+ in 1m LiFSI/DME (−3.40 V vs Fc/Fc+))。
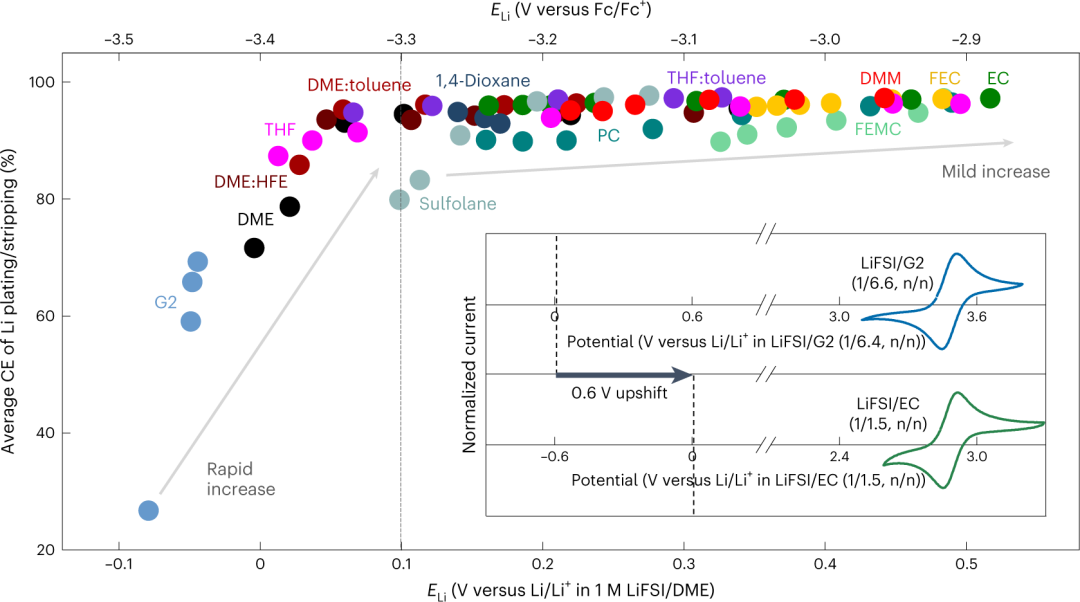
图2. 通常,在高ELi的电解质中观察到高库仑效率。在相同的条件下,使用Li|Cu电池进行电镀/剥离试验。从第2个循环到第20个循环,计算三个电池的平均库仑效率。插图:二茂铁在给定电解质中的循环伏安图。@Springer Nature
3. 库仑效率与ELi的相关性
图2为74种不同电解质中电镀/剥离锂的ELi与平均库伦效率的关系。总的来说,平均库仑效率随ELi的增加而增加,说明在ELi较高时(Li的还原能力较低),电解质的还原分解受到抑制。在此基础上,设计一种ELi>−3.3 V vs Fc/Fc+的电解液,以达到较高的平均库仑效率>95%。
值得注意的是,即使在相同的ELi下,库仑效率也因所用溶剂的不同而不同;醚类溶剂在−3.3 V(vs Fc/Fc+)下,库伦效率>90%,但环丁砜导致库伦效率低至约80%。这归因于电势窗口的差异(即溶剂热动力学电势窗口和ELi之间的差距)和SEI性质。对于醚类溶剂,在还原方向上具有较宽的电位窗口,−3.3 V的ELi(vs Fc/Fc+)足够高,以缩小ELi与溶剂电位窗口之间的差距。
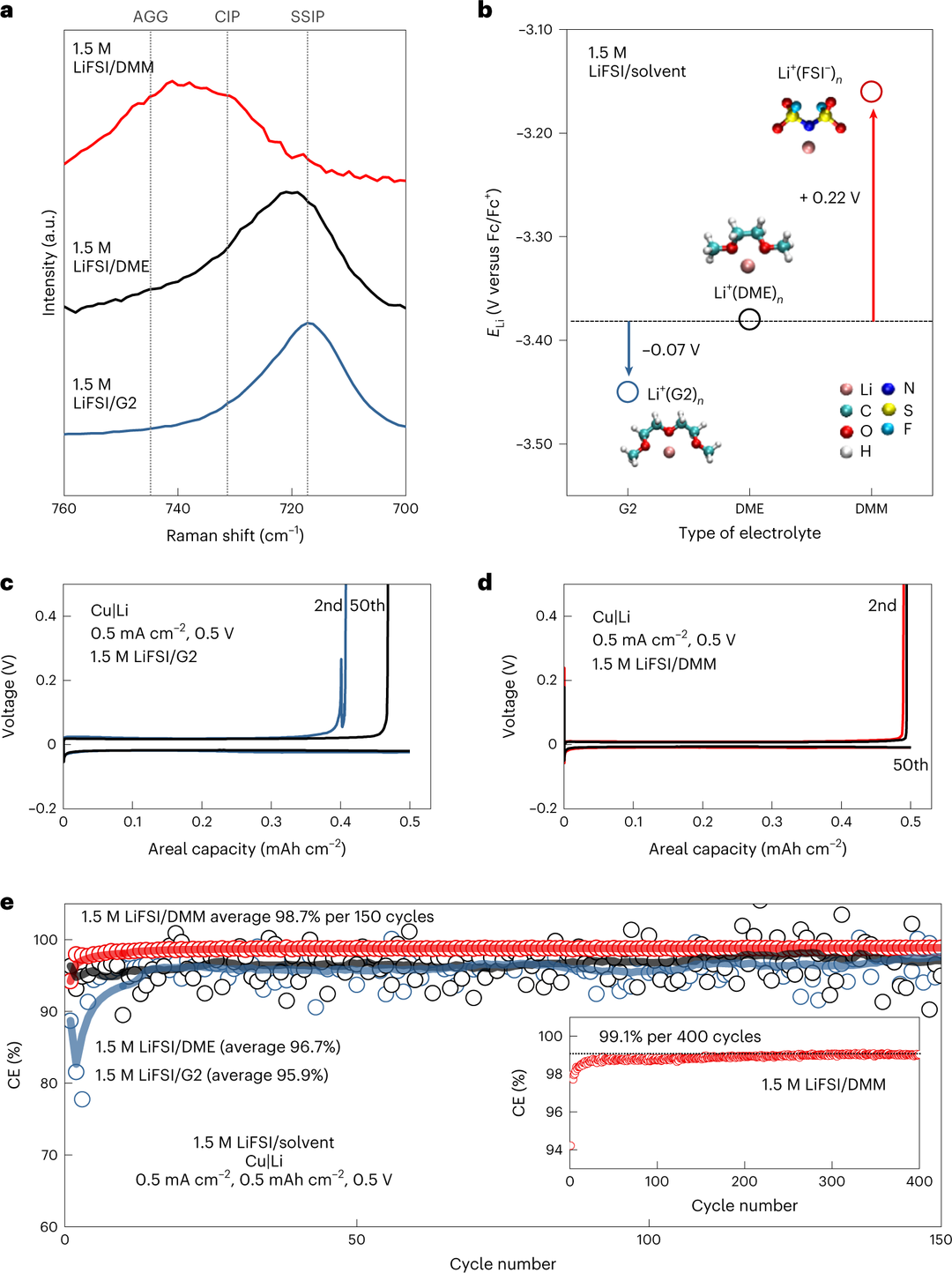
图3. (a)1.5 M LiFSI/G2、1.5 M LiFSI/DME和1.5 M LiFSI/DMM的拉曼光谱。峰位置在700 cm-1到760 cm-1之间代表了Li+和FSI-离子对的配位条件;(b)相对于Fc/Fc+的ELi;(c,d)电解液为1.5 M LiFSI/G2(蓝色)和1.5 M LiFSI/DMM(红色)时,Cu|Li电池的电压曲线;(e)在具有不同电解质的Cu|Li电池中,测量锂电镀/剥离反应的库伦效率。@Springer Nature
为了更清楚地证明ELi对库仑效率的影响,选取了三种具有相似电位窗口的醚类电解质:1.5 M LiFSI/二甘醇二甲醚(G2)、1.5 M LiFSI/DME和1.5 M LiFSI/二甲氧基甲烷(DMM)。这些电解质的ELi值差异显著:−3.45 V、−3.38 V和−3.16 V(vs Fc/Fc+),分别对应-0.05 V、0.02 V和0.24 V(vs Li/Li+ in 1 M LiFSI/DME)(图3b),这是由于Li+的不同溶剂化能导致。Cu|Li电池的库伦效率如图3c-e所示。在1.5 M LiFSI/G2中,ELi(vs Fc/Fc+)最低,为−3.45 V(−0.05 V vs Li/Li+ in 1 M LiFSI/DME),观察到库仑效率显著波动,表明电镀的Li与电解质之间存在不稳定性。
在ELi(−3.38 V vs Fc/Fc+)略高的1.5 M LiFSI/DME中(0.02 V vs Li/Li+ in 1 M LiFSI/DME),仍观察到库仑效率波动,但略有改善。然而,在1.5 M LiFSI/DMM中,ELi(vs Fc/Fc+)最高,为−3.16 V(0.24 V vs Li/Li+ in 1 M LiFSI/DME),观察到高度稳定的Li电镀/剥离行为,在400次循环中,库仑效率显著提高,平均库仑效率达到99.1%。
接下来,讨论ELi对电解质的依赖性。ELi通过测量六个相(I、II、III、IV、V和VI)组成的电池的电动势得出。T(I)|Pt(II)|Fc,Fc+,Li+(III)|Li+,SEI(IV)|Li(V)|T(VI),其中T(I)和T(VI)表示电池的两个金属端。在此基础上,推导出ELi如下:
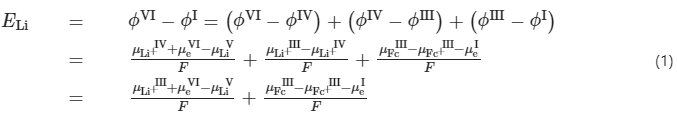
其中φ、μ和F分别为各相(I、II、III、IV、V、VI)的内势,各相中各物种的化学势和法拉第常数。根据IUPAC拟定的标准,假设Fc/Fc+的氧化还原电位是一个常数,与电解质组成无关。此外,μeVI和μLiV也不依赖于所使用的电解质。在此基础上,ELi如下所示:

值得注意的是,ELi与SEI(μLi+IV)中Li+的化学势无关。观察到的ELi变化是由电解质中Li+的化学势(μLi+III)不同引起的。
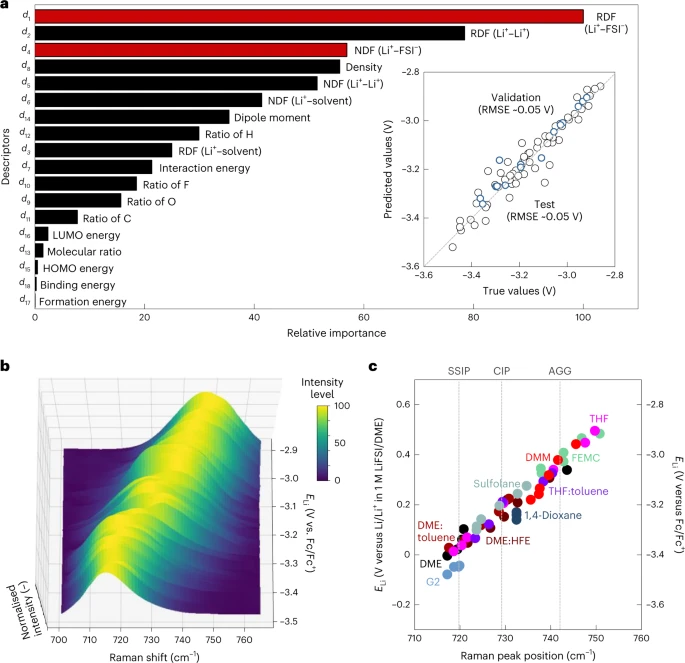
图4. (a)通过基于机器学习的PLS回归分析得到ELi的归一化预测函数系数。ELi的预测值和观测值之间的相关性以一个带有均方根误差(RMSE)的插图表示。蓝色和黑色的圆圈分别代表基于验证和测试数据的预测值;(b)各种电解质的拉曼光谱按其固有ELi值的顺序绘制。在700-760 cm-1(S-N-S拉伸振动模式,vs(S-N-S))范围内FSI−阴离子的峰位置代表了Li+-FSI−的离子配对状态;(c)各种电解质的ELi与FSI-阴离子的拉曼峰位置的关系。@Springer Nature
4. ELi的机器学习回归分析
根据定义,μLi+III表示在电解液中加入无穷小量的Li+时,摩尔吉布斯自由能的变化。由于Li+与溶剂分子或反阴离子结合,其配位环境会影响μLi+,进而影响ELi。为了证实这一点,使用偏最小二乘(PLS)回归和计算导出的描述符集(如径向分布函数(RDF)、成分、密度、偶极矩和最高占用分子轨道(HOMO)/最低未占用分子轨道值(LUMO))对描述符进行机器学习回归分析。
图4a的插图显示了回归结果的诊断图,结果显示验证数据和测试数据得到的实验ELi和PLS预测的ELi之间有很好的一致性(均方根误差,~0.05 V)。图4a将归一化预测函数系数按降序排列,说明Li+周围的配位环境(特别是与FSI−阴离子的配位)与ELi高度相关。
在此背景下,还利用拉曼光谱分析了Li+-FSI−在各种电解质中的配位状态。图4b、c显示了FSI−阴离子的拉曼光谱及其峰位置,结果表明存在Li+-FSI−离子配对。值得一提的是,在各种电解质中,拉曼峰位置与ELi密切相关。随着FSI−更多地与Li+配对,即从溶剂分离的离子对(SSIPs;没有FSI-配位的溶剂化Li+)到接触离子对(CIPs;Li+配位的FSI−)和聚集体(AGGs;(离子对的聚集),ELi增加。这种相关性与基于机器学习的预测相一致,即Li+的离子配对状态决定了μLi+,同时也决定了ELi。
5. 验证和一般含义
配位态、ELi和库仑效率之间的关系为制定合理的锂金属电池电解质设计策略提供了清晰的思路。如图2和图4所示,在低ELi范围内(从−3.5 V到−3.3 V vs Fc/Fc+,相当于−0.1 V到0.1 V vs Li/Li+ in 1 M LiFSI/DME),平均库仑效率迅速增加,其中配位态开始由离子对(CIPs)主导。
但在高ELi范围内(从−3.3 V到−2.9 V vs Fc/Fc+,相当于0.1 V到0.5 V vs Li/Li+ in 1 M LiFSI/DME),这一趋势有所减缓,配位状态从CIPs过渡到AGGs。这表明电解质的设计应使阴离子与Li+配位(至少在CIPs状态下),以达到95%的库仑效率。
用最先进的电解质(弱溶剂化电解质、浓缩电解质和非极性溶剂局部浓缩电解质)有望提高锂电镀/剥离的库仑效率。首先,弱溶剂化电解质促进CIPs和AGGs的形成,从而提高ELi,增加库仑效率。在1.5 M LiFSI/G2、1.5 M LiFSI/DME和1.5 M LiFSI/DMM中,可以清楚地观察到这一趋势。
最后,电解质驱动电位上升的概念可以推广到浓缩电解质和带有非极性溶剂的局部高浓电解质(例如高氟醚和甲苯,它们不与Li+溶剂化),两者的作用都类似于弱溶剂化电解质。随着盐浓度的增加或引入非极性溶剂,FSI−的拉曼峰逐渐从低波数范围(~720 cm−1;SSIPs)到更高的波数范围(>730 cm−1;CIPs和AGGs),也增加了ELi和库仑效率(图4b,c)。
05
成果启示
本研究表明,锂金属的热力学电极电位(ELi)对锂电镀/剥离的库仑效率有很大影响。具有高ELi的电解质削弱了Li金属的还原能力,使电解质的还原分解最小化,从而导致高库仑效率。基于机器学习的回归分析显示,ELi在很大程度上受到Li+-FSI−相互作用的影响。
溶剂化能顺序为:G2>DME>DMM。1.5 M LiFSI/G2、1.5 M LiFSI/DME和1.5 M LiFSI/DMM的FSI−拉曼峰分别位于718 cm−1、720 cm−1和740 cm−1;此外,离子配对的程度为G2
相应的,ELi与FSI−的拉曼位移密切相关,这代表Li+-FSI−离子配对程度。基于这些理解,分别使用强离子对LiFSI/DMM和LiFSI/DME:甲苯两种电解质实现了高度可逆的Li电镀/剥离(>99%)。这项工作并没有否定SEI的贡献,它在动力学上能够抑制电解质分解。离子对的形成可能会增加带负电荷的负极表面FSI-阴离子浓度,从而促进FSI-衍生SEI的形成,抑制SEI的膨胀。然而,即使存在FSI-衍生的SEI, 库仑效率也随着ELi的增加而显著提高。本工作发现的热力学指标将为设计下一代锂金属电池电解质提供新的机会。
审核编辑:刘清
-
关于锂电池电极材料SEM测试、氩离子截面解剖电极片2017-07-07 0
-
锂离子电池电极材料中的交叉效应研究2022-08-30 0
-
负极材料的性能和一般制备方法2009-10-26 1068
-
制约锂负极可充性的本质因素有哪些?2018-09-10 4548
-
宁德时代新专利利用负极电位安全阈值与负极电位估计值的大小关系2021-04-12 2142
-
电极电位和负极材料决定SEI结构演化的研究2022-09-15 2426
-
如何准确评估实际锂金属电池的可逆性呢2022-11-08 778
-
无氟SEI实现高度可逆的金属钠负极2022-11-18 1099
-
打开稳定低温锂金属负极的极化和可逆性限制2023-04-04 766
全部0条评论

快来发表一下你的评论吧 !

