

无氟SEI实现高度可逆的金属钠负极
描述
01
研究背景
金属钠负极的低还原电位和高理论容量使其有望实现高能量密度金属钠电池(SMBs),但其商业化面临诸多挑战,这些挑战与电解质相容性和负极界面现象相关。
与金属锂负极不同,在使用传统碳酸盐电解质时,金属钠负极的固体电解质界面(SEI)稳定性较差。这些电解质的自发化学还原导致不稳定的钝化膜,反复暴露负极到大量电解质溶液中,通过消耗活性材料加速电池失效。
与锂类似,金属钠负极也表现出枝晶形貌,导致长循环稳定性较差。此外,这些枝晶还可能导致电池自发短路和安全问题。因此,需要对电解质进行优化,以实现稳定的钠金属负极。
02
成果简介
近日,阿贡国家实验室Christopher Johnson教授和加州大学Vincent Lavallo教授在Angew上发表了题为“A Carboranyl Electrolyte Enabling Highly Reversible Sodium Metal Anodes via a “Fluorine-Free” SEI”的论文。该论文提出了一种采用 [HCB11H11]1-(1)作为阴离子的新型无氟电解质。
用这种电解质组装的Na对称电池在2.0 mA cm-2下表现出极低的过电位,为0.032 V,在半电池构型中具有99.5%的高库仑效率。循环后电极表面没有钠枝晶成核,并形成了稳定的无氟SEI。
03
研究亮点
(1)本工作首次报告了一种非氟化弱配位阴离子(WCAs),它使金属钠负极的循环库伦效率高达99.5%,具有优异的长循环稳定性。
(2)电解质表征结果显示,溶剂分离离子对和阴离子的异常分布决定了电解质的原位溶剂化结构。电极表面表征显示,在长循环过程中没有枝晶状金属钠成核。钝化膜的XPS表征显示,SEI主要由有机物种组成,含硼物种的数量可以忽略不计。
(3)电解质原位溶剂化结构的表征证明,阴离子的还原稳定性以及1的弱配位性,是获得高可逆金属钠负极的关键。
04
图文导读
[Na]+[HCB11H11]-通过HNMe+1与NaH在四氢呋喃中反应得到(图1a)。与典型的盐复分解方法相比,这里采用的合成策略只产生气态的副产物,以及Na1。Na1在二乙二醇二甲醚(G2)中的溶解度限制在~0.93 M,不能制备1.0 M标准电解质溶液。因此,本研究制备了0.9 M Na1溶液,得到Na1/G2作为电解质(图1b)。
通过同步辐射小角X射线散射(SAXS)实验与分子动力学模拟,对Na1/G2的原位溶剂化结构进行严格的表征。在高q区观察到的两个峰表明,阴离子进入两个不同的环境。多数阴离子-阴离子分隔距离为6.04 Å和11.5 Å(图1c, d)。第一个峰(6Å)对应于最接近的阴离子,它们之间没有溶剂,导致形成小的阴离子-阴离子聚集体。
由于Na1在0.9M二乙二醇二甲醚溶液中均匀分布,第二个峰(12Å)来自于阴离子的长程相互作用(图1e)。在计算模型中发现,Na1/G2含有<1%的Na+-碳硼烷接触离子对(CIP)。Na1/G2中的Na+溶剂化结构倾向于形成丰度大于99%的溶剂分离离子对(SSIP)。
电解质的固态晶体结构显示,饱和Na+络合物[Na(G2)2]+与碳硼酰B-H之间最近的相互作用距离为4.945 Å,说明Na1/G2中离子显著解离(图1b)。因此,电解质完全由离散的[Na(G2)n]+络合物和碳硼烷阴离子组成,它们在溶液中分布不均匀。
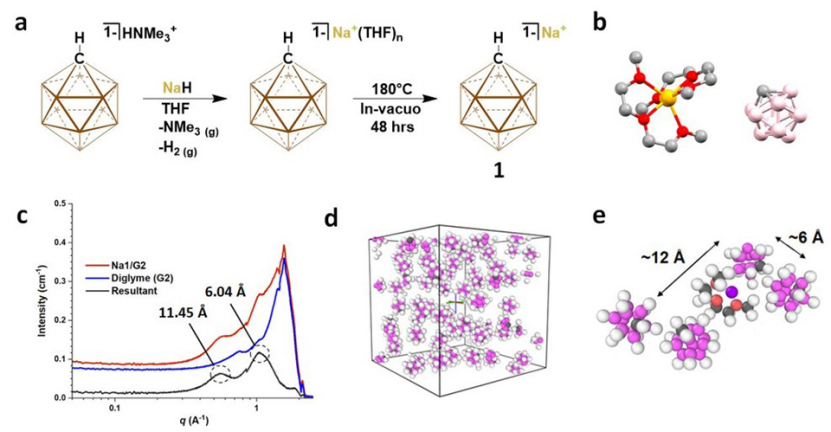
图 1、(a)通过HNMe3+1与NaH的脱质子化,合成和制备Na1。(b)通过单晶X射线衍射分析确定的Na1/G2分子结构。(c)SAXS光谱表征了Na1/G2中原位阴离子-阴离子分离和阴离子团簇的存在。(d)分子动力学系统中阴离子分散的照片和(e)阴离子-阴离子分离的放大图像。
图2显示,含Na1/G2的Na-Na电池在0.5 mA cm-2下显示出稳定的<10 mV极化。从循环开始到超过1000小时,该电位一直保持稳定,这表明Na1/G2的自发化学还原足以稳定地生成SEI(图2)。同样,Na-Na电池在1.0和2.0 mA cm-2下也能稳定循环,极化电压分别为15 mV和32 mV(图2)。

图 2、在不同电流密度和1.0 mAh cm-2面积容量下,采用Na1/G2电解质组装的Na-Na对称电池的循环性能。
接下来,组装了含Na1/G2的Na-Cu和Na-Al半电池,以评估裸集流体上的钠电镀和剥离过程。Na-Cu半电池的首圈库仑效率为96.5%,第二圈循环库仑效率为99.2%,这表明几乎不需要对电极表面进行修饰就可以实现高效的金属电沉积(图3a)。在前100个循环中,平均库仑效率保持在99.8%,在300个循环后,平均库仑效率保持在99.5%。
与对称电池相似,从第一个循环开始,铜电极上钠沉积和剥离表现出低的电压极化(图3b)。长循环后,电压极化逐渐增加,从第一圈的30.5 mV增加到300圈的45.2 mV。
这可能是由于铜电极上重复形成新的钠金属,G2的化学还原,以及溶剂消耗导致的电池内阻增加。沉积后拆卸的半电池显示出均匀的纯金属钠层,具有金属光泽,表明电解质和沉积的金属钠之间发生了最小的副反应(图3a插图)。
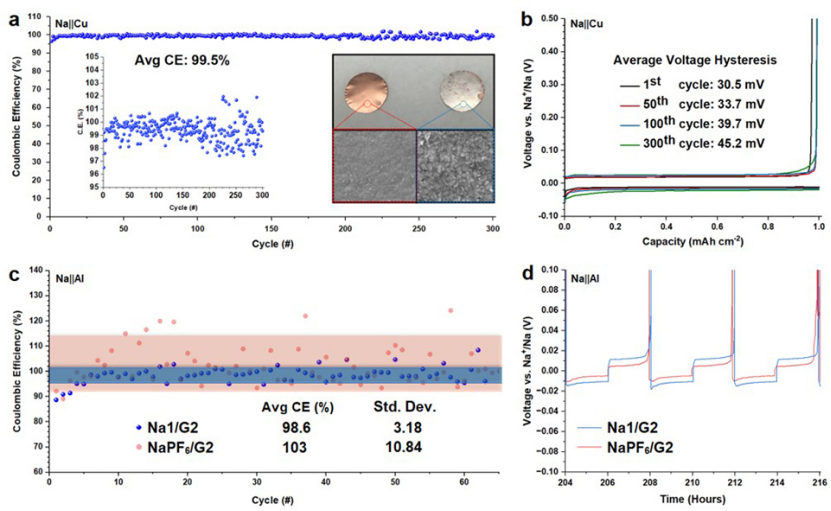
图 3、(a) 运行超过300次后,使用Na1/G2的Na-Cu半电池的库仑效率(CE)。Na-Cu半电池中原始铜电极和沉积1.0 mAh·cm-2Na在铜基底上后的照片,下面是对应电极表面的扫描电镜图像。(b)在0.5 mA·cm-2@1.0 mAh·cm-2下,含Na1/G2的Na-Cu半电池电压曲线。(c)Na-Al半电池的库伦效率和(d)含有Na1/G2和NaPF6/G2的Na-Al半电池电压曲线。
在Na1/G2组装的Na-Al半电池中观察到极高的库仑效率(98.6%),而在NaPF6/G2电解液中,电池放电容量不稳定,循环稳定性差(图3c),这表明化学惰性的Na1/G2与裸铝电极具有较高的兼容性,尽管NaPF6/G2在循环过程中表现出略低的过电位(图3d)。相比之下,1的高化学和电化学稳定性消除了Al和电解液之间的有害副反应。
接下来,通过扫描电子显微镜(SEM)和能量色散X射线能谱(EDS)映射来表征金属钠在Na1/G2中的成核过程,以揭示这种高度可逆行为的起源。研究了金属钠在不同荷电状态(SOC)下的成核过程,结果显示该过程没有枝晶状钠沉积(图4a-c)。在20%荷电状态下(0.2 mAh cm-2),铜电极表面有均匀的金属钠沉积薄层(图4b, d)。在满电状态下(1.0 mAhcm-2),可以观察到同样均匀的金属钠沉积(图4c, f)。
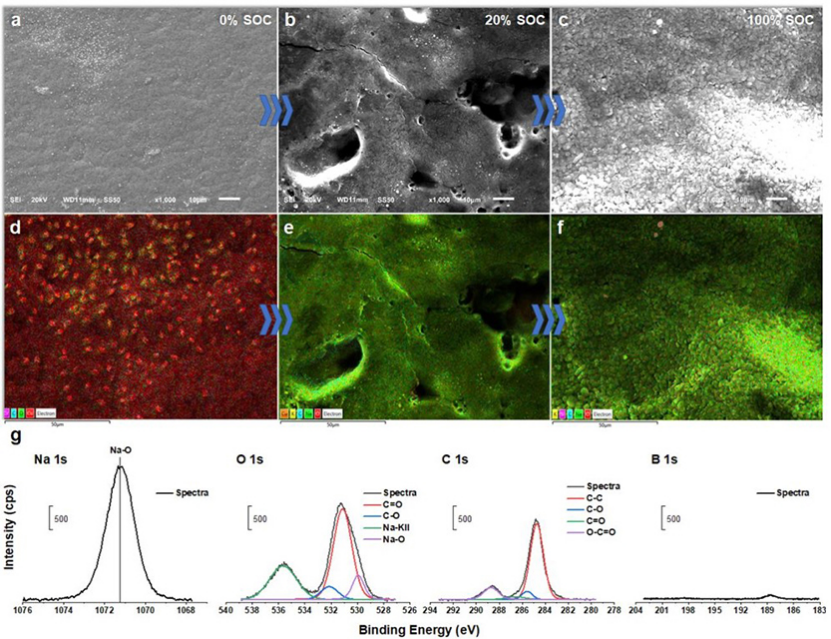
图 4、Na-Cu半电池在不同荷电状态下的SEM图像和相应的EDS映射。(a, d)0% SOC,原始Cu电极(b, e)20% SOC, 0.2 mAh cm-2和(c, f)100% SOC, 1.0 mAh cm-2。(g)从拆卸的Na-Cu半电池中回收的钠金属负极XPS光谱。
表面XPS分析显示,沉积的Na表面上的物质主要由含有Na-O, C-O, C-C和C-H的物种组成(图4g)。在表面检测到非常少量(约2.8%)的含硼物种,这与与原始1相关的B-H结合能相对应,表明簇的完整性保持。
05
总结与展望
本工作首次报告了一种非氟化弱配位阴离子(WCAs),并制备了Na1/G2电解液,它使金属钠负极的循环库伦效率高达99.5%,具有优异的长循环稳定性。采用Na1/G2的电池高度可逆,这可归因于多种因素,包括原位弱离子配位、无枝晶的Na金属成核以及不含阴离子还原产物的SEI。Na-Cu和Na-Al电池的高库伦效率得益于1的化学稳定性,以及仅由二乙二醇二甲醚化学还原形成的SEI。此外,Na1/G2的高热稳定性和导电性使其能够在常温下运行。
06
文献链接
A Carboranyl Electrolyte Enabling Highly Reversible Sodium Metal Anodes via a “Fluorine-Free” SEI. (Angewandte Chemie International Edition, 2022, DOI:10.1002/anie.202208158)
原文链接:
https://doi.org/10.1002/anie.202208158
审核编辑:刘清
-
水系电池金属负极腐蚀问题综述2025-02-18 2098
-
p-π共轭有机界面层助力钠金属电池稳定运行2025-01-14 1582
-
多功能高熵合金纳米层实现长寿命无负极钠金属电池2024-12-18 2957
-
一种新型的钠金属电池负极稳定化策略2024-10-28 2340
-
解锁钠金属电池的超高速率和长寿命2023-10-12 2211
-
基于复合纸的具有自校正功能的金属钠阳极!2023-07-31 2447
-
混合多功能界面作为人工SEI层实现无枝晶、长寿命的金属钠负极2023-06-29 3673
-
打开稳定低温锂金属负极的极化和可逆性限制2023-04-04 2479
-
精细调控金属电结晶形貌有望从根本上实现高度可逆的金属阳极2023-01-31 3698
-
采用二苯甲酮钠实现了HC负极的双功能预钠化2022-11-23 2277
-
关于钠离子电池负极材料,你知道多少2022-10-09 25727
-
钠金属全电池性能研究2022-09-22 2923
-
电极电位和负极材料决定SEI结构演化的研究2022-09-15 4002
全部0条评论

快来发表一下你的评论吧 !

