

开发一种不可燃的液态聚合物电解质
描述
【研究背景】
目前的电池电解质是可燃的,构成了一个重大的安全挑战。无溶剂聚合物电解质的开发就是为了解决这个问题,然而它们没有足够的离子传导性,无法在室温下进行电池操作。虽然凝胶电解质解决了离子导电性的限制,但其中的溶剂分子没有被锚定,安全功能因此受到影响。
【工作介绍】
本工作将溶剂分子与盐和聚合物锚定在一起,可以增加电解质的离子传导性,而不破坏其非可燃性。具体来说,开发了一种液态聚合物电解质,由LiFSI盐、二甲氧基乙烷(DME)溶剂和用离子溶解分子锚定的聚硅氧烷组成。DME与盐和聚合物配位,而与盐一起,它们协同塑化聚合物以增加离子传导性。
由此产生的不易燃聚合物电解质具有1.6 mS/cm的室温离子电导率和25°C-100°C的宽操作窗口。受益于其液体性质,该电解质可以与市面上的电极配对,而无需进一步的电池工程。本工作扩展了聚合物电解质的离子传导范围,并为下一代安全和可制造的电解质显示了一个有希望的设计途径。
【具体内容】
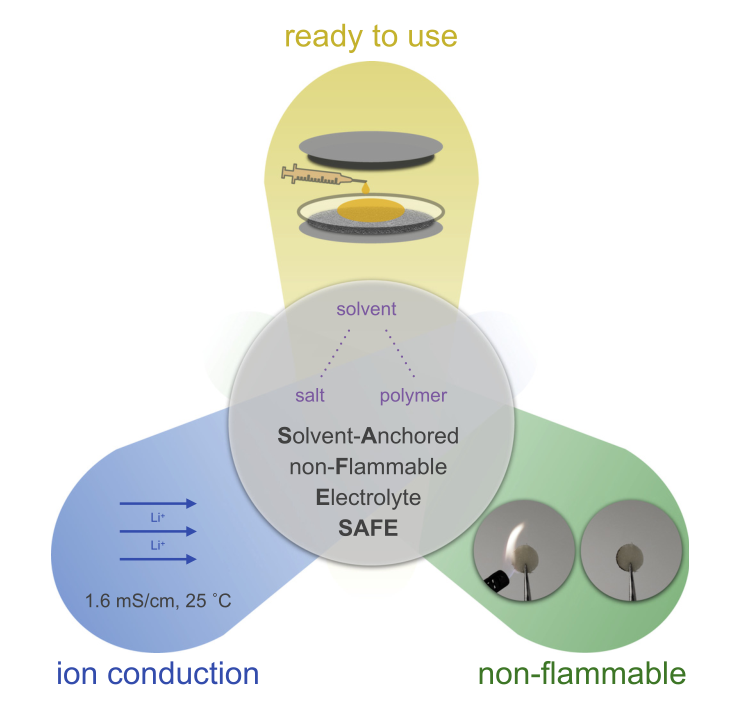
本工作提出了一种基于硅氧烷的聚合物,使用基于离子液体的溶解单元作为聚合物侧链(溶剂锚定不易燃电解质[SAFE])。灵活的低Tg主干促进了聚合物链的运动,提高了离子导电性。通过将离子溶解单元从聚合物骨架移到侧链上,减少了它们的空间阻碍,使盐的溶解度更高,从而进一步提高了离子传导性并降低了这种电解质的粘度。溶剂分子被纳入电解质中,以保持高的离子传导性而不影响其不燃性。这些溶剂存在于与盐和聚合物高度配位的环境中,不会削弱电解质的安全特性。
由此产生的高锂盐含量(盐:单体=8:1)的电解质,在配位的DME(二甲氧基乙烷)分子的存在下,是一种液体,在25℃时的离子电导率为1.6 mS/cm。与固态电解质(陶瓷或聚合物)相比,SAFE很容易与电极形成亲密接触,并且可以与市售的镍-锰-钴(NMC)氧化物阴极配对,无需进一步的电池工程。
通过将离子液体单元拴在聚合物侧链上,而不是使用小分子离子液体,限制了系统中非锂阳离子的移动,实现了高的锂迁移数(∼0.7)。证明了SAFE与NMC阴极和石墨阳极在25°C(C/10和C/3)下的稳定循环,超过400次,容量衰减可以忽略不计。这种电解质可以在广泛的温度范围内以实际的电流密度运行(25℃,0.27 mA/cm2 ,100℃,5.4 mA/cm2 ),并为聚合物电解质设定了导电性和性能标准。
材料设计
设计了一种由非极性硅氧烷骨架和吡咯烷(Py)双(氟磺酰)亚胺(FSI)极性离子侧链组成的两亲性聚合物电解质,如图所示 图1A,将该聚合物命名为PPyMS-FSI。选择硅氧烷骨架是因为它的化学稳定性和链的灵活性。选择PyFSI离子组是因为它的氧化稳定性和溶解盐的能力。
其他基于离子液体的聚合物电解质也得到了研究,特别是以聚合PyFSI离子液体作为聚合物骨架,以LiFSI(PDADFSI-LiFSI)作为盐。本工作聚合物电解质PPyMSMS-LiFSI在25℃时的离子电导率为8.3 × 10−2 mS/cm,较高的电导率源于硅氧烷聚合物骨架的低刚性。在这项研究中,通过将离子溶解基团移到聚合物侧链上,减少了离子液体的空间阻碍,增加了PyFSI单元与盐和溶剂配位的自由度(图1B)。
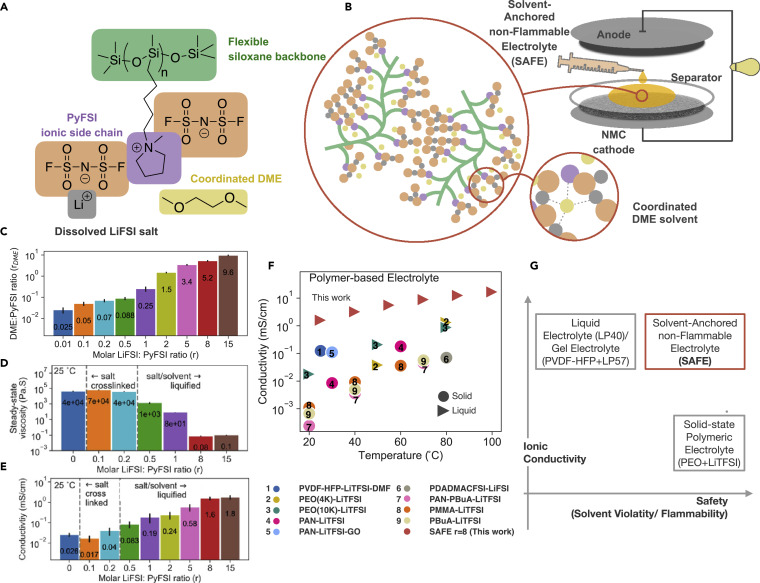
图1.不同盐/溶剂比例的SAFE。
(A)以LiFSI:PyFSI:DME=1:1:1的摩尔比绘制的电解质化学结构示意图。(B)SAFE添加到电池隔膜中,以及复合物的放大漫画(以LiFSI:PyFSI:DME=2:1:1.5的摩尔比绘制)结构。(C)随着盐含量的增加,干燥48小时后电解质中的DME含量。数据以平均值±SD表示。(D) 电解质的离子电导率随着盐含量的增加而增加,在25℃下测量。数据以平均值±SD表示。(E) 电解质的稳态粘度。数据以平均值±SD表示。(F) SAFE r = 8在不同温度下的电导率,并与其他干式盐中聚合物电解质进行比较。(G) 展示SAFE独特优势的示意图。
电解质成分的优化
SAFE是通过将LiFSI盐溶解在DME中和将PPyMS-FSI聚合物溶解在ACN(乙腈)中制备的。在真空炉中干燥48小时后,ACN可以完全去除,DME与聚合物和盐形成配位结构。用1H核磁共振(NMR)对不同盐浓度的电解质进行了定量分析,并在图1C中标记为rDME (DME和侧链的摩尔比)。盐含量r,它被定义为所添加的LiFSI盐和PyFSI聚合物侧链之间的摩尔比。
对于SAFE r = 8电解质,通过将干燥时间从48小时增加到96小时和144小时来优化系统中的DME量。从48小时到96小时,DME量(rDME )从5.25下降到2.53,但粘度从0.08 Pa.S增加到0.20 Pa.S,电导率从1.6 mS/cm下降到0.54 mS/cm。进一步延长干燥时间(144小时)导致盐分沉淀,而没有完全去除DME。在干燥时间为48小时时,体系中的DME是降低粘度和促进离子传导的最佳选择。
液态聚合物电解质
SAFE的机械性能和离子电导率不仅受溶剂的影响,也受盐含量的影响。在25°C时,测量了不同r值的聚合物复合物的稳态粘度(图1D)和离子传导性(图1E)。由于PyFSI侧链的离子性质,对纯PPyMS-FSI聚合物(一种粘稠的液体)的EIS(电化学阻抗光谱)测量显示,在25℃时,离子电导率为2.6 × 10−2 mS/cm。
当少量的LiFSI盐被添加到聚合物基体中时(即r=0.1-0.2),Li+ 与聚合物上的离子侧基建立了多配位结构,从而使聚合物链静电交联,限制了聚合物链的运动。在r = 0、r = 0.2和r = 0.5的复合物上用随频率变化的流变学来表征这种盐交联行为。无盐的聚合物(r = 0)在整个频率范围内显示出液体般的流变特性,损失模量(G″,液体特性)高于储存模量(G′,固体特性),而r = 0.2在8.5 rad/s时有一个G′和G″的交叉,显示出粘弹性固体般的行为。进一步增加盐和溶剂含量(r≥0.5)导致电解质在整个频率范围内再次变成液体,G″高于G′。固/液转换也反映在粘度和离子传导率的变化上:聚合物/盐混合物的稳态粘度从4×104 Pa⋅S(r = 0)增加到7×104 Pa⋅S(r = 0.1),然后下降到8×10−2 Pa⋅S(r = 8);电导率从2.6×10−2 mS/cm(r = 0)下降到1.7×10−2 mS/cm(r = 0.1),然后上升到1.6 mS/cm(r = 8)。差示扫描量热(DSC)曲线中,观察到PPyMS-FSI聚合物的Tg 在-25℃,而SAFE r = 8样品的Tg 在-64℃,接近没有离子相互作用的聚二甲基硅氧烷(PDMS)聚合物的Tg 。这些结果表明,添加的LiFSI盐和DME可以促进聚合物链的运动,限制聚合物侧链之间的离子相互作用。
将盐含量从r = 8增加到r = 15对离子传导性的影响有限。尽管rDME 从5.2增加到9.6,但DME和LiFSI之间的比率仍然相似(r = 8为0.65,r = 15为0.64)。在较低的盐含量r = 5时,DME和LiFSI之间的比率更高(0.68)。这表明在r = 8时已经达到了该系统的盐溶解极限。进一步增加盐含量需要加入相应比例的DME溶剂。
EIS结果通过使用Arrhenius方程拟合r = 8的电导率和温度信息,计算出离子传输所需的活化能为264 meV。当把SAFE r = 8的电导率与其他盐中聚合物电解质进行比较时,这种电解质在25℃至100℃的整个温度范围内显示出最高的离子电导率。
具体而言,最近关于基于PVDF-HFP LiTFSI的聚合物盐基电解质的带有13wt%的残留DMF。该电解质仍然是固体,并显示出0.124 mS/cm的室温离子传导率。对于短链聚乙二醇(聚氧化乙烯[PEO],分子量为10K),它也可以通过添加LiTFSI盐(Li:单体=0.125)来液化,并且在20℃时的粘度为55PaS。然而,由于其有限的离子溶解能力,液化的PEO电解质在30°C时只能达到0.06 mS/cm的离子传导率。
通过调整LiFSI和DME的用量,在不影响电解质安全特性的情况下保留了离子导电性。SAFE同时解决了传统液体/凝胶电解质的溶剂可燃性问题和固态聚合物电解质的离子导电率限制(图1 G)。
FSI、Li和DME的化学环境
锂阳离子和FSI阴离子的化学配位环境随着电解质成分的变化而变化。拉曼光谱可以测量键的特定振动模式的能级偏移,然后可以推断出该键的化学环境的变化。在这个系统中,聚合物的离子侧链和添加的锂盐都含有相同的FSI阴离子。如图所示 图2A中所示,在纯PDMS-PyFSI聚合物中测得的S-N-S键的振动能量为∼711 cm−1 ;在结晶LiFSI盐样品中,该能量为∼762 cm−1 。
这些结果与LiFSI盐和吡咯烷FSI离子液体的S-N-S键拉曼信号相似。随着盐和溶剂含量的增加,S-N-S键信号转移到更高的文数,表明FSI阴离子的配位环境更强。拉曼光谱发现与傅里叶变换红外光谱(FTIR)得到了进一步的证实,观察到含有S-N-S键拉伸振动的区域(图2B)。随着盐含量的增加,FTIR中的键波数在Li与FSI结合的方向上有所增加,但在结晶LiFSI的能量上没有观察到峰值。
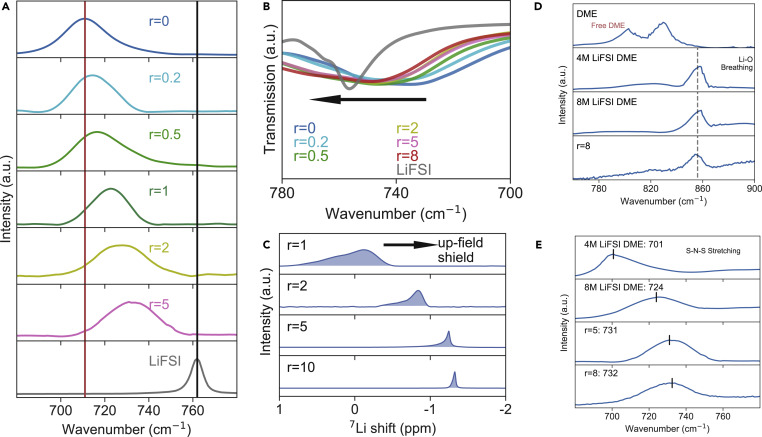
图2.Li+ , FSI− , DME的配位环境。
(A)聚合物-盐复合物的拉曼光谱集中在FSI阴离子上的S-N-S键的振动模式。(B)聚合物-盐复合物的傅里叶变换红外光谱(FTIR)集中在FSI阴离子上S-N-S键的振动模式的信号范围。(C) 在25°C测量的不同盐含量的聚合物的Li核磁共振(NMR)信号。(D) 拉曼光谱聚焦于DME振动,并标出Li-O呼吸键。(E)拉曼光谱聚焦S-N-S键拉伸,与4和8M LiFSIDME溶液(进料成分)相比。
应用核磁共振研究了Li阳离子的化学环境。在图2C中,随着聚合物中盐含量的增加,锂峰呈现出上场转移。上场转移表明,由于周围的电子云密度较高,锂核的屏蔽性更强。与拉曼和FTIR的观察一致,系统中盐含量的增加导致了更配位的溶解环境。随着盐含量的增加,核磁共振峰的宽度下降,这是由于电解质的粘度降低造成的。此外,高盐浓度下Li核的尖锐峰值(r = 8)也表明,添加的Li盐完全溶解在基体中,并存在于一个均匀的化学环境中。
用拉曼光谱对SAFE中DME的溶解环境进行了表征,并与高浓度LiFSIDME电解质进行了比较。图2D显示了DME的振动信号。当DME中没有LiFSI时,纯DME在几个确认中存在,导致两个明显的拉曼峰,其波数低于850 cm−1 。在4和8M LiFSI DME电解质中,Li-O峰出现在856 cm−1 ,表明Li阳离子与DME上的氧进行配位。
在r=5和r=8的电解质中,FSI阴离子的配位环境也与4和8M LiFSI DME电解质进行了比较(图2 E)。当盐浓度从4M增加到8M时,峰值位置从701 cm−1转移到724 cm−1 。与不含聚合物的DME电解质相比,SAFE中的S-N-S拉伸进一步蓝移至>730 cm−1 ,表明PPyMS-FSI聚合物也对高配位环境做出了贡献。
对r=1的电解质(LiFSIDME=10.25)进行了MD模拟,并分析了径向分布函数(RDF)来研究电解质成分之间的相互作用。在短距离(<1纳米),g(r)峰的值大于1,表明感兴趣的两个成分之间的相互作用,因为所选成分在参考成分附近的局部密度大于其在大块电解质中的浓度。
Li+ 与FSI− 中的氧原子和DME中的氧原子都显示出强烈的相互作用,在RDF中有明显的峰值。FSI− 与Li+ 有强烈的相互作用,但与DME没有明显的相互作用。除了与Li+ 相互作用外,还发现DME与聚合物侧链上的Py+ 基团有相互作用。总的来说,MD模拟结果与实验结果一致,即DME被固定在一个高度配位的富盐环境中,并且DME与Li+ 和聚合物都有相互作用。任何两个成分之间的平均力潜力(PMF)可以通过关系w(r)=-kB T ln(g(r))从RDF计算出来。PMF的最小值的大小是对两个成分之间相互作用强度的定量测量。
可以发现,DME上的氧与其他成分的配位性最强,因此被用来计算DME的相互作用强度。计算了Li+ -O(DME)和N(聚合物)-O(DME)相互作用的PMF,发现Li+ -O(DME)的相互作用强度为0.25 kB T,而N(聚合物)-O(DME)的相互作用强度为0.17 kB T。因此,DME与聚合物的相互作用强度略低于DME与Li+ 。这两种相互作用都弱于由Li+ -O (FSI− )PMF代表的离子计数相互作用,后者的强度为1.30 kB T。因此,这些相互作用可能不会强烈阻碍DME或Li+ 在溶液中的移动。
稳定性、反应性和电化学特性分析
选择SAFE r = 8进行进一步的电化学研究。在将其应用于电池的长期循环之前,首先分析了这种电解质在锂-铝电池中的氧化稳定性。对电池进行了线性伏安测试,确定SAFE r = 8电解质的氧化电压为6.7V,与Li (图3A).这样高的氧化电位足以与高电压的NMC电极配对。高氧化稳定性归功于电解质的高盐含量和稳定的成分(离子液体)。
接下来,使用扩散有序光谱(DOSY)核磁共振技术,在80°C测量了锂和氟原子核的迁移数。该电解质的迁移数被计算为0.71,表明该系统中的大部分流动成分是Li+ 。还通过电化学极化测量了Li|Li对称电池的迁移数,迁移数被计算为0.65。这与DOSY-NMR测量值一致,而且,在这两次测量中,都假设遵守了Nernst-Einstein关系,系统处于稀释极限。这是一个简化的模型,没有考虑到未分离的离子对/三联体,但它确实提供了关于电解质中离子运动的有用见解。
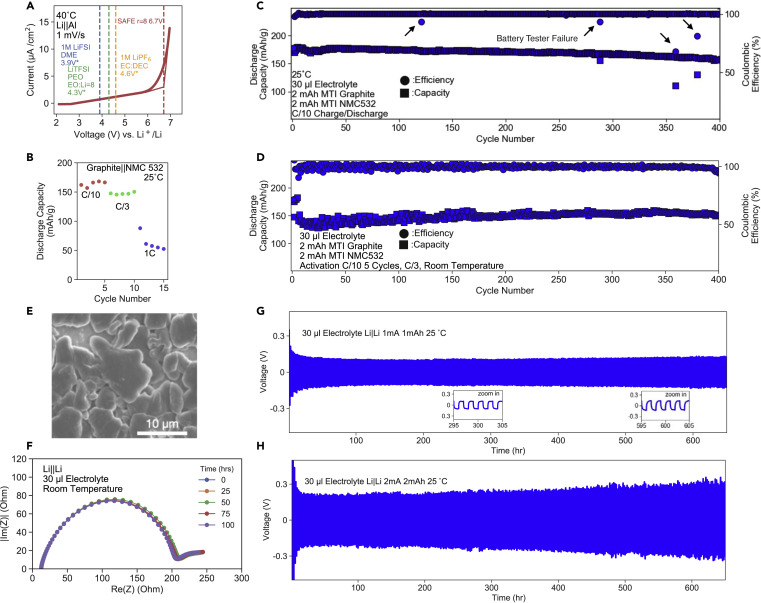
图3.SAFE的稳定性和电化学特性r=8
(A) 在Li-Al电池中对电解质进行的LSV。测得的氧化稳定性与其他普通聚合物/液体电解质的氧化稳定性进行了比较。(B) 石墨|NMC电池的容量与速率。(C)石墨|NMC电池在C/10速率下的长期循环。(D)石墨|NMC电池在C/3速率下的长期循环。(E)裸铜箔上的锂沉积形态的SEM图像(1 mAh/cm2 容量,0.1 mA/cm2 电流密度)。(F) 室温下各种静止时间后,SAFE r = 8的Li|Li对称电池的阻抗测量的奈奎斯特图。(G) Li|Li电池在1 mA/cm2 电流密度、1 mAh容量下的长期循环。(H) Li|Li电池在2 mA/cm2 电流密度、2 mAh容量下的长期循环。
长期的稳定性和电池应用
接下来研究了该电解质在石墨|NMC全电池设置中的循环情况。这种电解质在C/3时有150 mAh/g的容量,在C/10时有170 mAh/g的容量,当与市面上的NMC阴极(MTI,2 mAh/cm2 )配对时。将这些石墨|NMC电池在贫电解质(30μL)条件下以C/10的速率进行循环,400多个循环的容量衰减可以忽略不计(图3c)。对于C/3电池,我们也显示出稳定的长期性能,超过400个周期,没有明显的容量衰减(图3D)。电解质在Li-LNMO电池中循环时也表现出了高电压稳定性。
评估了电解质与金属锂阳极的兼容性。在电流密度为0.1 mAh/cm2 的铜箔上沉积了1 mAh/cm的金属锂2 。金属锂的扫描电子显微镜(SEM)沉积曲线(图3E)表明,沉积的金属锂的形态是颗粒状的和均匀的。放大的SEM图像表明,这种形态在电极上的大面积观察到。
固体-电解质界面(SEI)的稳定性是通过使用EIS测量跟踪Li|Li对称电池在很长一段时间(∼100小时)内的界面阻抗来进一步描述的。在室温下静置100小时后,界面阻抗几乎没有变化,这表明金属锂和电解质之间形成了一个稳定的界面(图3F)。
通过在室温下以不同的电流密度循环Li|Li电池,评估了r=8电解质与金属锂的长期稳定性。在电流密度为1 mA/cm2 ,容量为1 mAh/cm2 ,SAFE r = 8电解质显示出超过700小时的长期稳定循环(图3G)。在更高的电流密度为2 mA/cm2 ,容量为2 mAh/cm2 ,该电解质表现出超过650小时的稳定循环(图3 H)。
表征了金属锂和石墨阳极在不同的C速率下循环后的SEI的化学成分。在C/10或C/3下循环的石墨阳极具有类似的化学成分,其产品来自盐(Li2 O, -SOx )和溶剂/聚合物(-O-C)的分解。在1C速率下,充电/放电过程变成了电容性的,并且阳极表面大部分被有机分解产物(-O-C)覆盖。在金属锂阳极上也发现了类似的趋势,在1C速率下循环的阳极与在C/3或C/10速率下循环的电极相比,其表面化学性质明显不同。具体来说,在阳极表面出现了更多的聚合物物质,可能是由聚合物或溶剂分解产生的,而由盐组成的产品较少(Li2O, -SOx )。在50个循环之前和之后,拍摄了石墨|NMC电池的横截面,在循环之后,SAFE r = 8在电极和分离器上保持湿润。
热稳定性和电解质的操作窗口
对电池的长期热稳定性进行了研究,将电池长期放置在70℃的烘箱中,8天后电导率保持不变。为了证明聚合物对改善电解质的热稳定性和安全特性的影响,还合成了小分子Py12FSI离子液体,并组成了具有相同摩尔比的DME、LiFSI和PyFSI的小分子基电解质,将其命名为SM。
还比较了聚合物和SM电解质的长期热稳定性,SM电解质的电导率在70℃热保持3天后开始下降,而SAFE r = 8的电导率在热保持8天后保持不变。这些电解质的热稳定性是通过可燃性试验进一步评估的。用1 mL SAFE r = 8或碳酸乙烯酯(EC)和碳酸二乙酯(DEC)1M六氟磷酸锂(LiPF6 )10%碳酸氟乙烯酯(FEC)电解质浸泡。
接下来,我们将火焰喷灯放在浸泡过的玻璃棉附近3秒钟,然后移开火焰。对于碳酸酯电解质,燃烧一直持续到所有液体被耗尽。对于SAFE r = 8,只在玻璃棉上观察到轻微的炭化现象(可能是由于盐和聚合物的降解);更重要的是,燃烧没有持续。相比之下,SM电解质是可燃的,燃烧一直持续到所有的电解质被烧成黑色物质。
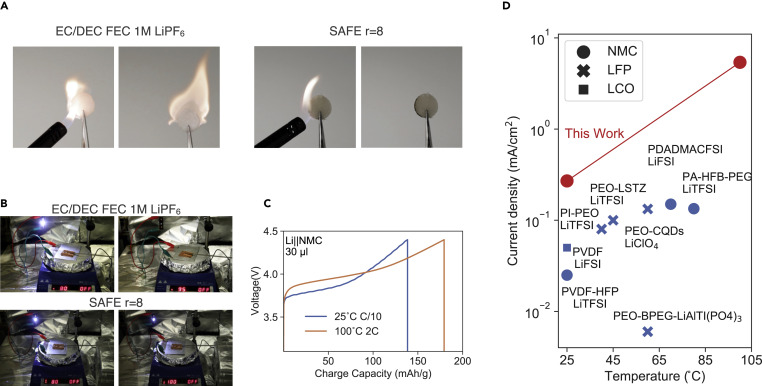
图4.SAFE的热稳定性r = 8
(A)用1 mL SAFE r = 8或EC/DEC 1M LiPF6 10% FEC电解质浸泡玻璃棉的快照。火炬与玻璃棉接触了3秒钟,然后移开。(B) 带有SAFE r = 8或EC/DEC 1 M LiPF6 10% FEC电解质的软包电池在放置在热板上时操作LED灯的快照,图片中标明热板的温度。(C) 含有30μL SAFE r=8、300μm Li阳极和2.7 mAh NMC 532 Li阴极的Li|NMC电池在25℃下以不同的C速率循环。(D) SAFE r = 8的电流密度与文献中其他干式聚合物电解质的比较。
对于基于碳酸酯的电解质,当热板加热到95°C时,LED突然关闭,这很可能是由于电解质蒸发和降解导致软包电池中离子传导通路的损失,使用聚合物基电解质的LED即使在热板温度保持在100°C 6分钟后仍然亮着。
通过记录发生显著产气的温度,进一步证明了SAFEr=8的热稳定性。对于EC/DEC电解质,由于DEC分子的挥发性,观察到软包电池从105°C开始就被溶剂蒸气压胀。聚合物电解质的显著产气发生在比盐分解(140℃)更高的温度(160℃),表明盐分解而不是溶剂产气是电解质热失效的原因。
为了量化聚合物电解质系统中DME溶剂的挥发性,并与其他电解质系统进行比较,用气相色谱室测量了100℃下不同电解质中不同有机溶剂的相对饱和度。通过对气相色谱仪输出的溶剂信号峰的曲线下面积进行积分,并计算出电解质和标准溶剂样品之间的积分比,得到了相对饱和度值。
对于SAFE r = 8的电解质,在真空炉中干燥48小时后,DME的相对饱和度为2%。进一步延长干燥时间到96小时,相对饱和度降低到0.6%。通过测量两种广泛报道的基于PVDF-HFP的凝胶电解质中最低沸点成分的相对饱和度,注意到这种聚合物液体电解质与其他经典凝胶电解质之间的差异。
在这两种情况下,相对饱和度都比我们报道的聚合物电解质要高(38%,80%)。还测量了经典碳酸酯电解质(EC/DEC)和高浓度醚电解质(4M LiFSI DME)的相对饱和度,发现它们的相对饱和度也高了几个数量级(分别为94%,84%)。还发现SM电解质的DME的相对饱和度是SAFE r = 8电解质的2倍多。这一系列的测量表明,聚合物电解质中残留的DME的挥发性明显低于其他凝胶和其他高浓度(基于离子液体)电解质中的有机溶剂。

在25°C和100°C的条件下对NMC锂电池进行了循环测试(图4C)。为了达到目标容量130 mAh/g,在25°C,需要 C/10 ,而在100°C,2C就足够了。这种液态聚合物电解质与市面上的NMC阴极配对在25°C时达到了0.27 mA/cm2 的电流密度,在100°C时达到了5.4 mA/cm2 。
【结论】
作者提出了一个将溶剂分子纳入聚合物电解质的概念,以获得具有高室温导电性的不易燃聚合物电解质。通过采用硅氧烷主干和离子液体功能侧链的两亲聚合物设计,提高了聚合物的盐溶解度。通过调整该电解质中的盐和配位溶剂的含量,最大限度地提高了离子导电性(1.6 mS/cm,25°C),而没有破坏电解质的安全功能或热稳定性。
这种电解质以液态的方式解决了固态电解质(聚合物和陶瓷基)的制造困难,并且可以很容易地与市面上的电极和隔膜整合。该电解质在石墨|NMC全电池中显示出稳定的长期运行,其运行范围为25℃至100℃。聚合物电解质的设计理念使下一代安全聚合物电解质的离子传导性和可制造性得到明显改善。
审核编辑:刘清
-
请问聚合物电解质是如何进行离子传导的呢?2024-03-15 3154
-
高锂金属负极形貌稳定性的聚电解质2023-08-16 2443
-
聚合物电解质离子电导率及界面稳定性的影响因素2023-02-03 5819
-
氟化石墨烯增强聚合物电解质用于固态锂金属电池2022-09-28 4300
-
聚合物固态电解质的合理设计2022-08-18 2048
-
原位固态化聚合物电解质基高性能准固态软包锂电池2022-06-22 11231
-
研究人员开发出一种基于聚合物的固体电解质 可用于生产自我修复商业电池2019-12-25 1150
-
锂电池VS聚合物锂电池,谁才是未来的主角?2018-08-17 7294
-
聚合物锂电池工作原理表现2013-06-14 3960
-
聚合物锂电池的生产2013-05-10 4093
-
对聚合物锂电池的优点和缺点进行分析2012-11-29 5164
-
锂离子电池聚合物电解质导电机理2009-12-09 2821
-
锂离子电池聚合物电解质导电机理是什么?2009-10-29 7793
-
聚合物电池的分类,锂聚合物电池的结构2009-05-24 4168
全部0条评论

快来发表一下你的评论吧 !

