

基于锂化普鲁士蓝类似物的锂离子电池正极
描述
一、全文概要
普鲁士蓝类似物(PBAs)是十分有前途的后锂电化学能量储存的活性材料。然而,由于PBAs在长期循环中的不稳定性,它们通常不适合用于非水锂离子存储。本研究评估了不同锂含量的PBAs用于非水锂离子存储的可行性。通过中子粉末衍射测量确定了锂化PBA的晶体结构,并通过X射线衍射测量和键价模拟研究水对结构稳定性和锂离子迁移的影响。此外,本研究证明了含有Li2-xFe(CN)6⋅nH2O (0≤x≤2)活性材料的正极与金属锂电极和含LiPF6的有机基电解质在纽扣电池配置中的初始放电容量为142 mAh g-1,在1.9 A g-1下循环后的放电容量保持率为80.7%。通过用石墨基负极取代金属锂,本研究还报告了一种能够在190 mA g-1下循环超过370次的纽扣电池,其稳定放电容量约为105 mAh g-1,在25 °C下放电容量保持率为98%。
二、正文部分
01 研究亮点
1、通过中子粉末衍射测量确定了锂化PBA的晶体结构,并通过X射线衍射测量和键价模拟研究水对结构稳定性和锂离子迁移的影响。
2、本研究证明了含有Li2-xFe(CN)6⋅nH2O (0≤x≤2)活性材料的正极与金属锂电极和含LiPF6的有机基电解质在纽扣电池配置中的初始放电容量为142 mAh g-1,在1.9 A g-1下循环后的放电容量保持率为80.7%。
3、通过用石墨基负极取代金属锂,本研究还报告了一种能够在190 mA g-1下循环超过370次的纽扣电池,其稳定放电容量约为105 mAh g-1,在25 °C下放电容量保持率为98%。
02 图文导读
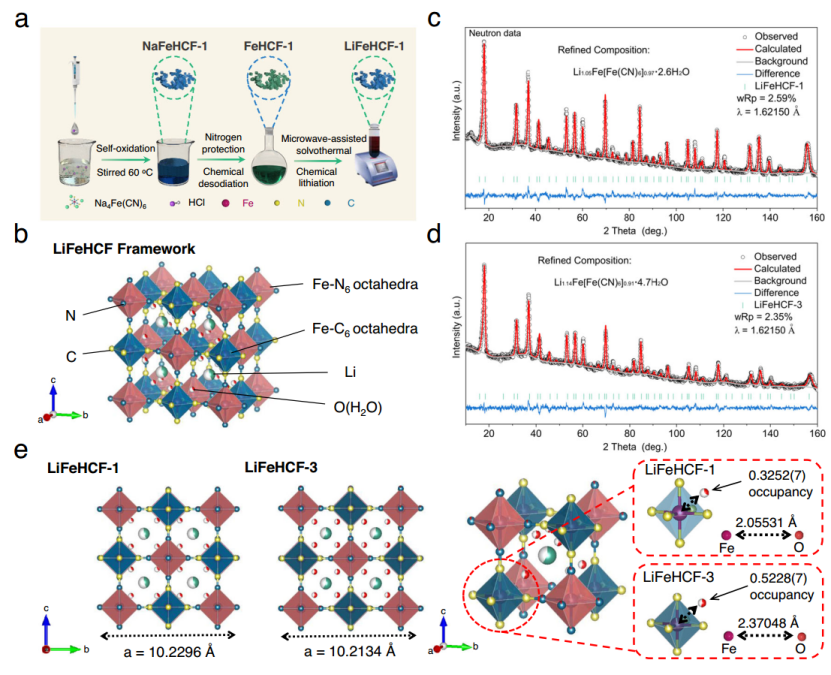
图1|材料合成策略和改进结果。a) LiFeHCF-1样品的合成路线示意图。b)锂化普鲁士蓝的晶体结构。c) LiFeHCF-1和d LiFeHCF-3样品的中子衍射图案和Rietveld细化结果。e) LiFeHCF-1和LiFeHCF-3样品的单元格参数和沸石水与Fe(CN)6八面体之间的配位环境比较。锂、碳、氮、铁(与碳配位)、铁(与氮配位)和氧原子分别以绿色、蓝色、黄色、紫色、深蓝色和红色表示。
本研究通过不同的合成方法系统地制备了一系列具有不同缺陷和水含量的LiFeHCF样品。具体的方法步骤在实验部分进行了描述。简而言之,LiFeHCF-1、LiFeHCF-2和LiFeHCF-3样品是通过离子交换工艺获得的,而LiFeHCF-4和LiFeHCF-5样品是通过自氧化/沉淀方法合成的。图1a显示了LiFeHCF-1通过FeFe(CN)6-1(FeHCF-1)的化学锂化的合成路线示意图,它首先通过从NaFe(CN)6-1(NaFeHCF-1)中化学提取钠而制备。LiFeHCF-2和LiFeHCF-3样品是使用NaFeHCF-2和NaFeHCF-3作为前体得到的,这些前体是通过柠檬酸盐辅助共沉淀法制备的。为了深入了解缺陷浓度和水分子的位置,样品被进一步用中子衍射分析(图1b-d)。本研究根据Herren的研究工作建立了最初的模型,其中铁离子与CN配体在空间群为Fm-3m的立方结构中八面体配位。在这个阶段,没有将H2O分子放入单元格中,因为它们的位置将由初步细化周期后的傅里叶变换不同图谱决定。如图1e所示,与LiFeHCF-3相比,LiFeHCF-1样品的晶格参数从10.2134增加到10.2296 Å,这意味着锂离子的扩散系数更高。
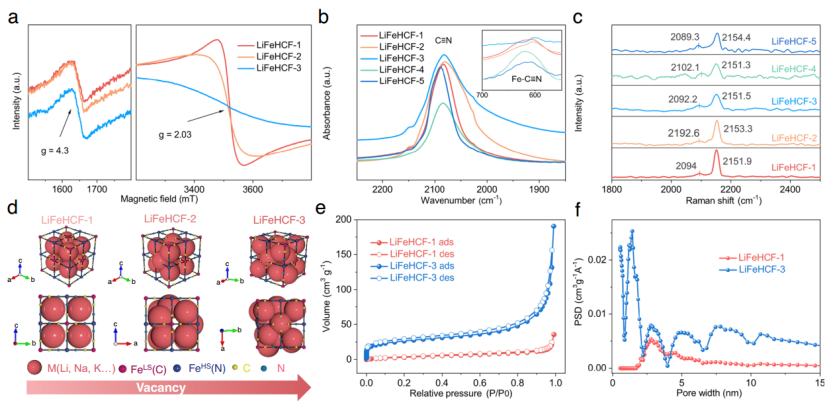
图2|不同LiFeHCF样品的结构特征。a) LiFeHCF-1、2和3样品的电子顺磁共振(EPR)光谱。b) 各种LiFeHCF材料的傅里叶变换红外光谱。c) LiFeHCF的拉曼光谱(1800-2550 cm-1)显示了(C≡N)-基团的演变。d )LiFeHCF样品特性和空位相关性示意图。LiFeHCF-1, LiFeHCF-3样品的N2吸附-解吸等温线(e)和孔隙大小分布(f)。
电子顺磁共振(EPR)是一种有效的表征技术,可以用来标准物质中的铁元素,特别是在研究过渡金属的配位环境和氧化状态时。图2a表明:LiFeHCF-1、LiFeHCF-2和LiFeHCF-3样品的EPR光谱在g因子=4.3和g因子=2.03处分别有特征峰。此外,1638 cm-1和3462 cm-1的峰是O-H键拉伸振动峰和面内弯曲振动峰,2082 cm-1的峰代表C≡N键的拉伸振动峰,它与过渡金属离子结合到CN-基团有关。值得注意的是,C≡N键的拉伸振动峰(图2b)揭示了LiFeHCF样品的Fe-C≡N基团的振动。与LiFeHCF-3相比,LiFeHCF-1在608 cm-1处有一个蓝移和更高的Fe-C≡N峰,这归因于更强的C≡N化学键和更稳定的Fe-C≡N基。在图2c中,拉曼光谱(1800-2550 cm-1)显示了特征的衍射峰,归因于C≡N基团与晶格中不同价位的铁离子结合。2151 cm-1和2094 cm-1的峰值逐渐增加,表明FeC6和FeN6八面体的对称性增加,这与EPR结果一致。基于上述分析,图2d示意了LiFeHCF-1、LiFeHCF-2和LiFeHCF-3中Fe-C≡N基团的分布。LiFeHCF-1具有更多对称的FeC6或FeN6八面体、良好的结晶性和较低的缺陷,而LiFeHCF-2和LiFeHCF-3中大量不完整的Fe-C≡N基团可能导致锂离子的不可逆插入/析出和沸石水的空间增加。LiFeHCF样品的不同结构通过氮气吸附/解吸的测量和分析得到了进一步验证。如图2e、f所示,LiFeHCF-3显示了比LiFeHCF-1更高的比表面积(55 m2 g-1 vs. 15 m2 g-1),以及更多的微孔(《2 nm)。高的表面积部分是由于LiFeHCF-3的颗粒大小减少引起的,这也表明了合成过程中产生的丰富的缺陷。
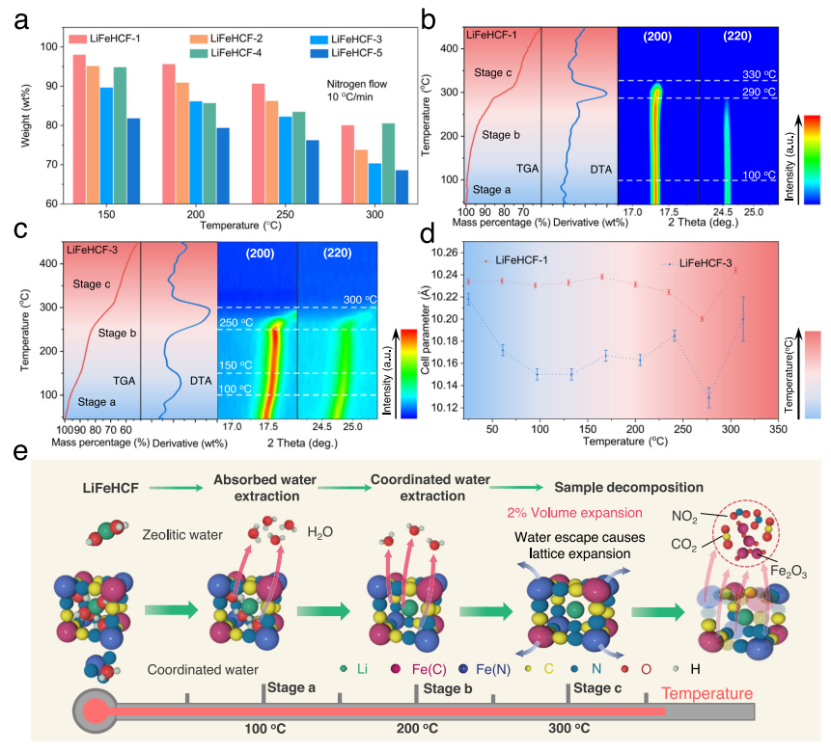
图3|在加热过程中表征不同的LiFeHCF样品。a) 不同LiFeHCF样品的重量变化。b LiFeHCF-1和c) LiFeHCF-3粉末样品在25℃至450℃加热过程中的结构演变。d) 加热过程中变形框架的LiFeHCF样品的电池参数变化的比较。e) LiFeHCF样品的脱水行为和化学降解机制示意图。
人们普遍认为,水的含量对普鲁士正极的电化学性能有重大影响。为此,本研究进行了热重分析(TGA)以确定LiFeHCF样品晶格中水的存在和含量。结果总结在图3a中,发现每个LiFeHCF样品的质量损失在150℃时分别为98.1%、95.2%、89.7%、94.9%和81.8%。当温度上升到300℃时,这些值分别变成了80.1%、73.8%、70.3%、80.5%和68.6%。这些结果表明,LiFeHCF-1和LiFeHCF-4样品中的水含量较少。通过在25到450℃之间进行的变温XRD,本研究进一步研究了LiFeHCF样品的脱水过程和化学降解过程。图3b、c显示了LiFeHCF-1和LiFeHCF-3的TGA(DTA,差热分析)曲线以及(200)和(220)衍射峰的等高线图。值得注意的是,LiFeHCF-3样品在a阶段表现出相对加宽和减弱的衍射峰,表明更多的沸石水从晶格中被移除,从而导致严重的晶格畸变和体积缩小。图3d显示了加热过程中晶胞参数变化的更详细比较。由于沸石水和配位水的释放,LiFeHCF-3的晶胞参数从10.218 Å下降到10.129 Å,并且单位晶胞体积收缩了2.7%。LiFeHCF样品的脱水行为和化学降解过程在图3e的示意图中得到了总结。不同类型的水对应于不同的提取温度和晶格变化。结果还表明,晶格中沸石水的存在对热稳定性有负面影响,这实际上是由不对称的Fe-C6/Fe-N6八面体的增加所导致的。
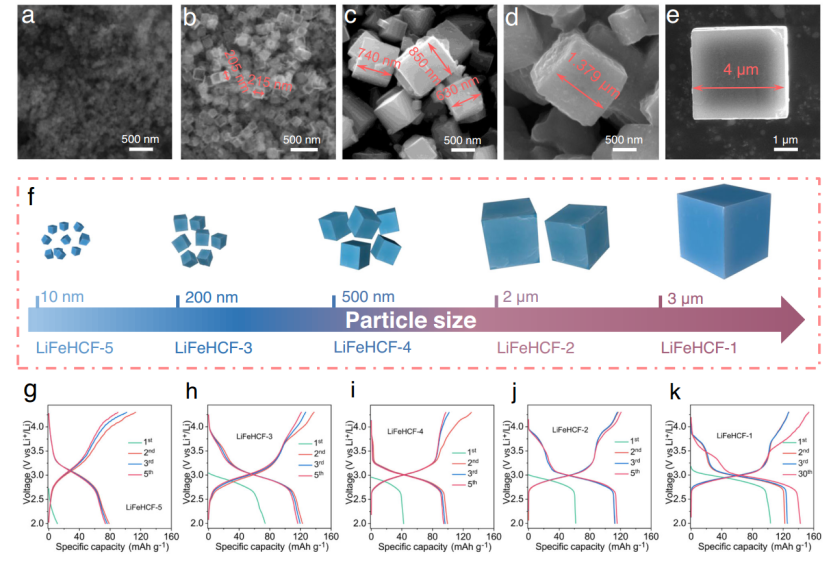
图4|颗粒大小对LiFeHCF样品的电化学性能的影响。a) LiFeHCF-5, b) LiFeHCF-3, c) LiFeHCF-4, d) LiFeHCF-2和e) LiFeHCF-1粉末样品的颗粒尺寸。所有的图像都来自于原位SEM测量。f) LiFeHCF样品的微晶晶粒大小示意图。g-k) 在19 mA g-1的特定电流下,LiFeHCF样品的相应容量-电压曲线。
图4a-f显示了LiFeHCF样品的典型晶粒尺寸。LiFeHCF-1的最大尺寸为~4μm,LiFeHCF-4立方体只有~650-850 nm。LiFeHCF-1样品具有高结晶度的单晶形态,而LiFeHCF-2和LiFeHCF-3样品的平均晶粒尺寸为~2 μm和~200 nm。它们的前体是通过相同的共沉淀方法合成的,只是使用了不同含量的柠檬酸钠。通过简单的共沉淀方法(使用Li4Fe(CN)6)制备的LiFeHCF-5样品具有最小的尺寸~10nm。所有的样品都有不同的成核率,快速的结晶可能导致空位的存在和沸石水的大量含量,阻碍了晶体尺寸的增长。本研究试图直接观察锂基普鲁士蓝晶格中的缺陷和水的位置,但样品对于高分辨率的电子显微镜和光谱学来说过于敏感,所以PBA的高分辨率图像很少被报道。
本研究还对LiFeHCF电极在纽扣电池中的性能进行了评估,使用金属锂作为反电极,在碳酸乙烯酯(EC)和碳酸二乙酯(DEC)电解质中使用1 M LiPF6。图4g-k显示了LiFeHCF-1、LiFeHCF-2、LiFeHCF-3、LiFeHCF-4和LiFeHCF-5样品在19 mA g-1的特定电流下的循环曲线。这些电池在第二个循环中提供的放电容量分别为126 mAh g-1、117 mAh g-1、122 mAh g-1、103 mAh g-1和80 mAh g-1。值得注意的是,具有最大颗粒尺寸的LiFeHCF-1样品有一个活化过程,并且在30个循环后出现了143 mAh g-1的最高放电容量(图4k)。
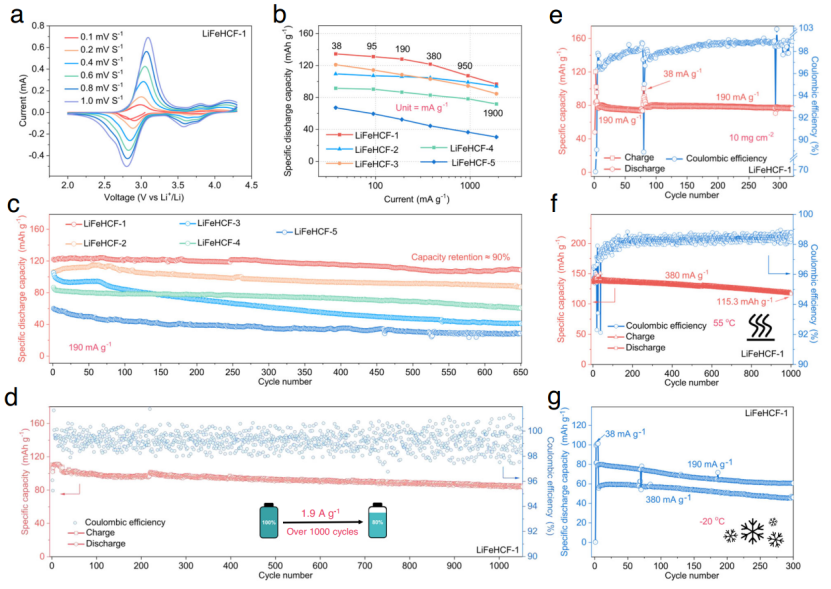
图5|LiFeHCF-1样品的电化学评估。a) 不同扫描速率下LiFeHCF-1样品的循环伏安曲线;b )不同特定电流下LiFeHCF样品的速率性能;c) 190 mA g-1下LiFeHCF样品的循环性能;d) 1.9 A g-1下LiFeHCF-1材料的长期循环性能;e) 高负载性能(10 mg cm-2);f, g) 在55 °C和-20 °C的高温和低温测试。所有的LiFeHCF电极都是在使用金属锂作为对电极的纽扣电池配置中进行评估的,并在25℃下进行测试(除非有不同的说明)。
所有的样品都可以在3.1V处观察到典型的放电电压峰值,但是LiFeHCF-1和LiFeHCF-2也在3.8V处有第二个峰值点,这与锂化过程中Fe3+/Fe2+对的还原反应有关。为了解LiFeHCF样品各种电压峰值的原因,本研究进行了循环伏安法(CV)测试。如图5a所示,3.1 V的正极峰源于与氮配合的高自旋Fe3+/Fe2+对的氧化还原反应,而3.8 V的高电位峰则与碳配合的低自旋Fe3+/Fe2+对有关。如图5b所示,本研究在非水性金属锂电池配置中进一步研究了LiFeHCF电极的速率能力。以LiFeHCF-1为正极的金属锂电池在所有样品中显示出最好的性能。在38、95、190、380、950和1900 mA g−1,容量分别为135、131、128、122、107和97 mAh g−1。
此外,LiFeHCF-1电极在190 mA g-1下表现出卓越的循环性能,提供了109 mAh g-1的可逆容量和650次循环后约90%的容量保持率。相比之下,LiFeHCF-2、LiFeHCF-3、LiFeHCF-4和LiFeHCF-5电极在190 mA g-1时的容量分别为87、41、61、29 mAh g-1,容量保持率为82.3%、40%、70%和47.4%(图5c)。对于LiFeHCF-3和LiFeHCF-5来说,在100次循环后会出现明显的容量衰减。这里的稳定性差可能与大量的空位有关,这些空位阻碍了锂离子通过《100》方向迁移。此外,结构中的沸石水在充/放电过程中逐渐被析出,这进一步加速了电解质的分解,并且降低了库仑效率。LiFeHCF-1电极在约1.9A g-1的高比电流下表现出明显的长期循环性能。如图5d所示,该电池在初始循环时提供118.9 mAh g-1的放电容量,并在1000个循环后保持80.7%的容量(每次循环有0.019%的容量衰减),库伦效率高达99.3%。即使是质量负荷为10mg cm−2 的正极中,金属锂纽扣电池在190 mA g−1的300次循环后,容量保持率依然高达98%(图5e)。本研究还发现它在55℃和-20℃也显示出良好的性能(图5f和g)。
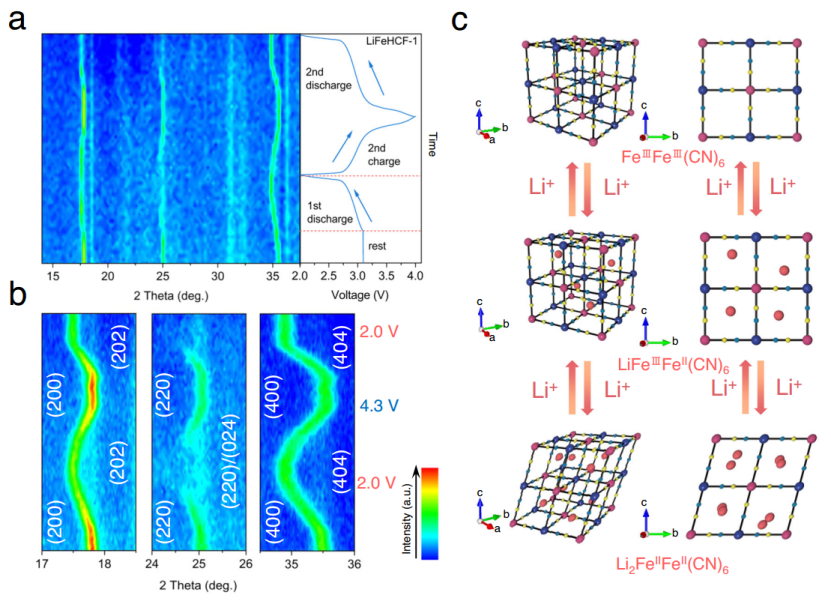
图6| LiFeHCF-1样品在充放电过程中的结构演变。a )操作XRD图。b(200)、(220)/(024)和(400)衍射的详细信息。c) Li插入/析出时的相演变示意图。
在图6a中,17.8°和35.5°的峰逐渐向低角度移动,25°的峰的消失表明锂化过程中单元格的体积增加。在第2次放电后,这些峰值恢复到初始位置,表明形成了富含锂的Li1+xFe(CN)6。图6b中显示了(200)、(220)和(400)峰区的扩大图。在第一次放电过程中,(200)峰逐渐从17.8°转移到17.52°,这表明在第二次锂插入过程中电池参数的变化。当电压达到2.0V时,Li+完全插入到Li1+xFe(CN)6晶格中,因而产生了一个新的相。另外,本研究发现25°的(220)衍射在放电到2.0 V后分裂成两个峰,这是含LiFeHCF-1的正极材料被高度锂化的另一个证据。如图6c所示,对于立方体FeIIIFeIII(CN)6来说,假设Li扩散的开始是通过《100》方向,当亚立方位点被占据一半时,由于伴随着晶格从立方体LiFeIIIFeII(CN)6转变为斜方体结构Li2FeIIFeII(CN)6的体积发生膨胀,扩散路径被改变为《111》方向,这与GITT结果一致。
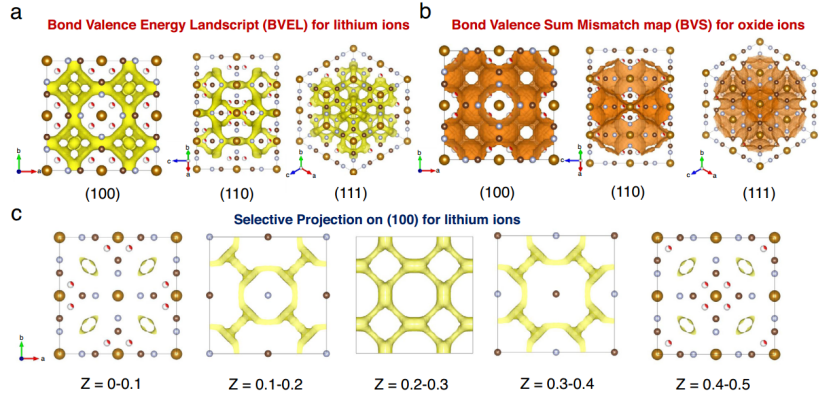
图7|理论上预测PBAs的锂离子的路径。a) LiFeHCF样品中锂离子的键价能态(BVEL)计算。b) 针对LiFeHCF样品中的氧化物离子的键价和失配图(BVS)计算。c 在(100)平面上不同Z值的BVEL。
为了了解锂离子的扩散行为,本研究对LiFeHCFs进行了键价能态(BVEL)计算。由于C和N原子在CN配体中是共价键,C和N上的电荷不容易被确定。如图7a所示,发现锂离子的扩散可以通过以(0.25, 0.25, 0)为中心的3.2×2.0 Å2椭圆孔窗进入到以(0.25, 0.25, 0)为中心的三维互连立方体3×3×3 Å3的纳米笼中。锂离子的扩散主要由两个因素驱动:1. 在放电过程中,当铁离子发生还原反应,负电荷框架与电荷在锂离子上的位置之间的库仑相互作用将其价态从3+变为2+;2. PBA化合物和其周围环境之间的化学势不同。最近,一些计算研究试图解释水分子如何在电化学循环中稳定PBA的结构。这启发了本研究去进一步研究水分子在PBAs中的扩散行为,因为在充放电过程中,水分子可以在非水电解质溶液和PBA结构之间进行交换。如图7b、c所示,PBA上的BVS失配图表明水分子的扩散途径与锂离子渗流网络相似,但扩散范围更广。这表明,如果水分子的浓度很高(》1.8 mol%或9.8 wt.%),就很容易阻碍锂离子的扩散。因此,尽量减少PBAs中的水含量和缺陷有助于优化含有PBAs正极的锂基电池的电化学储能性能。
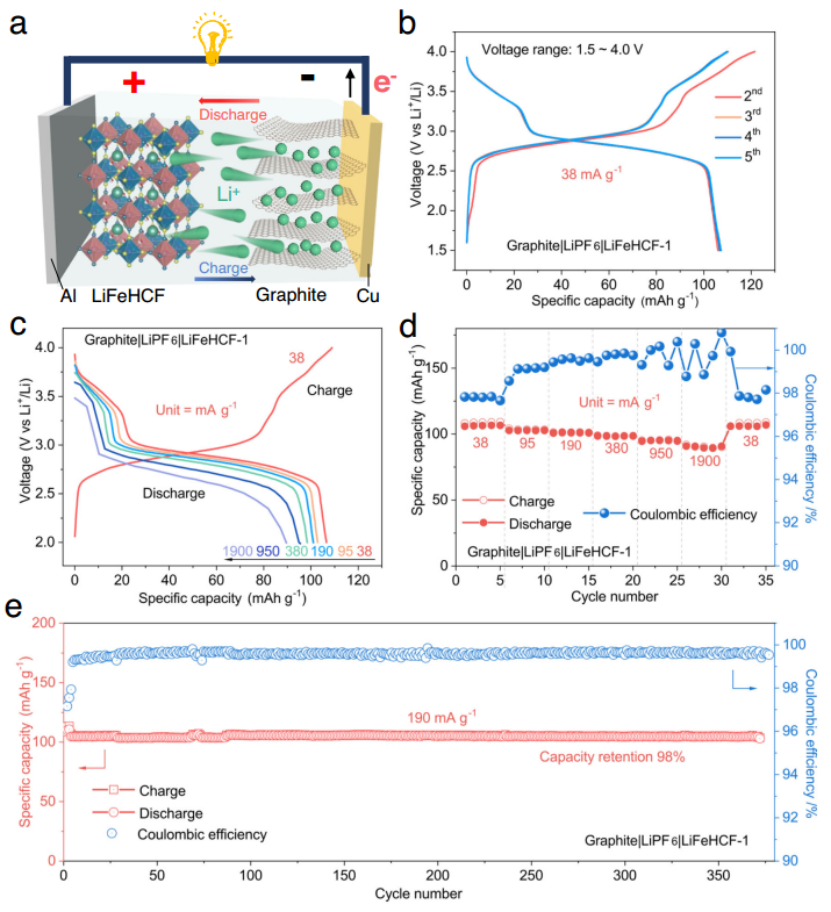
图8|LiFeHCF-1基正极与石墨基负极耦合的电化学性能。a)石墨||LiFeHCF全电池的示意图。b) 全电池在 38 mA g−1 时的恒电流充放电电压曲线。在38 mA g−1 至 1900 mA g−1内的电压曲线 (c) 和速率性能 (d)。e) 演示电池在190 mA g−1下的长期循环性能。
为了进一步验证LiFeHCF-1正极的实际应用,本研究为负极活性材料组装并测试了锂离子电池(图8a)。在38 mA g−1(考虑正极活性物质的质量)的特定电流下,石墨||LiFeHCF−1纽扣电池的可逆容量为106 mAh g−1(图8b),平均放电电压约为2.9 V,在1.5~4.0 V的电压范围内5次循环后没有出现容量衰减。在图8c、d中,全电池在95 mA g-1、190 mA g-1、380 mA g-1和950 mA g-1的不同速率下分别显示出104、102、99、95 mAh g-1的良好的可逆容量,并且在38 mA g-1的特定电流下比容量可以恢复到109 mAh g-1。有趣的是,该电池可以循环到1.9A g-1,提供约90 mAh g-1的特定放电容量。此外,图8e显示了在370次循环中105 mAh g-1的高容量和98%的容量保持率(平均库仑效率≈99.6%)。
03 总结和展望
本研究系统地研究了各种LiFeHCF样品并比较了它们在非水环境中的锂离子存储性能。通过使用先进的技术,包括粉末中子衍射、热重-红外光谱仪、操作变温X射线衍射和键价能态计算,揭示了沸石和晶体水在热稳定性和结构框架完整性方面的影响。定制的具有微米尺寸和单晶形态的LiFeHCF材料表现出》140 mAh g-1的高容量(在19 mA g-1时)和超过1000次循环的长寿命,以及吸引人的性能:高负载(10 mg cm-2),宽温度(-20至55℃)窗口和组成石墨||LiFeHCF锂离子电池。
审核编辑:郭婷
-
锂离子电池黏结剂2013-05-16 3032
-
锂离子电池的类型2013-05-17 5197
-
锂离子电池的设计2013-05-20 3556
-
聚合物锂离子电池的构成2013-06-06 3488
-
锂离子电池的工作原理和使用注意事项2014-10-29 6509
-
有机化合物可作为锂离子电池正极材料2015-11-17 5679
-
锂离子电池和锂电池的区别2015-12-28 5877
-
锂离子电池的最新正极材料:掺锰铌酸锂?2016-01-19 6460
-
【转】锂离子电池的维护和保存技巧分享2016-08-18 5021
-
锂空气电池未来或击败锂离子电池2018-10-09 2372
-
锂离子电池简介2020-11-03 2921
-
锂离子电池的预锂化技术2021-04-20 3071
-
如何选择动力型锂离子电池的正极材料?2021-05-12 3363
-
磷酸铁锂——新型锂离子电池正极材料2009-10-27 1487
-
锂离子电池的工作原理与结构2021-03-10 18889
全部0条评论

快来发表一下你的评论吧 !

