

一款基于非对称几何MoS2二极管的生物传感器
传感器
描述
据麦姆斯咨询报道,近日,西蒙弗雷泽大学(SimonFraserUniversity,简称SFU)的研究人员开发了一款基于非对称几何MoS2(二硫化钼)二极管的生物传感器,用于无标记、快速且高灵敏的特异性检测肿瘤坏死因子-α(TNF-α,一种促炎细胞因子)。
该传感器由肿瘤坏死因子-α结合寡核苷酸适配子功能化,以检测浓度低至10 fMol(飞摩尔)的肿瘤坏死因子-α,该浓度水平远低于健康血液中的典型浓度。寡核苷酸适配子和肿瘤坏死因子-α在传感器表面的相互作用诱导传感器表面能量的变化,从而改变MoS2二极管的电流-电压整流行为,这可以使用双电极结构读出。该二极管传感器的主要优点是制造工艺和电子读数简单,因此,它有潜力应用于快速且易于使用的即时诊断(POCT)工具。
细胞因子是在调节炎症反应中起重要作用的小蛋白。常见于血液、唾液和汗液等生物流体,它们作为各种健康状况和疾病的生物标志物,已引起人们的关注。细胞因子浓度的异常变化是失控炎症反应的一个指标,与阿尔茨海默病、癌症、肺结核、自身免疫性疾病和心血管疾病有关。
此外,2019年爆发新冠肺炎(COVID-19),其感染者伴随着高水平促炎细胞因子的释放,如白细胞介素(IL-1β和IL-6)和肿瘤坏死因子-α,这种现象被称为细胞因子风暴。
有研究表明,细胞因子抑制剂是提高新冠肺炎生存率的有效治疗方法。许多疾病的治疗在早期阶段最为有效。因此,监测和检测炎症细胞因子水平的早期变化对临床诊断具有重要意义。
健康青年和成年人群中血清肿瘤坏死因子-α的水平通常在200 fMol ~300 fMol的范围内。而儿童血清水平可低至12 fMol。因此,在飞摩尔范围内的检测限(LOD)在早期诊断应用中非常重要。
图1显示了使用不对称几何MoS2二极管的细胞因子测量程序。图1a展示的血液样本是如何在血液样本中测量肿瘤坏死因子-α浓度的概念说明。该传感器由二维半导体(2H相)多层MoS2晶体薄片组成,其顶部是热氧化的SiO2(氧化膜厚度为300 nm),接触两个Cr/Au(铬/金)电极。基于原子力显微镜(AFM)测量,典型的MoS2厚度在13 nm~60 nm之间。
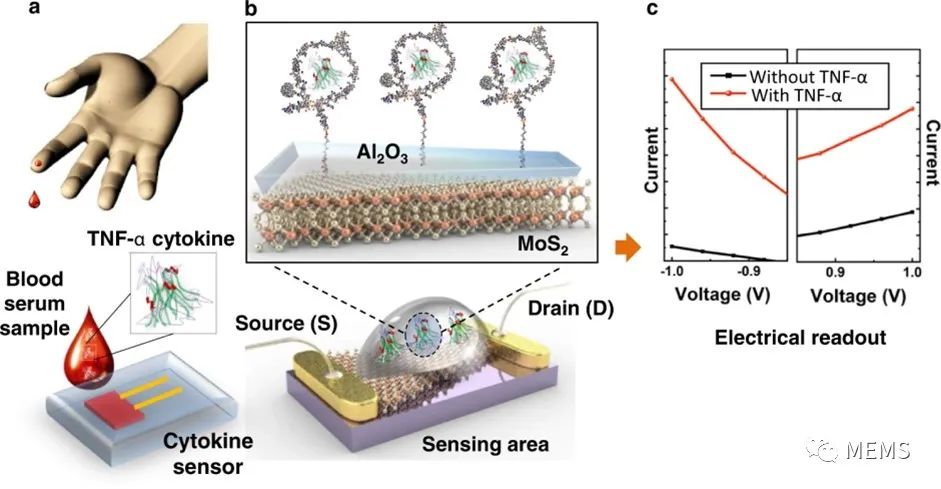
图1 细胞因子传感器操作概念示意图
该传感器功能化的分步流程如图2b所示。在低pH环境下,(缩水甘油氧丙基)三甲氧基硅烷(GOPS)在水溶液中耦合到Al2O3(三氧化二铝)表面。
通过1-1'羰基二咪唑(CDI)连接体的附着,随后肿瘤坏死因子-α结合适配体5’端胺与(缩水甘油氧丙基)三甲氧基硅烷活性位点偶联,(缩水甘油氧丙基)三甲氧基硅烷被激活。
DNA适配体用作生物标志物受体,因为它与目标分析物肿瘤坏死因子-α特异性结合,并且有可能重复使用。为了促进适配体寡核苷酸在传感表面上的耦合,研究人员将器件浸入10 μMol适配体的磷酸盐缓冲溶液(PBS)中。
该研究使用的适配体寡核苷酸在3'端有荧光染料(FAM),因此可以通过荧光光谱法验证适配体与传感器是否成功耦合。
图2d显示了有适配体功能化和没有适配体功能化情况下获得的荧光光谱测量结果。在裸样品中不存在荧光染料的发射光谱(525 nm处的峰值发射)。图2d的插图显示了传感器功能化前后的光学图像。
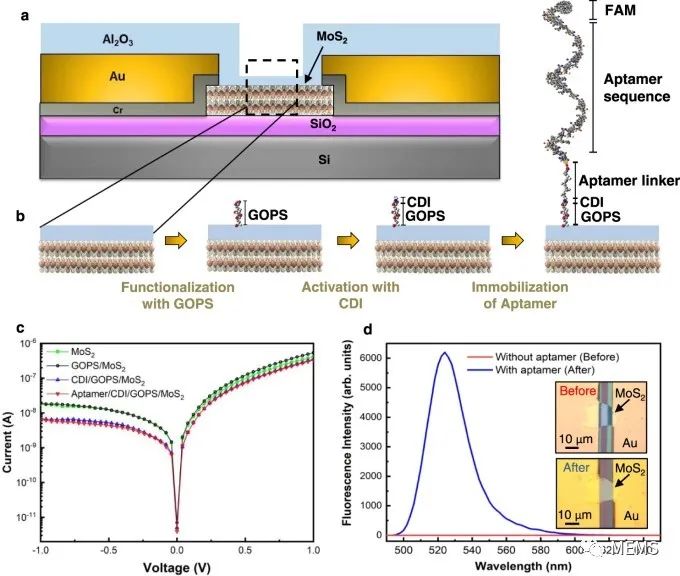
图2 非对称几何二极管传感器的功能化
单个装置的电流-电压响应随细胞因子浓度的变化如图3b(对数尺度)所示。随着细胞因子浓度的增加,整流系数(RF)升高。图3c显示了高电压(线性刻度)下电流-电压曲线的放大图示。
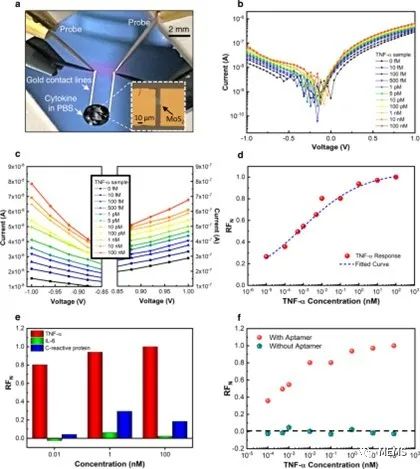
图3 传感器性能
如图4b所示,研究人员进行了液体门控测量,以支持该检测机制。图4c显示了漏极和源极(IDS)Au(金)触点之间的电流-电压响应,该响应是二极管传感器在负栅源电压(VGS)从0递减到−1V时获得的,通过将一滴纯磷酸盐缓冲溶液施加到传感区域。电流-电压响应显示电流在−0.75V和0V电压之间有明显波动 ,研究人员认为这是由于磷酸盐缓冲溶液存在的缘故,因为空气中的电流-电压响应没有显示这种现象。
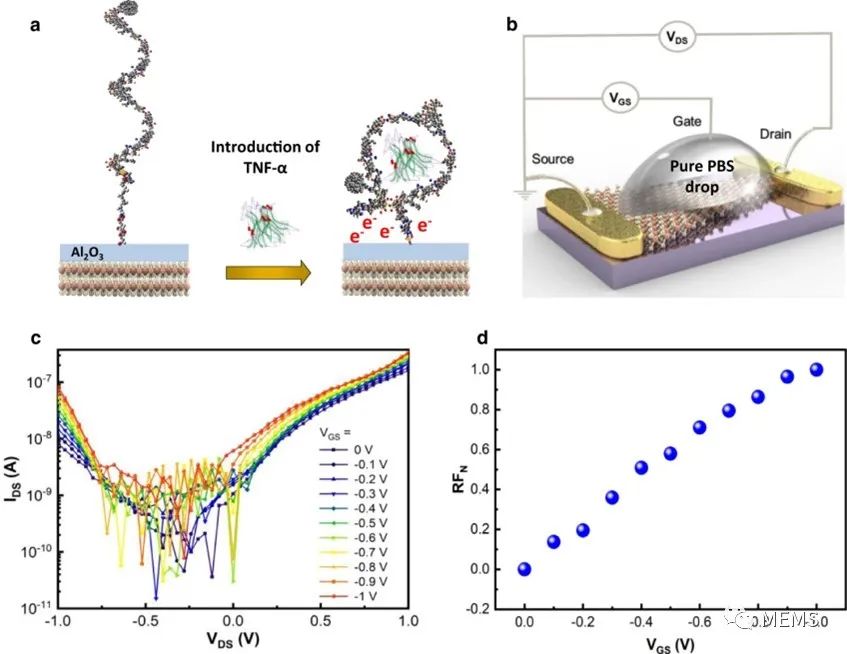
图4 检测机制
综上所述,研究人员提出了一种基于非对称几何MoS2二极管传感器检测肿瘤坏死因子-α的方法,检测浓度低至10 fMol,并结合了10 fMol至1 nMol的宽动态检测范围。
通过稀释的肿瘤坏死因子-α溶液与适配体功能化的传感器表面相互作用,2分钟获得测量肿瘤坏死因子-α的电流-电压响应曲线。该论文介绍的传感器在使用简单的双电极设计,快速检测肿瘤坏死因子-α的飞摩尔浓度方面显示出良好的结果,使其适用于易使用和快速的即时检测。
审核编辑:刘清
-
TPSMB非对称系列TVS二极管:汽车应用的理想保护方案2025-12-15 771
-
Littelfuse推出新型TPSMB非对称TVS二极管2025-01-02 1301
-
Littelfuse推出TPSMB非对称TVS二极管系列2024-12-30 1465
-
mos管体二极管的作用是什么2024-01-31 9622
-
什么是红外二极管?发光二极管?红外二极管与发光二极管的区别2024-01-26 4395
-
MOS管体二极管是什么?MOS管体二极管的作用2024-01-23 8923
-
我的传感器二极管构建2023-07-10 467
-
mos管为什么会有寄生二极管 寄生二极管的示意图/作用参数/方向判定2023-02-19 19006
-
MOS管的体二极管来源与作用2023-01-11 36699
-
防水晶体管在生物传感器中的应用是什么?2021-06-17 1666
-
电机续流二极管疑问2018-02-28 6803
-
MOS管中的二极管起什么作用2016-12-20 7149
-
高性能Si基MOS肖特基二极管式氢气传感器研究2015-11-10 803
-
生物传感器的原理2008-01-09 1383
全部0条评论

快来发表一下你的评论吧 !

