

新型锂化普鲁士蓝锂电正极简介
描述
【研究背景】
传统的锂离子电池采用过渡金属氧化物作为正极,其具备比能量高,循环性能好等优点。然而,受限于结构中O 2p轨道和M 3d轨道的重合,这种层状LiMO2型化合物在荷电态下稳定性不可避免地会降低,由此带来安全隐患。和层状氧化物相比,聚阴离子型化合物(如LiFePO4),结构中存在强共价键P-O,因此其热稳定性显著增强。同时,得益于聚阴离子基团的诱导效应,其工作电位也较高。
但是这类聚阴离子化合物容量往往较低,难以满足高比能电池的需求。。 普鲁士蓝类似物(PBAs)具有开放通道结构,适用于碱离子的可逆嵌入脱出,在一定条件下优化后的产物可发生双电子反应。然而,PBAs在锂离子电池中应用极少,原因有以下两点:锂化的PBA材料电压较低;PBA体系较大的孔隙位点难以稳定地存储锂。因此,针对PBA体系正极材料作用机理的研究及晶体结构调控,以提升其可逆储锂性能研发极为重要。
【成果简介】
近日,天津理工大学何广教授团队在Nature Communications上发表题为“Lithiated Prussian blue analogues as positive electrode active materials for stable non-aqueous lithium-ion batteries”的研究论文。作者通过中子粉末衍射测量确定了锂化PBAs的晶体结构,并通过原位XRD和键价模拟计算等研究了水对体系结构稳定性和Li+迁移的影响。该工作为PBAs体系稳定性的提升,及其作为锂离子电池正极材料的应用提供了新的研究思路。
【研究亮点】
(1)通过调节PBAs材料的嵌锂量,首次证明了Li2-xFeFe(CN)6⋅nH2O (0≤x≤2)活性材料可以适用于传统的有机电解液锂离子电池,在金属锂半电池体系中19 mA g−1电流密度下的初始放电容量为142 mAh g−1,在1.9 A g−1下1000次循环后,达到80.7 %的容量保持率。
(2)通过用石墨基负极取代锂金属制备全电池,能够实现在190 mA g−1电流密度下循环370次以上,稳定放电容量约为105 mAh g−1,在25°C下放电容量保持率为98 %。
【图文导读】
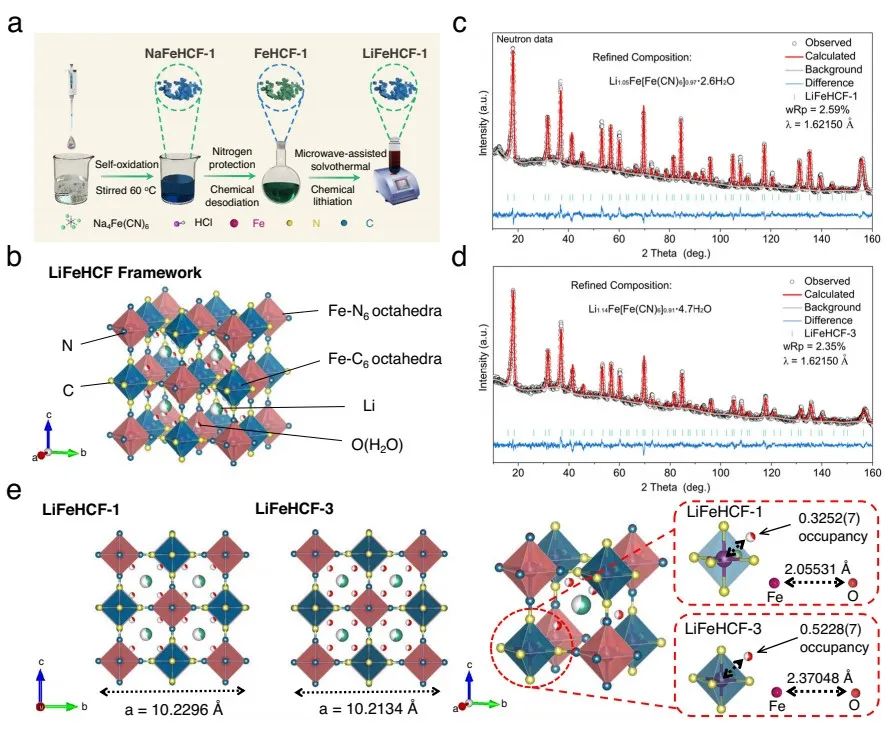
图1 (a)LiFeHCF-1的合成示意图。(b)锂化普鲁士蓝的晶体结构。(c)LiFeHCF-1和(d)LiFeHCF-3的中子衍射及精修结果。(e)LiFeHCF-1和LiFeHCF-3 的具体晶胞参数和配位环境对比。
受作者利用不同的方法合成了了一些列缺陷和结晶水含量不同的LiFeHCF样品,方法如图1a所示。为了了解缺陷浓度和水分子的位置,作者对样品进行了中子衍射分析(图1b-d)。对应的结果如图1e所示,与LiFeHCF-3相比,LiFeHCF-1样品的晶格参数从10.2134增加到10.2296 Å,这意味着Li+的扩散系数更高。空位位置的水分子会阻碍Li+的迁移,但适当靠近Fe(CN)6八面体的水分子有助于维持结构的稳定。
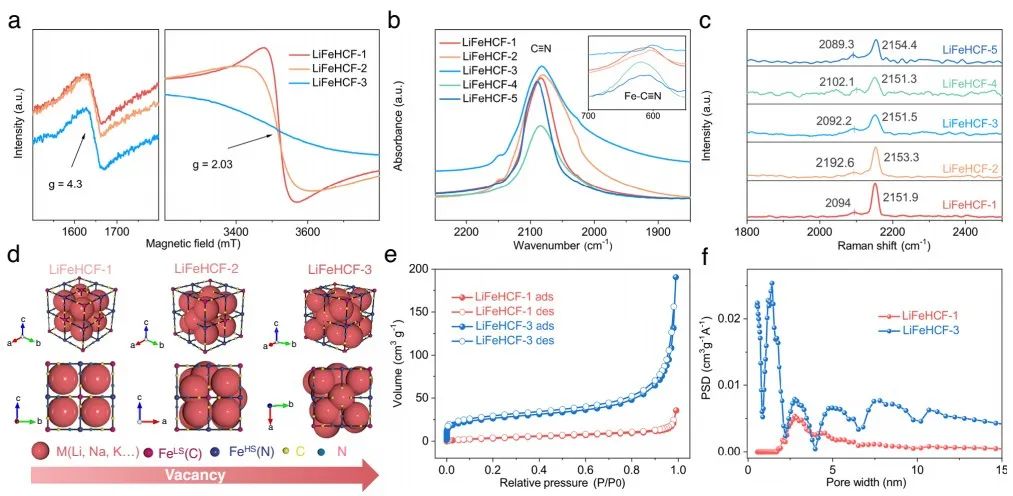
图2 (a)LiFeHCF-1、LiFeHCF-2和LiFeHCF-3的电子顺磁共振(EPR)测试结果。(b)不同LiFeHCF样品的红外测试结果。(c)不同LiFeHCF样品的Raman测试(1800-2550 cm-1)结果。(d)LiFeHCF样品的特征和空位相关性的示意图。LiFeHCF-1和LiFeHCF-3样品的比表面积测试(e)及孔径分布图(f)。
如图2a所示,电子顺磁共振(EPR)是一种有效的表征技术,可用于验证物质中铁的种类,特别适用于研究过渡金属的配位环境和氧化态。g=4.3处的峰属于四配位或畸变四配位的孤立Fe3+,g=2.03处的峰属于高度对称的六配位孤立Fe3+或聚合铁离子的特征峰。
如图2b的红外测试显示,C≡N键的拉伸振动峰对应LiFeHCF样品中Fe-C≡N基团的振动。与LiFeHCF-3相比,LiFeHCF-1在608 cm−1处Fe-C≡N有一个蓝移和更高的峰值,这是由于其C≡N化学键更强,Fe-C≡N基团更稳定。 在图2c中,从拉曼(1800-2550 cm−1)结果可以看出,晶格中与不同价铁离子结合的C≡N基团的特征衍射峰。
基于以上分析,图2d给出了LiFeHCF-1、LiFeHCF-2、LiFeHCF-3中Fe-C≡N的分布情况。通过对LiFeHCF样品的BET测试和分析,进一步验证了LiFeHCF样品的不同结构。如图2e-f所示,LiFeHCF-3比LiFeHCF-1具有更高的比表面积(55 m2 g−1 vs. 15 m2 g−1),以及更多的微孔分布(<2 nm)。
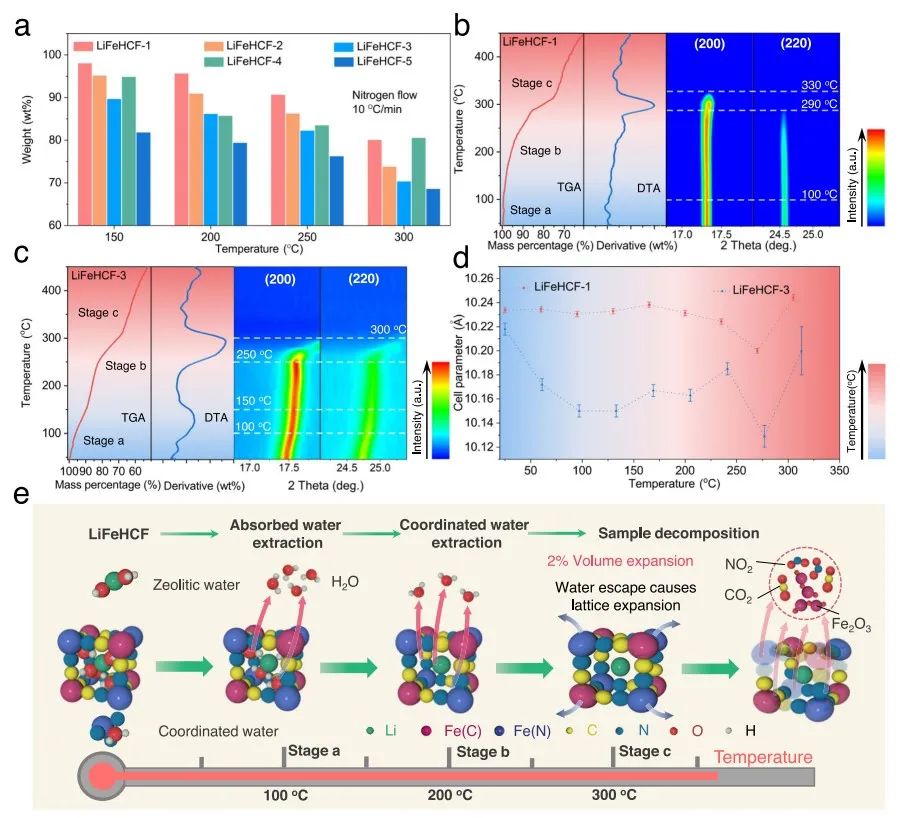
图3 (a)不同LiFeHCF样品的质量变化。(b)LiFeHCF-1和(c)LiFeHCF-3样品25-450℃加热过程中的结构演变。(d)加热过程中晶胞参数的变化。(e)LiFeHCF材料的失水和化学降解机理的示意图。
图3a为热重测试结果,结果表明,LiFeHCF-1和LiFeHCF-4样品中的结晶水较少。图3b-c显示了LiFeHCF-1和LiFeHCF-3的TGA (DTA,差热分析)曲线和(200)、(220)衍射峰等高线图。
结果显示,LiFeHCF-3样品在a阶段的衍射峰相对变宽和减弱,表明更多的水从晶格中逸出,导致晶格严重变形和体积缩小。图3d显示了加热过程中晶胞参数变化的详细对比。图3e则为LiFeHCF样品的脱水行为和化学分解过程示意图。
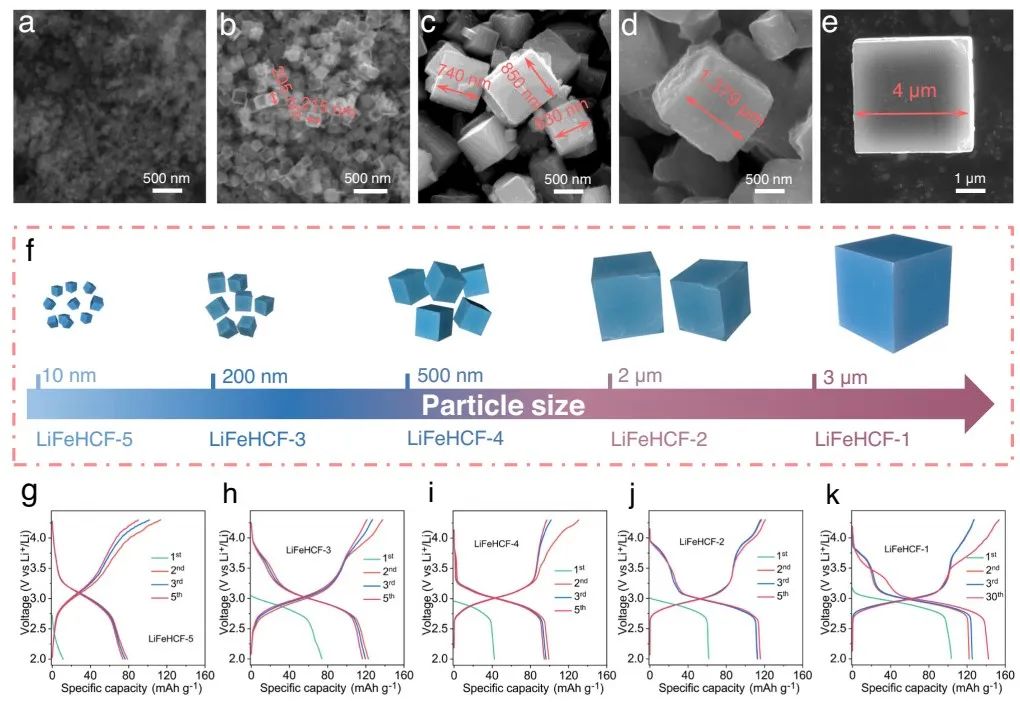
图4 (a)LiFeHCF-5, (b)LiFeHCF-3, (c)LiFeHCF-4, (d)LiFeHCF-2, (e)LiFeHCF-1样品的粒径。(f)LiFeHCF样品微晶尺寸示意图。(g-k)在19 mA/g电流密度下,LiFeHCF样品的充放电曲线。
图4a-e为不同样品的SEM图。在合成的过程中,所有样品都有不同的成核速率,快速结晶可能导致存在空位和水含量增大,从而阻碍晶粒尺寸的长大。LiFeHCF电极采用锂金属纽扣电池评价性能,在EC和DEC中加入1 M LiPF6。图4g-k显示了在特定电流为19 mA g−1时,LiFeHCF-1、LiFeHCF-2、LiFeHCF-3、LiFeHCF-4和LiFeHCF-5样品的恒流充放电曲线,其中粒径最大的LiFeHCF-1样品具有活化过程,在30次循环后达到最高放电容量143 mAh g−1(图4k)。
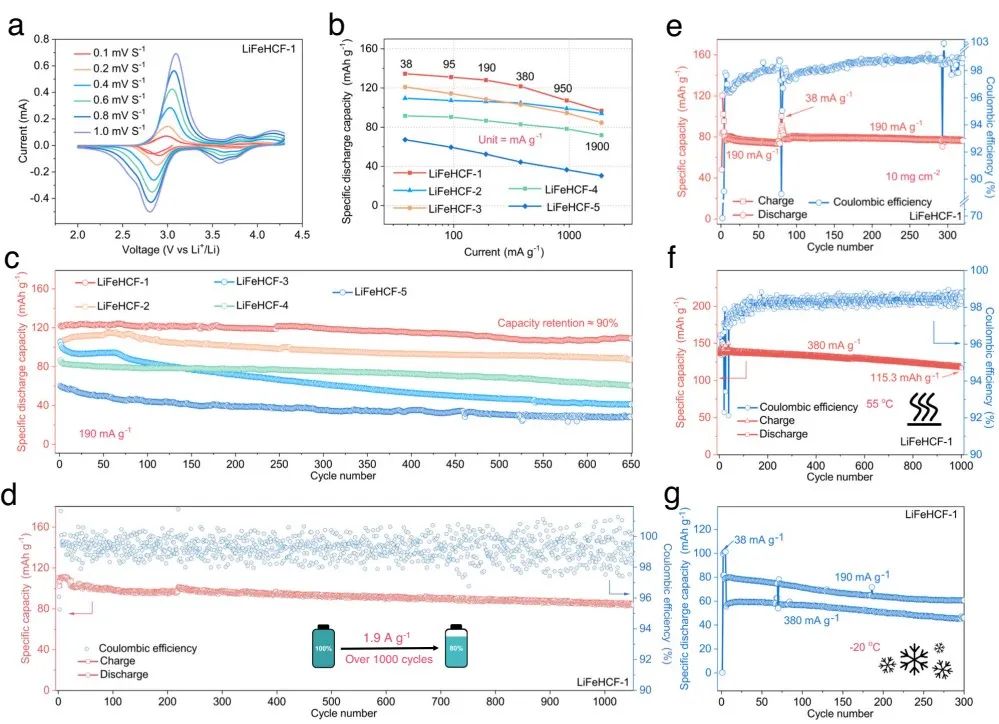
图5 (a) 在不同扫速下,LiFeHCF-1样品的CV曲线。(b)不同LiFeHCF样品的倍率性能图。(c)在190 mA/g电流密度下,LiFeHCF样品的循环稳定性。(d)在1.9 A/g电流密度下,LiFeHCF-1样品的长循环性能。(e)10 mg/cm2高负载量下的性能。(f-g)高(55℃)低(-20℃)温下的测试性能。
如图5a所示,3.1 V处的峰对应氮配位的高自旋Fe3+/Fe2+氧化还原反应,3.8 V处的高电位峰属于碳配位的低自旋Fe3+/Fe2+的氧化还原反应。进一步研究了在非水锂金属电池中LiFeHCF电极的倍率性能,如图5b所示。在190 mA g−1电流密度下,LiFeHCF-1电极表现出优异的循环性能,可提供109 mAh g−1的可逆容量,并且在650次循环后,保持良好的90%,性能优于其他样品(图5c)。
如图5d所示,电池在初始实现了118.9 mAh g−1的放电容量,并在1000次循环后中保持80.7%(每周期0.019%的容量衰退)。即使正极质量负载为10 mg cm−2,锂金属纽扣电池在190 mA g−1下循环300次后,容量保持率为98%(图5e),在55°C和- 20°C时也表现出良好的性能(图5f和g)。
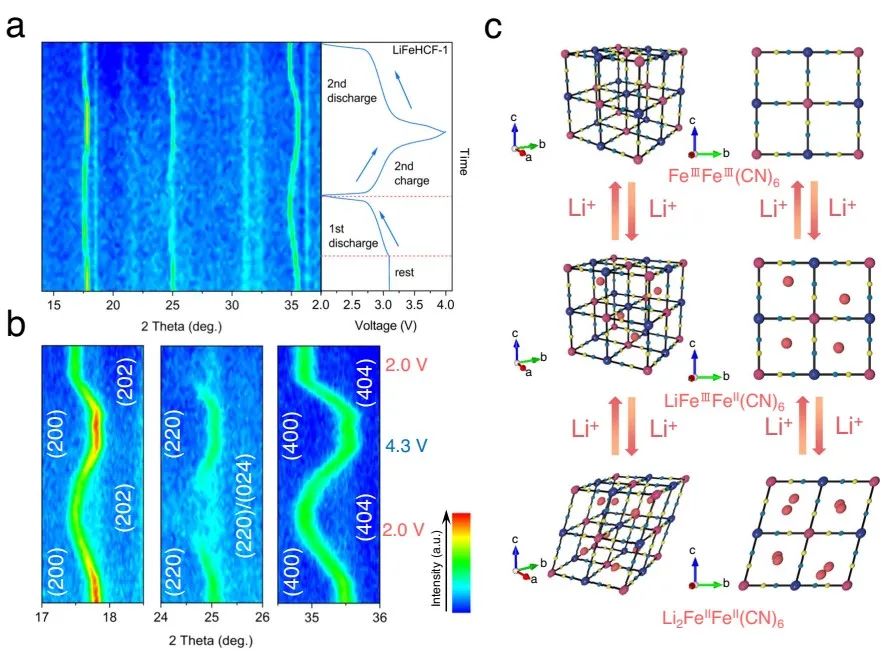
图6 LiFeHCF-1样品充放电过程结构解析。(a)原位XRD。(b)(200),(220)/(024)以及(400)的衍射峰位详细信息。(c)Li嵌入脱出过程中的相转换过程。
利用原位XRD探究循环过程中的结构相变(图6a-b)。最终结果分析如图6c所示,如图6c所示,假设Li扩散的开始是通过立方FeIIIFeIII(CN)6的<100>晶向扩散。当立方的空位占到一半时,扩散路径变为<100>晶向,由立方LiFeIIIFeII(CN)6向菱方结构Li2FeIIFeII(CN)6晶格转变,这与GITT测试结果一致。
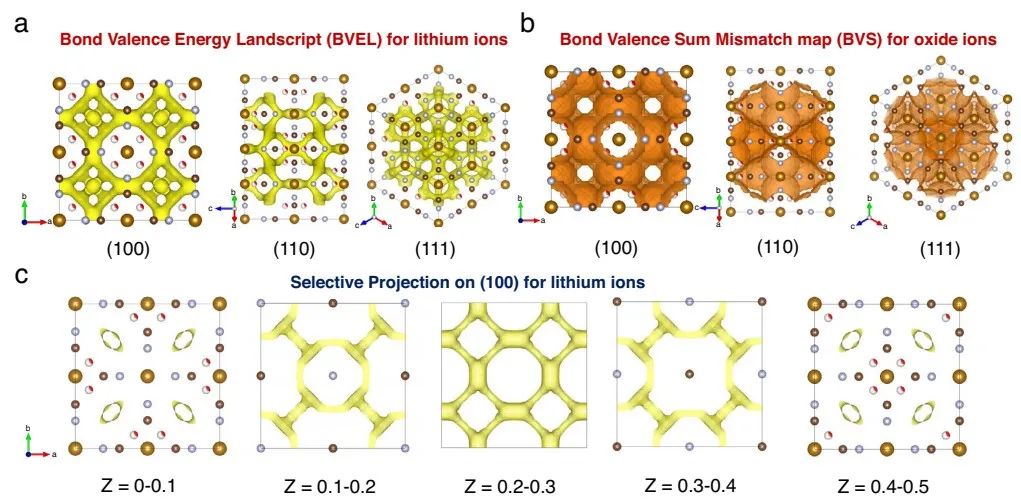
图7 (a) LiFeHCF中锂离子的键价能分布(BVEL)计算。(b)LiFeHCF中氧化物离子的键价和不匹配图(BVS)计算。(c)在(100)面上对应不同Z值的BVEL图。
为进一步了解Li+的扩散行为,作者还进行了键价能图(BVEL)计算。如图7a所示,作者揭示了Li+扩散可以通过以(0.25,0.25,0)为中心的3.2×2.0 Å2椭球孔窗口进入以(0.25,0.25,0.25)为中心的三维互联立方3× 3×3 Å3纳米笼中。如图7b、c所示,PBA上的BVS失配图表明,水分子的扩散途径与锂离子渗流网络相似,但扩散行为更广。这表明,当水分子浓度较高时,水分子很容易阻断Li+的扩散途径。因此,尽量减少PBAs的含水量和缺陷含量,有助于优化PBAs正极的性能。
【总结和展望】
作者系统地研究了各种LiFeHCF样品的制备,并比较了其有机体系的锂离子存储性能。采用粉末中子衍射、热重-红外光谱、原位XRD和键价计算等先进技术,揭示了结晶水对热稳定性和结构框架完整性的影响,实现LiFeHCF材料的精确调控,微米大小,容量超过140 mAh g−1 (19 mA g−1)以及超过1000次循环的长寿命,同时在高负载(10 mg cm−2),宽温域(-20-55°C)和搭配石墨负极的全电池体系中也能发挥出优异的性能。
审核编辑:刘清
-
锂离子电池的最新正极材料:掺锰铌酸锂?2016-01-19 6297
-
锂电池正极材料锂锰氧化物的改性与循环寿命2009-11-03 496
-
锂电池正极浆料主要成分有哪些?2009-10-22 2014
-
锂电池正极材料的性能有哪些?2009-10-24 2694
-
磷酸铁锂——新型锂离子电池正极材料2009-10-27 1372
-
普鲁士蓝薄膜电极的制作及充放电研究2011-02-21 729
-
丰元锂能的正极材料自动化产线4大优势的简单分析2017-12-31 9315
-
什么是锂电池预锂化2018-06-06 644
-
新锂想投资7.5亿元正极材料项目2020-09-04 4231
-
几类常见的锂电池体系正极材料的工作原理2020-12-18 11633
-
基于锂化普鲁士蓝类似物的锂离子电池正极2022-12-20 2960
-
新型梯度“单晶”富锂正极材料2023-02-01 4043
-
磷酸铁锂正极材料8月报2023-09-12 2113
-
磷酸铁锂是正极材料吗2024-05-19 2865
-
筛选理想的预锂化正极应用于无负极金属锂电池2024-12-24 1600
全部0条评论

快来发表一下你的评论吧 !

