

基于微柱阵列的微流控芯片实现癌症患者血液中CTCs的有效分离
描述
恶性肿瘤已成为我国死亡率最高的重大疾病之一,90%以上的肿瘤病人死亡是因为肿瘤的转移和复发。
因此,一些学者对这一疾病的发生、发展进行了研究,早在1896年,Ashworth提出了循环肿瘤细胞的概念,循环肿瘤细胞(CTCs)指从原位肿瘤病灶脱落,侵袭并进入外周血液循环系统的肿瘤细胞,该细胞被认为是肿瘤转移的必要前提。然而,外周血中CTCs数量极少,如何捕获它们就成为了挑战。
近期,荷兰埃因霍温科技大学的研究人员通过引入一种新型高效的基于微柱阵列的微流控芯片,实现了癌症患者血液中CTCs的有效分离。
为了达到CTCs分离的最大效率并提高捕获纯度,研究人员探究了微柱的几何形状和模式对癌细胞分离的影响。首先,研究人员将微柱设计成圆形、矩形、三角形和菱形等四种不同的几何形状,并用COMSOL Multiphysics模拟了微柱排列的影响。
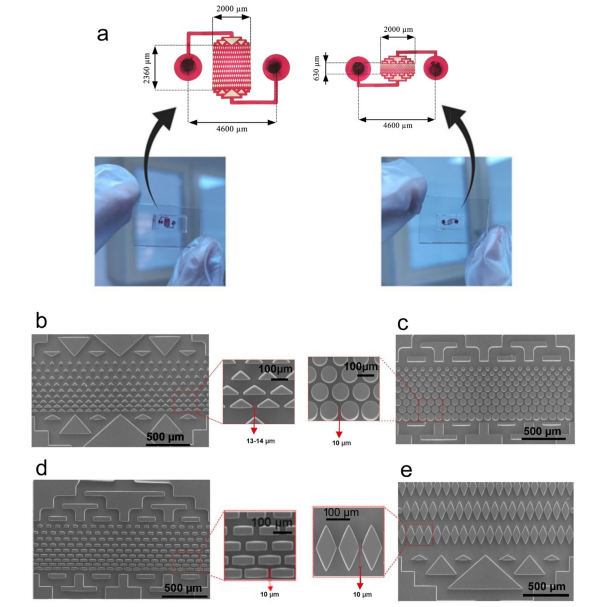
图1 不同几何形状的微流控芯片
结果表明,柱间距离相同的芯片上方的总压降要高于柱间距离逐渐减小的芯片。相应地,在这种状态下,细胞承受的压力更大、破裂的风险更高,且细胞活力更低。
在此基础上,研究人员进一步探讨了流速和压力对柱间距离逐渐减小的芯片的影响,发现细胞的生存能力主要取决于微柱的几何形状。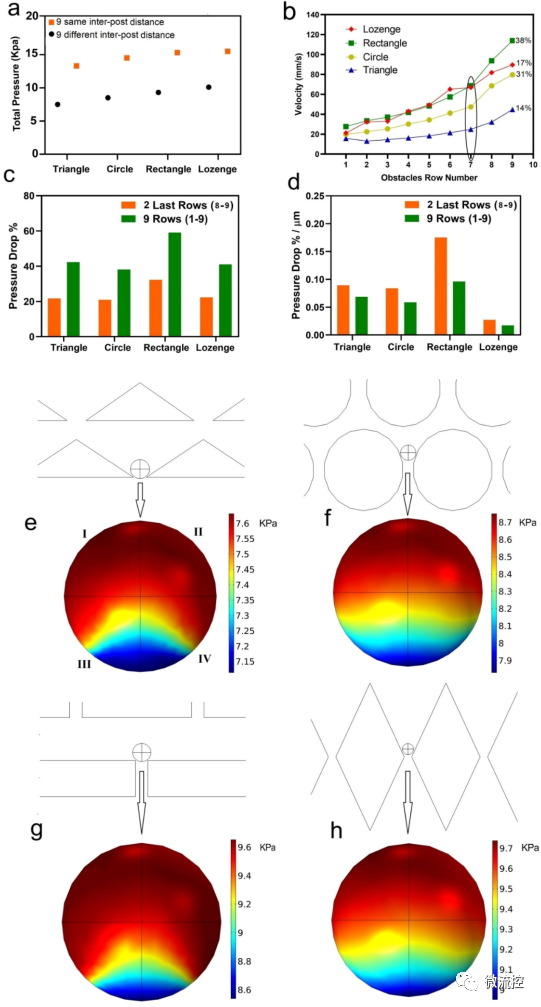
图2 不同几何形状的微流控芯片内流体压力和速度的数值模拟结果
CTCs分离具有许多性能特征,包括捕获效率、富集因子和细胞活力。为了验证所制造的芯片可以有效分离不同癌症细胞CTCs,研究人员使用了两种癌细胞系测试了芯片的性能,一种是前列腺癌细胞系PC3,另一种是乳腺癌细胞系MDA-MB-231。结果表明,菱形微流控芯片具有更好的分离性能,其捕获效率大于85%,纯度大于90%,且分离细胞存活率高达97%。
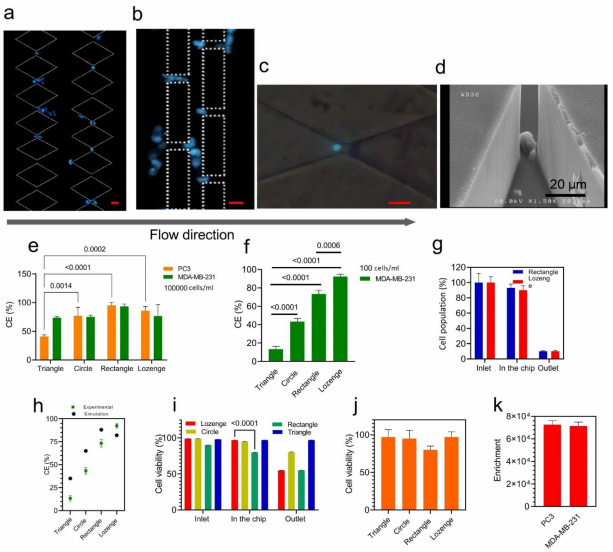
图3 基于不同癌症细胞评估不同类型的微流控芯片性能
最后,研究人员还利用12名乳腺癌患者的血液样本对所设计的微流控芯片的CTCs检测性能进行了验证。
结果证明,所设计的微流控芯片检测到的CTC数值与患者的乳腺癌进展之间具有明确的相关关系,显示出良好的监测癌症发展进程和辅助癌症个性化治疗的潜力。
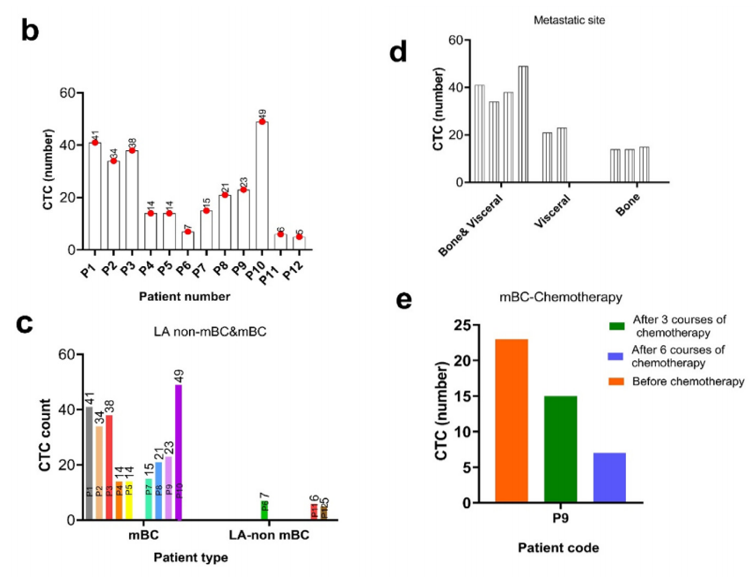
图4 乳腺癌患者循环肿瘤细胞(CTCs)的检测与计数
论文链接:
https://doi.org/10.1016/j.jare.2022.08.005
审核编辑:刘清
-
S型微流控芯片的优势2024-11-01 1432
-
微流控阵列芯片和普通芯片的区别2024-10-30 1503
-
微流控柱阵列装置中微小液滴的形成原理介绍2023-12-11 2391
-
微流控芯片在液体活检中的应用2023-07-25 1250
-
POCT中的“颠覆性技术”——微流控芯片应用实例分享2023-03-22 2927
-
采用离心微流控芯片实现血液中白细胞的分离提取2022-10-31 4337
-
一种用于分泌型自噬小体分离检测的三维微流控芯片2022-07-29 2890
-
一种CTCs分选微流控系统2022-07-22 1459
-
基于液滴微流体的微流控芯片系统的研究2022-03-02 6265
-
一种从患者血液样本中有效分离异质性CTCs的简单、广谱的方法2021-06-11 3371
-
一种用于外泌体分离富集和检测的微流控芯片2018-12-31 5536
-
微流控分析芯片2018-06-22 2489
-
无奇不有!生物芯片也能分离血液中癌细胞2015-12-21 1790
全部0条评论

快来发表一下你的评论吧 !

