

Chem:创纪录!锂金属库伦效率达99.72%!
描述
01
导读
锂离子电池(LIBs)的成功商业化对人们的日常生活产生了深远的影响,尽管近年来对高能量密度LIBs的需求明显增加,但基于石墨负极的电池容量无法满足人们需求。从这个意义上说,锂金属由于其高能量密度而成为最终的负极选择,但以碳酸酯为代表的有机溶剂对锂金属负极(LMA)的热力学不稳定性会导致连续的副反应。其中,无机固体电解质(SEI)组分(LiF,Li2O和Li3N)与LMA表面的弱相互作用,其高杨氏模量和高界面能已被证明可以有效抑制锂枝晶传播并促进锂离子扩散。由于富含有机物的SEI与石墨负极的相容性,碳酸盐电解液已成功应用于传统锂离子电池,在(脱)插层过程中体积变化很小(~13%)。然而,当与LMA匹配时,通常使用碳酸盐电解液中易形成多孔、厚且脆弱的SEI层,其具有低剪切模量,因此通常观察到低库仑效率,从而说明了调整SEI层的成分、厚度和机械性能至关重要。电解液在稳定锂金属表面和高压循环中起着关键作用,特别是局部高浓度电解液(LHCEs),由于其独特的溶剂化结构而优于最先进的电解液。然而,LHCEs中的溶剂化结构,特别是弱配位稀释剂,与SEI组成之间的直接关系还不清楚,而这对于实现超过99.5%的高库仑效率(CE)至关重要。
02
成果简介
近日,权威期刊Chem上发表了一篇题为“Electrolyte engineering for highly inorganic solid electrolyte interphase in high-performance lithium metal batteries”的文章。瑞士弗里堡大学Ali Coskun教授联合韩国首尔国立大学Jang Wook Choi教授等人引入了一类基于二(2,2,2-三氟乙氧基)甲烷(BTFM)和1,2-二甲氧基乙烷的电解液来调节阴离子分解,使SEI中氧化锂(Li2O)含量高达63%,且分布高度均匀。这些独特的特性使库伦效率达到了创纪录的99.72%,并证明了均匀分布的高Li2O SEI对库伦效率的影响。实验结果表明,N/P比为2.5的Li|LiNi0.8Co0.1Mn0.1O2全电池在1C的条件下循环200次后,仍然能够实现90%的容量保持率,在3C的倍率下循环596次后仍然具有80%的容量保持率。
03 关键创新
(1)本文揭示了电解液在增强阴离子分解动力学方面的关键作用,通过降低离子的去溶剂化能,在SEI中实现了均匀、高氧化锂含量至关重要;
(2)由此构成的全电池在1C的条件下循环200次后,仍然能够实现90%的容量保持率,在3C的倍率下循环596次后,仍然具有80%的容量保持率。
04
核心内容解读
1.电解液设计和表征
作者首先对所报告的溶剂和醚类稀释剂进行计算,并按最小ESP( 静电势)值进行分类(图1A)。传统的高于最小ESP值(>120 kJ mol-1)的醚基稀释剂被定义为NCD,而低于最小ESP值的溶剂(<150 kJ mol-1)被定义为强配溶剂(SCS),将NCD和SCS之间的ESP范围定义为弱配位稀释剂(WCD),本文首次展示了WCD在实现均匀分布的最佳阴离子分解方面的关键作用,以达到超过99.5%的高库伦效率。实验结果表明,在BTFM和DME中以7:1和3:1的体积比溶解1 M和2 M LiFSI后,两种电解液均表现出高达5.5 V的抗氧化耐受性,含有BTFM助溶剂的电池的平均库伦效率值明显提高,分别为99.36%(1M LiFSI-7BTFM-1DME)和99.72%(2M LiFSI-3BTFM-1DME),这也是迄今为止报告的最高值。此外,对不同电解液的Li|Cu半电池进行了长循环测试,1 M LiFSI-7BTFM-1DME和2 M LiFSI-3BTFM-1DME电解液的电池在400和500个循环内分别显示出稳定的99.4%的库伦效率。
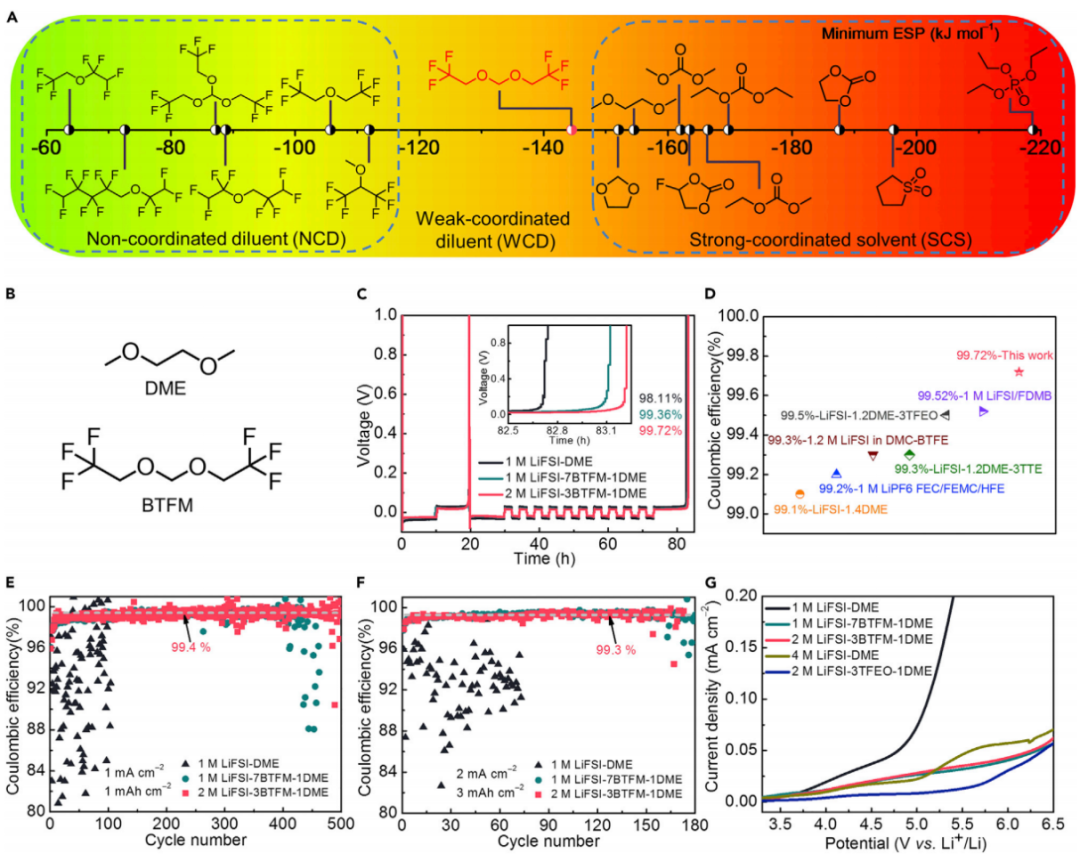
图1 A)计算的稀释剂和溶剂的最小静电势(ESP)。B)二甲醚和BTFM溶剂的化学结构。C)三种电解液的库伦效率测试。D)库伦效率值与以往报告的对比。E,F)三种电解液的Li|Cu半电池的循环测试。G)抗氧化耐受性测试。@ Elsevier
2.锂金属形貌表征
由于库伦效率性能与锂沉积密切相关,通过SEM分析,以证明不同电解液对锂沉积形貌的影响(图2)。实验结果表明,基于1 M LiFSI-7BTFM-1DME的电池锂沉积显示出均匀分布的块状锂,间隙很小(图2B)。同时,在2 M LiFSI-3BTFM-1DME电解液中,较大的块状锂,较小的比面积和较少的裂纹,减少了锂金属与电解液之间的接触和副反应(图2C)。即使循环20次后,1 M LiFSI-7BTFM-1DME和 2 M LiFSI-3BTFM-1DME电解液中的沉积锂都具有更优异的形貌(图2F和2I),这些结果清楚地表明了电解液设计对锂沉积形貌和厚度具有深远影响。

图2 A-C)在不同电解液中循环一次后,在铜箔上的沉积形貌SEM图像。D-F)在不同电解液中循环20次后,在铜箔上的沉积形貌SEM图像。G-I)在不同电解液中循环20次后在铜箔上的横截面SEM图像。@Elsevier
3.锂金属电池的性能
基于优异的锂金属半电池性能和高压稳定性,在少量锂的Li|NCM811全电池和无负极的Cu|NCM811全电池中进一步评估了BTFM基电解液的性能。Li|NCM811全电池(N/P=2.5)在不同电解液中和在1 C下的循环性能如图3A所示,基于BTFM的电解液明显改善了Li|NCM811全电池的性能,1 M LiFSI-7BTFM-1DME电池的容量循环150次后保持在125.9 mAh g-1,容量保持值为81%,使用2 M LiFSI-3BTFM-1DME的全电池表现出最佳的循环稳定性,循环200次后容量为147.4 mAh g-1,且具有90%的容量保持率,这表明通过电解液工程保护锂金属在少量的锂金属全电池中起着关键作用。此外,具有1 M LiFSI-7BTFM-1DME和2 M LiFSI-3BTFM-1DME电解液的无负极全电池在80次循环后,分别表现出更好的容量保持率,分别为51%和64%,这可归因于其强大的SEI形成、受控的锂沉积形貌和优异的锂金属性能。
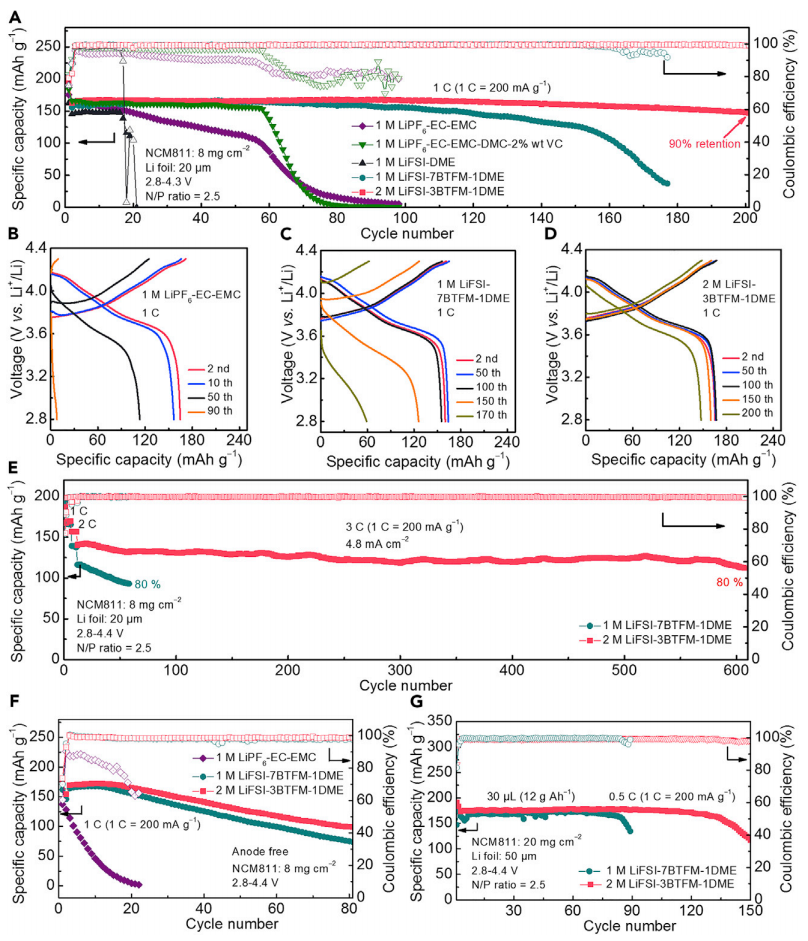
图3 A)在不同电解液中,Li|NCM811全电池的循环性能;B-D)相应的电压曲线;E)高倍率下的循环性能;F)无负极锂金属电池性能;G)苛刻条件下的循环性能。@ Elsevier
4.界面表征
为了说明基于BTFM的电解液的优异性能,进行了X射线光电子能谱(XPS)分析,探测了Li|NCM811全电池在1 C下循环30次后Li负极和NCM正极SEI和CEI组成,对于基于BTFM的电解液,SEI层(及其表面)中的C含量要低得多(<5wt%),说明基于BTFM的电解液的SEI层组成更加均匀, 并且无机物质含量更高,在循环过程中优先掺入无机物种时,SEI层内的锂含量应相对较高。同时,由基于BTFM的电解液形成的SEI层中的锂含量最初随着溅射深度的增加而增加,但在溅射4分钟后达到近似恒定值,这清楚地表明在基于BTFM的电解液中形成了更均匀和富含无机物的SEI层。
此外,图4M证明了SEI层中Li+O含量与库伦效率值之间的可能趋势,值得注意的是,2 M LiFSI-3BTFM-1DME SEI表现出最高的Li+O含量(89%),以及最高的库伦效率值,这一结果清楚地表明,Li2Ox的存在对于获得2 M LiFSI-3BTFM-1DME电解液中99.72%的创纪录最高库伦效率发挥了关键作用。
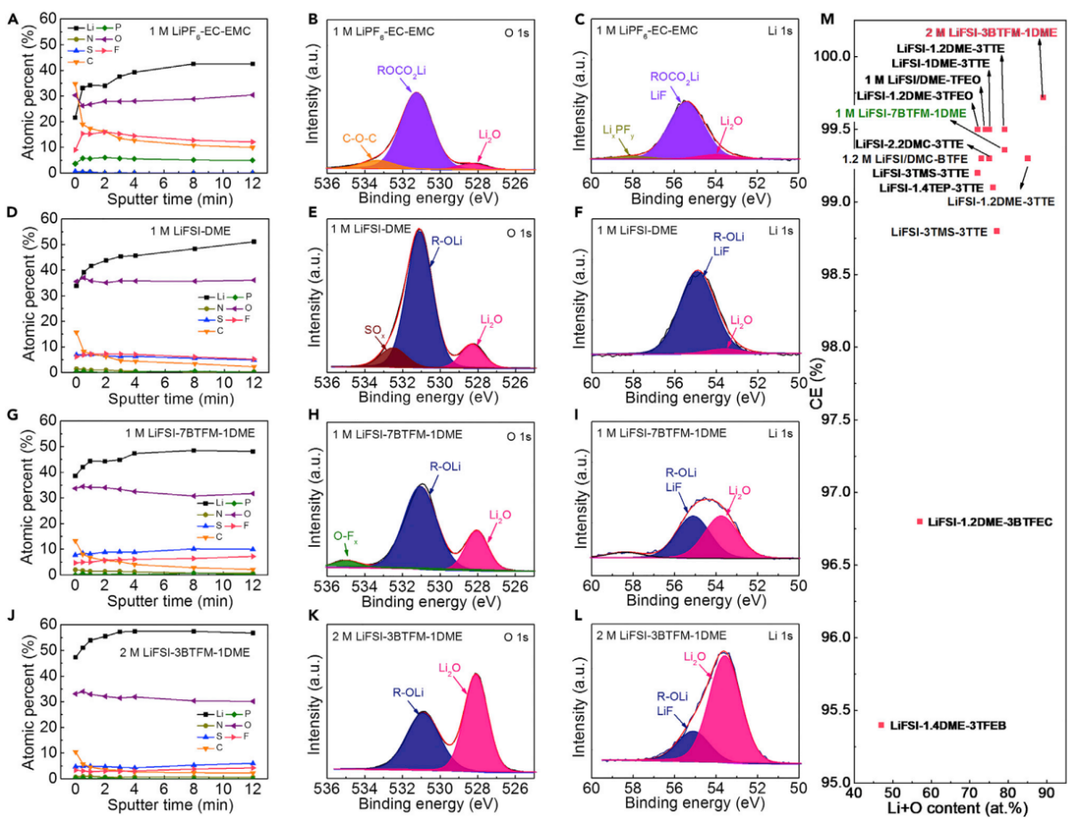
图4 A-L)Li|NCM811全电池中锂金属负极表面SEI层的XPS分析。M)基于BTFM和先前报道的电解液SEI层中的Li+O原子含量与库伦效率值的关系@ Elsevier
5.溶剂化结构
虽然通过XPS分析阐明了SEI和CEI的组成,但电解液分解的相关形成机制仍有待进一步探索(图5)。首先使用拉曼光谱来探测不同电解质中的溶剂化结构(图5A),随着BTFM的引入,游离FSI阴离子的峰值消失了,伴随着748 cm-1处新峰的出现,分配给聚集体(AGG)溶剂化结构,反映了Li和FSI阴离子之间的强配位作用。这一结果非常重要,表明与碳酸酯基稀释剂不同,BTFM作为WCD不会干扰高浓度团簇的形成。此外,通过傅里叶变换红外(FTIR)光谱分析比较了不同电解液的溶剂化结构,伴随着游离DME分子的消失,FSI阴离子与Li+之间的配位性也很强。
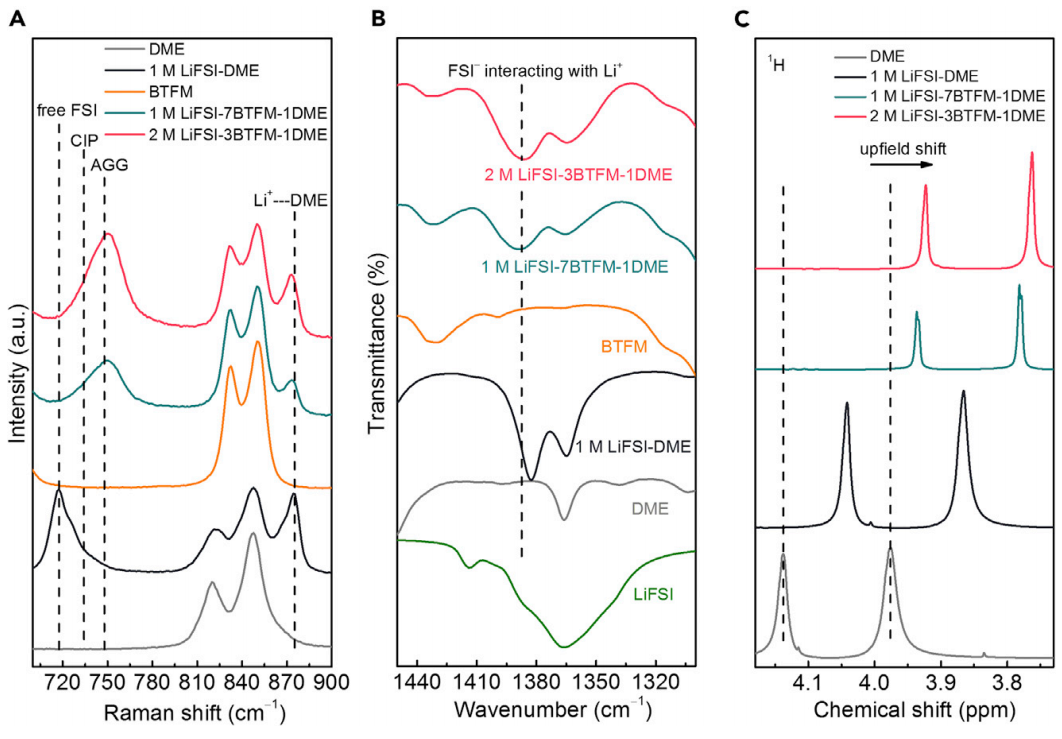
图5 A)不同溶剂和电解液的拉曼光谱;B)不同溶剂和电解液的FTIR光谱;C)不同溶剂和电解液的核磁共振图谱。@Elsevier
05
成果启示
本文介绍了一类基于BTFM的电解液溶剂作为弱配位稀释剂,实现了高无机组分含量SEI和优良的锂负极性能。同时,还揭示了这些电解液在维持聚簇和增强阴离子分解动力学方面的关键作用,通过降低离子的去溶剂化能,在SEI中实现了均匀、高氧化锂含量,使最高库伦效率值达到99.72%,这一结果离无负极全电池99.9%的最终目标又迈进了一步。这项工作不仅强调了氧化锂对高库伦效率的关键作用,而且还强调了通过精心设计的稀释剂和电解液工程来控制SEI的组成、形貌和均匀性的重要性。这些发现也有望指导新型弱配位稀释剂的设计,以进一步推进高电压锂金属电池的发展。
审核编辑 :李倩
-
2018年机器人北美出货量创纪录 达35,000台2019-03-13 976
-
金属锂(Li)的简介2009-12-01 16501
-
Lebara Group 公布创纪录的3.71亿欧元营收2010-01-13 930
-
2020年PC市场将受到创纪录的冲击 主板与显卡出货量大幅下滑2020-03-19 4686
-
金属锂电池聚合物电解质PEO不耐氧化的原因分析2020-04-20 6837
-
中国近期公布创纪录的2021年5G发展蓝图2021-01-06 3066
-
英伟达2021财年第四财季营收同比大增,创纪录的50亿美元2021-02-25 2095
-
探索影响锂金属电池库伦效率的隐藏因素2022-11-16 3769
-
Omdia:2022年,绝非半导体行业创纪录的一年2023-03-07 1338
-
全固态锂金属电池的锂阳极夹层设计2024-10-31 1725
全部0条评论

快来发表一下你的评论吧 !

