

固态电解质实现室温可充的Li2O基锂空气电池
锂电池
描述
具有可充电电池形式的储能对于包括运输和电网储备在内的一系列应用变得越来越重要,锂空气电池因其低成本和高能量密度而提供了巨大的前景,且在能量密度方面具有与汽油竞争的空间。然而,在大多数系统中,反应途径涉及一个或两个电子转移,导致形成过氧化锂(Li2O2)或超氧化锂(LiO2)。
在此,美国伊利诺斯州理工大学Mohammad Asadi助理教授和美国阿贡国家实验室Larry A. Curtiss教授描述一种在室温(25°C)下利用有机和无机电解质优势的锂空气电池,这一发现为在室温下实现锂基化学提供了新的设计机会,同时该电池的能量密度远远高于目前锂离子技术的要求。
研究背景
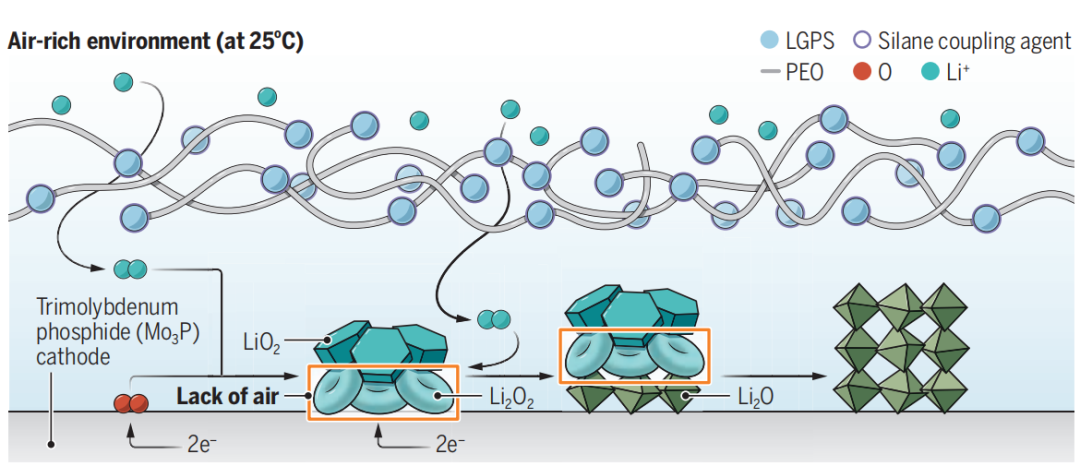
锂空气/O2电池的主要反应产物可以是三种化合物之一:超氧化锂(LiO2,每个氧需要一个电子)、过氧化锂(Li2O2,每个氧需要两个电子)和氧化锂(Li2O,每个氧需要四个电子),最高的容量来自产生Li2O,但在室温和富含空气的环境中,氧(O2)更喜欢接收两个电子形成Li2O2,而不是四个电子产生Li2O,Li2O2在热力学上比Li2O更稳定。
同时,基于O2 /Li2O2的Li-O2电池存在涉及LiO2中间体的副反应,可以降解电极和电解质。另外,由于没有LiO2中间体,不在空气/O2气氛下的双电子Li2O2 /Li2O反应更稳定。但是,Li2O2 /Li2O反应不太可能在富含空气/O2的环境下进行,O2/Li2O2反应会占主导。 因此,这使得很难通过结合两个双电子反应(O2/Li2O2和Li2O2 /Li2O)来实现高能容量的四电子反应。
虽然在使用熔融盐电解质和高选择性催化剂的高温(~150°C)下已经实现了四电子Li-O2反应,但温度要求增加了运行成本。 内容详解 研究发现,在室温下使用具有高离子电导率的稳定固态电解质和催化气体扩散层,可以实现该反应,且固态电解质因其与液态电解质相比使用更安全而受到关注。
同时,基于聚氧化乙烯(PEO)的聚合物电解质,可以通过调节PEO和Li盐浓度,以及通过添加纳米颗粒、交联剂和增塑剂来合理调控。 本文利用硅烷偶联剂mPEO-TMS(3-[methoxy(polyethyleneoxy)6-9 propyl]trimethoxysilane)与含有Li10GeP2S12(LGPS)纳米颗粒化学结合,合成了固态电解质。
其中,LGPS纳米颗粒是高导电,富含锂的离子导体。 同时,本文使用mPEO-TMS的原因在于:
(i)与PEO相比,其分子结构相似,避免了它们之间的任何相分离;
(ii)其较高的锂离子转移数(tLi+);
(iii)以-OCH3为末端,改善了固态电解质的电化学稳定性窗口和Li负极稳定性。
在该复合聚合物电解质(CPE)中,平均微晶尺寸为17±6 nm的LGPS纳米颗粒通过LGPS中Li2S基团中的S原子,与mPEO-TMS中的Si的强化学键合与mPEO-TMS链连接,保护LGPS不在锂金属负极和活性正极界面上分解。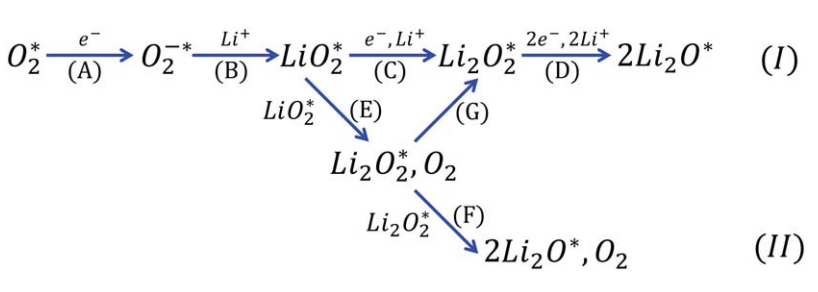
图1. Li2O的形成途径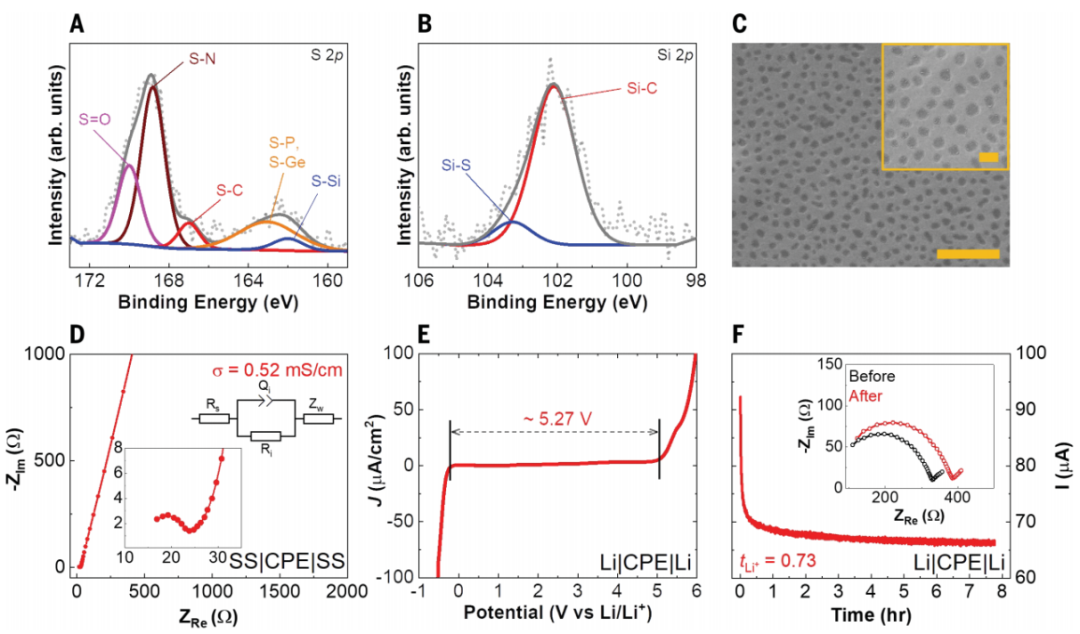
图2. CPE的理化和电化学表征
实验结果表明,作者利用这种设计良好的固态电解质和先前报道的催化剂(Mo3P),在25℃下实现了1000次循环的可逆四电子氧化锂反应。
在前15 min最初观察到LiO2和Li2O2的形成,之后Li2O成为主要放电产物,作者推测,LiO2/Li2O2的初始均匀形成在正极壁上,这可以为进一步的电化学还原提供所需的混合电子/离子传导性质。
在达到稳定状态后,Li2O2在LiO2下被隔离,没有O2存在,而Li2O2直接与正极接触,有利于电子传导,从而允许Li2O2基于双电子还原为Li2O。
结合两个双电子反应(O2/Li2O2和Li2O2/Li2O),得到了非常理想的锂空气化学反应。此外,通过原位拉曼光谱、差分电化学质谱和X射线衍射验证了Li2O的形成。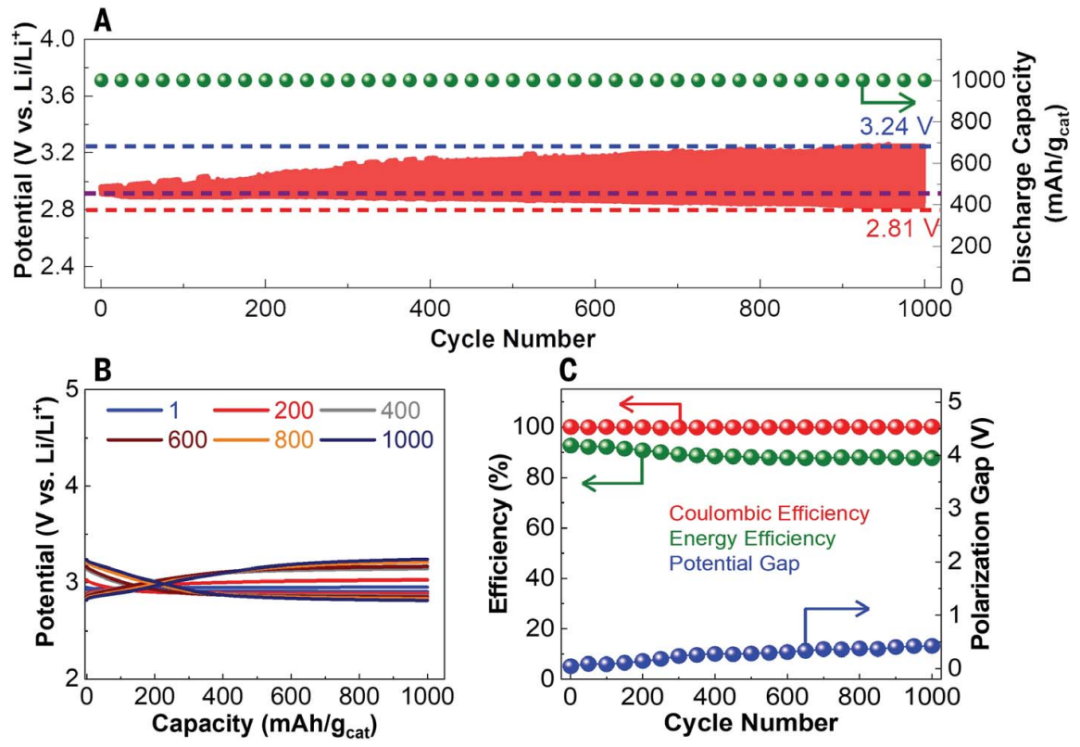
图3. 固态锂空气电池在电流密度为1 A/g和容量为1 Ah/g测试情况下的性能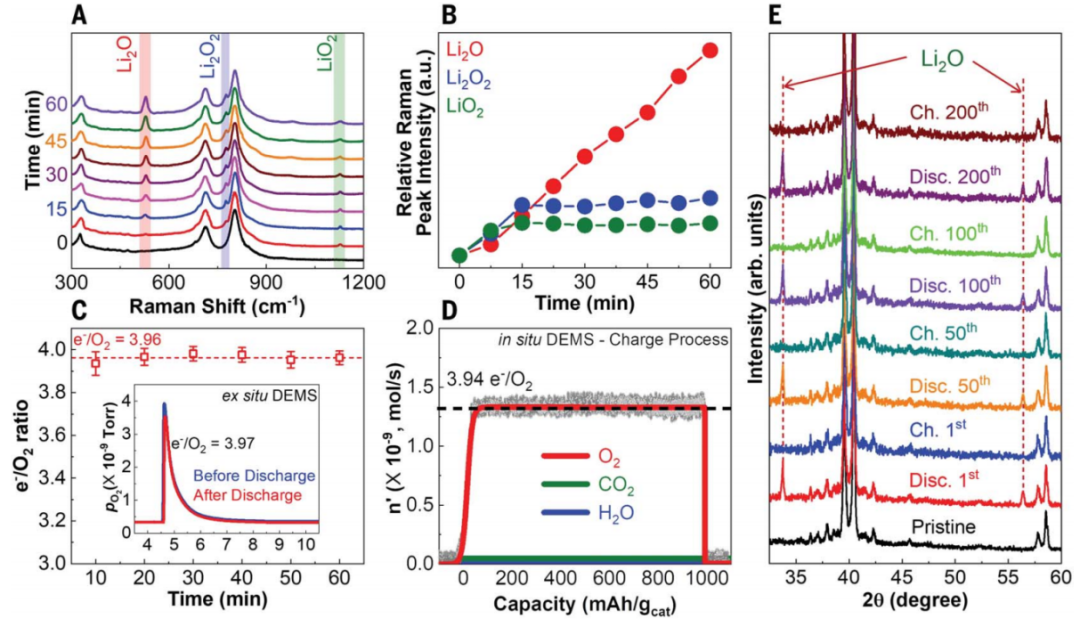
图4. 循环后产物分析
审核编辑:刘清
-
超声波焊接有利于解决固态电池的枝晶问题2025-02-15 707
-
科普:锂空气电池是什么?2016-01-11 3130
-
解密:锂空气电池2016-01-12 5607
-
基于溶液制造固态电池电解质2020-03-23 2973
-
剖析稳定锂金属电池的长效固体电解质界面2021-06-04 3612
-
原位固态化聚合物电解质基高性能准固态软包锂电池2022-06-22 11206
-
氟化石墨烯增强聚合物电解质用于固态锂金属电池2022-09-28 4298
-
改变电解质分布调控固态界面实现高性能固态电池2022-10-21 4132
-
如何有效构建固体电解质的高亲锂界面?2022-11-24 2368
-
关于全固态锂金属电池的高性能硫化物电解质2023-01-16 4025
-
高电压稳定的固态电解质实现高能量、高安全的固态锂金属电池2023-03-27 2346
-
锂金属电池室温固态聚合物电解质的锂离子传导机制2023-04-15 4530
-
铌酸锂调控固态电解质电场结构促进锂离子高效传输!2024-05-09 2959
-
清华大学:自由空间对硫化物固态电解质表面及内部裂纹处锂沉积行为的影响2025-02-14 1141
-
致密化硫化物电解质实现无枝晶高电流锂沉积2026-05-19 93
全部0条评论

快来发表一下你的评论吧 !

