

MBenes新领域:高活性CO氧化催化剂科普
描述
CO是人类社会生产生活产生的危害极大的污染物,消除CO是环境治理的重要任务之一,对于工业生产也具有重大意义。CO氧化反应(COOR)的转化效率非常依赖于催化剂的活性。在本文中,作者选择了18种氧官能化MBenes作为研究对象,探索其CO氧化催化活性及活性机理。
研究表明,有4种氧官能化MBenes展现出比CeO2更高的本征CO氧化催化活性,并可承受1000 K的高温。其中,orth-Mo2B2O2, hex-V2B2O2, hex-Cr2B2O2的COOR催化活性甚至优于部分贵金属负载型催化剂,因此可以直接用作CO氧化催化剂。
而hex-Mo2B2O2可以代替CeO2作为负载型COOR催化剂的基底材料,通过表面修饰获得更高的催化活性。进一步研究表明,氧官能化MBenes的COOR催化活性随成分变化展现出元素周期性,过渡金属越靠近周期表的右上方,催化活性越高。此外,研究还发现最大反应吉布斯自由能还与氧空位形成能具有高度相关的线性关系,因此可以将氧空位形成能作为快速筛选高活性CO氧化催化材料的指标之一,从而大幅降低筛选的工作量。
背景介绍
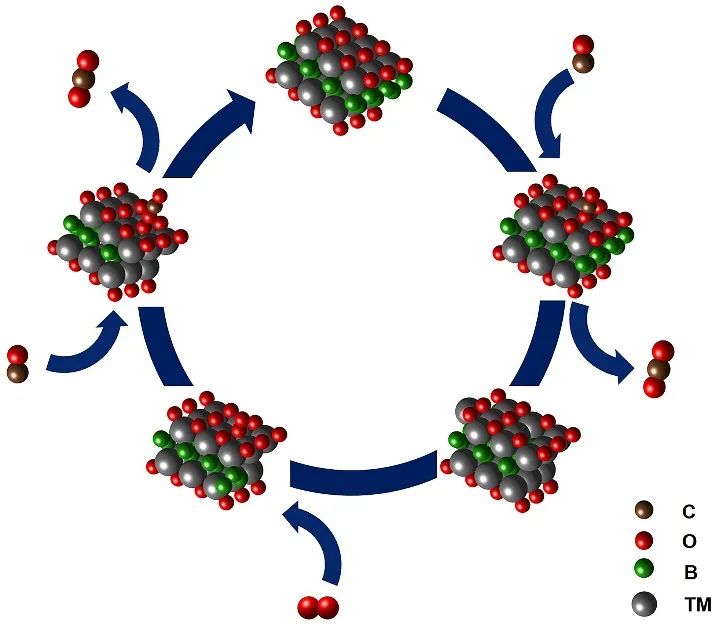
CO氧化反应(COOR)是处理CO废气的重要反应,尤其是汽车尾气。目前汽车尾气处理装置中使用的催化剂多为CeO2基贵金属催化剂,其原理是CeO2基底与贵金属共同发挥催化作用,反应机制为Mars–van Krevelen(M-vK)机制。然而,这类催化剂大多依赖贵金属,并且CeO2的本征COOR催化活性较低。
因此,寻找具有高本征催化活性的非贵金属COOR催化剂对降低成本和提高效率具有重要意义。我们的初步研究表明,原始MBenes表面上极易形成氧官能团,并容易带有氧空位,说明表面氧原子的结合强度不高,易于利用,有望展现高本征COOR催化活性。因此,本文围绕18种正交型和六方型氧官能化MBenes(orth/hex-M2B2O2,M=Ti,V,Cr,Zr,Nb,Mo,Hf,Ta,W)进行了COOR催化性质研究。
研究目标
筛选具有本征COOR催化活性高于CeO2的氧官能化MBenes,阐明COOR催化微观机理,并基于筛选数据构建COOR催化活性的描述符。
图文精读
CO氧化反应(COOR)有三种不同的反应机制:Langmuir–Hinshelwood (L–H) 机制,Eley–Rideal (E–R) 机制和Mars–van Krevelen (M–vK) 机制(机理示意图)。目前汽车尾气处理装置三元催化转化器中使用的催化剂多以M-vK机制进行反应。在该机制中,催化剂本身的晶格氧原子直接参与反应将CO氧化为CO2,而缺失的氧原子由氧气分子进行补充。因此,以M-vK机制进行COOR催化的材料必须具有易于利用的氧原子。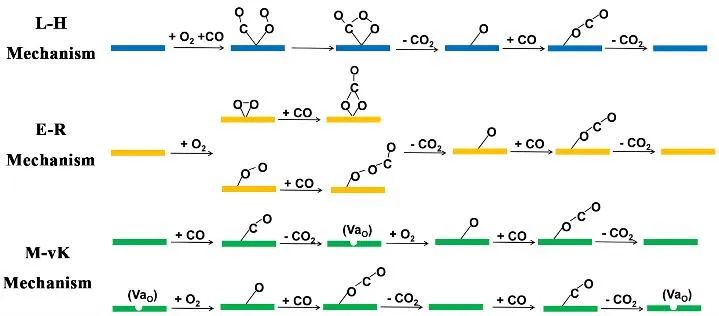
机理示意图
COOR催化的三种机制:L-H机制,E-R机制和M-vK机制
MBenes表面为暴露的过渡金属原子层,容易与氧气发生反应形成表面氧官能团。本文研究的18种氧官能化MBenes的结构如图1所示,在常温下所对应的氧官能团形成能全部为负值。这意味着在常温下暴露在空气中的MBenes表面会自发形成氧官能团。
在18种M2B2O2表面,形成一个氧空位所需要的能量范围在2.55 eV~5.59 eV之间。作为对比,Ti2CO2和Ti3C2O2 MXenes的氧空位形成能分别为4.5 eV和5.0 eV(图2)。实验研究表明,制备得到的Ti2CO2和Ti3C2O2表面具有大量氧原子空位,说明M2B2O2也易形成表面氧空位,这为其以M-vK机制进行COOR催化奠定了基础。
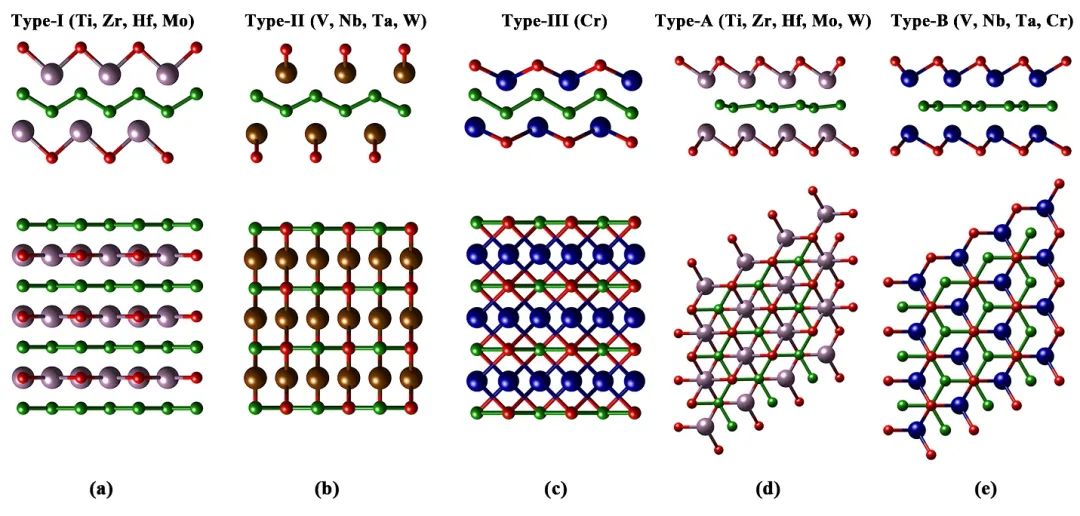
图1 氧官能化MBenes的结构:(a) type-I,(b) type-II和(c) type-III型orth-M2B2O2以及(d) type-A和(e) type-B型hex-M2B2O2。B原子和O原子用绿色和红色表示,其他颜色代表不同的过渡金属原子
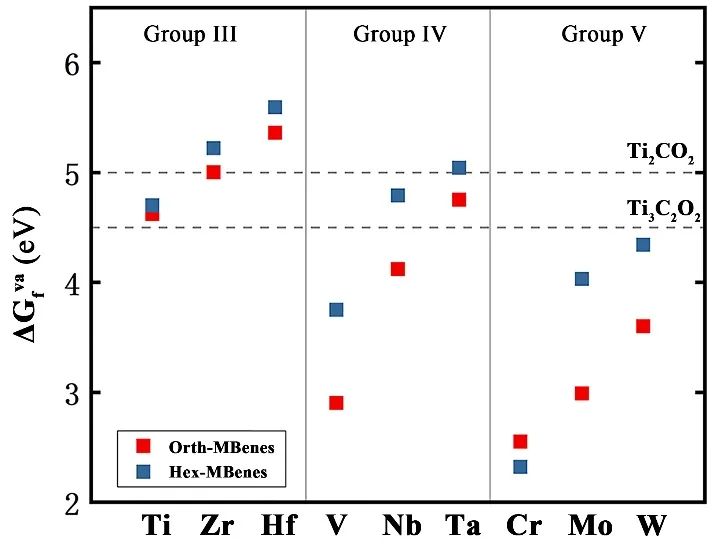
图2 氧官能化MBenes以及Ti2CO2和Ti3C2O2的氧空位形成能 如图3a所示,氧空位处O2的吸附能全部为负值,而CO的吸附能为正值,说明M2B2O2表面的氧空位可以自发吸附O2分子,并且吸附能力远高于CO。O2分子填补了氧空位,同时在表面留下一个凸出的氧原子,如图3b所示。
O2吸附在空位处后,O-O键被不同程度地拉长。Bader电荷计算结果表明,O-O键的延长量与O2分子从基底获得的电子数目成正相关,展现出高度的线性相关性(图3c)。
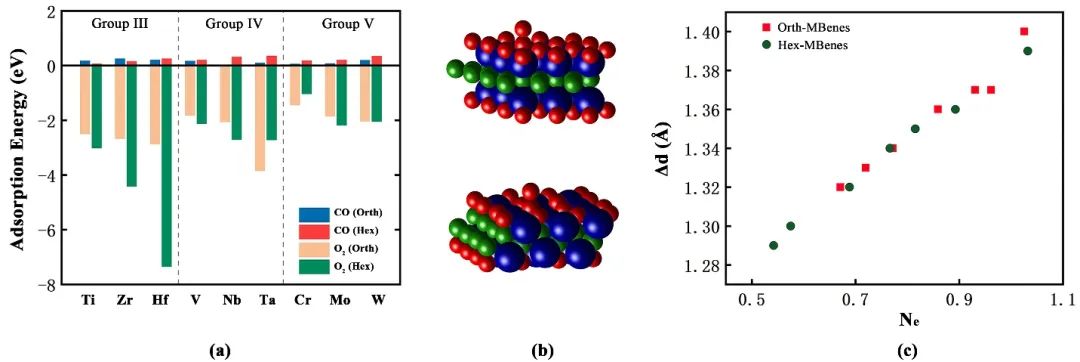
图3 (a) O2和CO在orth-M2B2O2和hex-M2B2O2中氧空位处的吸附能;(b) 氧气吸附在氧空位处后的结构;(c) O–O键延长量(Δd) 和O2分子获得的电子数目 (Ne)之间的关系 O2分子被活化后,O-O键极易发生断裂。
当CO分子靠近催化剂时,外端的O原子脱离基底的束缚,直接与CO分子结合形成CO2分子。对于所研究的18种M2B2O2,这一过程都是自发进行的,并且会放出大量的能量(反应吉布斯自由能=-4 ~ -6 eV);CO2分子呈游离态而不是结合在M2B2O2基底上。Bader电荷分析结果表明,CO2和M2B2O2之间几乎不存在电子转移,说明CO2在M2B2O2上的吸附方式为物理吸附。
因此,CO2脱附仅需要0~0.5 eV的能量(图4a)。对于本文考察的所有M2B2O2来说,最大反应吉布斯自由能都在第四步或第五步,即第二个CO分子的吸附或第二个CO2分子的脱附过程。在18种M2B2O2中,有8个体系的最大反应吉布斯自由能小于CeO2,分别是orth-V2B2O2、orth-Cr2B2O2、orth-Nb2B2O2、orth-Mo2B2O2、orth-W2B2O2、hex-V2B2O2、hex-Cr2B2O2和hex-Mo2B2O2。
并且,其中部分体系的最大反应吉布斯自由能甚至低于CeO2负载型Pt/Au单原子催化剂,展现出极高的COOR催化活性。进一步的AIMD研究表明,orth-Mo2B2O2、hex-Mo2B2O2、hex-V2B2O2和hex-Cr2B2O2可以在1000 K高温下保持结构稳定。因此,这些氧官能化MBenes可在COOR催化中直接用作催化剂,或作为负载型催化剂的基底材料。
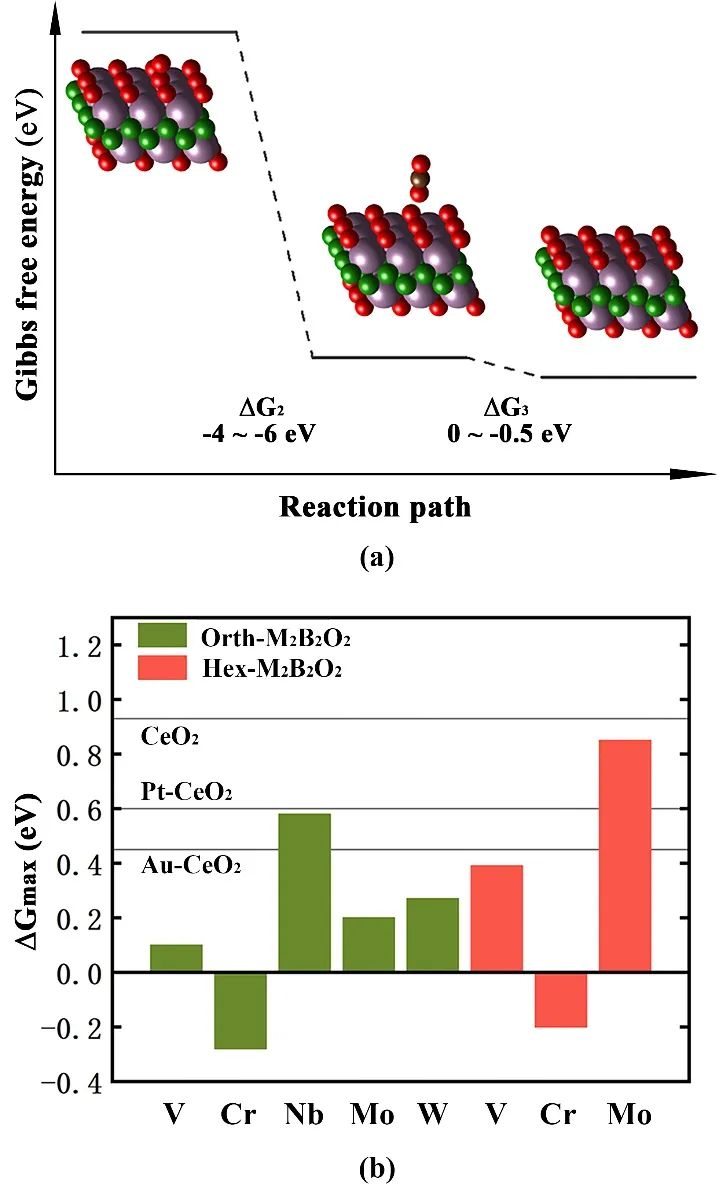
图4 (a) 第一个CO2形成过程的吉布斯自由能阶梯图;(b) orth-V2B2O2、orth-Cr2B2O2、orth-Nb2B2O2、orth-Mo2B2O2、orth-W2B2O2、hex-V2B2O2、hex-Cr2B2O2和hex-Mo2B2O2的COOR最大反应吉布斯自由能,横线代表CeO2, Pt–CeO2 和Au–CeO2的最大反应吉布斯自由能 从图5a和b所示的三维柱状图中可以看出,同种结构的M2B2O2的最大反应吉布斯自由能随过渡金属种类的变化展现出周期性变化规律:在同一周期内,M的原子序数越大,最大反应吉布斯自由能越小;在同一族内,M原子序数越大,最大反应吉布斯自由能越小。即M越靠近元素周期表的右上方,所对应的M2B2O2的最大反应吉布斯自由能越小,COOR催化活性越高。
由于氧空位形成能也展现出了相同的周期性变化规律(图2),因此,将最大反应吉布斯自由能与氧空位形成能联系起来后发现,两者之间呈高度线性相关,拟合系数达到0.94;作为比较,CeO2也示于图中,在拟合直线附近(图5c)。这说明氧空位形成能的值可以直接反映出最大反应吉布斯自由能的大小,即COOR催化活性。
因此,可以将氧空位形成能作为COOR催化活性的描述符。在筛选COOR催化剂时,只需要计算材料的氧空位形成能,无需对每一步基元反应进行吉布斯自由能的计算,即可在大量候选材料中筛选出高活性COOR催化剂,从而节约了大量的筛选成本。
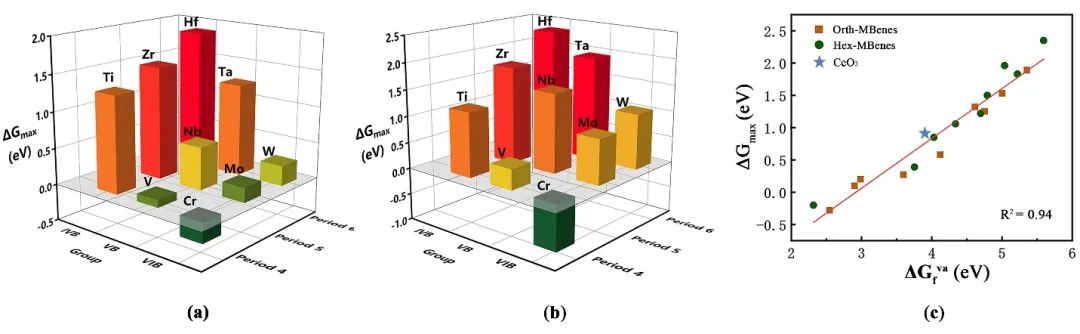
图5 (a) orth-M2B2O2和(b) hex-M2B2O2 的最大反应吉布斯自由能随过渡金属种类变化的示意图;(c)orth-M2B2O2和hex-M2B2O2的最大反应吉布斯自由能与氧空位形成能的关系
总结与展望
在本文中,我们展示了氧官能化MBenes在COOR热催化领域的应用,这是基于其表面的氧原子易于被利用的特性。经过筛选得到的高活性氧官能化MBenes不仅可以用作非贵金属COOR催化剂,同时也可将其用作催化剂基底来进一步提高COOR催化活性。更重要的是,我们发现了氧空位形成能可以作为COOR催化活性的描述符,从而大幅降低筛选工作的计算量。 本文研究发现,成分相同的情况下,六方型M2B2O2比正交型M2B2O2具有更高的热稳定性,因此可在热催化领域发挥作用。另一方面,目前实验上成功制备的MBenes全部为正交型,这也启发我们可以在利用高温条件下的稳定性制备六方型MBenes。作为一类新兴的二维材料,MBenes大多被用于电催化反应研究,尤其是还原反应,而很少被用作热催化反应和氧化反应的催化剂。希望本文可以为MBenes在热催化和氧化催化领域的发展提供启发。
审核编辑:刘清
- 相关推荐
- 热点推荐
- 催化剂
-
石墨烯负载金属氧化物催化剂的制备方法2023-08-11 2349
-
构建提高酸性水氧化催化剂稳定性的氧扩散路径2023-08-02 1975
-
CO2辅助生成富含晶界的Cu催化剂实现高效CO-CO偶联2023-03-17 2077
-
揭示卤素掺杂Sn基催化剂促进CO2电还原制甲酸盐原因2022-12-29 4186
-
如何提高HEAs催化剂的催化活性和优选设计研究2022-12-14 1884
-
“纳米岛”型催化剂突破传统催化剂活性和稳定性的矛盾2022-11-18 1748
-
应变效应对催化剂活性的影响2022-10-26 3605
-
Mo配位FeCoNiMo碳负载高熵电催化析氧催化剂图文解析2022-09-20 3475
-
生成CO的催化剂与Cu之间的相互作用2022-08-22 3989
-
低结晶和异质结构AuPt-Ru@CNT像高效多功能电催化剂2022-05-31 757
-
高活性生物质碳负载Fe/Pt单原子双功能催化剂开发2021-02-12 3589
-
高效电催化二氧化碳还原反应催化剂成功研制2020-03-30 5491
-
CH4与CO检测气敏元件中催化剂的制备与反应性能研究2016-12-17 818
-
碱性醇类燃料电池新型催化剂的研究2011-03-11 1980
全部0条评论

快来发表一下你的评论吧 !

