

一种基于微流控的血管芯片模型设计
描述
由美国北卡罗来纳大学教堂山分校医学院(UNC School of Medicine)William Polacheck博士领导的研究小组设计了一种基于微流控的血管芯片模型,用于模拟一种罕见的遗传疾病。这种疾病会影响静脉、动脉、毛细血管和淋巴管的结构。
我们的身体由6万英里长的复杂管道组成,这些管道在输送营养物质到全身、进行废物处理以及为我们的器官提供新鲜氧气和血液方面发挥着至关重要的作用。
这个复杂的管道系统有时候会出现问题并导致一些包括脉管畸形(VMs)在内的病变。脉管畸形是一组罕见的遗传疾病,在出生时就会导致静脉、动脉、毛细血管或淋巴管的异常,并可以通过阻塞、排水不畅、形成囊肿和缠结来干扰我们重要的管道功能。
据麦姆斯咨询报道,为了解决进一步研究的需要,北卡罗来纳大学教堂山分校(UNC)-北卡罗来纳州立大学(NCSU)生物医学工程和细胞生物学与生理学联合系的助理教授William Polacheck博士和他来自UNC的团队开发了一种血管芯片模型,用于模拟由PIK3CA基因(PIK3CA基因和多种类型的淋巴、毛细血管和静脉畸形有关)突变引起的脉管畸形。该研究近期以“Microphysiological model of PIK3CA-driven vascular malformations reveals a role of dysregulated Rac1 and mTORC1/2 in lesion formation”为题发表在美国科学促进会(AAAS)的Science Advances期刊上。
Polacheck说:“PIK3CA突变存在许多‘先有鸡还是先有蛋’的问题。比如,是PIK3CA的突变导致其它方面出现问题,还是环境中有其它因素导致突变产生更严重的影响?利用基于微流控的血管芯片模型构建一个更可控的环境,使我们能够获得一个孤立的系统,并弄清楚疾病的遗传与细胞中发生的事情之间的关系。”
脉管畸形是由引导全身脉管系统发育的基因发生突变而导致的结果。磷脂酰肌醇-4,5-二磷酸3-激酶催化亚基α(PIK3CA)就是其中一种基因。激活PIK3CA的突变通常会导致较小血管的畸形,导致血液在皮肤下聚集。这种特殊类型的脉管畸形通常在出生时就能够被发现。然而,由于在儿童发育阶段脉管畸形会发生许多变化,因此研究人员很难对其进行研究。
组建中的团队
UNC儿科血液肿瘤学教授、医学博士Julie Blatt认为需要一种新的方法来模拟这种影响了她大多数患者的疾病。长期以来,她一直对脉管畸形患者的临床管理以及利用癌症药物治疗脉管畸形疾病感兴趣。Blatt博士对生物医学工程师Polacheck之前的论文手稿印象深刻,于是拿起电话,对Polacheck进行了陌生拜访,询问他是否可以创建一个PIK3CA特异性脉管畸形微流控模型。
Blatt博士说;“我认为,跨学科研究将极大促进该微流控模型应用于患者的可能性。Polacheck实验室已经优先研究了与患者相关的基因突变以及我们知道或认为会有好处的药物。”
大约在同一时间,Wen Yih Aw博士在UNC Catalyst(这是Eshelman药学院下设的一个专注于了解罕见疾病的研究小组)担任博士后研究员。Aw原先与Polacheck实验室合作研究血管型埃勒斯-当洛斯综合征项目,最终,Aw加入了Polacheck实验室,并利用她的分子生物学专业知识帮助开发基于微流控的血管芯片模型。
除了Blatt博士和Aw博士之外,该实验室还与正在帮助分析网络结构的UNC文理学院数学系和计算医学项目的Boyce Griffith博士进行了持续的合作。
基于微流控的血管芯片模型工作机制
基于微流控的血管芯片模型是非常小的、大约一毫米大小的三维(3D)器件,可用于控制或模拟体内环境。在该研究中,由健康的人内皮细胞或表达PIK3CA突变的内皮细胞组成的一小块血管位于器件的中心。利用该模型,研究人员可以观察血管形成的过程,并在模型中引入特定的化学物质和机械力来模拟人体状况。随着PIK3CA突变的引入,可以观察到扩张且不规则的血管形成。此外,为了确认该模型是否可以准确模拟疾病状态,研究小组接下来进行了一项药物疗效研究。
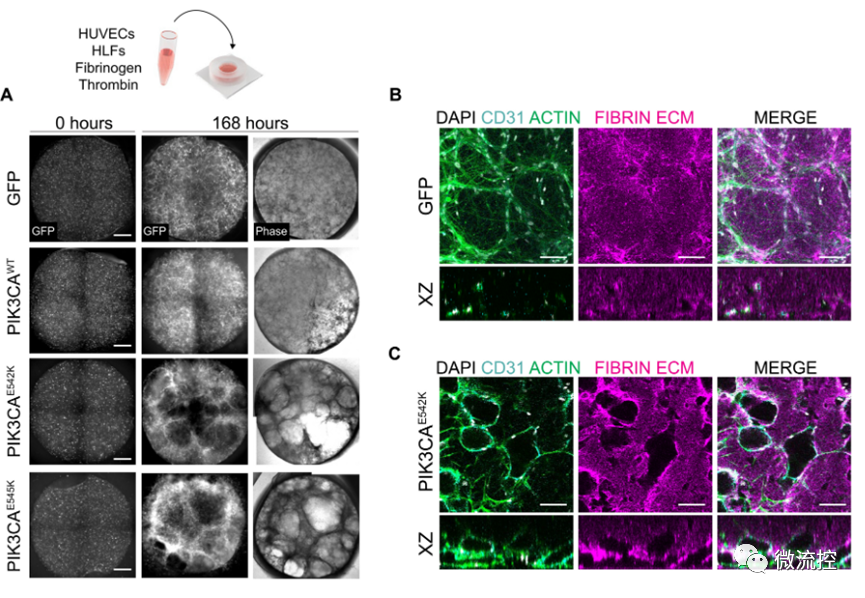
PIK3CA亚型表达激活的内皮细胞3D微流控模型,复现与脉管畸形相关的不规则和扩张的血管表型
目前有两种药物用于治疗脉管畸形:雷帕霉素和阿培利司。后者是一种新发现的PIK3CA特异性抑制剂,最近被FDA批准用于治疗某些类型的乳腺癌以及和PIK3CA相关的过度生长疾病谱系。到目前为止,在小鼠模型和患者身上的临床前研究表明,阿培利司在逆转脉管畸形缺陷方面更有效。
在选择了这两种药物后,Polacheck和Aw将其应用到构建的微流控器件上。这项研究的第一作者Aw说:“通过对药物治疗前后的血管成像,我们观察到扩张的血管经历了血管收缩,或多或少地恢复到正常的形状和功能。我们非常高兴能够用我们建立的血管芯片模型进行体外模拟实验。”
展望未来,Aw和Polacheck希望能够利用脉管畸形患者的组织来复现这一研究,尤其是那些没有PIK3CA突变或没有明确遗传信息的患者。此外,该基于微流控的血管芯片模型目前可以用来评估新的药物或进行协同药物研究。
多样化的未来研究路径
目前,该微流控模型已被证实是有效的,因此,Aw和Polacheck计划用该模型来研究突变细胞的行为,以及突变如何影响淋巴组织的畸形。
这种疾病最初始于发生PIK3CA突变的单个细胞。然后,就像链式反应一样,该细胞突变的影响会扩散到周围的细胞,直到畸形完全形成。该微流控模型目前还无法模拟这一自然过程。
Aw目前正在研究一种新的微流控模型。她的目标是创建一个平台,能够引发健康细胞的突变,并观察突变在感兴趣的组织中的发展。最终希望该平台能够真正帮助研究人员了解突变是如何影响其它细胞并在体内扩散。
脉管畸形也可以发生在淋巴组织中。与血管不同的是,淋巴管负责在全身循环多余的液体,并充当免疫细胞到达感染部位的高速通道。目前,人们对淋巴内皮细胞的基本细胞生物学特性知之甚少,所以Polacheck希望能基于淋巴组织做一项类似的研究。Polacheck说:“淋巴管的功能与血管不同,所以二者的研究结果也略有不同。通过对两者的研究结果,我们也将能够了解这两种组织的基本生物学特性。”
审核编辑:刘清
-
有没有可能发展出稳定的水凝胶微流控芯片制造方法?2018-11-07 4618
-
一种用于外泌体分离富集和检测的微流控芯片2018-12-31 5565
-
芯片上的器官模型 有专门的微流控平台2020-03-23 3950
-
一种整合型的微流控芯片新设计2020-11-25 4440
-
一种新型的微流控-电化学检测系统2021-05-30 4223
-
一种用于评估药物体外递送效果的肺-肿瘤-血管芯片模型2022-05-26 5773
-
基于微流控的血管芯片来模拟人体血管内部剪切力分布状况2022-06-14 4803
-
一文读懂什么是微流控芯片2022-08-24 10451
-
基于纸基微流控芯片的工作原理2022-10-24 5949
-
一种多层纸基微流控芯片设计2023-04-21 4118
-
介绍一种高通量多重比色离心微流控芯片2023-06-29 2391
-
介绍一种高灵敏度多靶标核酸检测微流控芯片2023-08-16 2860
-
一种光固化通道数字微流控芯片(pCDMF)2024-01-03 1630
-
介绍一种用于绝对定量的微腔式数字PCR微流控芯片2024-03-04 2439
-
芯片上集成功能性血管化类器官的微流控平台2024-11-18 1057
全部0条评论

快来发表一下你的评论吧 !

