

基于强化学习的生物分子手性传感器
描述
手性是自然界物体最基本的属性之一,在诸多领域中具有重要的作用。尤其在医疗生物化学领域中,检测与区别同一组分相反手性的对映异构体是一个非常重要的课题。自然界中的大部分生物分子的手性光学响应非常微弱,且其波段常常位于紫外光波段,因此直接检测分子的光学手性非常困难。
由于表面等离激元具有放大光学手性信号的能力,所以基于表面等离激元的手性探测被认为是未来生物分子检测的有力手段。该方法的关键在于针对目标生物分子寻找合适的金属纳米结构,使得二者的耦合信号尽量显著。然而,表面等离激元与生物分子的耦合机制非常复杂,难以准确地进行定量分析,这极大地增加了金属纳米结构的设计难度。
近年来,人工智能的高速发展催生了一批卓越的自学习算法,强化学习正是其中之一。它通过与环境进行交互获得的结果指导行为的改变,类似于一个生物体不断适应环境的过程。机器学习的引入也大幅推动了微纳光子学的发展,在设计光子晶体、超材料和集成硅光子器件等领域都取得了令人瞩目的成就。
近期,北京大学物理学院方哲宇教授课题组尝试利用强化学习方法设计了生物分子手性传感器件,实现了对葡萄糖对映异构体的高灵敏手性动态监测(图1)。该探测技术的基本原理是利用金属表面等离激元与生物手性分子的耦合效应,这一耦合会导致加入生物分子前后金属纳米结构的远场手性光谱发生变化,通过捕捉光谱前后的变化,就可以实现对生物手性分子的传感。

图1 生物分子的手性传感
该工作采用强化学习来实现高手性纳米结构的设计,在利用神经网络模型引导探索参数空间的同时,不断更新神经网络模型的参数,其工作流程如图2所示。相比于传统的有监督学习,强化学习大幅减少了模拟计算消耗的计算资源。在经典的有监督学习中,首先需要进行大量的电磁模拟来获得各种构型金属纳米结构的光学响应,再根据神经网络的预测寻找优秀的金属纳米结构。
而神经网络的准确预测需要所有构型的训练数据,这其中包含了大量弱手性结构,浪费了大量的计算资源和计算时间。而强化学习模型选择参数探索与模型训练同时进行,经过数轮探索后可以将探索范围基本锁定在高手性结构的范围内,从而大幅减少模拟计算的次数。整个设计过程充分实现了智能化,对未来微纳光子学器件的设计有极高的引导意义和参加价值。
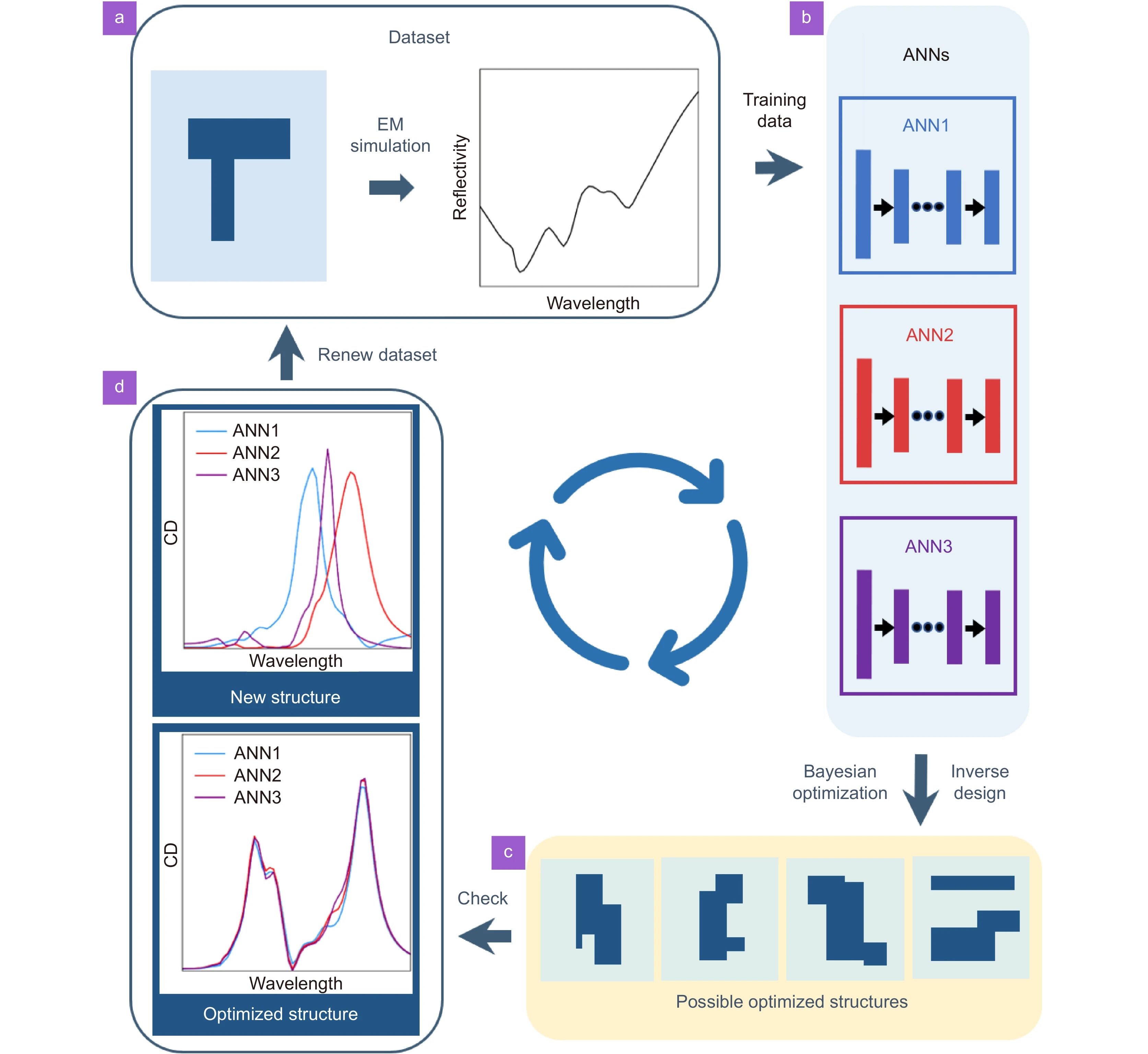
图2 基于强化学习的算法框架
该工作将金属纳米结构制备在微流控芯片底部,通过实时观测光谱的变化来实现对通入微流控芯片的样品溶液的手性检测。相比于传统生物化学方法,这一探测手段具有极高的便捷性,不需要化学反应就可以实现手性甄别,样品需求量低且没有破坏性,具有优秀的应用价值,对各种生物大分子都具有实现高灵敏手性探测的潜力。
审核编辑:刘清
-
电化学生物传感器在生物检测领域的显著优势2024-04-29 2439
-
三郡科技:电化学生物传感器电极与生物芯片的异同2024-04-28 3240
-
生物分子传感器研究进展2023-05-17 1553
-
深度强化学习实战2021-01-10 2918
-
浅析化学传感器和纳米传感器2019-07-02 2168
-
反向强化学习的思路2019-04-03 2460
-
电化学生物传感器前景2018-12-17 13420
-
DNA场效应管传感器的分子设计2018-10-25 2604
-
将深度学习和强化学习相结合的深度强化学习DRL2018-06-29 28820
-
电化学生物传感器之医学应用2018-03-21 13324
-
化学与生物传感器2011-02-16 1026
-
压电生物传感器及其研究进展2009-07-14 850
-
分子自组装及其在传感器中的应用2009-07-06 534
-
光纤DNA生物传感器的研究动向2009-07-02 642
全部0条评论

快来发表一下你的评论吧 !

