

弱溶剂间相互作用提高电池电解质稳定性
描述
研究背景
在金属离子电池中,电解质在运输金属离子(如Li+)方面起着重要作用,但了解电解质性能与行为之间的关系仍然具有挑战性。近些年来,通过改变溶剂、阴离子、添加剂等的类型和数量来改变金属离子(M+)—溶剂、M+ —阴离子对和阴离子—溶剂之间的相互作用,从而调节电解质的性能的研究受到了广泛的关注。但是,溶剂-溶剂之间的相互作用却很少被提及,因为这种相互作用被认为是非常弱的,比M+—阴离子之间的离子-离子相互作用和M+—溶剂之间的离子-偶极子相互作用要弱1 - 2个数量级。但是,考虑到在商用电解质(1 M)中,溶剂的摩尔数要比阳离子和阴离子的摩尔数高10 ~ 12倍,因此,明确溶剂-溶剂之间的相互作用对电解质性能的影响是很有必要的。
成果简介
近日,中国科学院长春应化所明军教授通过核磁共振(NMR)等表征模拟发现电解质中存在弱溶剂-溶剂相互作用且具有显著的稳定电解质的功能。作者深入研究了碳酸乙烯脂(EC)溶剂在锂离子电池电解液中的作用。发现EC溶剂可以通过弱的分子间相互作用稳定线性碳酸盐溶剂电解质,特别是碳酸二乙酯(DEC)电解质,增强Li+ (EC)x(DEC)y配合物轨道间的能量差,从而表现出较强的抗还原能力。该观点在其他金属离子电池(如Na+, K+)中得到了进一步的验证,该发现对设计电解质和深入理解电池性能具有重要意义。该工作以“Weak Solvent−Solvent Interaction Enables High Stability of Battery Electrolyte”为题发表在ACS energy letters上。
研究亮点
1、作者基于核磁等方法发现EC溶剂的引入可以与DEC溶剂形成弱的溶剂间相互作用以稳定电解质。
2、通过模拟计算认为溶剂间的相互作用可以影响Li+ (EC)x(DEC)y配合物轨道之间的能量差(即ΔE = HOMO−LUMO),以提高电解质的抗还原能力。
3、这种弱的溶剂间相互作用也存在于EMC基电解质及K/Na离子电池的电解质中,影响电解质性能。
4、需要深入研究,进一步量化溶剂-溶剂间的相互作用,以估计出通过相互作用强度稳定电解质的临界值。
图文导读
由图1b可知,当加入EC至EC/DEC的摩尔比达到3/7时,从透明溶液中可以判断副反应完全被抑制。在LiPF6存在的情况下,为了保证电解液的稳定性,EC/DEC的摩尔比应大于4/6,说明LiPF6可以加速副反应。该结果表明EC与DEC之间的弱溶剂-溶剂相互作用对锂金属的稳定起决定性作用,而不是阴离子-溶剂相互作用。
在Li||Li对称电池和Li||Cu不对称电池中可以进一步证明EC在DEC基电解质中的必要性(图1c,d)。我们发现,当电解液中EC/DEC的摩尔比小于4/6时,电解液的不稳定性在锂沉积剥离过程中进一步放大,可以观察到较大的过电位以及电池快速失效(图1c)。
相比之下,在EC/DEC的摩尔比达到4/6或更高时(图1c),可获得较低的极化(约22 mV)和超过250 h的循环寿命。Li / Cu不对称电池的初始库仑效率也证实了上述结果(图1d)。此外,Li||石墨半电池进一步证明了EC在DEC基电解质中的必要性,当EC/DEC摩尔比增加到4/6或更高时,与金属锂不相容的DEC电解质会变得相容并表现出稳定的循环寿命。这些结果表明,添加EC后,电解质的稳定性有很大提高。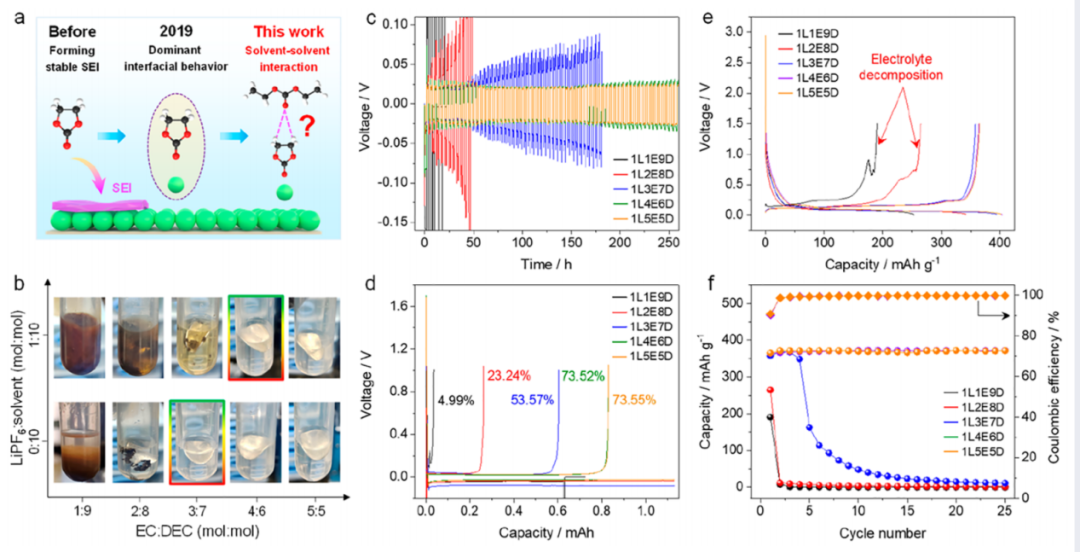
图1. 不同溶剂-溶剂相互作用对电解质稳定性的影响:(a)对EC在电解质中作用的认识历史;(b)金属锂在不同EC/DEC含量比例的电解液中的稳定性比较;(c)在不同EC/DEC含量比例的电解液中的Li / Li电池的电压/时间曲线, (d)Li/Cu半电池的相对的库仑效率;(e)初始循环中的充放电曲线,(f)Li||石墨半电池的循环稳定性。
在没有LiPF6存在的情况下,我们发现添加EC溶剂时,C=O上氧的化学位移向高场移动,而C−O−C上的氧峰没有明显的变化(图2a)。这意味着EC和DEC溶剂可以通过富电子的O (δO−)和缺电子的H (δH+)进行相互作用(图2a所示),从而导致O上的电子云密度增加,表现出屏蔽效应的增强。
当EC和DEC溶剂混合时,EC和DEC上H的化学位移在1H NMR谱上都向高场移动,这进一步证明了EC和DEC之间存在δO−—δH+相互作用(图3b)。C−O−C上可以忽略不计的氧的化学位移的变化表明这种溶剂-溶剂相互作用应该是相对较弱的。
傅里叶变换红外(FTIR)中,通过将EC/DEC的摩尔比从0/10增加到4/6,DEC分子的C=O峰的位置移向更低的波数,此外,该峰的半峰宽也从26.8 拓展到31.7 cm-1。进一步表明溶剂之间的弱相互作用(图2c)。在LiPF6存在的情况下,EC /DEC的溶剂-溶剂相互作用更为明显,因为在NMR谱中的C=O上的17O的峰位转移到更高场(图2d)。
这应该归因于电解质中Li+-溶剂相互作用对溶剂-溶剂相互作用的诱导效应。7 Li NMR谱中Li+化学位移的变化可以进一步证明溶剂-溶剂相互作用的存在和影响,当EC/DEC的摩尔比从1/9增加到4/6时,7 Li化学位移向较低的场移动(图2e)。这一结果表明,Li+的屏蔽作用减弱了,它与溶剂分子的相互作用被减少。
此外,所有基于EC/DEC的电解质的7Li化学位移均低于单一溶剂(即EC或DEC),充分说明了溶剂-溶剂相互作用对Li+溶剂化过程的影响。在19F NMR谱中也可以观察到同样的趋势,其中所有基于EC/DEC的电解质的19F的化学位移向低场强移动,并且比使用单一溶剂(即EC或DEC)的电解质的19F的化学位移要低(图2f)。
这说明溶剂-溶剂相互作用减弱了Li+的屏蔽作用,提高Li+与PF6−之间的静电相互作用,进而增强了Li+对PF6−的去屏蔽作用。这种变化也证明了溶剂-溶剂相互作用的存在及对电解质内部结构的影响。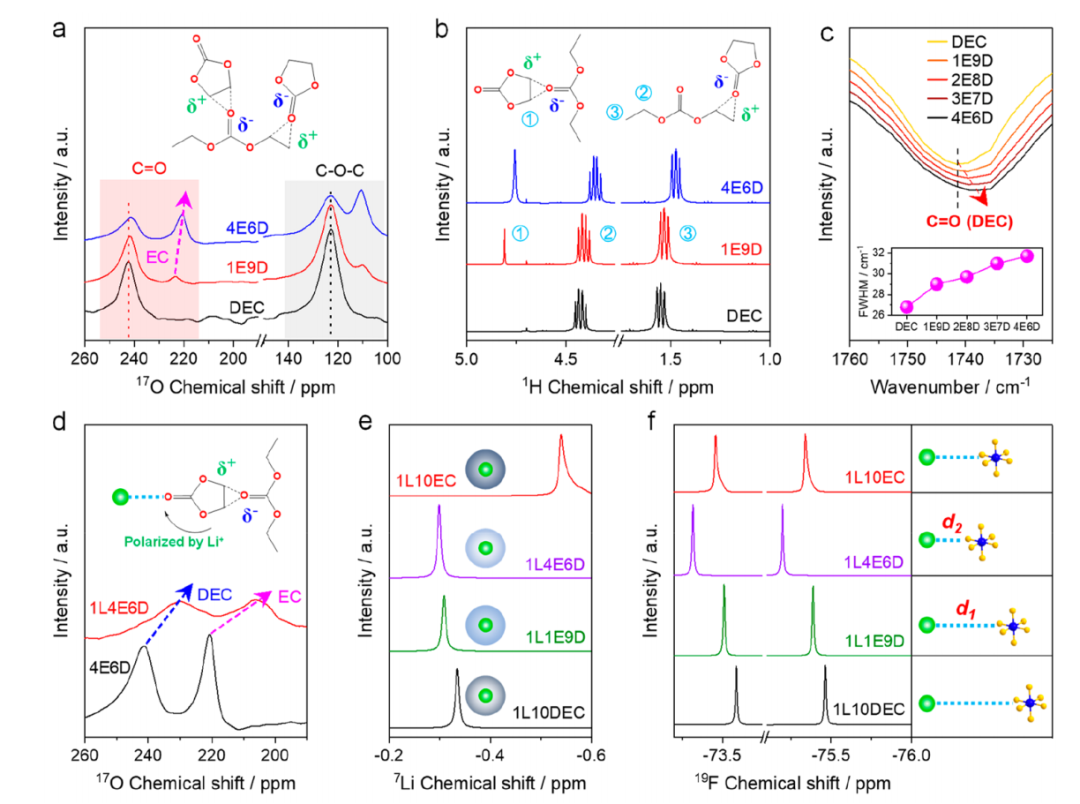
图2. 弱溶剂-溶剂相互作用的光谱表征:(a) 17O核磁共振,(b) 1 H核磁共振,(c)含有不同量EC的EC/DEC混合溶剂的拉曼光谱;(d)加入LiPF6前后溶液的17O NMR谱;(e)含有不同量EC的EC/DEC基电解质的7Li NMR和(f) 19F NMR谱。
在COSY 光谱中,发现EC−H与DEC−H之间的耦合概率随着EC量的增加而增加,表现出更强的耦合信号(图3a及b)。加入锂盐后,由于Li+对EC分子的极化作用,EC分子与DEC分子之间的弱溶剂-溶剂相互作用进一步增强(图3c),这大大增加了1 H−1 H耦合的强度,在COSY光谱中表现出额外增加的信号(图3d及e)。
这一结果与7Li核磁共振谱相吻合。基于上述分析,电解质的溶剂化结构如图3f及g所示。在1L1E9D电解质(即LiPF6DEC = 19摩尔比)中,由于EC溶剂的不足,DEC溶剂仍然主导Li+溶剂化结构的第一层,其中溶剂-溶剂相互作用也很弱。与之形成鲜明对比的是,在1L4E6D电解质(即LiPF6DEC = 16摩尔比)中,EC足以占据Li+溶剂化结构的第一层,其中EC—DEC的相互作用要比1L1E9D电解质中的强得多。
因此,随着EC— DEC溶剂间相互作用的增强,Li+—溶剂相互作用被削弱,而Li+—PF6 -相互作用被增强。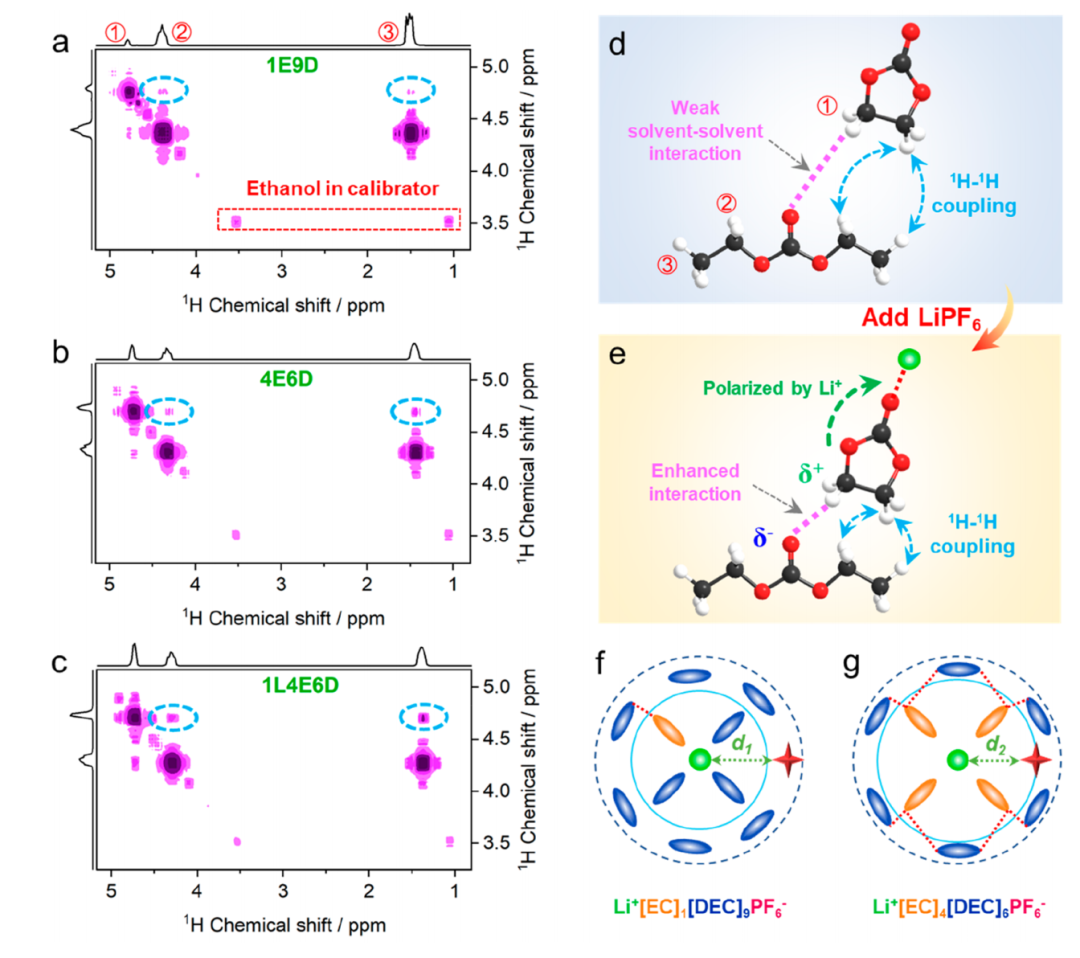
图3弱溶剂-溶剂相互作用的二维1H—1H的COSY谱。(a) 1E9D, (b) 4E6D和(c) 1L4E6D电解质溶液。(d, e)添加锂盐后耦合信号增强示意图。(f) 1L1E9D和(g) 1L4E6D电解质的溶剂化结构示意图。
模拟结果进一步证明了在DEC基电解液中加入EC溶剂后,形成EC- DEC溶剂间相互作用的趋势。首先,我们发现当EC/DEC的摩尔比从0/ 10,1 /9增加到4/6时,DEC出现在DEC周围的频率变低(图4a)。这意味着当EC溶剂加入到DEC基电解质中时,EC分子可以取代DEC分子出现在DEC周围,形成EC—DEC相互作用。
此外,EC—EC、EC—DEC和DEC—DEC溶剂间相互作用的分子间作用力分别为−11.11、−8.90和−8.56 kcal mol−1(图4b),数值非常接近,表明EC与DEC溶剂具有良好的混溶能力。这一结果进一步证实了EC— DEC溶剂间相互作用的可能性。
此外,Li+ (EC)x(DEC)y配合物轨道之间的能量差(即ΔE = HOMO '−LUMO)被用来评估溶剂-溶剂相互作用的影响,其中最低的未占据分子轨道(LUMO)被用来表示Li+ (EC)x(DEC)y配合物的关键轨道,当额外接收一个电子时,相应的轨道就变成了HOMO '(即Li0 (EC)x(DEC)y配合物)。Li+ (EC)x(DEC)y配合物(即x + y = 10)作为该模型的基本单位。轨道之间的能量差越大,电子转移越困难,Li+ (EC)x(DEC)y配合物的稳定性就越高。
当EC/DEC的摩尔比从0/10,1/9增加到4/6时,Li+ (EC)x(DEC)y的ΔE值从0.0636、0.0696增加到0.0767 Hartree (图4c及d)。当EC/ DEC的摩尔比增加到4/6或更高时,电解质就变得稳定和或对锂更兼容。这些结果表明,形成的EC—DEC的溶剂间相互作用对电解液的稳定性有显著影响。此外,作者在EMC溶剂及K/Na离子电池用电解质中进一步验证了这种溶剂-溶剂相互作用对电解质稳定性的影响。
作者认为这些结果表明,在不同的电池体系中,当溶剂的摩尔比和阳离子的种类(如Li+、Na+、K+等)发生变化时,这种弱溶剂-溶剂相互作用也会发生变化。因此,需要深入该领域,进一步量化溶剂-溶剂间的相互作用,以估计出通过相互作用强度稳定电解质的临界值。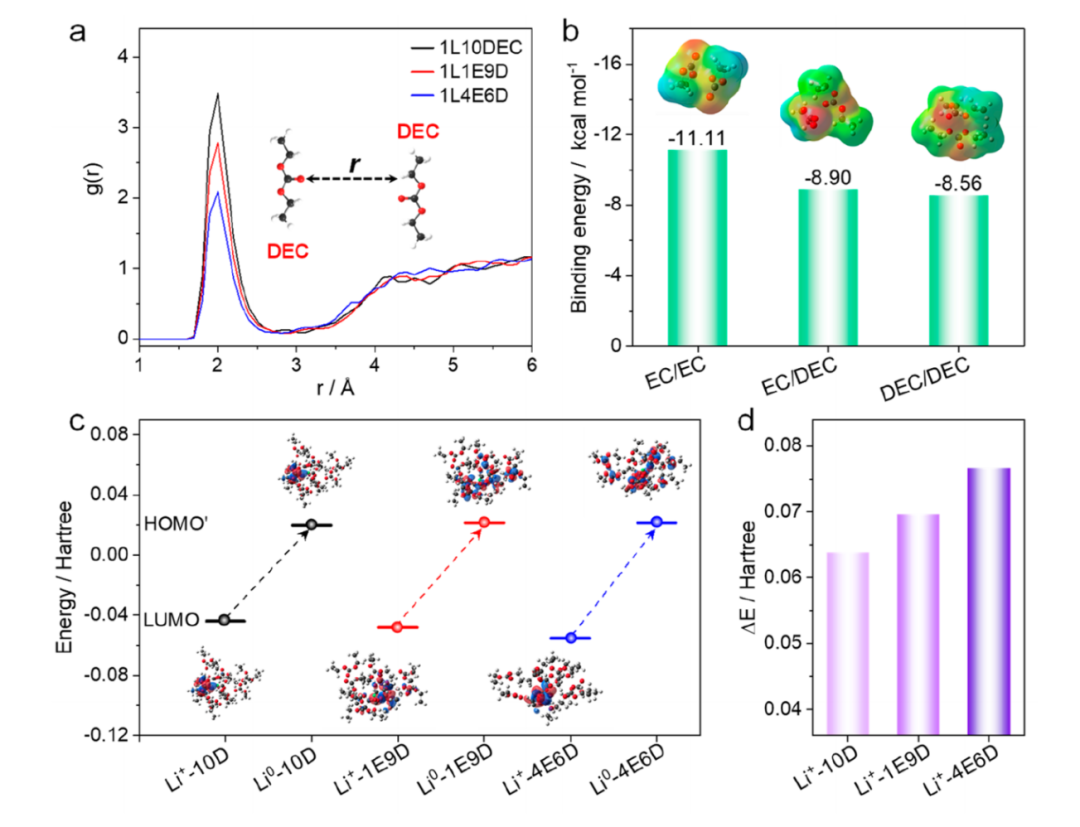
图4。理论计算和模拟:(a)不同EC含量的EC/DEC基电解质的径向分布函数(RDF);(b) EC−EC、EC−DEC和DEC−DEC的结合能;(c)在(Li+)和(Li0)接受一个额外电子之前和之后的HOMO−LUMO示意图以及(d)相应的ΔE值。
总结与展望
以最常用的EC/ DEC基电解质为例,EC-DMC的溶剂间相互作用不仅可以通过2D NMR检测到,而且可以改变Li +(溶剂)x(溶剂)y和Li0(溶剂)x(溶剂)y轨道之间的能量差,从而影响电解质的稳定性。这一发现更新了对EC溶剂在电池电解质中的作用的认识,不仅如此,这种溶剂-溶剂相互作用的效果也在其他类型的电解质和电池系统中得到了验证。这项工作揭示了弱溶剂-溶剂相互作用的重要性,这对未来在分子水平上设计高性能电解质具有一定指导意义。
审核编辑:刘清
-
锂离子电池电解液有机溶剂的发展趋势2013-06-17 5947
-
电池内的电解质是什么?2009-10-20 1234
-
电池电解液和电解质的区别_电池电解液和电解质的两种形态2020-04-16 25722
-
“分子桥”修饰提高锂金属负极/固态电解质界面稳定性2022-03-31 3926
-
浓度极化诱导相变稳定聚合物电解质中的锂镀2022-09-06 2962
-
相变电解质助力高稳定性锂金属电池2022-10-25 3365
-
关于高空气稳定性的硫化物固态电解质2022-11-02 6305
-
AM:用于安全锂金属电池的热响应电解质!2023-01-10 2658
-
聚合物电解质离子电导率及界面稳定性的影响因素2023-02-03 5784
-
锂金属电池室温固态聚合物电解质的锂离子传导机制2023-04-15 4528
-
高锂金属负极形貌稳定性的聚电解质2023-08-16 2429
-
利用三甲基硅化合物改善硫酸盐固态电解质与阴极材料的界面稳定性2023-11-01 3253
-
离子-偶极作用诱导实现PVDF电解质游离残留溶剂封装2023-11-21 5579
-
弱溶剂化少层碳界面实现硬碳负极的高首效和稳定循环2024-01-26 4499
-
无极电容器有电解质吗,无极电容器电解质怎么测2024-10-01 2047
全部0条评论

快来发表一下你的评论吧 !

