

氟化Li10GeP2S12实现稳定的全固态锂电池
描述
研究背景
在所有固体电解质中,硫化物电解质Li10GeP2S12表现出非常高的离子电导率,可以达到12 mS cm-1,与有机液体电解质相当。然而,Li10GeP2S12对水分和金属锂的不稳定性是其应用于全固态锂电池的两个挑战。Li10GeP2S12在潮湿的空气中容易水解并释放有毒的H2S,导致离子电导率显著下降。此外,金属锂和Li10GeP2S12之间的内在热力学不稳定性导致Li10GeP2S12的在接触锂金属时容易发生还原,产生含有混合离子-电子导电性的还原产物,这会加速Li10GeP2S12电解质的破坏,缩短循环寿命。
成果简介
近日,中科院宁波材料所姚霞银研究员团队提出了一种同时可以满足水分和界面稳定性的有效方法,通过气固反应在Li10GeP2S12颗粒的表面引入一层氟化锂涂层,形成了具有核壳结构的固态电解质LiF@Li10GeP2S12。密度函数理论计算验证了具有核壳结构的LiF@Li10GeP2S12有较低的吸附能量,大大抑制了 在Li10GeP2S12中的PS43-的分解。同时,LiF@Li10GeP2S12具有较低的电子传导率,为2.42 × 10-9 S cm-1,可以有效地抑制锂枝晶的增长,并防止锂和LiF@Li10GeP2S12之间的副反应,将临界电流密度从1.0 mA cm-2提高到了3.0 mA cm-2。基于LiF@Li10GeP2S12的全固态锂电池表现出了优异的倍率性能和循环稳定性,组装后的LiNbO3@LiCoO2/LiF@Li10GeP2S12/Li电池在1 C下的初始放电容量为101.0 mAh g-1,循环1000次后容量保持率为94.8%。
研究亮点
核壳固体电解质LiF@Li10GeP2S12中疏水性的LiF外壳可以减少水分子的吸附点,使得电解质在相对湿度为30%的空气中暴露时具有优异的稳定性。
在LiF壳的作用下,Li10GeP2S12的电子传导率降低了一个数量级,这可以显著抑制锂枝晶的生长,减少Li10GeP2S12和锂之间的副反应,提高电池寿命。
图文导读
图1a展示了核壳LiF@Li10GeP2S12的合成过程,通过这种气固反应可以得到均匀的LiF涂层,厚度在10 nm左右(图1b)。LiF@Li10GeP2S12的选区电子衍射(SAED)图中显示了三个衍射环,分别对应于LiF的(220)、(200)和(111)平面(PDF#45-1460)(图1c)。高分辨率透射电子显微镜(HRTEM)和能量色散分析(EDS)线扫描图像显示了Ge和F的相对含量变化,可以看出F位于外壳的外部(图1d)。此外,如图1e所示,高角度的环形暗场扫描透射电子显微镜(HAADF-STEM)图像和相应的LiF@Li10GeP2S12的EDS元素图谱图像清楚地表明整个颗粒中Ge和F的均匀元素分布。LiF@Li10GeP2S12的X射线光电子能谱(XPS)光谱中出现了一个明显的峰值684.9 eV,证明了LiF@Li10GeP2S12颗粒表面形成了LiF(图1f)。
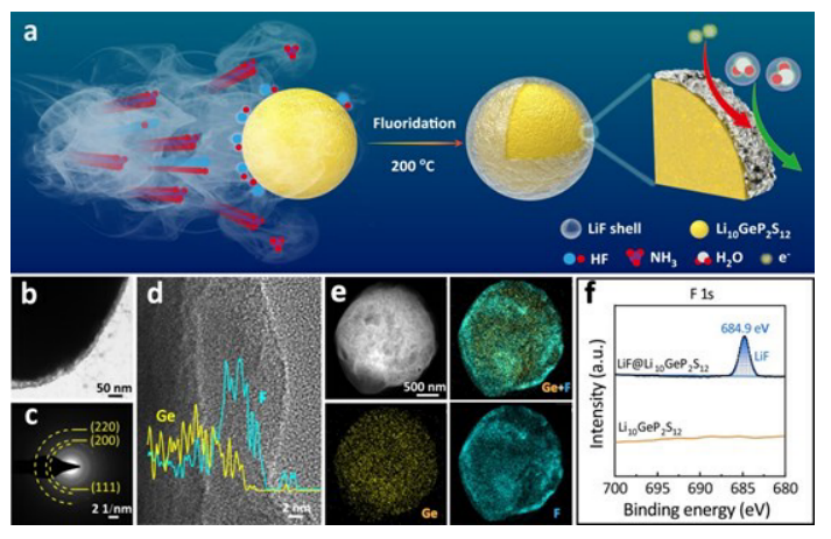
图1. a) LiF@Li10GeP2S12的示意图; b)HRTEM和EDS线扫描图像; e) HAADF-STEM图像和LiF@Li10GeP2S12的元素图谱; f) Li10GeP2S12和LiF@Li10GeP2S12的F 1s XPS图谱。
文章分析了LiF@Li10GeP2S12和Li10GeP2S12在相对湿度为30%的空气中的水分稳定性,如图2a所示,Li10GeP2S12的H2S生成率为0.00544 cm3 g -1 min-1,直到180分钟,产生的H2S总量达到0.648 cm3 g-1。相比之下,LiF@Li10GeP2S12的H2S生成速度慢得多,为0.00352 cm3 g-1 min-1,在40分钟时达到最大值0.147 cm3 g-1,比Li10GePs12的低4.4倍。为了深入了解Li10GeP2S12在潮湿空气中的降解机制,通过DFT计算,系统地揭示了原子尺度的可能吸附和反应行为(图2b-f)。
此外,LiF@Li10GeP2S12在空气中暴露后没有显示出明显的结构变化,如图2g、h所示,相比于LiF@Li10GeP2S12,空气暴露后的Li10GeP2S12的P 2p XPS光谱 的P 2p XPS谱出现了四个峰,其在131.5 eV和132.5 eV处有两个主要的峰,这两个峰被认为是Li10GeP2S12的PS43-,在132.9 eV和133.9 eV出现了两个额外的强峰,源于PS43-水解产生的P-O,这与图2中的DFT计算结果密切一致。此外,与P-O相关的峰的强度在LiF@Li10GeP2S12中要低得多,这说明PS43-的水解程度很小。
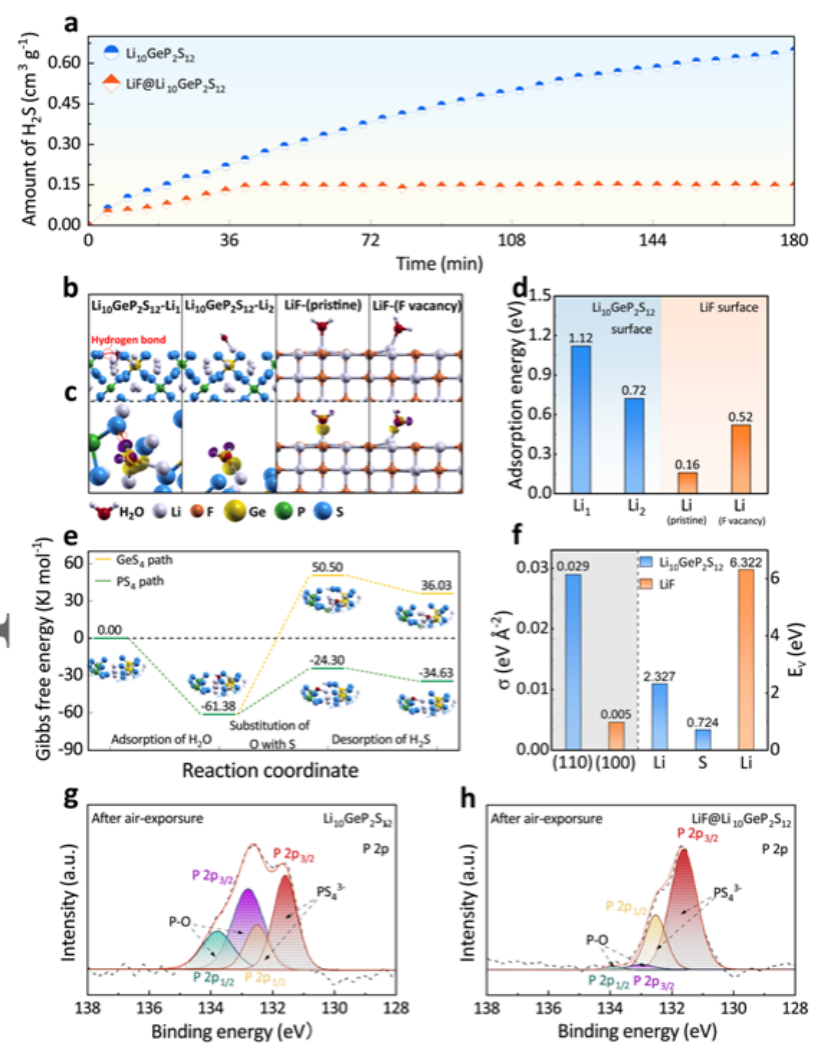
图2. a) Li10GeP2S12和LiF@Li10GeP2S12的H2S气体的时间-数量曲线。b,c) H2O在Li10GeP2S12(110)和LiF(100)上的吸附构型,以及相应的吸附过程引起的不同的电子密度,其中电子积累和消耗的区域分别用黄色和紫色表示。d) H2O在不同位点的吸附能量。e)H2O H2S在Li10GeP2S12 (110)表面的转变,沿着两个可能的反应路径的自由能变化 f) Li10GeP2S12和LiF的表面能(σ)和空位形成能(Ev)。g) Li10GeP2S12和h) LiF@Li10GeP2S12在空气中暴露40分钟后的P 2p XPS光谱。
图3a显示,Li/LiF@Li10GeP2S12/Li电池的临界电流密度(CCD)值为3.0 mA cm-2,远高于Li/Li10GeP2S12/Li电池的1.0 mA cm-2。这主要归因于LiF@Li10GeP2S12低的电子电导率,它可以减少锂直接沉积在体相内造成锂枝晶穿透短路。通过直接电流极化测试了Li10GeP2S12和LiF@Li10GeP2S12的电子电导率,可见在引入LiF涂层后电子电导率大幅下降,从1. 09 × 10-8 S cm-1降至2.42 × 10-9 S cm-1(图3b)。为了揭示电子传导性下降的机理,作者计算了Li10GeP2S12和LiF表面和块体中原子的投影态密度(PDOS)(图3c-d)。
较低的电子传导率意味着在电解质和金属锂的界面上的电子转移较少,这有利于减少界面侧反应产生的电子和离子混合导电材料。如图3e所示Li/LiF@Li10GeP2S12/Li 电池可以在0.1 mA cm-2/0.1 mAh cm-2,25 ℃条件下实现稳定的锂电镀/剥离超过1000小时。相反,Li/Li10GeP2S12/Li的极化电压在368小时后急剧上升到±2.25V,这是由于Li10GeP2S12和金属锂之间严重的界面反应导致了高阻抗。
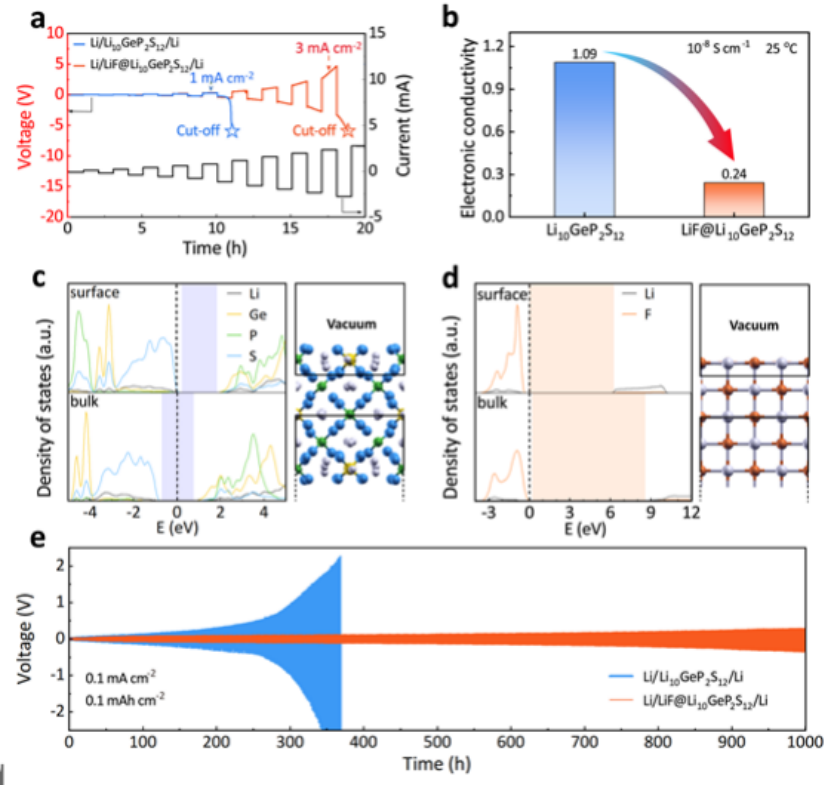
图3. a) Li/Li10GeP2S12/Li和Li/LiF@Li10GeP2S12/Li在阶梯式增加电流密度下的静电循环。b) Li10GeP2S12和LiF@Li10GeP2S12/Li的电子电导率。LiF@Li10GeP2S12。c) Li10GeP2S12和LiF@Li10GeP2S12的表面和大块原子的预测状态密度。e) Li/Li对称的Li10GeP2S12和LiF电池的循环性能。Li10GeP2S12和LiF@Li10GeP2S12的循环性能。
由于LiF具有较宽的电化学窗口,基于LiF@Li10GeP2S12的全固态锂电池可以匹配高电压LiCoO2正极。作者采用LiNbO3@LiCoO2为正极,对比了采用Li10GeP2S12和LiF@Li10GeP2S12不同电解质的全固态锂电池在0.1C下的循环性能,如图4a所示。很明显,LiNbO3@LiCoO2/Li10GeP2S12/Li在7个循环后容量保持率只有45.4%,而LiF@Li10GeP2S12电解质全固态锂电池表现出高初始放电容量,为 130.8 mAh g-1,100次循环后容量保持率保持在97.0%。此外,LiNbO3@LiCoO2/LiF@Li10GeP2S12/Li电池也具有很好的倍率性能,在0.1C、0.2C、0.5C、1C、2C和3C时,分别达到132.8、128.9、120.7、103.1、80.7和65.1 mAh g-1,在倍率恢复到0.1C之后,容量可以恢复到128.5 mAh g-1(图4 b、c)。LiNbO3@LiCoO2/LiF@Li10GeP2S12/Li全固态锂电池在大倍率下也具有很好的循环稳定性,其在1C下初始放电比容量为101.0 mAh g-1,稳定循环1000次后容量保持率为94.8%(图4 d)。
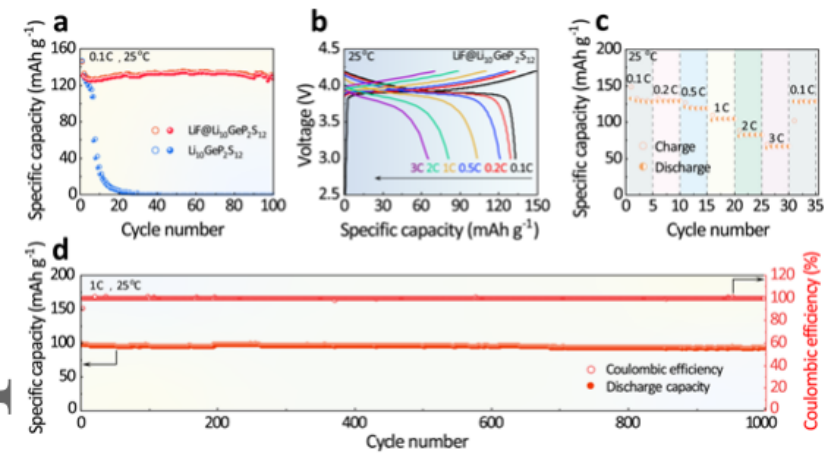
图4. a) LiNbO3@LiCoO2/Li10GeP2S12/Li和LiNbO3@LiCoO2/LiF@Li10GeP2S12/Li在0.1 C的循环性能。b) LiNbO3@LiCoO2/LiF@Li10GeP2S12/Li从0.1 C到3 C的充放电曲线和c) 倍率能力。d) Li NbO3@LiCoO2/LiF@Li10GeP2S12/Li在1C时的循环性能。
总结与展望
总之,该团队通过气相氟化技术开发的LiF@Li10GeP2S12核壳电解质表现出了出色的湿度和对锂稳定性。LiF@Li10GeP2S12在空气暴露40分钟后,离子电导率为1.46 × 10-3 S cm-1。此外,该 LiF@Li10GeP2S12的电子电导率较低,为2.42 × 10-9 S cm-1,抑制了锂枝晶的生长,并阻止了锂枝晶的侧向生长。组装后的 LiNbO3@LiCoO2/LiF@Li10GeP2S12/Li全固态锂电池表现出卓越的循环速率性能,在1C下稳定循环1000次循环,在0.1C、0.2C、0.5C、1C、2C和3C时,分别达到132.8、128.9、120.7、103.1、80.7和65.1 mAh g-1。该研究为硫化物电解质的水解机制和稳定硫化物电解质在全固态锂电池中对水分和锂的影响提供了新的视角。
审核编辑:刘清
-
日本开发出“超离子”固态锂电池2011-08-08 2925
-
苹果的新专利--全固态电池2015-12-23 4785
-
锂电池VS聚合物锂电池,谁才是未来的主角?2018-08-17 7311
-
全固态电池是什么2021-07-12 2745
-
全固态薄膜锂离子电池2009-12-29 831
-
中国科学院李泓:全固态锂电池开发面临四个挑战2017-02-13 5270
-
浅谈全固态锂电池的优势和挑战2019-01-21 12289
-
全固态或固态锂电池是什么,它的潜在优势分析2020-04-03 6952
-
全固态锂电池中锂枝晶的生长及抑制机理的研究分析2020-04-26 9228
-
干货:全固态锂电池的分类和应用2020-07-27 7308
-
全固态锂电池领域的研究及实际应用2022-09-27 4426
-
关于全固态锂电池的6大成果2023-01-05 2914
-
增强富锂反钙钛矿的水分稳定性实现可持续的全固态锂电池2023-01-16 1472
-
梯度包覆策略助力高性能全固态锂电池2023-01-30 1658
-
离子-电子共导核壳结构实现高性能全固态Li2S电池2023-02-03 3168
全部0条评论

快来发表一下你的评论吧 !

