

短波红外成像使人脑肿瘤的高对比度荧光引导手术成为可能
描述
区分肿瘤和健康组织是癌症手术的关键部分,光学成像技术将在其中发挥重要作用。
目前有几种方法利用不止一种波长的光进行照明,以最大限度地返回给临床医生的成像数据,并利用不同组织和细胞结构表现出的不同光谱和荧光响应来区分肿瘤和健康组织。
上述方法包括:(1)使用高光谱相机,例如HELICoiD项目设计的用于对人类脑癌成像的平台;(2)通过WUSTL双波长近红外(NIR)技术利用组织中光的波长相关衰减来确定荧光团深度。
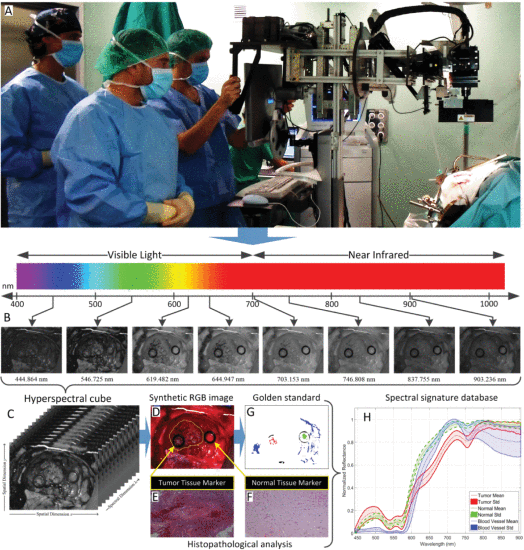
HELICoiD项目之体内高光谱人脑成像(来源:DOI: 10.1109/ACCESS.2019.2904788)
据麦姆斯咨询报道,近期,英国伦敦大学学院(University College London)的一个研究项目现已展示了一种多光谱近红外(NIR)和短波红外(SWIR)荧光成像设备,研究人员称这是该设备中的全球首创。在Cancer Research期刊中介绍该设备最初用于治疗儿童神经母细胞瘤。
“荧光引导手术使用从700 nm到950 nm发光的近红外染料,与可见光波长相比,组织显示出更少的自发荧光,从而实现更高的目标与背景的信号比。”该科研团队在其论文中评论道,“然而,人们对1000 nm至1350 nm(短波红外区域)的窗口越来越感兴趣。因为在该区域中,自发荧光、吸收和散射进一步减少。”
该研究指出,目前缺乏临床认可的短波红外荧光团染料,但用于这些波长成像的铟镓砷(InGaAs)传感器成本的降低刺激了能够测量短波红外荧光的设备的开发,从而产生了研究临床使用短波红外成像技术的愿望。
对新成像技术的需求不断增长
伦敦大学学院通过将两种近红外染料(包括一种已知在短波红外范围内也有活性的染料)与dinutuximab-beta蛋白结合,合成了一种适合其研究的短波红外染料。研究人员设计了一个定制的成像平台,其中组织被一组波长在785 nm到1350 nm之间的光照射,产生近红外和短波红外荧光,后者由低温冷却的InGaAs相机收集。
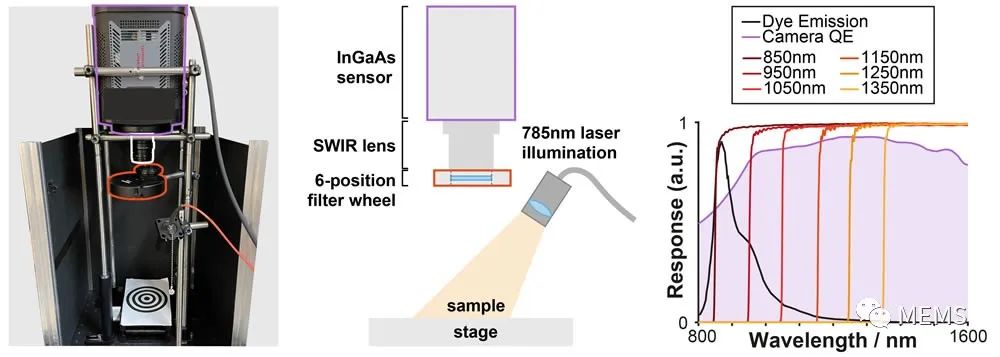
对组织模型的测试表明,近红外/短波红外成像平台实现了0.9立方毫米的最小检测体积和高达3毫米的深度穿透。根据该研究项目,一项评估小鼠肿瘤吸收标记物的初步研究证实,与单独的体内近红外成像相比,短波红外荧光成像能够实现更高的肿瘤与背景的信号比以及更好的深度穿透。
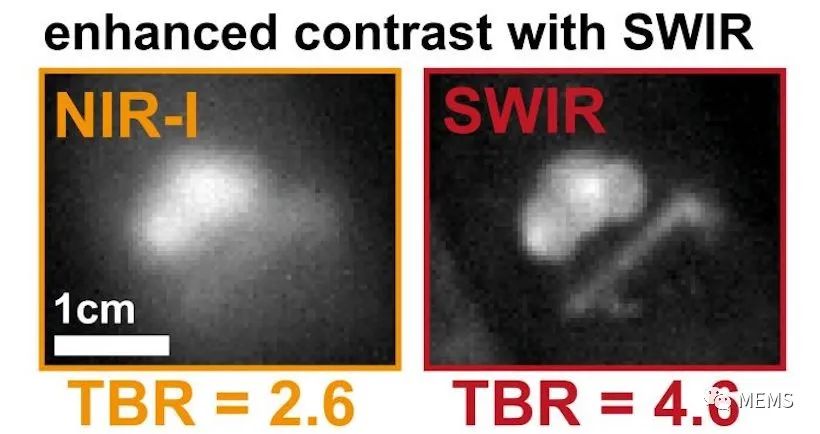
短波红外成像增强了肿瘤组织的对比度并改善了肿瘤与背景的信号比
接下来,伦敦大学学院和大奥蒙德街医院将努力在未来12个月内将该技术快速应用于手术室,以造福患有神经母细胞瘤的儿童。
“小儿外科肿瘤学面临着对有助于在手术中可视化肿瘤的新成像技术和设备的日益增长的需求。”该研究论文的第一作者Laura Privitera评论道,“荧光引导手术是一项改变游戏规则的创新,它将帮助外科医生获得更安全、更完整的肿瘤切除术。我期待看到这项技术应用于临床手术。”
审核编辑:刘清
-
到底什么叫显示器对比度2011-02-23 2708
-
为什么DM365 对比度提高的时候,图像亮度也被提上去了,这是什么原因啊?2018-06-15 1731
-
LT1183CS LCD对比度正升压转换器的典型应用电路2019-04-09 1938
-
用于治疗脑肿瘤和癫痫的新型柔性传感器2022-02-26 1063
-
液晶电视的对比度2009-12-31 1584
-
LCD背光及对比度调节2010-07-31 12009
-
激光干扰下红外成像系统性能预测研究2011-11-04 618
-
诊治脑肿瘤的希望--AI“虚拟活检”2018-07-11 826
-
利用近红外荧光成像导航确保手术的精确度2018-07-30 6535
-
中国成功研发出新型近红外二区荧光成像系统及手术导航技术2020-06-01 8410
-
便携式扬声器电源:使低音成为可能2022-11-04 691
-
动态背光可提高对比度并调整小型LCD面板的功耗2023-01-17 4704
-
投影机中对比度与动态对比度的区别及运用2024-12-20 3538
-
荧光成像内窥镜—激光技术在医疗成像与治疗中的创新应用2025-03-26 969
-
tFUS如何有效的脑肿瘤干预?2026-02-26 301
全部0条评论

快来发表一下你的评论吧 !

