

镶嵌水凝胶微球的传热微针,用于骨关节炎治疗
描述
病变细胞的定位和细胞器功能的靶向调控可以促进病变修复。然而,常规调节难以到达深部病变和靶向线粒体。基于此,上海交通大学医学院崔文国教授团队采用动态螺旋镶嵌技术构建螺旋镶嵌微/纳米水凝胶微球传热微针(ST针),利用分子链运动响应热刺激来调节无取向三嵌段聚合物的粘附,作为热能和生物因子的传输系统(图1a)。ST针系统利用其物理特性,准确到达病灶深处,基于动态螺旋镶嵌机制,去除水凝胶微球的镶嵌状态,释放热能和生物因子,治疗骨关节炎(图1b)。该体系实现了热能与生物因子协同调节线粒体,从而抑制软骨细胞凋亡(图1c)。相关研究成果以“Localization of Lesion Cells and Targeted Mitochondria Via Embedded Hydrogel Microsphere using Heat Transfer Microneedles”为题发表在Adv. Funct. Mater.期刊上。
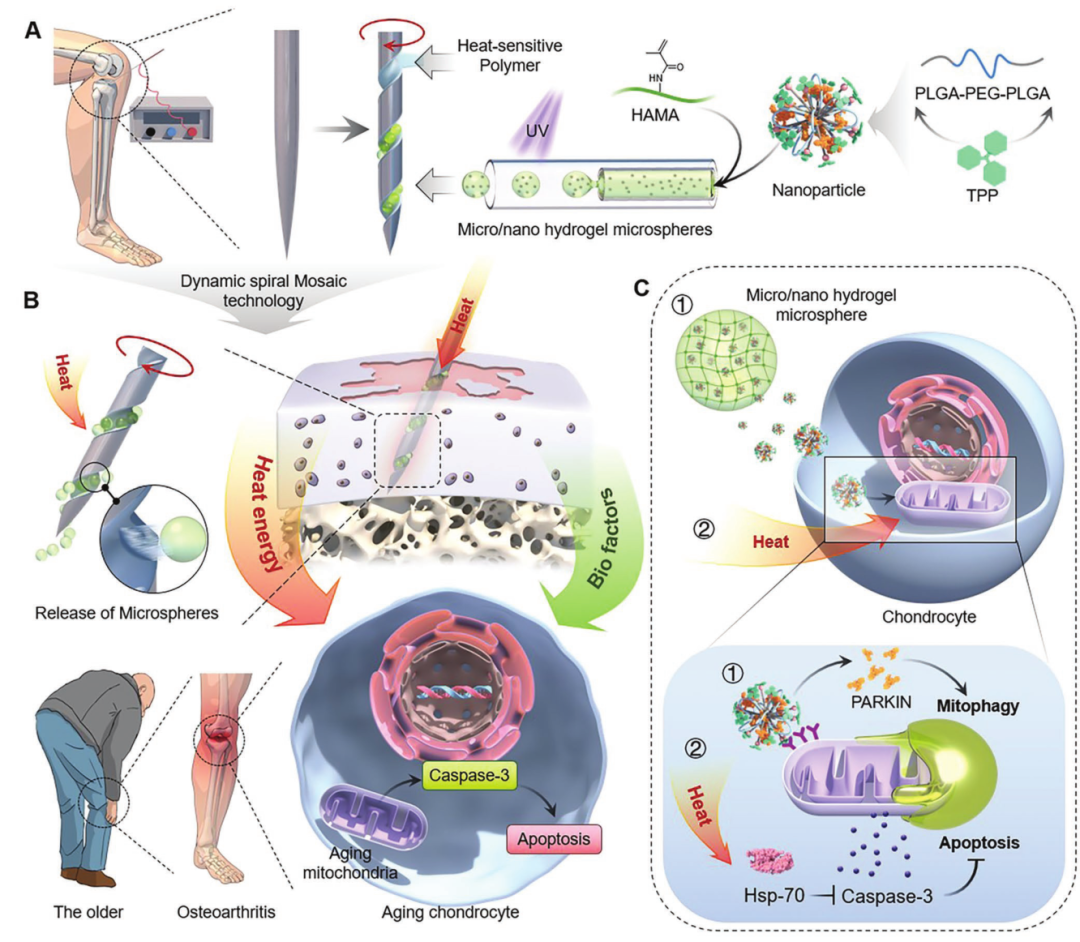
图1 传输热能和生物因子的ST针系统示意图
微针将热能传输至深部病变
中国针灸微针(CA针)是中医最成熟的传热工具,被广泛用于治疗各种疾病,如手腕(图2Ai)、腰部(图2Aii)、和肩膀(图2Aiii)疼痛。在该研究中,研究人员选择CA针的尾部(C点)和尖端(D点)来确定温度。艾草柱燃烧后,C点的温度从≈26.5℃升高到≈37.5℃(总升高≈9℃),随后达到热平衡,温度不再进一步升高(图2C)。随后,随着热量从C点转移到D点(图2D),在D点观察到从基本温度升高到28.2℃(总增加≈1.7℃)。实验在室温(25℃)下进行;因此,针头散发的热量相对较大,导致尖端温度降低。
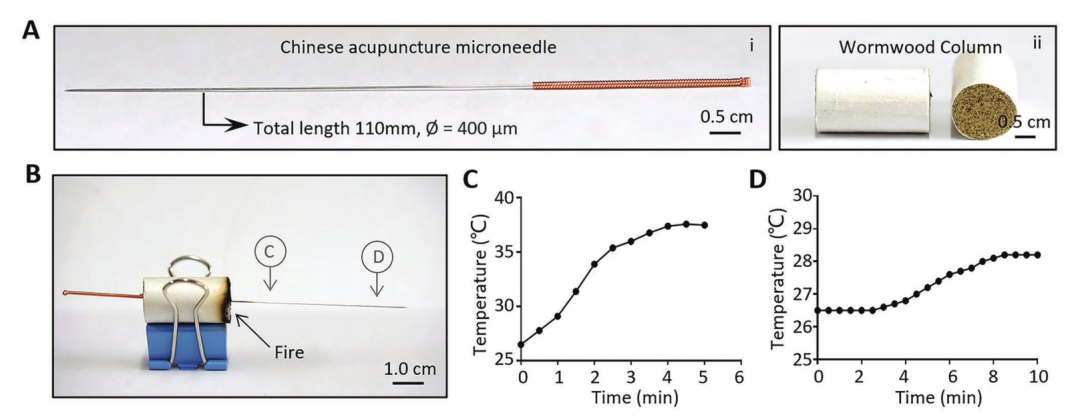
图2 使用CA针的传统传热的特点
热敏粘合剂聚合物及微/纳米水凝胶微球的合成与表征
随后研究人员合成了热敏粘合剂聚合物(图3A),然后对其流变曲线、储能模量和损耗模量曲线、不同温度下的流动性进行了一系列表征(图3B-E)。
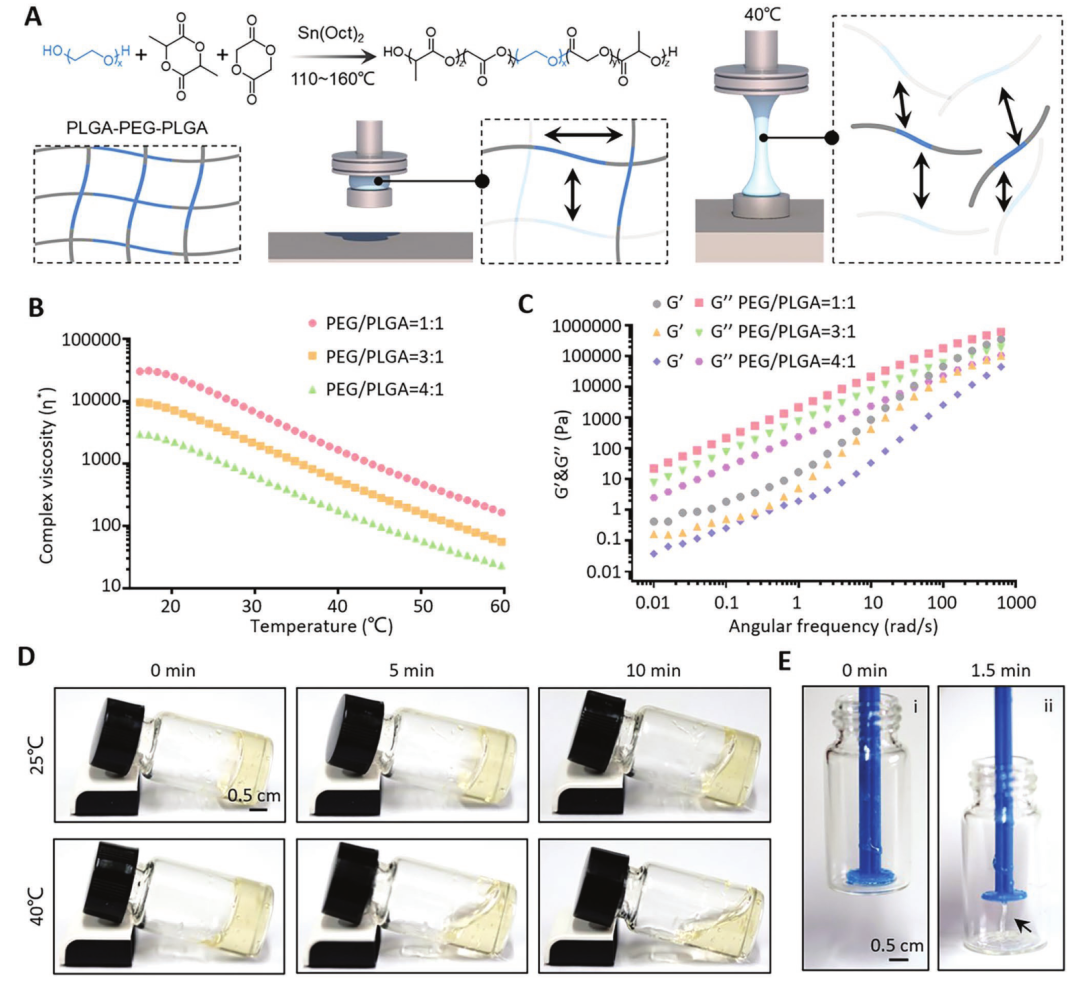
图3 热敏粘合剂聚合物的特性
随后研究人员合成了以线粒体为靶点的微/纳米微球(图4A)。对其进行TEM、粒径分布、Zeta电位、光电子显微镜、尺寸分布、SEM等一系列表征(图4B-H)。
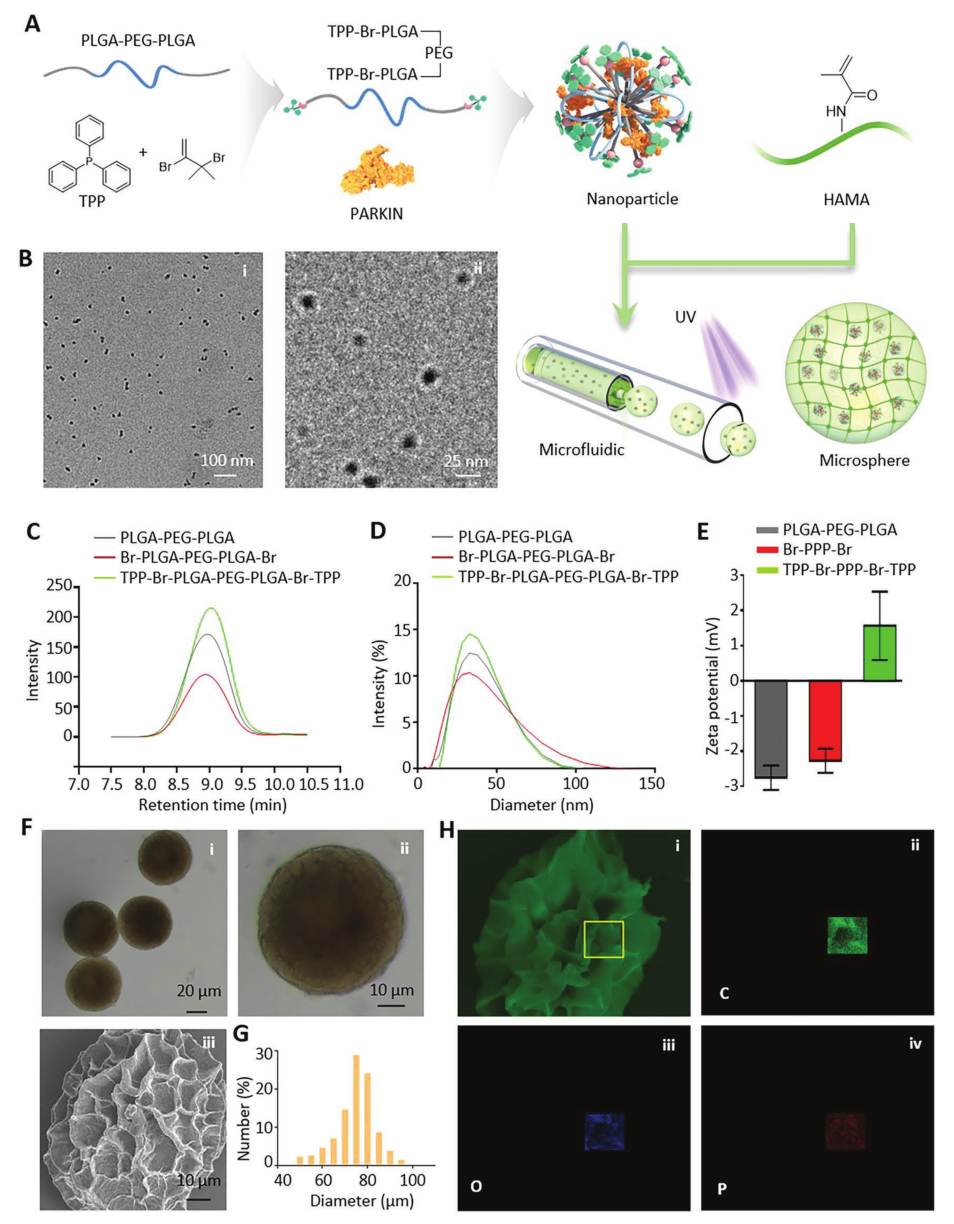
图4 靶向线粒体的微/纳米微球的表征
螺旋镶嵌水凝胶微球CA针的构建,以及传输热能和水凝胶微球的能力
为了提高CA针加载水凝胶微球的能力,在针尖(ST针)上构建了螺纹槽结构,并与传统的CA针进行了比较(图5A)。利用热敏聚合物的粘合特性,将水凝胶微球粘贴在CA针上并嵌入到ST针上。通过旋转ST针释放水凝胶微球,并允许水凝胶微球留在病变部位以实现长期治疗(图5B)。随后,通过模拟兔子的临床治疗,验证了ST针系统传输热量的能力。温度检测器探头放置在皮肤上ST针的入口处,而尖端位于组织内(图5C)。两个温度之间的关系符合一阶函数:Y = 0.9356X − 4.078(图5D)。这些发现表明ST针具有良好的导热性,可以将热量传输到更深的病灶。将载有荧光染料的水凝胶微球嵌入ST针中,以验证ST针系统可以传输水凝胶微球。ST针系统传输水凝胶微球的效率可以通过测量治疗前后ST针和穿刺部位的荧光强度来评估。结果表明,在热敏粘合剂聚合物和螺纹槽的保护作用下,ST针系统可以成功地将水凝胶微球传输到体内(图5F)。因此,ST针系统可以将水凝胶微球传输到组织中,并在热刺激下释放,并留置在病灶中。
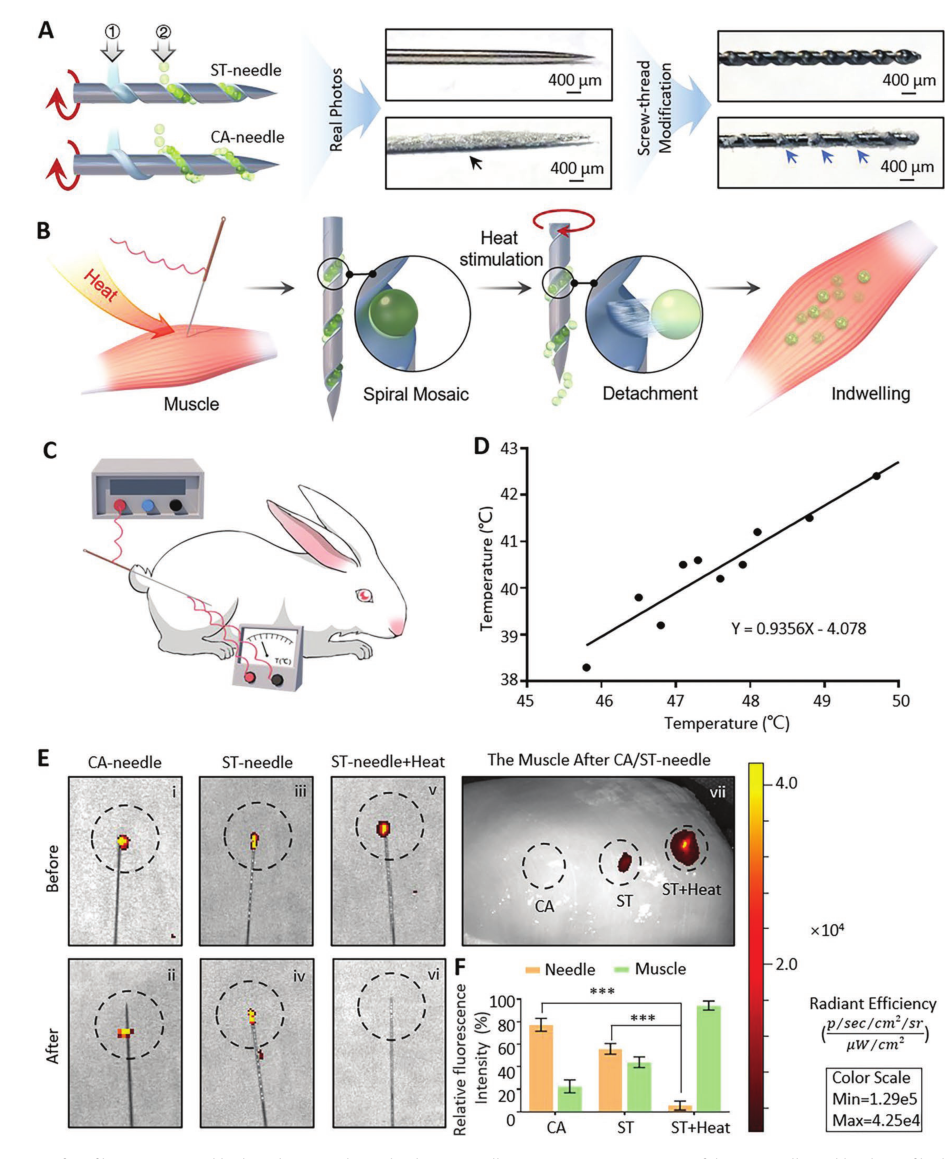
图5 通过ST针系统传输热能和水凝胶微球
热传输ST针在骨关节炎治疗中的应用
使用ST针治疗骨关节炎(OA)时,必须穿过软骨基质的致密屏障才能到达深部软骨病变的软骨细胞。然后,软骨细胞通过释放热能和生物因子进行调节(图6A)。因此,为验证ST针能否穿过软骨基质的物理屏障,高效传输水凝胶微球,进行了兔膝关节软骨模拟穿刺实验(图6B),结果表明CA针无法将水凝胶微球传输到软骨基质深处的病变处,ST针可以。为了证明ST针系统可以将热量传输到软骨,研究人员对未经处理的软骨样本进行了热成像(图6C)。实验结果表明,热疗部位的温度显着升高≈4.5℃。随后,利用兔软骨进行的荧光残留实验表明,CA针上残留荧光的比例明显高于ST针(图6D),表明ST针能够成功突破软骨的物理屏障,并将水凝胶微球传输到软骨中(图6E)。
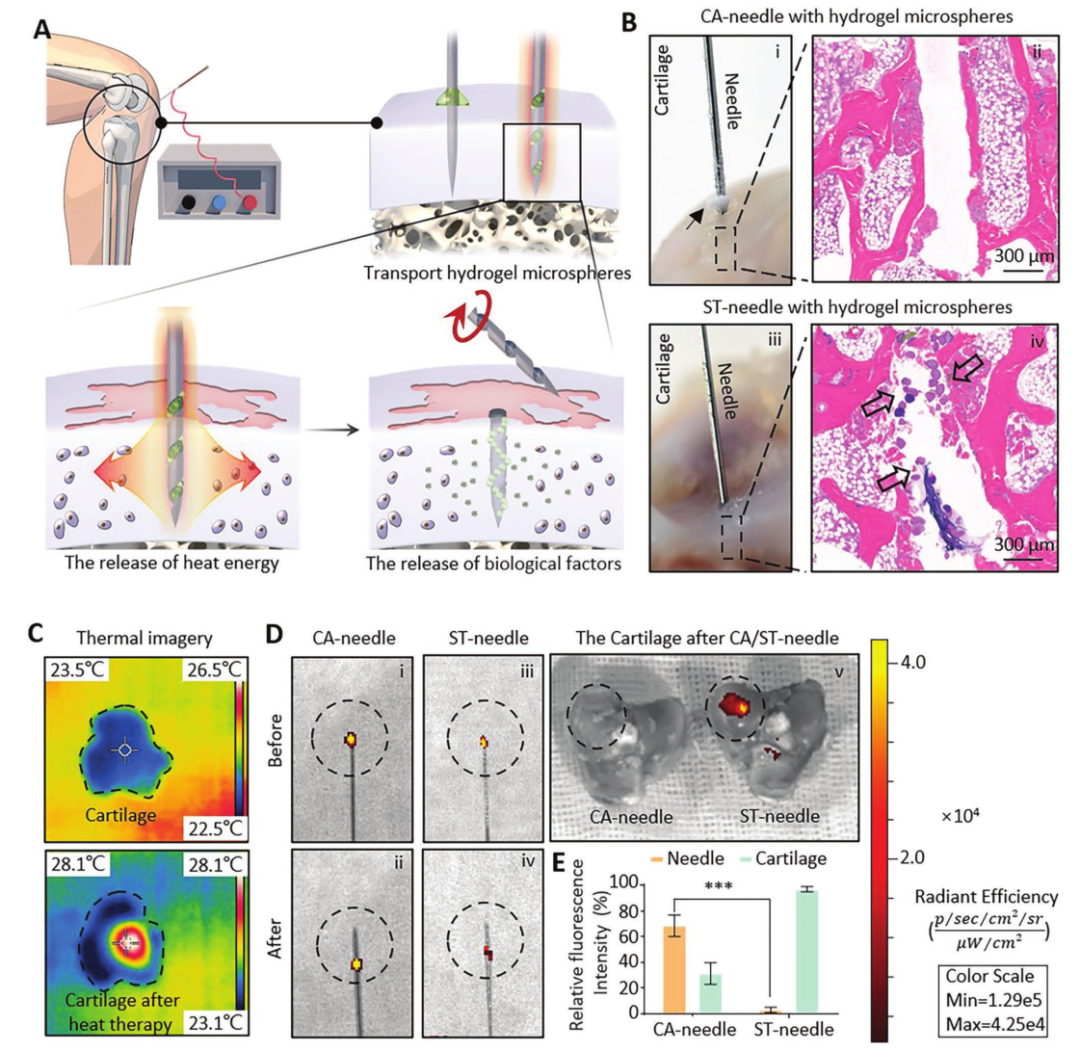
图6 ST针系统在骨关节炎治疗中的应用
使用ST针系统靶向调节软骨细胞线粒体的机制
ST针作为热能和生物因子的双重传输系统,能够通过热能快速抑制线粒体凋亡,通过水凝胶微球释放生物因子诱导线粒体自噬,从而实现协同靶向调控线粒体功能和抑制软骨细胞细胞凋亡(图7)。ST针释放的热能刺激软骨细胞,促进HSP-70的分泌。然而,HSP-70可以抑制caspase-3分泌和线粒体凋亡。ST针系统释放的水凝胶微球保留在病灶内并继续释放纳米粒子。在TPP结构的引导下,纳米粒子进入软骨细胞并靶向线粒体。此外,促进线粒体自噬的PARIN因子被释放,老化的线粒体被清除。
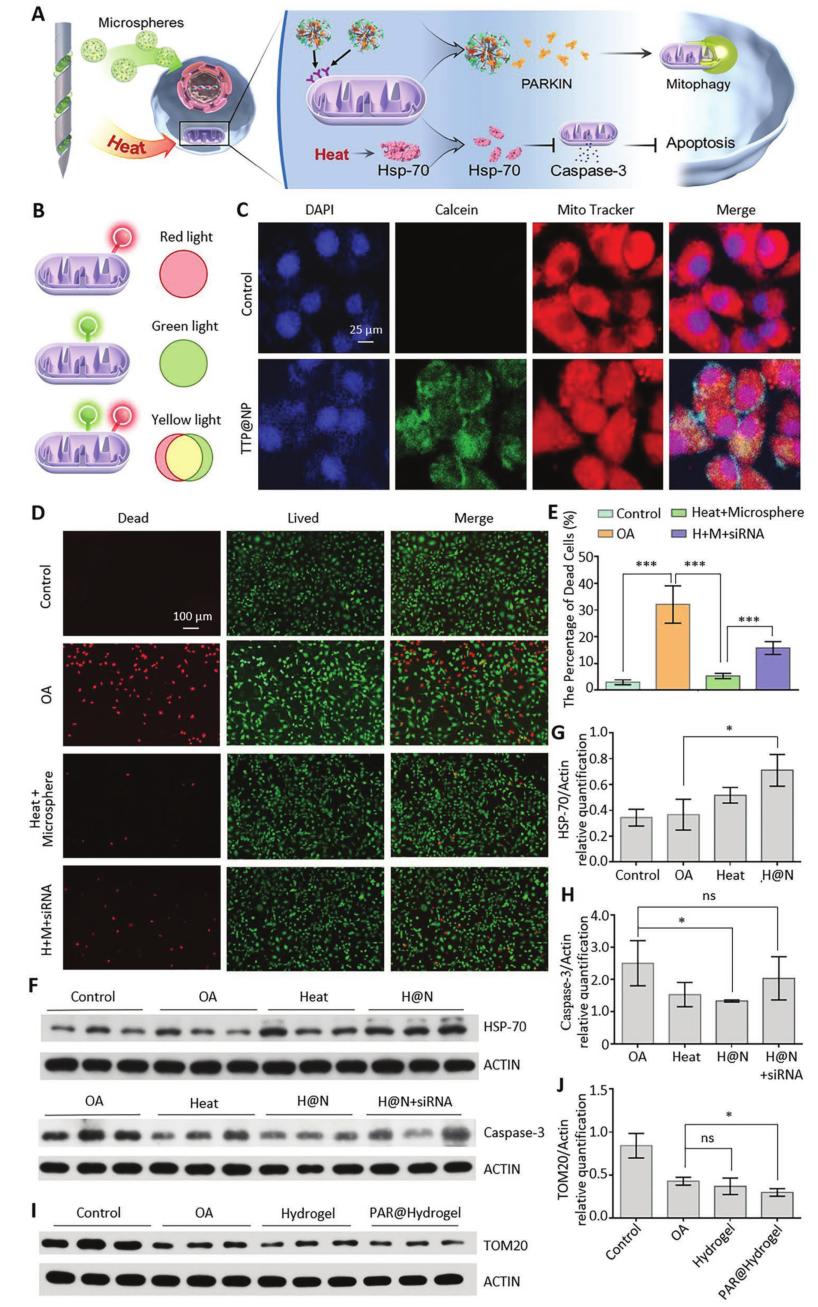
图7 热能和微/纳米水凝胶微球共调节的分子机制
ST针系统可显着改善软骨细胞功能并治疗OA
随后,开发了OA大鼠模型以验证ST针系统治疗OA的疗效(图8)。组织学染色结果表明,通过ST针调节线粒体可显著改善软骨细胞的生命周期,从而有效治疗骨关节炎。
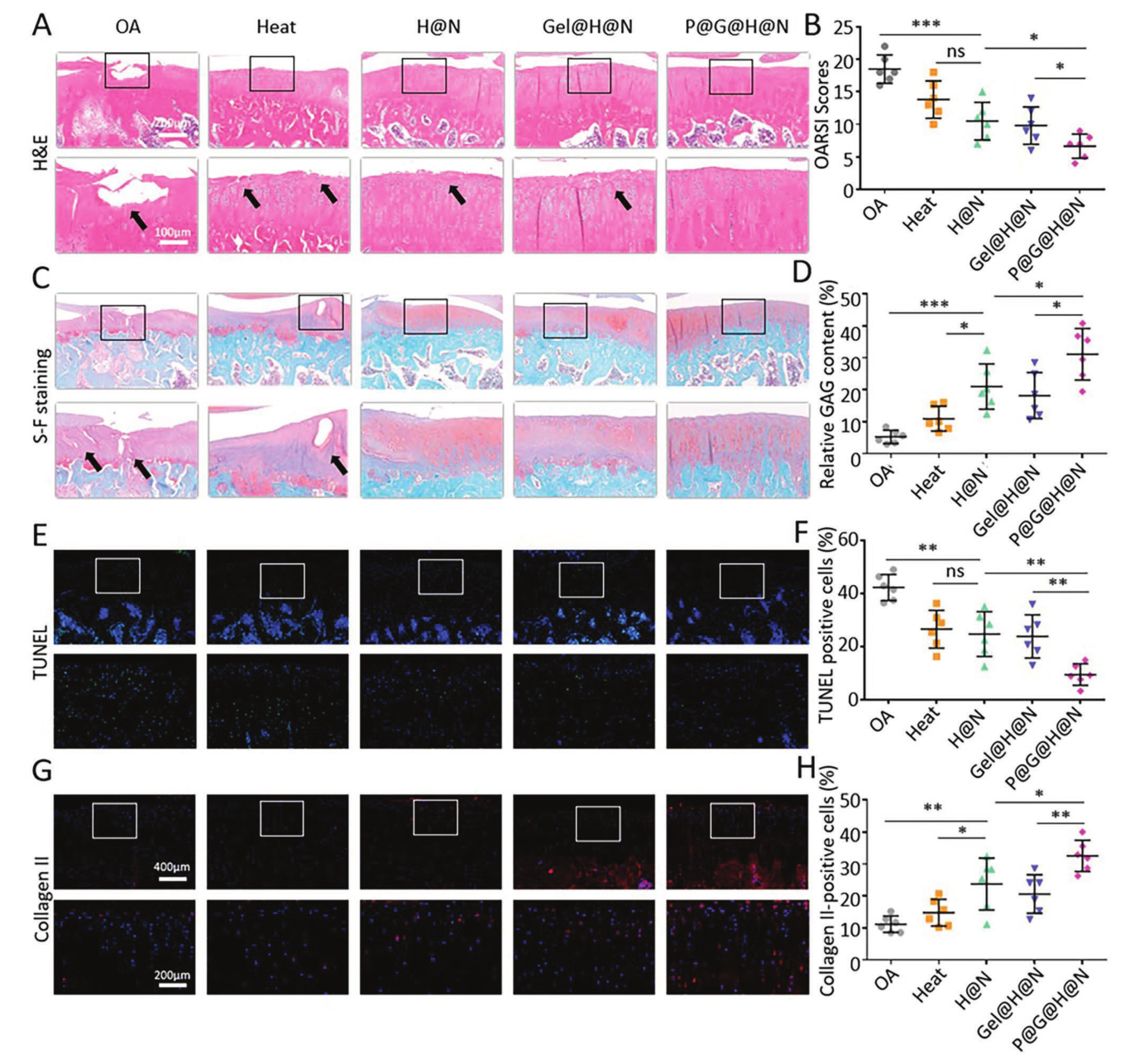
图8 使用ST针系统治疗骨关节炎的动物实验
综上,在这项研究中,创新性地使用动态螺旋镶嵌技术开发了具有螺旋镶嵌微/纳米水凝胶微球的传热微针作为热能和生物因子的双重传输系统,利用分子链运动响应热刺激调节无取向三嵌段聚合物的粘合力。ST针系统利用其优异的物理特性,准确到达病灶深处,将热量传输给病灶细胞。热量激活ST针系统的动态螺旋镶嵌机制,去除水凝胶微球的镶嵌状态,实现热量和水凝胶微球同时到达病灶。通过热能快速抑制线粒体凋亡和释放生物因子的水凝胶微球诱导长期线粒体自噬,实现了热能和生物因子对线粒体功能的协同靶向调控。OA大鼠模型进一步验证了ST针系统能够抑制软骨细胞凋亡,促进软骨损伤修复,从而缓解OA。这项研究的结果对未来生物材料的设计和各种疾病治疗策略的规划具有重要意义。
论文链接
https://doi.org/10.1002/adfm.202212730
审核编辑 :李倩
-
初创公司:正在使用深度学习来更有效、更经济地诊断膝关节2018-01-25 4752
-
治疗关节炎新技术:生物3D打印组织2018-07-16 4062
-
国产机器人完成辅助关节置换手术 机器人的精度是传统手术无法企及的2020-01-10 1023
-
科学家新发明3D成像技术,将有助于关节炎的护理2020-03-30 762
-
微电机更好地治疗类风湿性关节炎2021-02-25 2194
-
PharmaTher研发水凝胶微针贴剂,用于治疗神经类疾病2021-04-29 6792
-
微流控技术中使用的不同类型的水凝胶2022-09-28 4245
-
超声波驱动的微针贴片,用于细菌感染痤疮的高效治疗2023-03-23 2345
-
缓释微针贴片用于脱发长效治疗2023-07-10 3134
-
利用3D生物打印构建关节类器官的策略与应用2023-10-22 3537
-
基于溶解性微针和粘合性透皮贴剂的给药系统,用于治疗类风湿性关节炎2024-01-17 3260
-
iPhone和Apple Watch助医生诊断类风湿性关节炎2024-02-21 1185
-
基于颜色变化水凝胶的集成微流控压力传感2024-03-26 2118
全部0条评论

快来发表一下你的评论吧 !

