

近红外光控制的工程细菌用于增强实体瘤治疗效果
描述
近年来,合成生物学的快速发展为肿瘤细菌疗法的深度优化带来新的契机。基于合成生物学手段,科学家们能够利用基因工程改造的微生物或细胞而非传统的化学小分子或生物制剂,作为新型疾病治疗方法的开发基础。人工设计的携带有合成基因线路的微生物或细胞能够响应疾病标志物或者外界信号,实现对药物释放位置、释放时间和释放剂量的控制,已逐渐发展为人类对抗疾病的强有力武器。
在传统的细菌改造基础上,经过理性设计的基因通路赋予了底盘细菌更多样化的治疗能力,弥补了天然菌株在肿瘤治疗方面的缺陷,肿瘤细菌疗法也因此成为极富应用前景的新型肿瘤疗法。现有肿瘤细菌疗法的优化策略主要集中在新型药物的应用、新型可控释放方式的引入等,但是却忽略了细菌自身行为对肿瘤治疗效果的影响,缺乏对肿瘤治疗过程中细菌行为的持续控制。肿瘤治疗是一个长期的过程,可控持续的药物释放是提高肿瘤治疗效果的关键,虽然在材料领域通过高分子水凝胶和脂质等已经实现了药物的持续释放,但是在肿瘤细菌疗法中仍然是一个挑战。
近日,中国科学院深圳先进技术研究院合成生物学研究所金帆课题组在国际学术期刊National Science Review上发表了题为“Programming the lifestyles of engineered bacteria for cancer therapy”的研究成果。通过合成生物学的设计,研究人员成功地将铜绿假单胞菌菌株改造成为具有实体瘤治疗功效的工程菌。在治疗过程中,该工程菌的全局表型可被近红外光的辐照程序精确的控制,即:在弱定殖、定殖以及裂解释药三种表型切换,从而更有效地消融瘤体达到治疗效果,具有巨大的潜在应用价值。深圳先进院合成所助理研究员张荣荣为论文共同第一作者及共同通讯作者,金帆研究员为文章通讯作者。
在自然界中,铜绿假单胞菌在有利的环境中处于浮游状态,其在表面定殖的能力较弱;而在不利的环境中则会进入生物被膜状态,其表面定殖能力大大增强。受到自然界中细菌生存方式的启发,研究团队为工程菌设计了浮游状态和生物被膜状态以实现对其定殖能力的控制,其中浮游状态细菌的定殖能力较弱,能够减少对正常组织的伤害;而生物被膜状态细菌的定殖能力较强,能够增加其在肿瘤组织内的定殖量。研究团队通过敲除毒力因子调控蛋白编码基因vfr和三型分泌系统相关基因exoS和exoT构建了减毒的铜绿假单胞菌菌株作为肿瘤细菌疗法中的新型底盘菌株。铜绿假单胞菌在浮游状态和生物被膜状态两种生活方式之间的切换与第二信使分子环二鸟苷酸(c-di-GMP)的浓度密切相关,为此,研究团队使用两个基因模块对细菌胞内的c-di-GMP浓度进行控制,分别是:
1)通过组成型启动子表达磷酸二酯酶PA2133以分解c-di-GMP,使细菌维持较低的胞内c-di-GMP水平,进入浮游状态;
2)引入可在近红外光照射下合成c-di-GMP的光敏蛋白BphS,近红外光照射可使细菌胞内c-di-GMP水平升高,细菌进入生物被膜状态。
此外,为了实现治疗药物的控制释放,研究团队为工程菌设计了第三种生活方式,即裂解状态,通过c-di-GMP响应型启动子表达裂解基因,可使细菌在c-di-GMP升高后进入裂解状态(图1)。这样,细菌的三种生活方式便均与c-di-GMP的浓度相关。通过改变近红外光的照射强度,可以控制活化的BphS蛋白的数量,进而调节工程菌胞内的c-di-GMP的浓度,从而实现对细菌生活方式的控制。
除了光照强度的影响,理论模拟的结果表明:PA2133上游的核糖体结合位点(RBS1)与抗终止蛋白Q上游的核糖体结合位点(RBS2)的强度将对使细菌进入不同的生活方式所需的近红外光光强产生巨大的影响。
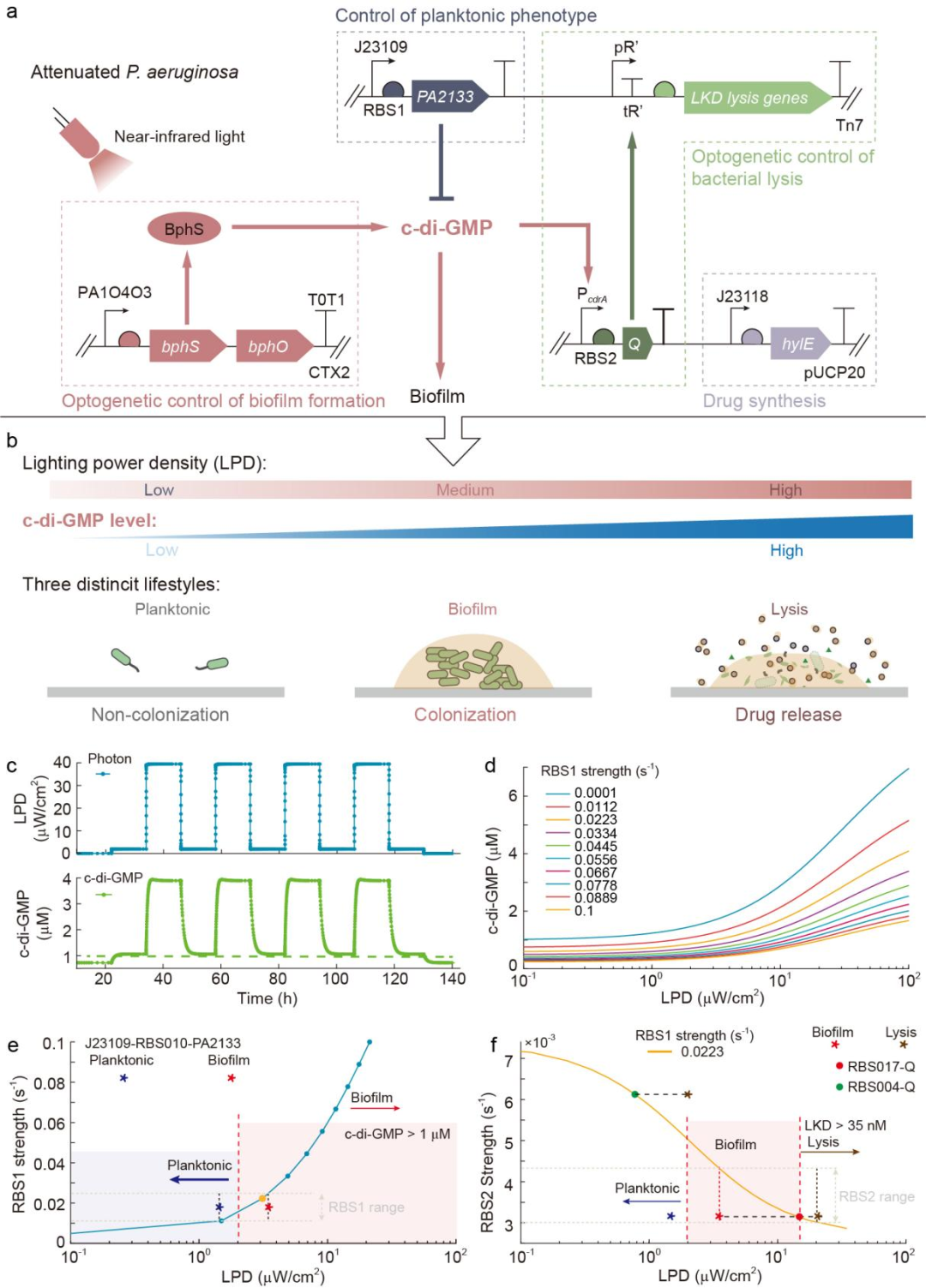
图1 用于编程细菌生活方式的基因线路的设计
为了获得能够在不同强度的近红外光照射下呈现三种生活方式的工程菌,研究团队对RBS1和RBS2进行批量替换,并通过96孔光照装置对候选菌株进行批量筛选,随后利用显微镜进行验证,最终得到的工程化菌株被命名为H017(图
2)。通过层级性调控近红外光的照射强度可以编程H017的生活方式,当对H017施加中等强度-高强度循环的近红外光光照程序时,细菌将进入生物被膜状态-裂解状态生活方式循环。
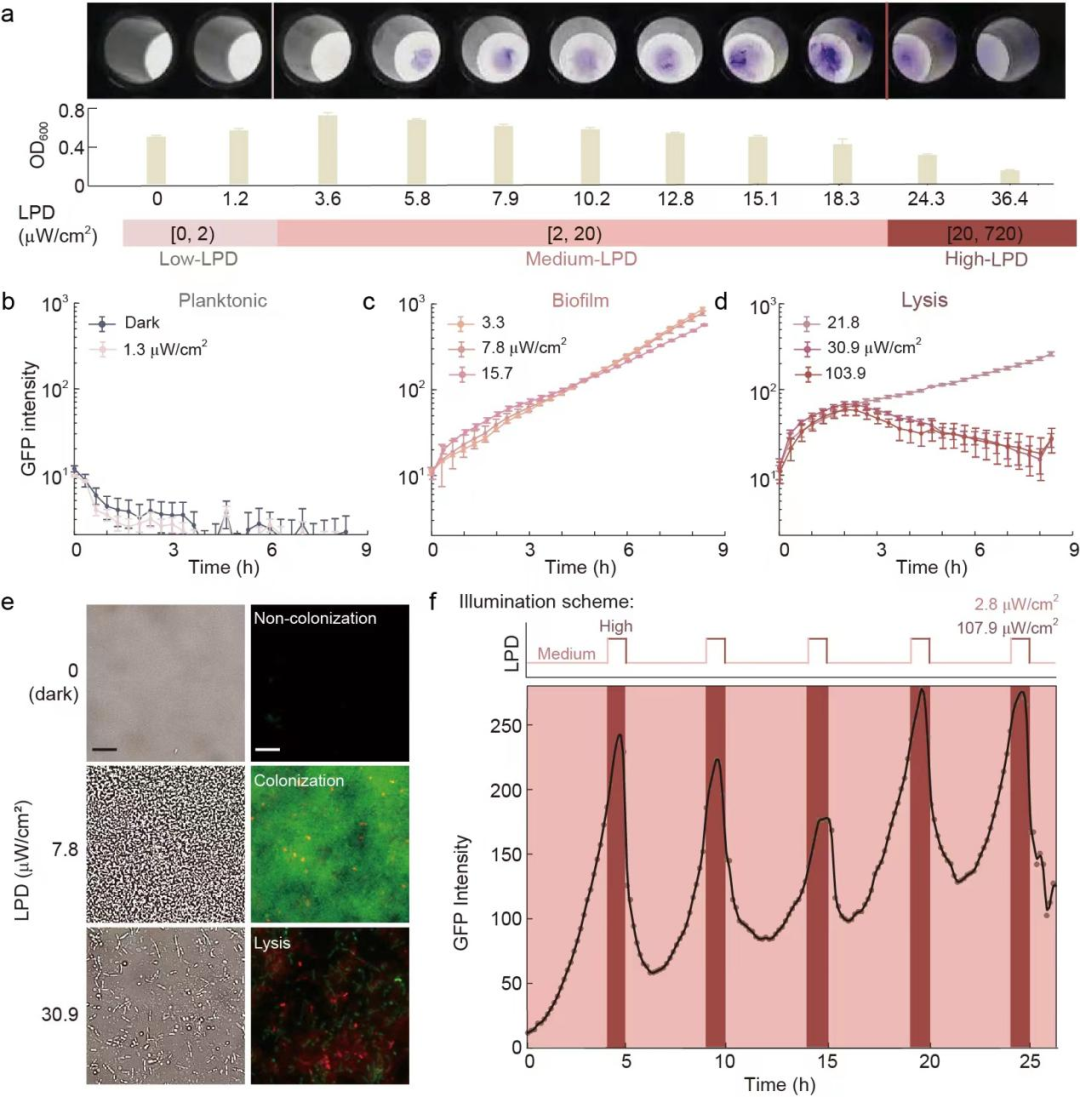
图2 通过层级性调节近红外光的强度编程细菌生活方式
为了在体外验证工程菌的三种生活方式在肿瘤治疗中的作用,研究团队在微流通道中进行了细菌-细胞共培养实验(图3)。研究团队首先证实,当对指定区域的细胞施加不同强度的近红外光光照时,工程菌能够精确地在该区域内进入对应的生活方式。当对指定区域的细胞施加中等强度-高强度的光照程序时,H017先进入生物被膜状态并大量定殖在细胞表面,随后进入裂解状态释放治疗药物造成细胞坏死。以上结果表明,能够通过近红外光对工程菌的生活方式进行高时空分辨率的控制。此外,综合对照组实现的结果,研究团队发现生物被膜状态的药物累积过程与裂解状态的药物释放过程是H017杀伤肿瘤细胞的关键。
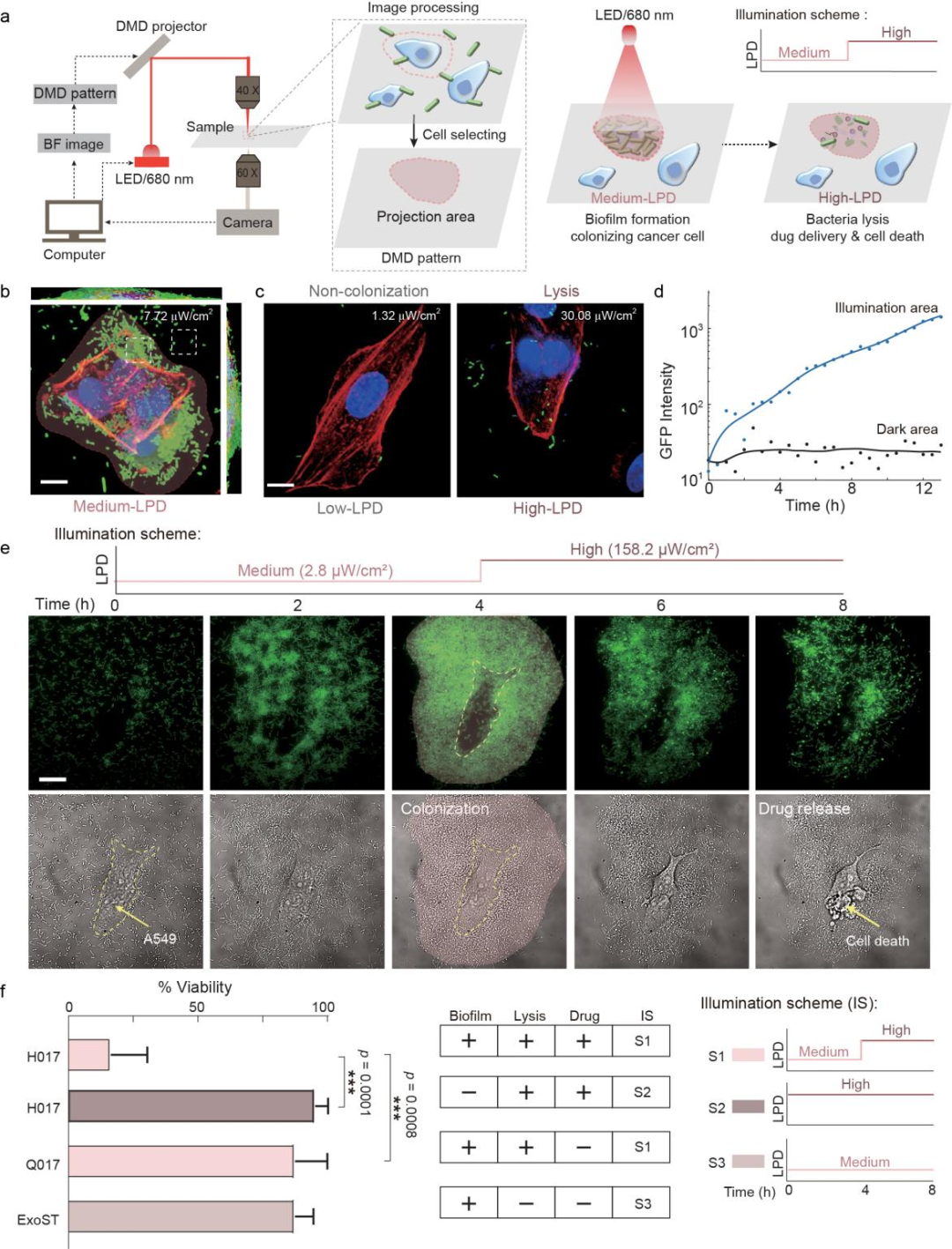
图3 编程细菌“生物被膜-裂解”生活方式转换实现药物的控制释放
随后,研究团队使用小鼠皮下瘤模型探究能否通过近红外光控制工程菌在瘤内的生活方式并实现预期的功能(图4)。结果显示,在瘤内注菌后,避光培养三天组的小鼠(D3)肿瘤组织内的细菌数量与注射PBS组没有显著差异,表明进入浮游状态生活方式的细菌难以在肿瘤内定殖;中等光强照射三天组的小鼠(M3)肿瘤组织内的细菌数量与D3组相比显著增加,表明进入生物被膜状态生活方式的细菌在肿瘤组织内的定殖能力大大增强;中等光强照射两天高光强照射一天组的小鼠(M2-H1)与M3组相比,细菌数量显著降低,且M2-H1组的肿瘤组织切片中能够看出明显的坏死区域,表明细菌裂解后释放药物并杀伤了肿瘤细胞;中等光强照射两天高光强照射一天再中等光强照射两天组的小鼠(M2-H1-M2)与M2-H1组相比,细菌数量再次上升,这表明细菌在中等光强照射后,再次进入定殖生长状态。此外,在中等光强近红外光照射七天后,瘤内的工程菌仍然具有裂解能力,表明该基因线路具有较好的稳定性。综合以上结果可知,不同强度的近红外光照射能够使瘤内细菌进入对应的生活方式并实现预期的功能,而通过连续改变的光照程序能够实现对瘤内细菌生活方式的持续控制。
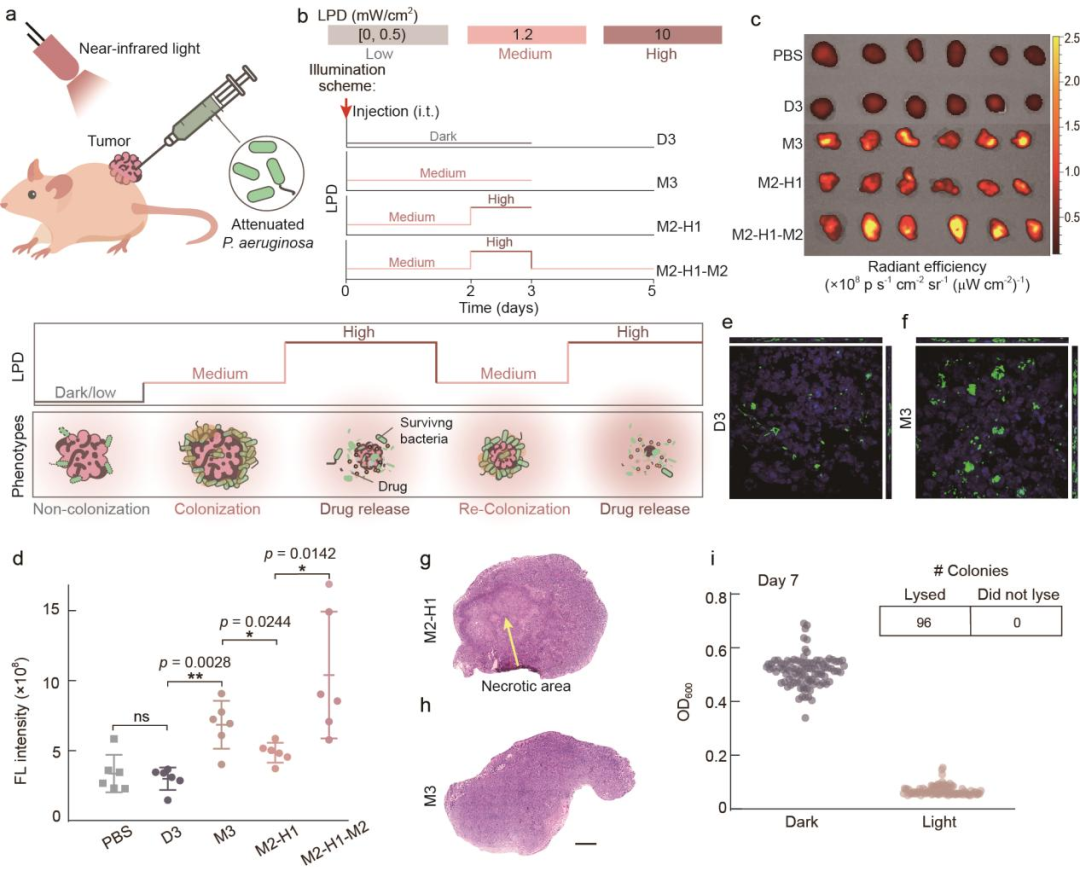
图4 通过近红外光操控实体瘤内的细菌生活方式
最后,研究团队探究能否通过编程工程菌生活方式增强其肿瘤治疗效果(图5)。当H017仅作为药物递送载体时,高强度的近红外光光照能够使H017裂解释放药物,完成肿瘤治疗。团队在20天的实验周期内,通过8次注菌,有效抑制了肿瘤生长。接下来,研究团队通过光照程序对细菌的生活方式进行控制,以实现对药物累积和药物释放的持续控制。结果显示,在对小鼠施加两个循环周期的中等强度2天-高强度1天的近红外光光照程序(M2-H1×2)后,小鼠肿瘤生长受到了抑制,而对照组无法抑制小鼠肿瘤生长。在更长周期的实验中(M2-H1×6),通过光照时间编程细菌生活方式进行肿瘤治疗使所有小鼠的肿瘤生长受到了抑制,其中30%小鼠的肿瘤完全消失,而对照组小鼠的肿瘤则持续生长。以上结果表明,编程细菌生活方式在肿瘤的长期治疗过程中具有显著优势,能够在较少的注菌次数下获得更好的肿瘤抑制效果。
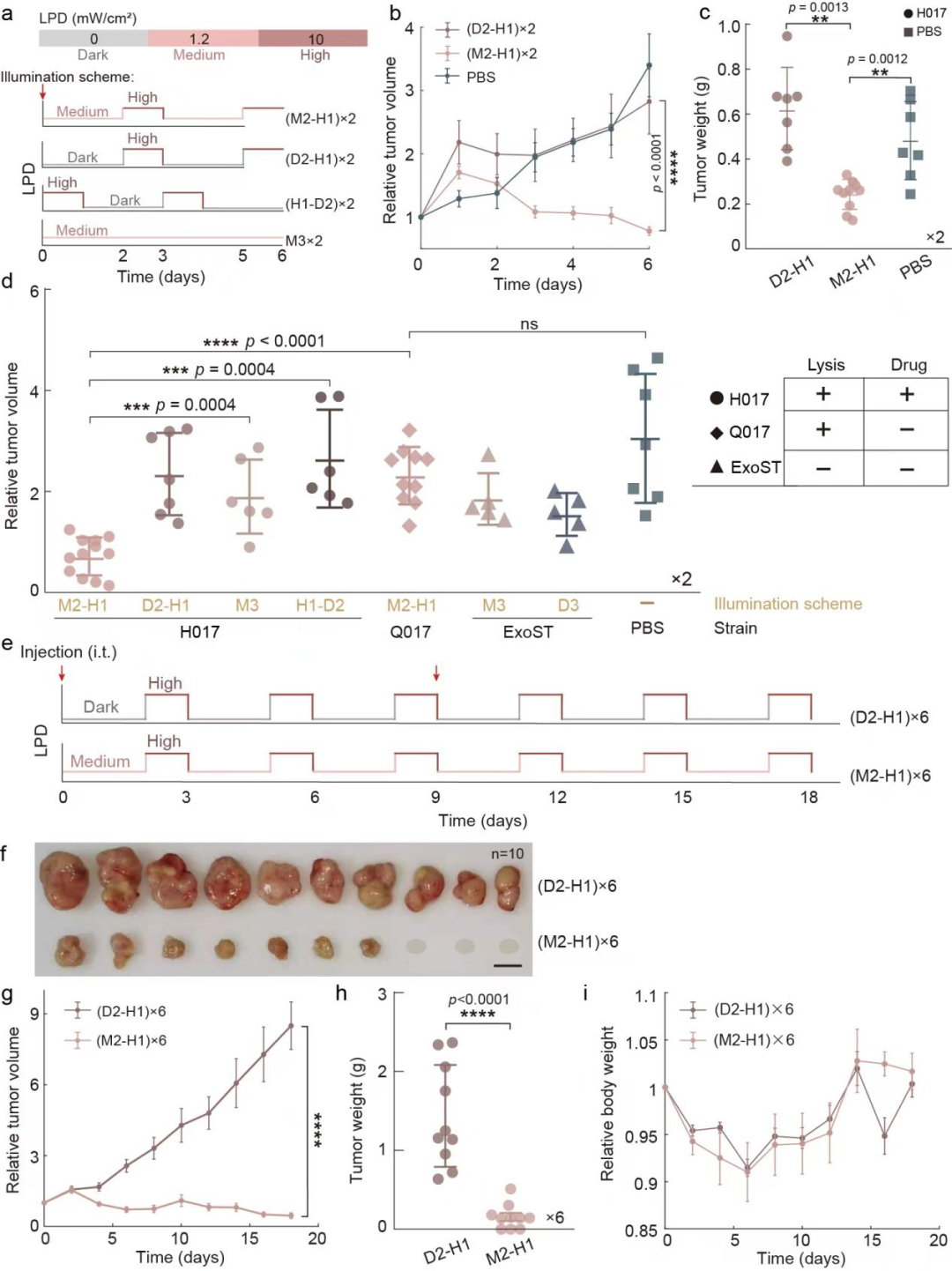
图5 编程瘤内细菌生活方式促进实体瘤消退
审核编辑:刘清
-
近红外光谱仪校准方法 近红外光谱仪与紫外光谱仪区别2024-12-06 2325
-
Aigtek功率放大器在高功率近红外光梳系统中的应用2024-11-11 1163
-
近红外光谱仪的原理 近红外光谱仪的采样方式2024-02-04 4252
-
近红外光谱仪是干什么用的 近红外光谱仪使用方法2024-01-25 4868
-
近红外光谱技术发展及原理2023-05-22 3444
-
近红外与中红外光谱分析的区别2023-05-16 3178
-
模块化设计的磁控工程细菌实现肿瘤精准免疫治疗2023-04-07 2838
-
红外光的基本原理2022-01-24 1182
-
基于近红外光电传感技术的溢油监测系统设计2018-11-02 2452
-
近红外光谱技术概述2010-11-10 2901
-
近红外光谱原理2008-08-12 4441
-
红外光控制开头电路图2007-12-12 949
全部0条评论

快来发表一下你的评论吧 !

