

质谱(Mass Spectrometry)|质谱分析
电子说
描述
质谱是有机化合物鉴定的有力工具之一,包括相对分子质量测定、化学式确定及结构鉴定等。
1、相对分子质量的测定
从分子离子峰的质荷比可以准确地测定其相对分子质量。理论上可认为除同位素峰外,分子离子峰应该是最高质量处的峰,但有时由于分子离子的稳定性差而观察不到分子离子峰。在纯样品质谱中,分子离子峰应具有以下性质:
(1)原则上除同位素峰外,分子离子峰是最高质量的峰。但某些样品会形成质子化离子峰及缔合离子峰。下图是样品可能会形成的加合离子。在ESI源条件下,双电荷离子如(M+2H)^2+^,(M-2H)^2-^和二聚体离子如(2M+H)^+^,(2M+HCOO)^-^也经常被观测到。
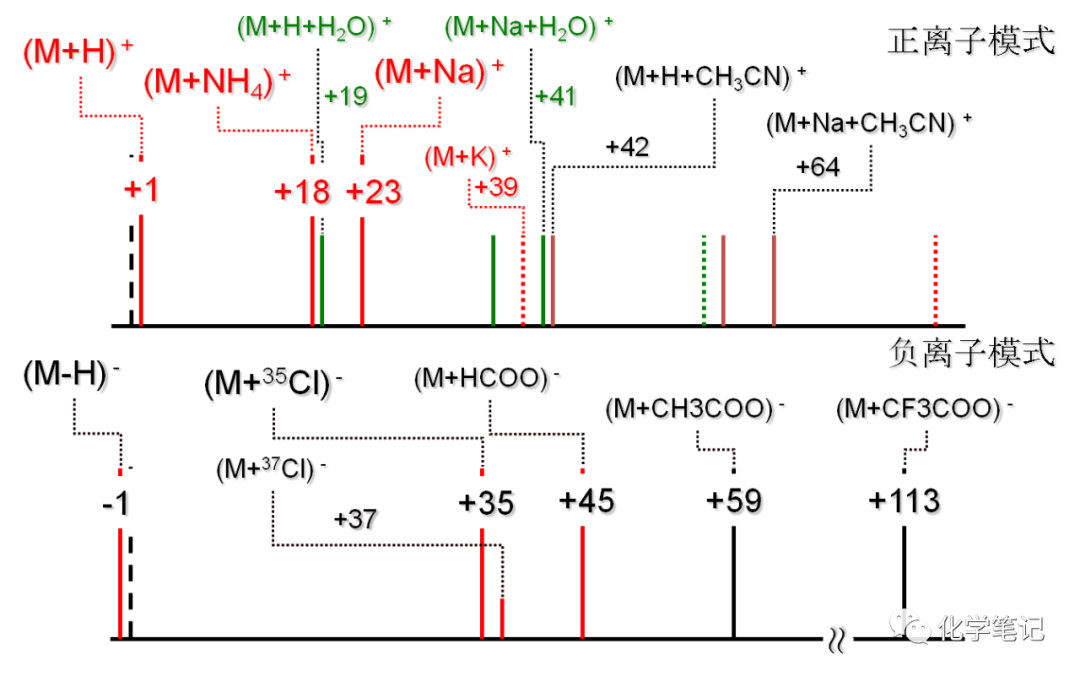
(2)符合氮规则:在只含C、H、O、N的化合物中,不含或含偶数个氮原子的分子的质量数为偶数,含有奇数个氮原子的分子的质量数为奇数。这是因为在由C、H、O、N、P、卤素等元素组成的有机分子中,只有氮原子的化合价为奇数而质量数为偶数。
(3)存在合理的碎片丢失。有机分子经离子化后,分子离子可能丢失一个H或CH 3 、H2O、C2H4等碎片,相应会出现M-1、M-15、M-18、M-28的碎片峰。
2、化学式的确定
(1)高分辨的质谱仪可以精确地测定分子离子或碎片离子的质荷比,则可利用化合物的确切质量推算出其元素组成。如CO与N 2 ,两者的质量数都是28,但两者确切质量为27.9949与28.0061,若质谱仪测得的质荷比为28.0040,则可推断其为N 2 。
(2)有些元素具有天然存在的稳定同位素,所以在质谱图上出现一些M+1、M+2的峰,由这些同位素形成的离子峰称为同位素离子峰。

分子离子的同位素离子峰相对强度之比符合统计规律:
对于碳原子来说,^12^C的天然丰度为98.9%,^13^C的天然丰度为1.07%,从M+1峰与M峰强度的比值,可估算出分子中含碳的数目,碳原子的数目上限=I(M+1)/I(M)÷1.1%,式中I(M+1)和I(M)分别表示M+1峰和M峰的强度。因此,含有一个碳原子的化合物如甲烷,M=17 与M=16的峰强度之比应该为0.011.
其他元素也有同样的规律,含有一个氯原子的化合物中,I(M+2)/I(M)=32.5%,而在含有一个溴原子的化合物中,I(M+2)/I(M)=1.对于含有C、Br、Cl等同位素天然丰度较高的元素的化合物,其同位素离子峰相对强度可由(a+b)^n^展开式计算,式中a、b分别为该元素轻、重同位素的相对丰度,n为分子中该元素个数。在含有两个氯原子的化合物中,a=3,b=1,n=2,故(a+b) ^2^ =9+6+1,则其分子离子峰与相应同位素离子峰强度之比为9:6:1.
3、结构鉴定
通过对谱图中各碎片离子、亚稳离子、分子离子的化学式、m/z、相对峰高等信息分析,根据各类化合物的分裂规律,找出各碎片离子产生的途径,从而拼凑出整个分子结构。
有机质谱中常见的裂解反应如下:
(1)α裂解:在奇电子离子中,与其相邻原子的外侧键断裂,属于该原子的一个电子转移,并与游离基中心的未成对电子形成新键,构成较稳定的碎片离子。
(2)i裂解:在奇电子离子中,与正电荷中心相连的键的一对电子全被正电荷所吸引,造成单键的断裂和电荷的转移。
(3)σ裂解:分子中σ键在电子轰击下失去一个电子,随后分子裂开生成碎片离子。
(4)γ裂解:由自由基引发、重新组成新键而在γ位导致碎裂的过程。
(5)麦氏重排:具有γ**- 氢原子的侧链苯、烯烃、环氧化合物、醛、酮等经过六元环状过渡态使γ -**氢转移到带有正电荷的原子上,同时在α、β原子间发生裂解。
(6)逆Diels-Alder(RDA)裂解:具有环己烯结构类型的化合物可发生此类裂解,一般形成一个共轭二烯正离子和一个烯烃中性碎片。

-
二次离子质谱分析仪 (SIMS)2018-09-12 4309
-
ACS使用机械臂和质谱分析不规则三维形状的表面2018-11-27 2408
-
质谱分析技术最新进展及应用交流会顺利举办2012-03-29 1333
-
北京大学在多维度单细胞质谱流式分析领域取得重要进展2020-11-10 3688
-
质谱(Mass Spectrometry)|质谱仪器2023-06-01 11986
-
质谱分析如何支持半导体发展需求?2023-11-07 1148
-
英迈质谱流路分配器:精准控制,引领质谱分析新高度2024-12-26 952
全部0条评论

快来发表一下你的评论吧 !

