

用于生物膜感染糖尿病伤口愈合的防治一体化纳米酶微针
描述
如何促进细菌生物膜感染的糖尿病伤口的愈合是一项亟需解决的全球公共卫生问题。然而,由于生物膜感染部位的低药物渗透性及伤口愈合中潜在的再感染风险,现有的治疗方法疗效受限。
近期,中国药科大学戴建君/鞠艳敏团队设计了一种防治一体化的纳米酶微针(Fe2C/GOx@MNs)用于耐甲氧西林金黄色葡萄球菌(MRSA)生物膜感染的糖尿病伤口愈合。具有足够机械强度的可溶性针尖可提高Fe2C纳米颗粒(Fe2C NPs)及葡萄糖氧化酶(GOx)的渗透能力以实现高效的生物膜消除。与此同时,具有良好的透气性、吸湿性和抗菌性壳聚糖背衬层(CS)可防止伤口愈合过程中的再次感染。重要的是,Fe2C/GOx@MNs的生物膜清除和再感染预防能力在MRSA生物膜感染的糖尿病小鼠伤口模型中亦得到了证实,表明其在细菌生物膜感染伤口愈合方面具有良好的临床应用前景。该研究以“An Integrated Therapeutic and Preventive Nanozyme-Based Microneedle for Biofilm-Infected Diabetic Wound Healing”为题发表在Advanced Healthcare Materials期刊上。
该研究以负载Fe2C NPs和GOx的高生物相容性的聚乙烯醇(PVA)作为可溶性针尖,以5%CS溶液作为背衬层,最终经过干燥、脱模得到防治一体化的分层微针(Fe2C/GOx@MNs)。该微针应用于生物膜感染的伤口组织时,其针尖可突破伤口部位腐烂组织及致密生物膜所产生的渗透屏障,借助伤口部位组织液将具有抗菌活性的Fe2C NPs/GOx快速释放入生物膜内部。盟友GOx的加入打破了伤口部位pH和H2O2浓度对Fe2C NPs抗生物膜能力的限制,加速MRSA生物膜的清除。进一步的研究阐明大量·OH的产生及细菌氧化还原稳态的失衡是Fe2C/GOx@MNs主要的抗生物膜机制。此外,壳聚糖背衬层具备良好的透气性、吸湿性和抗菌性能,不仅作为在伤口与外部环境之间的物理屏障作用,还阻止了环境中细菌在伤口愈合过程中发起的再次入侵(方案1)。以上结果证明该防治一体化纳米酶微针有可能成为理想的促进生物膜感染的糖尿病伤口愈合的候选材料,并可应用于各种相关的生物医学领域。
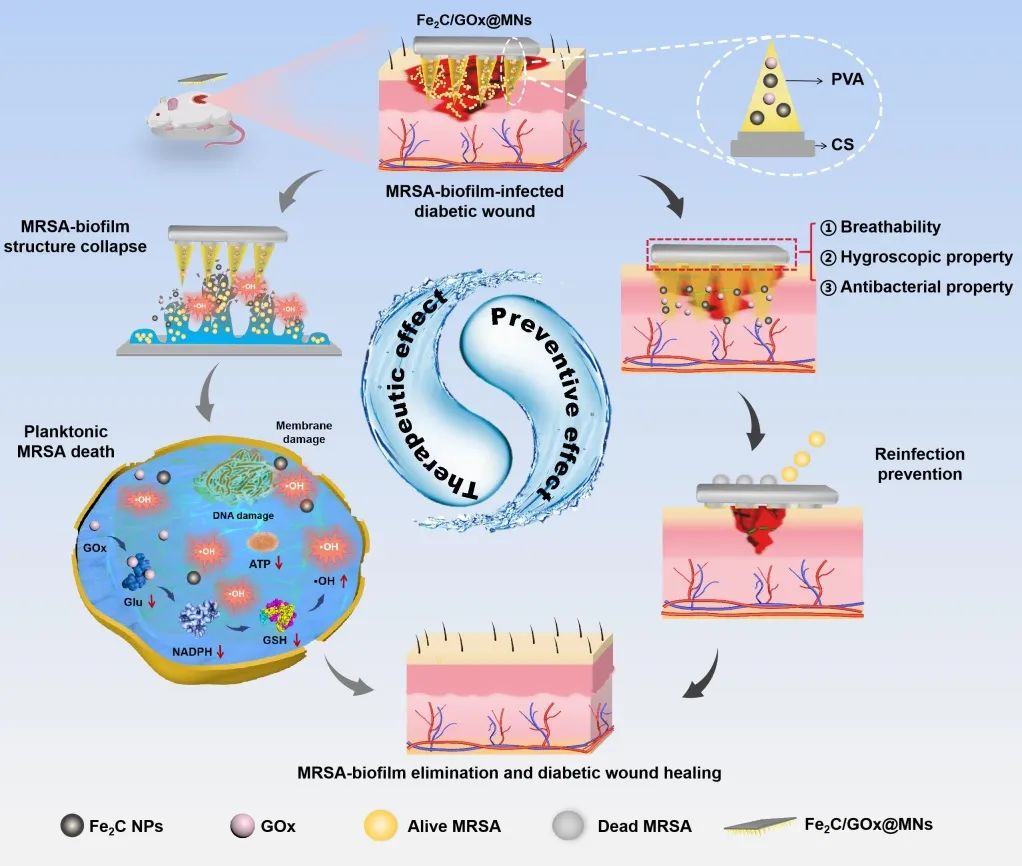
方案1 Fe2C/GOx@MNs清除糖尿病创面MRSA生物膜及预防再感染示意图
Fe2C/GOx@MNs的制备与表征
将Fe2C NPs与GOx及25%PVA溶液混匀经离心以填充到聚二甲基硅氧烷模具腔中,然后轻轻加入5%CS的醋酸溶液覆盖针尖,最终脱模得到微针贴片。为了确保Fe2C/GOx@MNs能突破伤口部位腐烂组织及致密生物膜所产生的渗透屏障,研究者对其结构及针尖机械性能进行全方位的测定,证实该微针贴片呈现分层结构且针尖具有足够的机械力(0.7 N/针),能够成功穿刺皮肤。具有优良的吸湿性能和抗菌性能的背衬层可通过吸收创面渗出液抑制创面化脓,防止再感染的发生。研究者通过进一步的探索发现CS背衬层不仅呈现吸湿溶胀性能,且对MRSA具有显著的杀伤能力。
大量的研究表明高水平的H2O2和低pH可以增强纳米酶活性。GOx可以催化葡萄糖分解生成H2O2和葡萄糖酸,已被报道可用于打破来源于环境的H2O2和pH限制。因此,在该研究中,研究者借助草酸钛钾、pH计及3,3',5,5' -四甲基联苯胺对反应体系中H2O2、酸碱度及·OH进行检测。结果发现,GOx的加入提升了反应体系中H2O2的浓度同时也降低了pH值。更重要的是,Fe2C NPs的类过氧化物酶活性得到了大大的增强,产生了更多的·OH。该结果在溶液体系及微针贴片中均得到了证实(图1)。
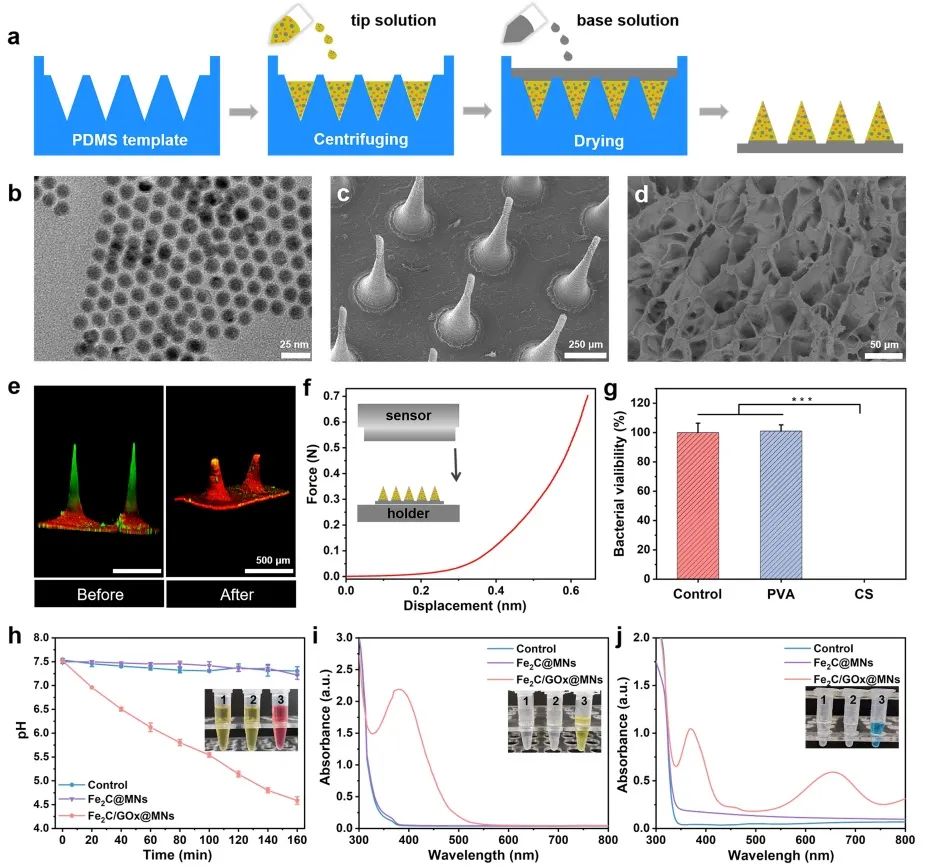
图1 Fe2C/GOx@MNs表征
Fe2C NPs/GOx体外抗生物膜性能测定及机理研究
在将Fe2C NPs/GOx装入MNs之前,研究者在模拟糖尿病伤口条件下通过标准平板计数法、结晶紫法、荧光染色法对其体外抗菌性能进行评估。结果表明Fe2C NPs/GOx在体外呈现强的抗生物膜性能,其生物膜清除率高达93.21 ± 0.37%,且GOx的加入对生物膜的清除起正向促进作用(图2)。
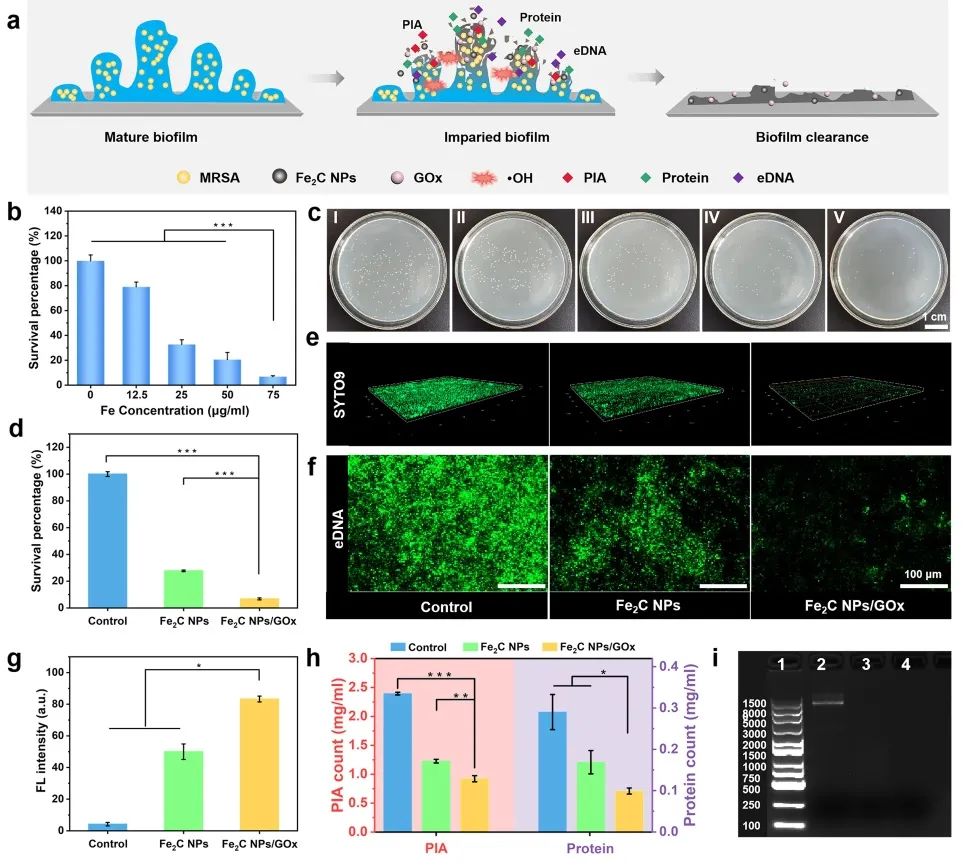
图2 Fe2C NPs/GOx体外抗生物膜性能及其对EPS的损伤能力测定
为了进一步阐明Fe2C NPs/GOx的抗生物膜机制,研究者通过细致研究及多次验证,将其抗生物膜机理总结如下:首先,·OH通过破坏胞外基质的主要成分(eDNA、PIA和蛋白质)诱导生物膜结构解体。随后,MRSA的细胞膜和细胞壁被破坏,细胞内成分(离子、蛋白质和DNA)外排。其次,磷酸戊糖途径的抑制及相关酶的失活导致细胞内谷胱甘肽含量降低,进而破坏了细菌氧化还原稳态。最后,·OH超载进一步导致细菌基因组DNA断裂,代谢抑制,加剧细胞结构的破坏,最终实现生物膜清除(图3)。
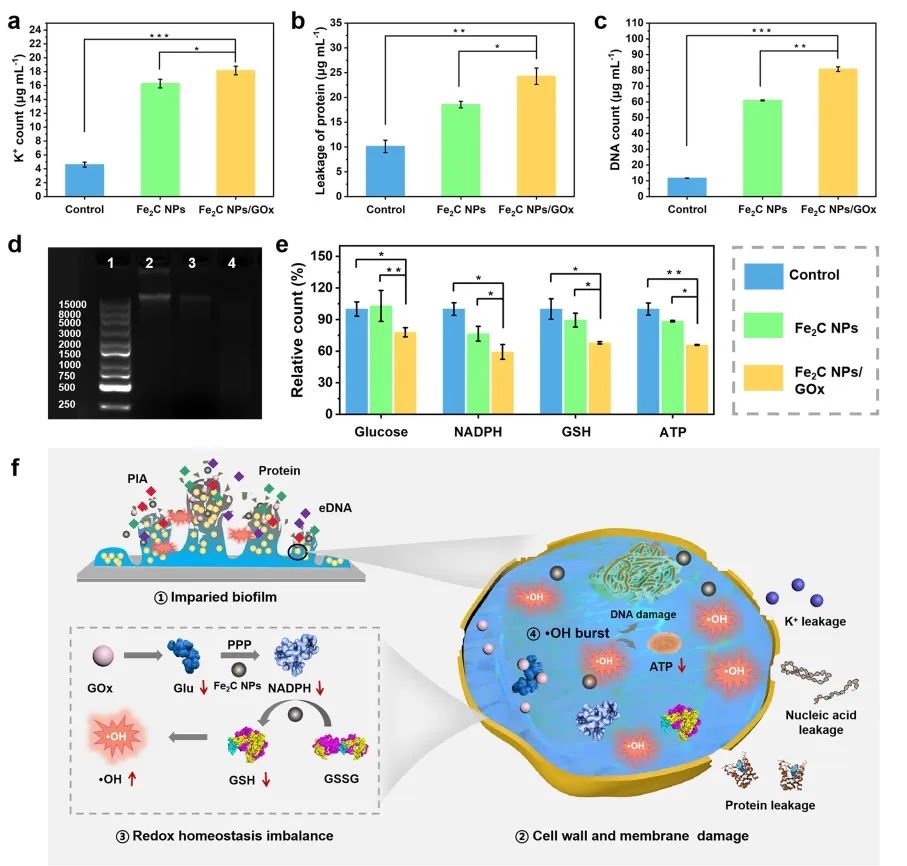
图3 Fe2C NPs/GOx抗生物膜机制
Fe2C/GOx@MNs体内抗生物膜性能测定及促伤口愈合能力评估
鉴于Fe2C NPs/GOx出色的体外抗生物膜活性,研究者随后在MRSA生物膜感染的糖尿病伤口模型中评估了Fe2C/GOx@MNs的抗生物膜性能和促伤口愈合能力。结果表明相比于溶液处理组,微针处理组的生物膜清除率及伤口愈合率明显得到了提升。更重要的是,在GOx的辅助下,抗生物膜能力增强,伤口愈合速率加快,Fe2C/GOx@MNs(PVA)组和Fe2C/GOx@MNs组在第9天几乎看不到伤口,且仅有少量MRSA菌落被观察到。
为了进一步明确Fe2C NPs/GOx的促伤口愈合能力,研究者利用H&E染色、Masson染色和免疫荧光染色对伤口组织进行评估。结果表明,Fe2C/GOx@MNs通过减少炎症、促进胶原沉积、加速血管生成和成熟,对MRSA生物膜感染的糖尿病创面愈合具有显著的促进作用(图4)。
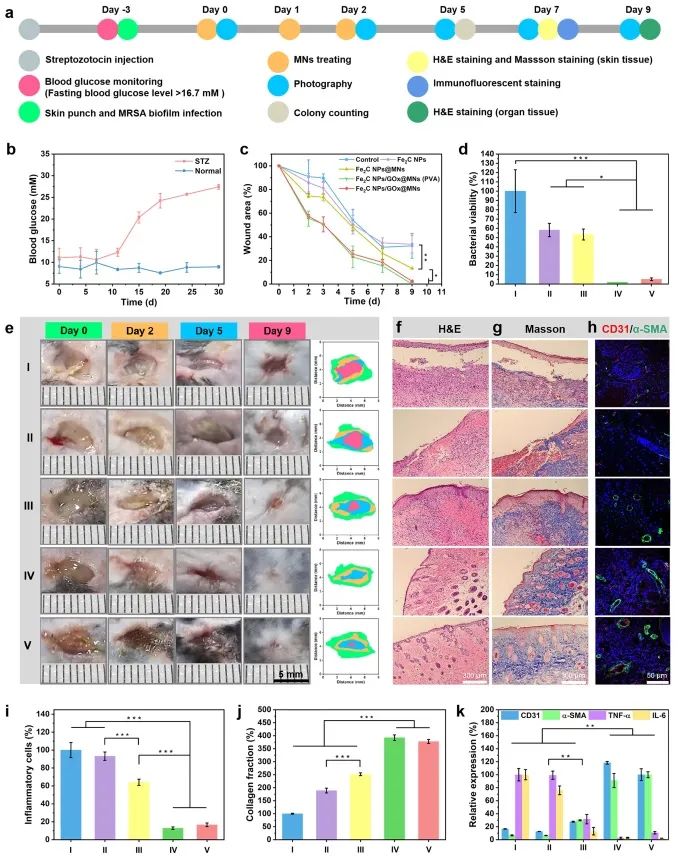
图4 Fe2C/GOx@MNs体内抗生物膜性能及促伤口愈合能力评估
Fe2C/GOx@MNs体内预防再感染能力评估
虽然优良的抗生物膜能力对于伤口的愈合是必要的,但是未愈合的伤口暴露在空气中很容易会出现再次感染,进一步阻碍伤口的愈合。基于此,研究者通过将MRSA菌液滴加到微针贴片处理后的伤口处以模拟再次感染的发生,从而验证微针贴片CS背衬层的预防再感染能力。结果表明,菌液处理后,PVA组创面面积明显增大而CS背衬层组则减小且与对照组无差异,证明CS背衬层能够杀死入侵的MRSA,保护未愈合创面。另外,标准平板计数法和革兰氏染色的结论与上述一致(图5)。
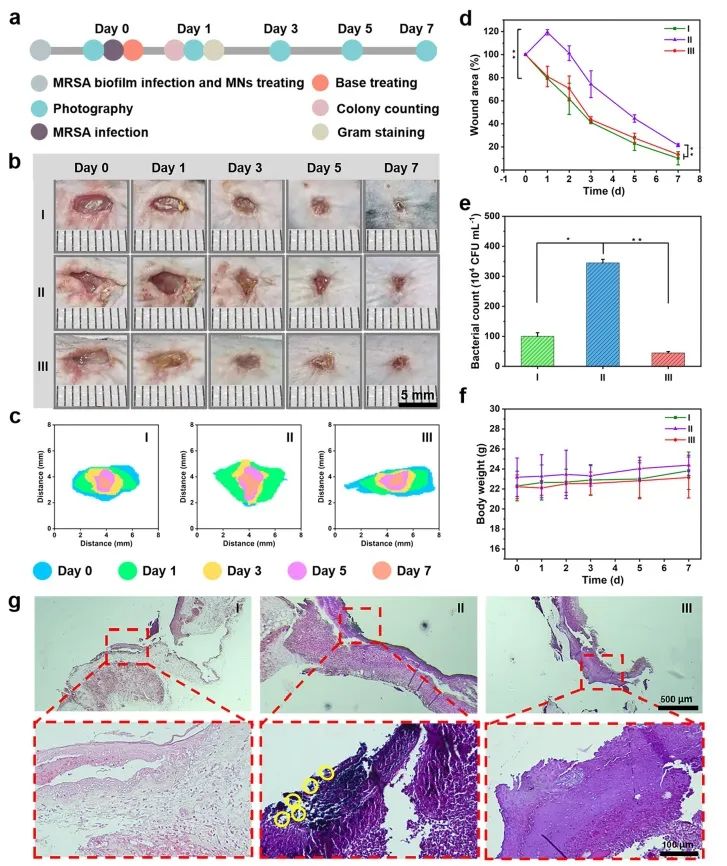
图5 Fe2C/GOx@MNs体内预防再感染性能评估
综上所述,研究者设计了一种基于纳米酶的防治一体化Fe2C/GOx@MNs微针贴片,并在体内外水平对其抗生物膜性能及促伤口愈合能力进行了全面的验证。该微针贴片的可溶性针尖可克服各种物理障碍,将Fe2C NPs/GOx递送至生物膜内部,高效去除生物膜。同时,具有良好透气性、吸湿性和抗菌性的壳聚糖背衬层可以防止伤口愈合过程中再次感染。体外和体内实验结果均显示GOx对Fe2C NPs有增强的抗菌作用。同时,体内实验结果也证明微针的应用可以提高抗生物膜效果。此外,CS保护层在体内的再感染预防能力也得到了验证。上述工作表明该平台在生物膜感染伤口愈合和保护方面具有广阔的应用前景。
审核编辑:刘清
-
以色列面向生物传感器和电路的蛋白质纳米线2018-11-20 2124
-
面向生物传感器和电路的蛋白质纳米线2018-12-03 2013
-
ML之Sklearn:利用八种ML算法对根据糖尿病数据集预测新个体是否患糖尿病2018-12-20 4164
-
rFGF212—2型糖尿病的新治疗靶点2019-09-25 1926
-
智能创可贴:内置处理器,可以追踪伤口的愈合情况检查是否感染和发炎2018-08-12 2965
-
物联网IoT装置如何帮助人们管控糖尿病2018-12-23 2133
-
集成糖尿病管理系统解析2020-07-03 1351
-
Apple Watch 就能预测糖尿病2020-07-13 2110
-
一种基于介孔微针离子泳的集成可穿戴诊疗一体化系统2021-06-15 3110
-
中山大学研发一种基于介孔微针离子泳的集成可穿戴诊疗一体化系统2021-06-16 3172
-
基于透明质酸微针的胰岛素智能给药系统,用于糖尿病治疗2023-06-02 3164
-
如何利用科技发展治愈糖尿病2023-07-03 1565
-
用于糖尿病创面的防疤痕愈合的自供电酶联微针贴片2023-07-30 3907
-
用于促进生物膜清除和糖尿病伤口愈合的多酶级联双层微针反应系统2023-09-12 8995
-
一种具有长效抗菌效果的活性益生菌微针贴片,用于治疗慢性感染伤口2024-05-16 3344
全部0条评论

快来发表一下你的评论吧 !

