

基于特征谱带的高光谱遥感矿物谱系识别
电子说
描述
引言
高光谱的光谱识别是高光谱区分于多光谱的主要标准,也是高光谱的优势所在。目前高光谱岩矿蚀变信息识别与提取的方法主要为基于光谱波形参数、波谱相似性测度、混合光谱模型等。在具有大量已知地物光谱时这些方法适应性强,图像地物识别更有用。但明显不足是由于实际地物光谱变异、获取数据受观测角以及颗粒大小的影响而造成光谱变化,准确匹配比较困难,造成岩矿识别与分析上的混淆和误差。
矿物光谱特征
在当前光学遥感摄影普遍使用的谱段范围(0.4~2.5μm)内,岩矿标型光谱特征都与碳酸根、水、羟基和铁离子等阴离子基团或一些阳离子有关。矿物吸收特征的差异主要取决于矿物晶体物化属性的不同,即阴阳离子的化合价、阳离子的配位数目、主要阳离子的质量、键的共价程度、阴阳离子间的距离、晶体对称的不同。这些特征吸收指的是矿物独特而较稳定的吸收谱带。这些谱带在不同的矿物中有较稳定的波长位置,具较稳定独特的波形,指示着某种矿物的存在。一般而言,阳离子(如Fe2+,Fe3+和Mn3+等)因电子跃迁而在可见光区或近红外具有特征谱带,阴离子基团(如CO32-,H2O,OH-与金属-OH基团等)因弯曲振动而在短波红外产生倍频与合频光的谱特征。
2.1 矿物光谱特征
(1)Mn离子:这里主要分析水锰矿、硬锰矿、菱锰矿、锰铝榴石与锰橄榄石中Mn的光谱特征。Mn2+是典型的d5电子构架,其谱带主要产生于电子跃迁。在可见光区域(图1),锰的特征谱带主要为0.45μm与0.55μm以及在0.36~0.41μm附近的3处吸收特征,或在0.4~0.6μm区域产生的一个较陡的半吸收特征。
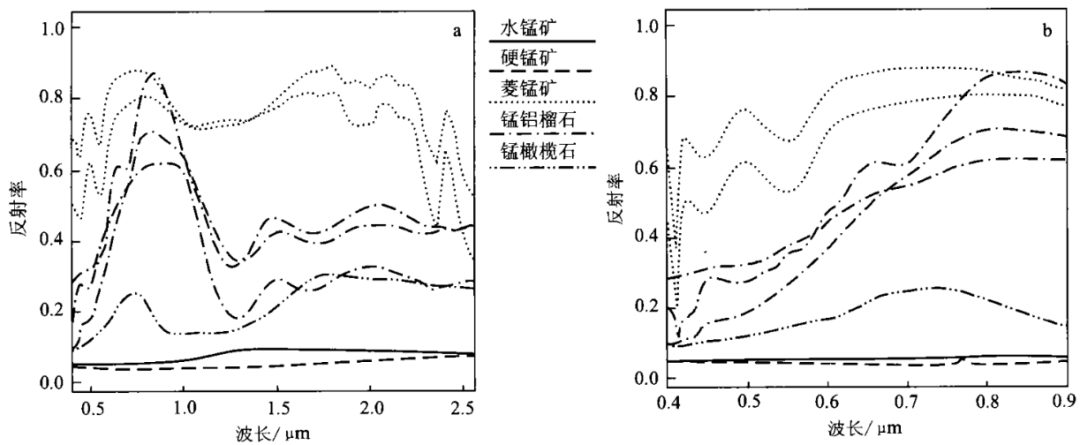
图1含锰矿物光谱
右图为左图的局部放大
(2)Fe离子:在矿物的组成成分中,Fe是一个非常重要的元素。由晶体场理论可知,Fe2+的基态D在四面体场中分裂为较高的五重线能级Eg和较低的五重线能级T2g;由于仅存在一个自旋容许跃迁,从而在1.0~1.1μm附近产生一个常见的强而宽的谱带;Fe3+有一个对称的基态S,在任何晶体场中都不分裂,到4G态所形成的更高能级的跃迁均为自旋禁戒,因而光谱相对较弱,但在0.6~0.9μm间产生强的吸收谱带。对于不同类型铁化合物,因其分子结构、晶体结构以及透明度的差异,其特征谱形差别较大。图2为一些含铁矿物的波谱曲线。
从光谱曲线可知,铁硅酸盐矿物的特征谱带位于0.9μm,呈对称展布于0.8~1.0μm光谱区域。铁的氢氧化合物特征谱带位于1.0μm附近,成非对称展布于0.7~1.40μm之间。而铁的碳酸盐矿物吸收谱带呈宽缓平直状展布于0.8~1.5μm之间。但铁的氧化物和硫化物因矿物颜色的影响,属于不透明矿物系列,出现光谱吸收限,光谱特征被掩盖,轻微的氧化或蚀变可能使铁的一些特征波谱显现出来。
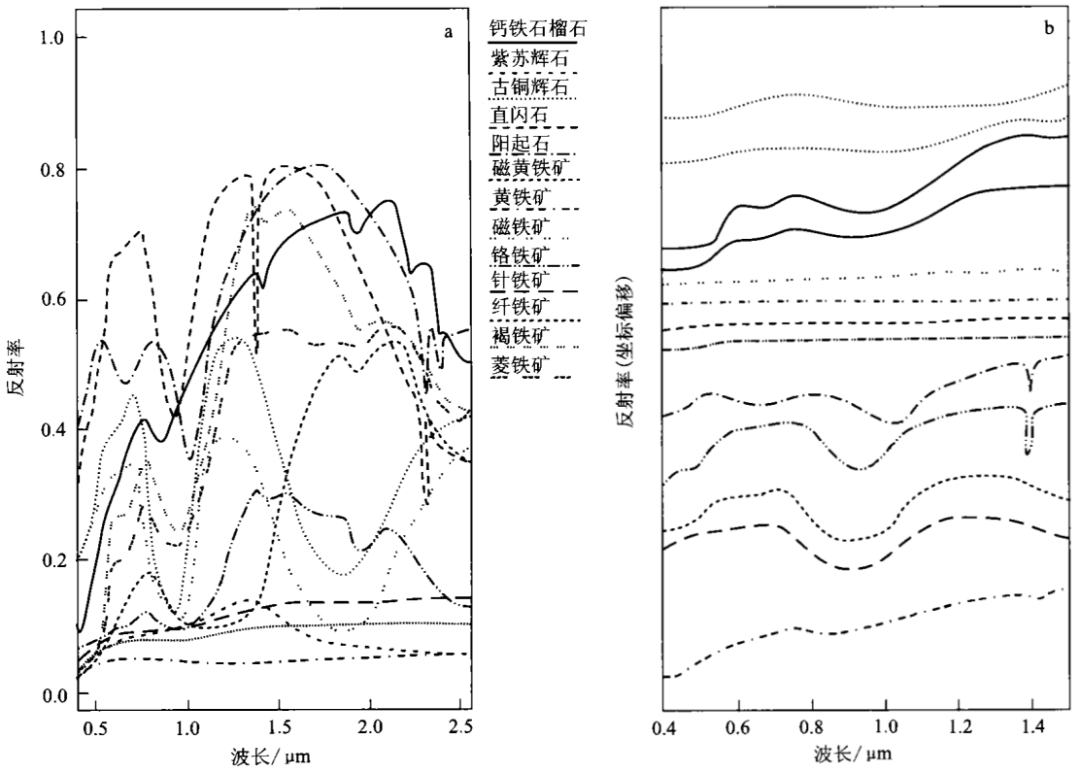
图2铁化合物光谱下图纵坐标偏移,以便能够清楚展示不同铁化合物的光谱特征
左图:Al的氧化物与氢氧化物;右图:Al的硅酸盐矿物
(3)铝离子(Al3+)类矿物光谱:铝离子在大多矿物中均能发现,尤其是硅酸盐矿物。铝在硅酸盐矿物结构中起着双重作用。一是呈四次配位,代替部分的Si4+而进入络阴离子,形成铝硅酸盐;二是呈六次配位,存在于硅氧骨干之外,起一般阳离子作用,形成铝的硅酸盐;或者兼有上述两者的特性。图3为这些矿物的波谱曲线。
铝的氧化物波谱为1.4μm附近的反射峰较强。铝的氢氧化物中,三水铝石由于所含较强的Al-O-H键的伸缩振动的合频或倍频的作用,在1.4~1.6μm间产生尖锐的由主要的1.435μm与次要的1.558μm组成的“二元”吸收特征。硬水铝石因Al3+充填由O2-和(OH)-形成的1/2的八面体空隙,Al-O-H键较弱而在1.408μm产生较弱的吸收特征。
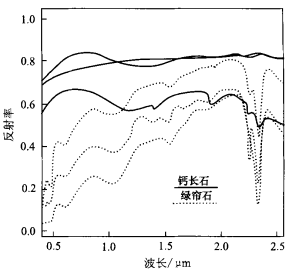
图4钙长石-绿帘石光谱
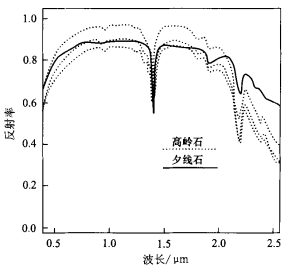
图5高岭石-夕线石光谱
铝的硅酸盐矿物(图3,4,5)的特征光谱与[AlO4]并不相关,与[AlSi3O8]相关性也不明显。铝在硅酸盐中的光谱行为主要是铝阳离子的电子跃迁以及Al-OH基团伸缩振动的合频与倍频的作用,而在短波红外光谱产生特征吸收光谱。随着Al-OH键力的增强与数量的增多,硅酸盐矿物的特征更多地凸显出OH基团的尖锐且窄的吸收特征。由于Al-OH基团在不同晶体结构中能级的差异,其吸收谱带的形态、位置以及次级吸收峰的形态都有所不同。从图3下图可见,钠长石光谱特征并不明显;白云母与高岭石均因较强的Al-OH键而表现出较为一致的1.42μm与2.15μm的特征吸收峰,但在2.0~2.5μm之间的吸收峰形态却存在较大的差异,这是二者识别与区分的标志,是Al在晶体结构中不同占位的光谱外在表现。
在低温条件下,[AlO4]四面体的体积稍大于[SiO4]四面体,从而易转变为六次配位形式。如钙长石Ca[Al2Si2O8]转变成绿帘石Ca2(Al,Fe)3O(OH)[SiO4][Si2O7],使A全部处于八面体配位中,成为最稳定的形式。绿帘石光谱特征(图4)较钙长石复杂,并具有与高岭石或白云母相同的谱形,但相对于后二者,其特征谱带的位置相对向长波方向移动。这主要是由于绿帘石晶体中具有Fe的类质同象,影响了Al在晶体中键力与键长,从而使能级分裂的大小或OH基团伸缩弯曲振动的方向发生变化造成的。
在高温富Al环境,[AlO4]可由六次配位转变为部分的Al的四次配位。如高岭石Al4[Si4O10](OH)8在1000~1500°C的条件下可部分地转变为夕线石Al[AlSiO5]。比较二者的光谱特征(图5)可见,在2.2μm附近的主要特征吸收差异不大,主要差别是高岭石中OH基团振动产生的吸收峰较夕线石尖锐,次级吸收峰特征较明显。总的来说,Al离子自身以及硅铝四面体并无特征吸收,含铝硅酸盐或铝的铝硅酸盐矿物的光谱特征更主要是Al-OH键振动的合频或倍频的结果,这将在金属-OH的光谱特征中加以进一步论述。
2.2 阴离子光谱特征
(1)金属-OH:由于阴阳离子之间键的共价程度、阴阳离子间的距离造成晶体对称度等的不同,使金属-OH基团光谱产生一定的差异。
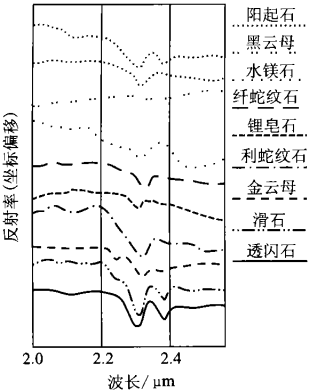
图6 Mg-OH特征离子光谱特征
图6主要为含Mg-OH键矿物的光谱。该类矿物最为显著的是在2.30μm附近具有强吸收特征峰。阳起石强吸收谱带位于2315nm处,黑云母2335nm水镁石2315nm,叶蛇纹石2325nm,纤蛇纹石2325nm,锂皂石2305nm,利蛇纹石2315~2325nm,金云母2325nm,滑石2315nm,透闪石2315nm。含Mg-OH的矿物光谱以2315~2335nm的最大吸收谱带为特征,这也是识别含Mg-OH键矿物的显著标志。
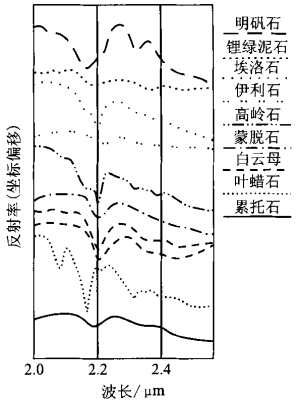
图7 Al-OH特征离子光谱
图7主要是含Al-OH键矿物的光谱。该类矿物最显著的吸收特征是由位于2.20μm附近的最大吸收峰以及其两侧的一些次一级吸收峰构成“二元结构”。明矾石的特征吸收谱带位于2165nm和2325nm处;锂绿泥石为2175nm和2365nm;埃洛石为2205nm和2165nm;伊利石为2215nm和2355nm;高岭石为2205nm和2165nm;蒙脱石为2205nm和2215nm;白云母2195~2225nm和2355nm;叶蜡石2165nm和2315nm;累托石2195nm;黄玉2085nm和2155nm,2215nm。可见含Al-OH键的矿物的识别光谱位于2165nm~2215nm之间。
(2)CO32-:在碳酸盐CO3络阴离子中,C与O之间为键力强的共价键,而CO3与金属阳离子则以离子键为主。在1.3μm以前,碳酸盐矿物的光谱特征主要是由金属离子跃迁所决定;而1.3μm以后,其光谱特征是基团振动所产生,即CO32或一些水分子本身的倍频或合频模式振动产生(图8)。在近红外区,碳酸盐通常出现5个显著的特征谱带:2.55μm,2.35μm,2.16μm,2.0μm和1.9μm,第Ⅰ、第Ⅱ是较清楚的双重谱带,强度比其余3个强;碳酸盐岩矿物最显著的识别特征是2.3~2.4μm之间具有单一的特征吸收,对称性左宽右窄,有别于其它类矿物光谱特征。同时该类绝大多数矿物也具有2.1~2.2μm以及2.5μm附近的次一级特征吸收。所含阳离子的不同,而在0.4~1.2μm区间出现阳离子跃迁的光谱特征,可用于识别不同类型的碳酸盐岩矿物。
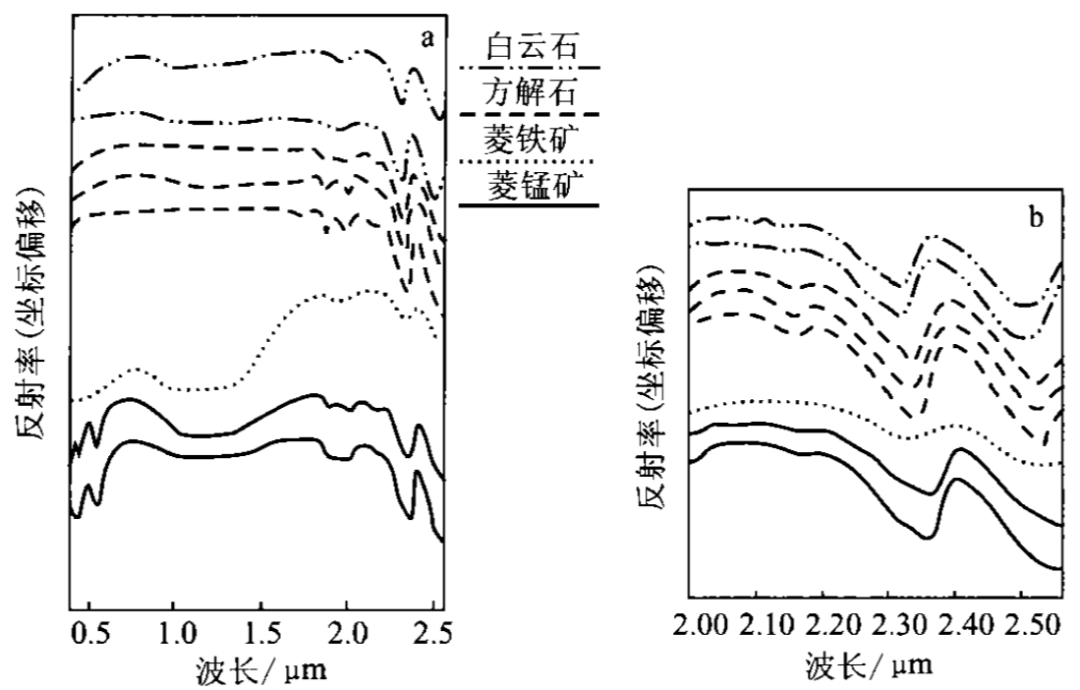
图8 碳酸盐岩矿物光谱特征
右图为左图局部放大;两图的纵坐标已偏移
推荐:
无人机机载高光谱成像系统iSpecHyper-VM100
一款基于小型多旋翼无人机机载高光谱成像系统,该系统由高光谱成像相机、稳定云台、机载控制与数据采集模块、机载供电模块等部分组成。无人机机载高光谱成像系统通过独特的内置式或外部扫描和稳定控制,有效地解决了在微型无人机搭载推扫式高光谱照相机时,由于振动引起的图像质量较差的问题,并具备较高的光谱分辨率和良好的成像性能。

审核编辑 黄宇
-
高光谱遥感在矿物填图中的应用2021-09-02 1207
-
高光谱遥感技术在地质领域的应用研究2022-05-17 4077
-
基于高光谱遥感森林树种识别的应用研究2022-05-26 3753
-
高光谱遥感岩矿识别方法综述2022-07-25 3350
-
高光谱遥感在精准农业生产中的应用2022-08-15 3364
-
基于光谱匹配的高光谱遥感露天矿物识别方法研究2022-09-28 3930
-
农作物高光谱遥感识别和分类-莱森光学2022-11-21 3388
-
高光谱遥感蚀变矿物信息提取研究2023-07-13 1672
-
高光谱成像系统:高光谱数据光谱分辨率对矿物识别的影响分析2023-08-14 2685
-
航空高光谱遥感区域成矿背景研究2023-08-16 2190
-
航空高光谱遥感区域成矿背景研究—以甘肃柳园-方山口地区为例2.02023-08-24 1400
-
高光谱成像技术:矿物光谱识别特征参数2023-09-18 2269
-
矿物识别谱系与识别规则2023-10-20 1509
-
土壤矿物对松嫩平原主要土壤类型反射光谱特征的影响机理2023-11-22 1613
-
便携式高光谱成像系统:岩矿高光谱遥感2024-06-21 2062
全部0条评论

快来发表一下你的评论吧 !

