

利用惯性-磁微流控技术实现恶性肿瘤细胞的快速、高纯度分离
描述
大量血细胞和淋巴细胞的存在严重影响了恶性胸腹腔积液中恶性肿瘤细胞检测的灵敏度。微流控技术能够根据复杂细胞群体的物理和生化特性精确分离和富集靶细胞,具有成本低、操作简单、精度高、并行处理能力强等优点,为基础生物学研究和临床诊断提供了重要的工具。然而,由于恶性胸腹腔积液大体积的处理需求以及白细胞和恶性肿瘤细胞之间存在尺寸重叠问题,目前已报道的主动或被动的微流控技术无法保证在高通量样品处理过程中兼顾肿瘤细胞分离的回收率和纯度。
近期,东南大学项楠教授课题组报道了一种集成梯形螺旋芯片和免疫磁性芯片的惯性-磁性细胞分离(IMCS)装置,用于从恶性胸腹腔积液中恶性肿瘤细胞的高通量、高回收率和高纯度分离,相关成果以“Inertia-magnetic microfluidics for rapid and high-purity separation of malignant tumor cells”为题发表在国际化学权威杂志Sensors and Actuators: B. Chemical上。文章第一作者为倪陈博士,通讯作者为项楠教授。
该团队设计的IMCS装置集成了梯形螺旋芯片和免疫磁性芯片,完美地将被动微流控技术的高通量优势和主动微流控技术的高精度优势进行有机结合,同步提升了恶性肿瘤细胞分离的回收率和纯度。具体而言(见图1),该团队首先对临床样本进行预处理,裂解样本中的红细胞并对白细胞进行磁珠标记;随后不同尺寸的细胞在设计的梯形螺旋芯片中受到剪切梯度和壁效应引起的惯性升力和二次流引起的Dean阻力的联合作用下,被分别聚焦至不同的平衡位置,从而实现对尺寸小于10 µm白细胞的快速去除;最后大尺寸白细胞在免疫磁性芯片中磁场作用下逐渐被推离原本的平衡位置,从而实现与尺寸相近肿瘤细胞的进一步高效分离。针对梯形螺旋芯片和免疫磁性芯片可实现细胞分离的不同流速条件,该团队在表征两个芯片最佳流速范围后,通过设计添加流阻芯片来实现两个分选芯片的高性能集成。
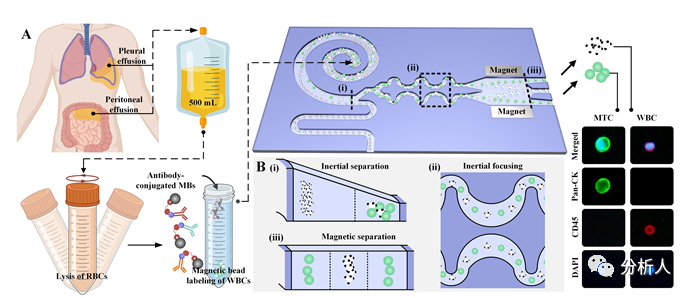
图1 IMCS装置的工作流程的示意图,该装置用于从大体积恶性胸腹腔积液中恶性肿瘤细胞的高通量、高回收率和高纯度分离
基于稳定运行的IMCS装置,该团队分别对A549、MCF-7和MDA-MB-231细胞进行了与白细胞混合后的分离测试(见图2)。研究表明,不同种类的肿瘤细胞均可实现与白细胞的高效分离,该装置可以在3.2 mL/min的处理通量下快速实现对肿瘤细胞高回收率(> 90%)和高纯度(> 70%)的分离。最后,该团队将开发的IMCS装置运用于临床恶性胸腹腔积液中稀有恶性肿瘤细胞的富集和纯化(见图3),实现了对恶性肿瘤细胞平均纯度高达70.52%的有效分离,纯化后的样品可直接用于恶性肿瘤细胞的体外培养、药敏试验、基因测序等生物医学应用。临床实验证明了该装置对促进癌症诊断和药物研究具有潜力。
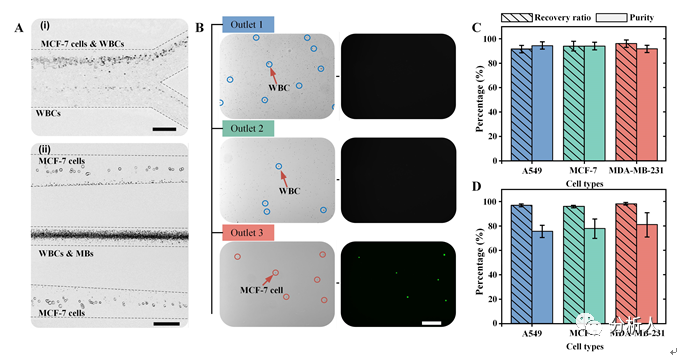
图2 (A)芯片出口处的细胞分布图像;(B)收集液中明场和荧光显微图像;不同肿瘤细胞浓度的分选性能表征:(C)~ 10⁵ cells/mL;(D)~ 10³ cells/mL
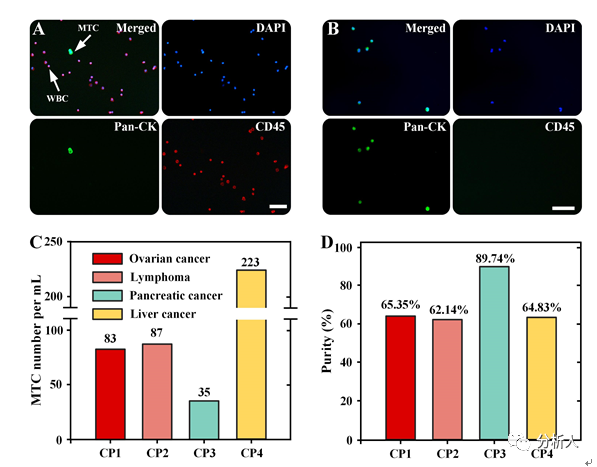
图3 恶性胸腹腔积液中恶性肿瘤细胞高纯度分选的临床试验结果
相比于使用单一技术的传统微流控装置,该研究工作结合了基于尺寸的被动分离技术和基于免疫磁珠的主动技术的优势,可以在高通量条件下精确地从尺寸相似的白细胞中分离稀有恶性肿瘤细胞。该装置有望提高大体积恶性胸腹腔积液中细胞学检查的灵敏度和效率。
审核编辑:刘清
- 相关推荐
- 热点推荐
- 微流控系统
-
Aigtek高电压放大器微流控细胞筛选测试2025-01-20 927
-
ATA-320功率放大器在免疫磁珠法分离细胞实验中的应用2024-09-25 1578
-
安泰ATA-7050高压放大器在微流控细胞分选中的应用2024-03-01 1399
-
惯性微流控器件的微制造方法2023-11-02 2232
-
利用微流控芯片高通量收集血液中的循环肿瘤细胞检测癌症2023-07-21 5590
-
利用惯性微流控技术实现微通道内非尺寸依赖的细胞可控三维聚焦2023-06-19 4046
-
宽带功率放大器基于微流控技术的细胞分选的应用2023-04-27 1281
-
综述:基于磁泳的微流控分离技术研究进展2022-12-27 2269
-
采用离心微流控芯片实现血液中白细胞的分离提取2022-10-31 4304
-
一种高效的微流控细胞芯片,通过快速筛选允许细胞实现病毒的分离和培养2022-06-07 4684
-
基于NI嵌入式控制器实现检测和分离循环肿瘤细胞研究2021-04-19 2998
-
光诱导介电泳系统与微流体技术结合开发高纯度细胞纯化分离设备2018-12-05 4707
-
微流控芯片细胞分析技术的分类及优点2018-10-10 12619
全部0条评论

快来发表一下你的评论吧 !

