

用于智能药物递送的可穿戴声学响应微针阵列
描述
在个性化医疗的需求中,便捷安全的微针给药技术在近些年快速发展,其能够极大地提升医疗体验,降低成本,已经被广泛应用于实践中。而不同场景往往需要不同的给药配置,特别是对于急性疾病,快速响应的给药具有重要意义,这也对传统基于溶解释放等被动式微针提出了挑战。
近日,厦门大学陈鹭剑教授与胡学佳助理教授提出了一种新型的主动药物递送机制,研究团队在声学与微结构相互作用机理研究的基础上,提出利用锆钛酸铅(PZT)在微针针尖诱导涡流,产生微泵效应,并通过贴片的集成设计,实现智能的按需药物释放。相关研究以“On-demand transdermal drug delivery platform based on wearable acoustic microneedle array”为题发表在Chemical Engineering Journal期刊上。
该研究提出的智能的声响应药物释放微针如图1所示,该可穿戴器件包括一个PZT驱动电路,PZT贴片和空心微针,并通过蓝牙与手机交互,通过预先设定程序或者实时调控,能够控制PZT产生声波信号,并驱动特殊设计的针尖尖端产生高频振动。这种振动在针尖产生了能量耗散并制造涡流效应,其能够将针内药物主动向外泵送。
而通过程序控制的声波信号强度与持续时间调制,能够实现较为精准的药物递送。如图2所示,该空心微针阵列由10 × 10个微针单元组成,利用3D打印工艺制造,每个单元高1000微米。扫描电子显微镜(SEM)图表明,打印的器件具有较高的精度,保证了针尖的锐度以及均一性(图2a),从而使得针尖可在声学驱动下产生较强的涡流效应。此外,对该打印的微针的性能测试也表明,该光敏树脂材料具有较高的强度,从而可以保证良好的刺入性能,且能避免体内折断风险。
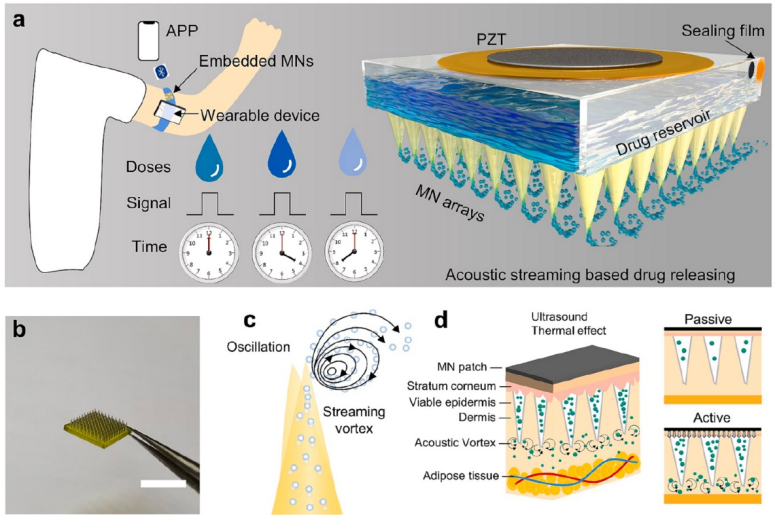
图1 声学响应智能微针示意图
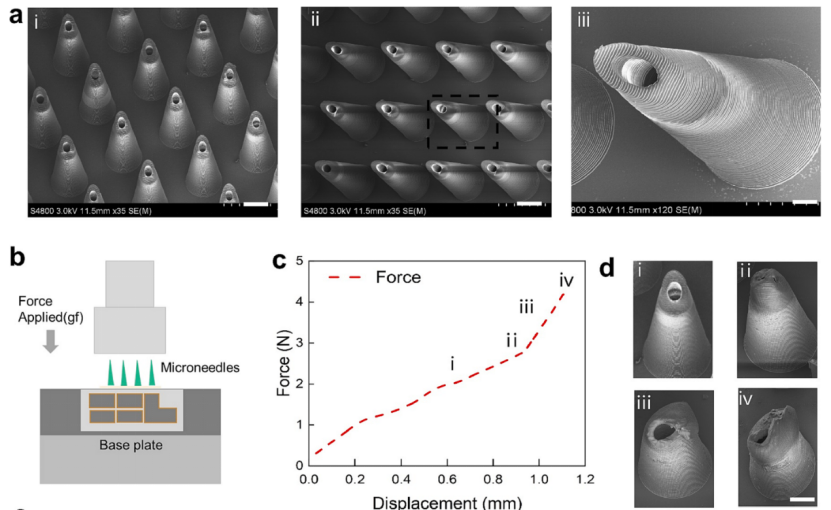
图2 3D打印的空心微针阵列:(a)微针阵列SEM图;(b)微针力学性能测试示意图;(c-d)微针单个针尖力学测试数据及对应微针形变图
随后,该研究通过有限元模拟以及染料模拟实验论证了该针尖涡流的微泵效应,模拟结果中箭头展示了流场分布,颜色图绘制了声场能量梯度,实验中声学信号设置为34 KHz,幅度为40 Vpp,实验与模拟结果能较好吻合。而为了更好地模拟在皮下的泵送效果,在图3h中,研究人员使用组织模拟凝胶验证药物注入效果,当声信号幅度设置在40 Vpp左右时,可以看到荧光药物能够快速在凝胶中释放并累积。
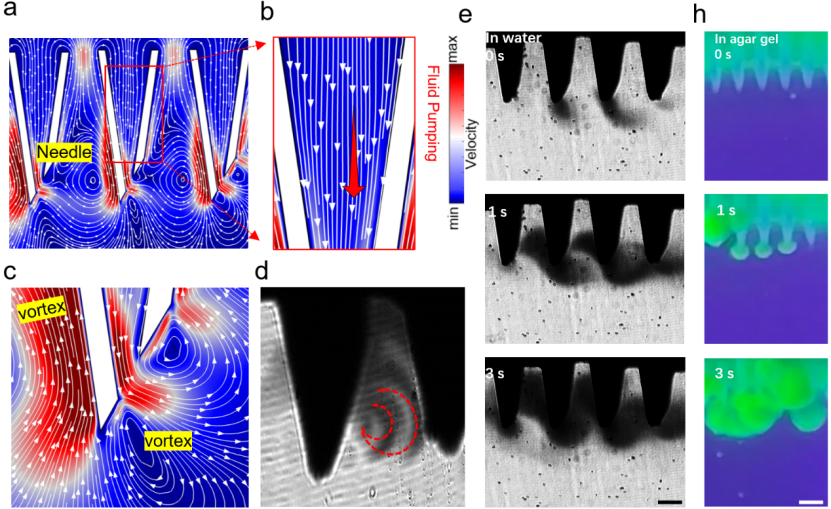
图3 声学响应的微针涡流效应模拟与实验结果:
(a-c)有限元模拟针尖涡流微泵效应,在34 Khz声波激励下,针尖结构附近产生两个涡流区域,并产生自内向外的相反涡流场,引导内部流体向外抽注;
(d-e)使用模拟药物验证声学激励的涡流与泵送效应;
(h)在凝胶中验证微针泵送能力 最后,研究团队论证了该器件应用于小鼠进行主动药物递送的潜力。微针中装载10%荧光素钠,通过预先设定的程序释放,并实时进行眼底荧光成像。荧光素钠作为眼底荧光素血管造影技术中常用的药物,当循环至眼底血管中时,能够发出被观察到的荧光,从而通过记录眼底荧光强度方便实时计算反应体内的药物浓度。图4a ~ 4c展示了该微针贴片在声信号下作用的热效应以及撤去微针后皮肤的恢复情况。而图4d ~ 4f则展示了在主动声波信号施加后眼底荧光的变化。研究结果表明,通过控制声波信号的时间与强度,能够较为精准的控制药物释放的时间以及药物注射量,从而满足不同的给药需求。
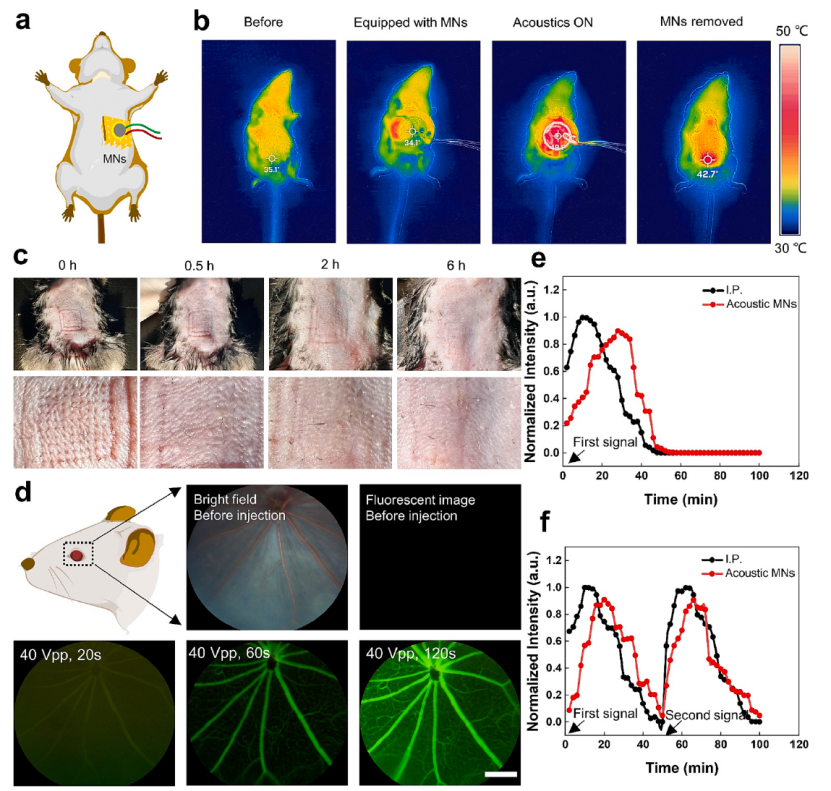
图4 (a)小鼠体内的声学主动药物递送;(b)微针贴片区域在声场信号施加情况下温度变化;(c)小鼠腹部微针针孔随着时间推移快速愈合;(d)使用微针注入荧光素钠药物,并记录的小鼠眼底荧光图;(e-f)基于微针的单次与多次药物注入情况下,眼底荧光随时间变化
综上所述,该智能微针通过声波耦合驱动技术,提供了一种精准而有效的药物递送策略,声波相比于其他响应技术具有易于集成、低成本且生物亲和的优势,方便进行可穿戴设计和智能化控制。此外针尖的声波空化以及声热效应具有促进药物在组织内吸收的潜力。这些独特优势也让该技术在个性化医疗场景下展现出较大的应用前景。
审核编辑:刘清
-
“智能+可穿戴”,戒烟新思路2015-11-16 3759
-
智能服装拯救可穿戴设备“冷市场”?2018-11-19 3288
-
豆腐成为药物递送微载体2019-02-02 2996
-
大电流弹片微针模组应用于智能可穿戴设备性能测试2020-09-06 1505
-
一种基于介孔微针离子泳的集成可穿戴诊疗一体化系统2021-06-15 3011
-
一种近红外光响应的脂质体纳米药物递送平台开发2023-02-06 2478
-
用于药物输送的溶解微针的性能增强方法研究进展2023-02-23 2390
-
可穿戴自供电载药电子微针系统,用于炎症性皮肤疾病治疗2023-04-04 3130
-
基于电沉积法制备的纳米微针实现药物在原代细胞内的有效递送2023-04-18 2558
-
基于三维组装微针离子传感器的生理离子波动透皮监测可穿戴系统2023-08-21 1998
-
用于微纳机器人多级磁控递送研究的体外测试平台2024-01-13 2016
-
基于医用胶带的可溶解倒钩微针,可提高皮肤附着力和药物递送效率2024-04-20 2186
-
半侵入式"可穿戴诊所"——微针技术的创新应用2024-11-09 38174
全部0条评论

快来发表一下你的评论吧 !

