

阴离子-溶剂相互作用的见解
描述
引言
全球能源转型将推动电池在更广泛的应用和更恶劣的条件下运行。电动汽车或大规模储能技术迫切需要锂金属电池的温度滥用耐受性,尤其是在低温的极端条件下。商用碳酸盐基电解质无法在低于-20℃的低温下运行,面临冻结问题和由此导致的离子通过界面层的缓慢传输。电解质是在超低温(例如,低于-20°C)下实现可逆锂沉积/剥离的关键。
合理的电解质设计主要集中在调整Li+溶剂化结构上,因为溶剂化结构不仅影响Li+在本体电解质中的传输,而且还会改变固体电解质界面(SEI)组成。Li+溶剂化结构已在实验和理论上被广泛研究。最近,阴离子参与的溶剂化结构也被报道,它也可以改变SEI的形成和Li+的去溶剂化动力学。然而,即使在最简单的单盐、单溶剂电解质系统中,阴离子-溶剂相互作用仍然没有完全理解。阴离子-溶剂相互作用可以有几个好处。首先,无溶剂相互作用促进了锂盐的离解,导致了更高的离子电导率。其次,更强的阴离子-溶剂相互作用限制了阴离子的迁移率,并提高了Li+的转移数(t+)。最后,阴离子-溶剂相互作用抑制了溶剂还原,并促进了阴离子衍生的富含无机物的SEI的形成,这提高了Li沉积/剥离库仑效率(CE)。
正文部分
01 成果简介
近日,马里兰大学的王春生教授,Jijian Xu与香港城市大学的Anh T. Ngo等人在双(3-氟丙基)醚(BFPE)的弱Li+阳离子溶剂化溶剂中系统地检测了双(三氟甲磺酰)亚胺(TFSI)、双(氟磺酰)亚胺(FSI)和衍生的不对称(氟磺酰)(三氟甲磺酰)亚胺(FTFSI)的三种阴离子。原位液体二次离子质谱分析表明,FTFSI-和FSI-阴离子与BFPE 溶剂相关,同时检测到微弱的TFSI-/BFPE簇信号。分子模型进一步揭示阴离子-溶剂相互作用伴随着类氢键相互作用的形成。阴离子溶剂化增强了Li+阳离子转移数并减少了固体电解质界面中的有机成分,从而将-30℃低温下的Li沉积/脱锂库仑效率从TFSI基电解质中的42.4%提高到1.5 M LiFTFSI 中的98.7%和LiFSI-BFPE 电解质中的97.9%。阴离子-溶剂相互作用,特别是不对称阴离子溶剂化也加速了Li+去溶剂化动力学。具有强阴离子-溶剂相互作用的1.5 M LiFTFSI-BFPE电解质使LiNi0.8Mn0.1Co0.1O2(NMC811)||Li (20 μm) 全电池即使在-40 °C下也具有稳定的循环性能,保留了超过92% 的初始性能容量(115 mAh/g,100次循环后)。阴离子-溶剂相互作用的见解使我们能够合理设计锂金属电池及其他电池的电解质,以实现高性能。该研究以题目为“Revealing the Anion-Solvent Interaction for Ultralow Temperature Lithium Metal Batteries”的论文发表在国际顶级期刊《Advanced Materials》。
02 图文导读
理化性质和溶剂化结构
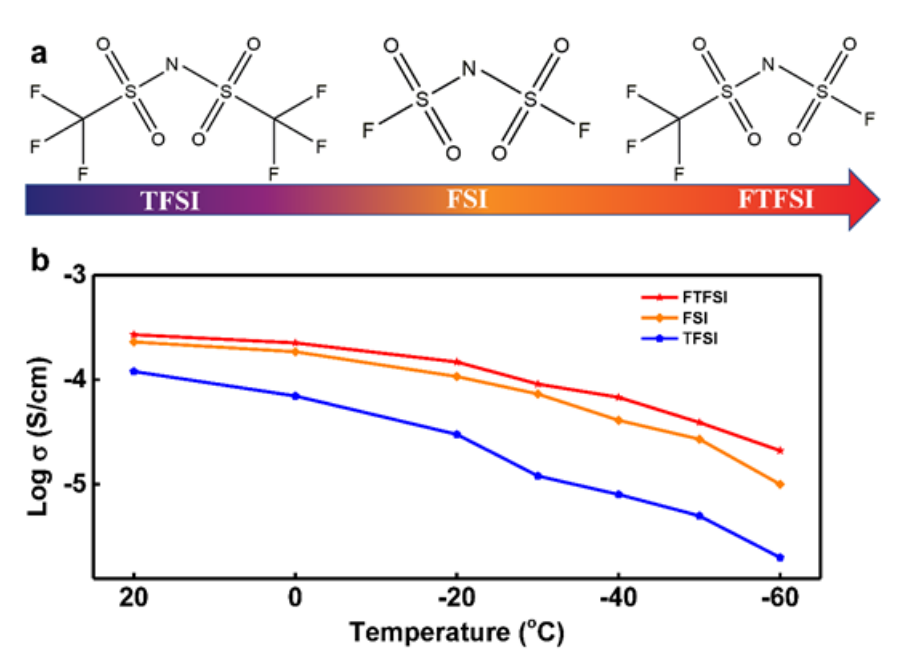
【图1】电解质的性质。(a)TFSI,FSI,FTFSI阴离子的化学结构。(b)LiTFSI、LiFSI、LiFTFSI-BFPE电解质电导率的温度依赖性。
为了研究阴离子-溶剂相互作用,系统地检测了三种具有代表性的阴离子,即双(三氟甲磺酰基)酰亚胺(TFSI)、双(氟磺酰基)亚胺(FSI)和不对称(氟磺酰)(三氟甲烷磺酰基)酰胺(FTFSI),它们对Li+-FTFSI、Li+-TFSI和Li+-FSI具有相似的离解能。其他不对称阴离子的阴离子溶剂化作用还有待探索。如图1a所示,FTFSI阴离子是TFSI和FSI阴离子之间的不对称杂化物。由于其不对称性,在-60和+20°C之间的整个温度范围内,LiFTFSI BFPE电解质的锂离子电导率高于LiFSI或LiTFSI BFPE电解液(图1b)。在20℃下,含有LiFTFSI和LiFSI的电解质具有相当的离子电导率,这与文献中报道的结果一致。例如,当温度降至-60°C时,与LiFSI BFPE电解质的0.010 mS/cm相比,含LiFTFSI的电解质具有更高的离子电导率,为0.021 mS/cm,更不用说LiTFSI BFPE电解液了。电导率的具体值列于表S1中。电导率的提高可能源于阴离子-溶剂的相互作用,这有助于盐的离解。使用扫描量热法(DSC)研究了含有LiTFSI、LiFSI和LiFTFSI的电解质在BFPE溶剂中的热行为,表明没有结晶或熔融(图S1)。请注意LiFTFSI在各种锂盐中具有最低的熔点,如表S2所示,尽管发现Li+-FTFSI、Li+-TFSI和Li+-FSI的离解能相似。
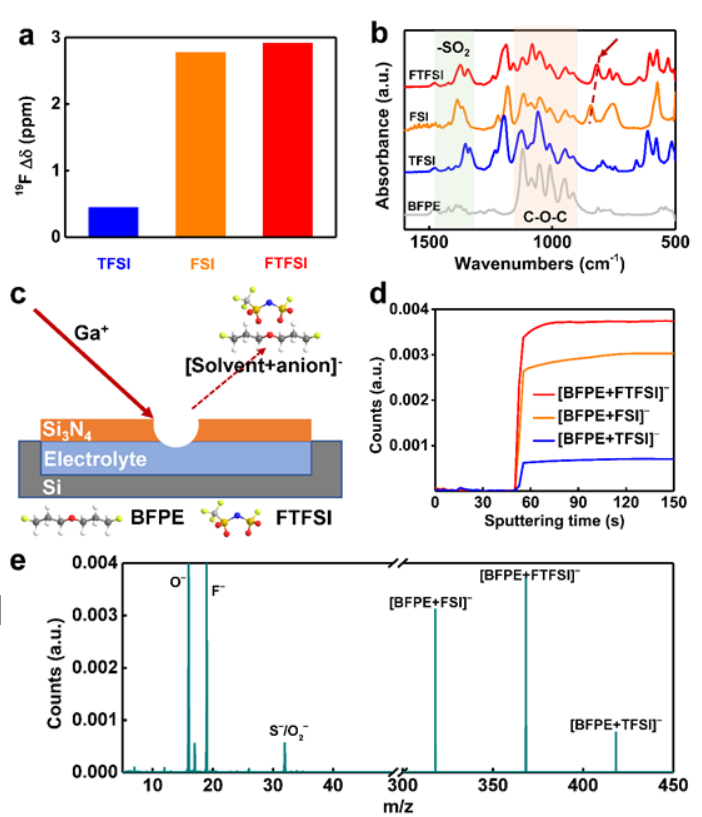
【图 2】阴离子-溶剂相互作用。(a)Δδ(BFPE溶剂的19F NMR光谱)在LiTFSI、LiFSI、LiFTFSI-BFPE电解质中的总结。(b) 电解质和裸BFPE溶剂的ATR-FTIR光谱。绿色区域:-SO2振动,橙色区域:C-O-C拉伸。(c) 通过硅支撑栅与氮化硅膜组装的原位液体SIMS电池的示意图设置。然后形成直径约为1μm的孔并装袋在原位SIMS分析期间通过聚焦离子分析。(d)0.5M LiFSI+0.5M LiFTFSI+0.50M LiTFSI在负离子模式下在BFPE电解质中的深度分布和(e)质谱。在大约50s的时间内,Si3N4膜被穿透并暴露出电池内的电解质。
使用不同电解质的19F NMR信号鉴定了FTFSI阴离子和BFPE溶剂之间的强相互作用,其显示了TFSI-BFPE<FSI-BFPE<FTFSI-BFPE序列的向上场移动(图2a)。使用衰减全反射傅立叶变换红外光谱(ATR-FTIR)进一步研究了阴离子的作用。如图2b所示,游离BFPE中C-O-C键的特征峰位于1120、1052、1008和949 cm−1处(灰线)。同时,在1300-1400 cm−1范围内观察到的双峰被指定为锂盐的-SO2拉伸。有趣的是,FTFSI-BFPE和FSI-BFPE电解质在830 cm−1附近出现了新的峰值,这些峰值由红色虚线和箭头勾勒,表明无溶剂相互作用。阴离子-溶剂相互作用限制了阴离子的迁移率,并提高了Li+的转移数(t+)。因此,如图S2所示,获得了高t+(FTFSI-BFPE为0.86,FSI-BF聚乙烯为0.83)。
利用原位液体二次离子质谱法(SIMS)研究了阴离子与溶剂的相互作用。FTFSI、FSI和TFSI的所有三种阴离子都以相同浓度0.5 M溶解在BFPE溶剂中。如图2c所示,通过钻一个小孔来进行液体电解质的操作数分析是可行的,这样探测主光束就可以与电解质相互作用。代表性[溶剂阴离子]簇的深度分布如图2d所示。在Si3N4膜溅射(~50s)后立即检测到[BFPE-FSI]−、[BFPE-FPI]−和[BFPE-TFSI]−信号,表明阴离子与BFPE溶剂形成缔合。峰的强度从[BFPE-TFSI]−到[BFPE-FSI]−再到[BFPE-FTFSI]−增加,表明阴离子与BFPE溶剂之间的相互作用变得越来越强。在100秒时,当信号变得相对稳定时,质谱被收回,如图2e所示。O−和F−峰在光谱中占主导地位,可能来自受损的锂盐和BFPE溶剂。更重要的是,清楚地观察到溶剂化阴离子峰,即[BFPE-TFSI]−(m/z=418)、[BFPE-FSI]−(m/z=318)和[BFPE-FTFSI]–(m/z=668)。[BFPE-FSI]−的强度高于[BFPE-FPSI]−,两者几乎都比[BFPE-TFSI]−高1个数量级,证实了更强的BFPE-FTFSI相互作用。
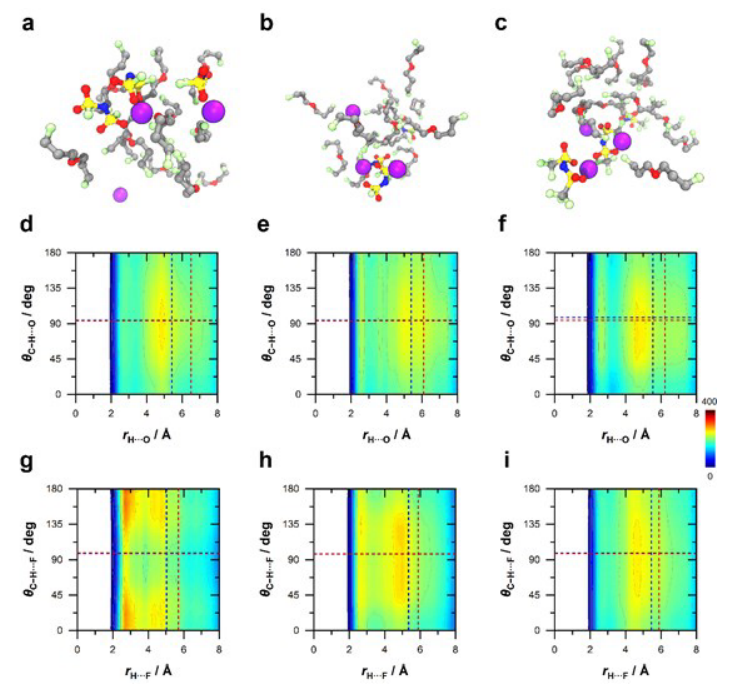
【图3】通过模拟的阴离子-溶剂相互作用。(a-c)通过AIMD模拟在298K下平衡的1.5M LiFSI-(a)、LiFTFSI-和LiTFSI基(c)BFPE电解质的快照。元素的颜色编码:灰色─C、 红色─ O、 石灰─ F、 黄色─ S、 蓝色─ N和紫色─Li原子(为了清楚起见,H原子被隐藏起来)。(d-i)溶剂分子之间的离子-分子相互作用,包括基于BFPE和FSI−(d,g)、FTFSI−,在298K下使用AIMD模拟分析的基于1.5M LiFSI/FTFSI/TFSI的BFPE系统中。对于虚线垂直线和水平线分别代表平均氢键距离和角度,使用经典MD模拟在298(红色)和233 K(蓝色)下分析。
分子建模,特别是从头算(AIMD)和经典分子动力学(MD),被用来理解离子分子水平上的阴离子-溶剂相互作用。LiFSI-BFPE(图3a)、LiFTFSI-BF聚乙烯(图3b)和LiTFSI-BFPE的代表性快照(图3c)表明,BFPE溶剂主要由与Li+阳离子有关的F原子配位。详细的Li配位统计数据表明,Li配位能力的顺序为TFSI−>FTFSI−>FSI−(图S3)。除了Li+阳离子溶剂化,还观察到阴离子溶剂化。对AIMD模拟的深入分析证实,FSI−和FTFSI−阴离子与溶剂具有高度相互作用。如图3g-i所示,阴离子-溶剂相互作用的强度伴随着H和F之间形成类似H键的相互作用。更有趣的是,发现溶剂和阴离子之间的H∙∙F和H∙・∙O相互作用的温度效应非常明显(图3d-i)。
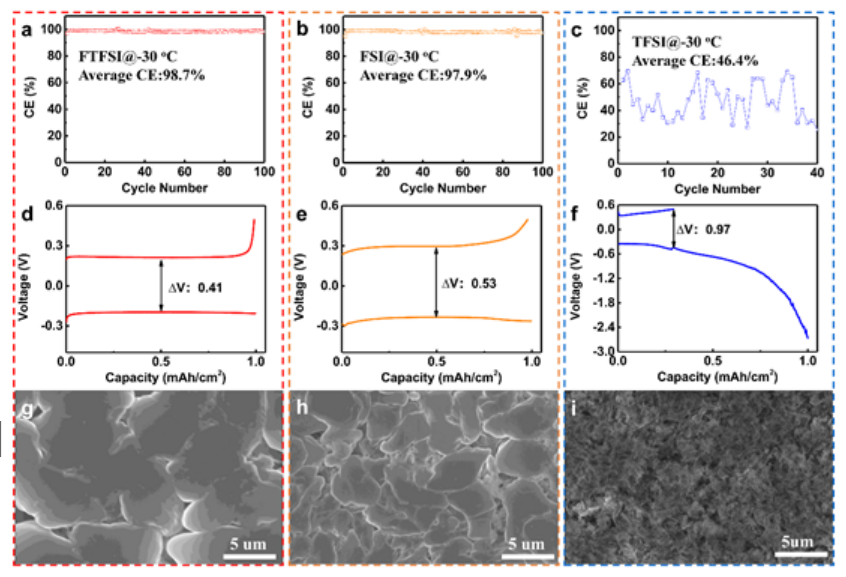
【图4】在-30摄氏度的超低温下,Li金属的沉积/剥离效率。(a-c)库仑效率(CE)与循环次数的关系,以及(d-f)分别使用LiFTFSI、LiFSI和LiTFSI-BFPE电解质在0.25mA/ cm2的电流密度下Li||Cu电池的第10次循环的选定电压分布。(g-i)在不同电解质中在铜箔上沉积的Li的相应SEM图像。
阴离子-溶剂相互作用已通过原位SIMS直接证实。然而,与模拟表明的室温下的Li+-溶剂相互作用相比,它仍然相对较弱。20-30 kcal mol−1范围内的典型阴离子溶剂化能小于~32 kcal mol−1的相应Li+溶剂化能。在室温下,阴离子-溶剂相互作用对锂金属负极电化学性能的影响很小。如图S4所示,LiFTFSI-BFPE电解质中的Li沉积/剥离循环性能略好于或类似于LiFSI-BFPE-电解质,但两种电解质中的Li-CE和过电位都比LiTFSI-BFPE好得多。由于离子传输缓慢,锂金属负极在低温下的可逆剥离和沉积极具挑战性,因此阴离子-溶剂相互作用的益处大大增强。在-30℃下,电流密度为0.25 mA/cm2时,在Cu电极上镀/剥离Li金属的循环性能如图4a-c所示。LiFTFSI BFPE电解质的CE在第一次循环中为96.8%(图4a),在3次循环内迅速升至99%以上,显示出优异的循环性能,在100次循环中具有98.7%的高平均CE。LiFSI BFPE电解质比LiFTFSI BF聚乙烯电解质稍差,显示出97.9%的略低的平均CE(图4b)。与此形成鲜明对比的是,LiTFSI-BFPE电解质的平均CE急剧下降至46.4%,表现出较差的循环性能(<40次循环,图4c)。此外,基于改进的CE测量方案,在25、0、-20、-30℃下,使用LiFTFSI BFPE电解质的CE测试为99.3%、99.2%、99.1%、98.8%(图S5)。
此外,具有LiFTFSI BFPE电解质的Li||Cu电池具有最低的过电位,410 mV(LiFTFSI-BFPE,图4d)<530 mV(LiFSI-BF聚乙烯,图4e)<<970 mV(LiTFSI-BFPE)。在LiFTFSI BFPE电解质中镀/脱锂的快速反应动力学归因于LiFTFSI-BFPE电解质的高离子电导率和富含LiF的SEI。
为了揭示阴离子-溶剂相互作用在决定锂金属电池电化学性能中的作用,对循环电极进行了扫描电子显微镜(SEM)和X射线光电子能谱(XPS)。图4 g-i分别显示了LiFTFSI、LiFSI和LiTFSI-BFPE电解质在-30℃下在铜箔上沉积的锂金属的形态。对于LiFTSI-BFPE和LiFSI-BFPE电解质,沉积的锂的表面是平坦的。LiFTFSI-BFPE中的Li颗粒尺寸为~10μm(图4g),LiFSI-BFPE-电解质中的Li粒径为~5μm。相反,在LiTFSI BFPE电解质中沉积的Li中观察到大量针状和多孔树枝状Li(图4i)。SEM图像证明,LiFTFSI-BFPE和LiFSI-BFPE-电解质有利于形成更致密、更致密的Li沉积物,对应于Li沉积/剥离的更高CE。
进一步对铜上的Li沉积物进行XPS分析,以研究SEI层的性质。图S6总结了在三种电解质中形成的SEI层的组成,以及作为不同蚀刻时间的函数的详细C1s、O1s和F1s光谱。根据结果,在LiFTFSI-BFPE和LiFSI-BFPE电解质中形成的SEI都是富含无机物的,其中LiF和Li2CO3是主要物种,而在LiTFSI-BFPE电解质中生成的SEI含有更多的有机物。据报道,在基于LiTFSI的电解质中形成的SEI层主要以溶剂还原为主,产生更多的有机物。此外,TFSI阴离子中的C-F键比FSI和FTSSI阴离子中的S-F键更不容易被还原,这解释了为什么在源自LiTFSI-BFPE电解质的SEI层上只能检测到少量的LiF。模拟结果验证了FTFSI阴离子促进更高的分解速率:FTFSI−>TFSI−>FSI−,导致在BFPE溶剂存在下形成Li2O和LiF等无机产物(图S7)。
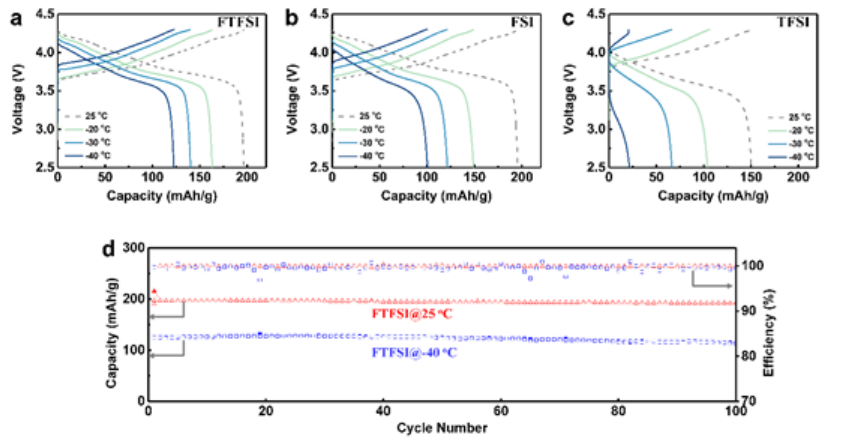
【图5】全电池的电化学性能。NMC811(2.0 mAh/ cm2)的典型电压分布||Li(20μm,2×在(a)LiFTFSI BFPE、(b)LiFSI BF聚乙烯和(c)LiTFSI BFPE的电解质中,在0.1 C,用于在各种温度下充电/放电。(d)NMC811||Li电池在LiFTFSI_BFPE电解质中25℃和-40℃的长循环性能。
LiFTFSI、LiFSI和LiTFSI-BFPE电解质的负极稳定性如图S8a所示,显示4.5 V时<0.005 mA/ cm2的低负极电流对所有三种电解质的Li/ Li+。更严格的浮动测试证实了LiFTFSI BFPE电解质在高电压下的高稳定性(图S8b),表明其有能力支持高电压正极,如LiNi0.8Mn0.1Co0.1O2(NMC811)。因此,NMC811(2.0 mAh/cm2)||Li(20μm,2×过量)的全电池进行组装以说明在各种温度下的阴离子溶剂效应。如图5a所示,当在25、-20、-30和-40℃下充电和放电时,使用LiFTFSI BFPE电解质的电池提供196、163、140和123 mAh/g(基于正极)。LiFSI BFPE电解质中的容量保持率略低,如图5b所示,在25、-20、-30和-40℃时的输出容量分别为196、149、121和101 mAh/g。在LiTFSI BFPE电解质的情况下,观察到显著的欧姆极化,容量显著降低(图5c),即与离子导电性结果和不均匀的锂沉积相一致。LiFTSI-BFPE和LiFSI-BFPE电解质之间低温容量保持率的相对增加可能是由于阴离子-溶剂相互作用的增加。
如图5d所示,LiFTFSI-BFPE电解质可以在25℃时2.5-4.3 V的电压范围内完全支持NMC811||Li电池的稳定充电/放电。即使在-40℃的超低温下,它在100次循环中仍能保持92%以上的初始容量(图5d)。更令人印象深刻的是,NMC811||Li电池能够在-50和-60℃的更低温度下充电/放电。如图S9所示,LiFTFSI BFPE电解质在-50℃和-60℃下分别可提供97.6 mAh/g和39.7 mAh/g的充电容量。这些全电池结果与Li||Cu效率和原位SIMS结果一致,表明具有强阴离子-溶剂相互作用的电解质适用于低温锂金属电池。
总结和展望
综上所述,通过研究了由溶解在氟化BFPE溶剂中的不同锂盐(LiFTFSI、LiFSI和LiTFSI)组成的电解质,以探测阴离子-溶剂相互作用的影响。通过原位SIMS,直接观察到[BFPE-TFSI]−至[BFPE-FSI]−,验证了阴离子与溶剂之间的相互作用。如分子建模所示,这种阴离子溶剂化是由溶剂和阴离子之间形成的H∙∙F和H∙・∙O相互作用引起的。研究发现,只有具有相对较强的阴离子-溶剂相互作用的电解质才能提供可逆的锂沉积/剥离,在-30℃时平均CE接近99%。此外,2.0 mAh/cm2NMC811||Li全电池具有2×过量的锂使用具有强阴离子-溶剂相互作用的1.5 M LiFTFSI BFPE电解质在-40℃的超低温下实现了100次循环,容量衰减最小,同时保持了63%的室温容量。这项工作证明阴离子-溶剂相互作用可能是锂金属电池及其他电池合理电解质设计的另一个未探索的领域。
审核编辑:刘清
-
离子束与材料的相互作用2024-12-19 1508
-
OptiSystem应用:EDFA中离子-离子相互作用效应2024-12-17 681
-
什么是自相互作用呢?中微子之间超越标准模型的相互作用,2023-08-30 2218
-
弱相互作用对有机光电性质调控的理论研究2023-07-31 2119
-
工程微生物相互作用的工具包2022-12-13 875
-
量子混沌:相互作用如何影响量子多体系统的局域化?2022-10-27 1693
-
阴离子实现无枝晶长循环锌离子电池的设计2022-09-28 1763
-
电流和磁场的相互作用2021-08-27 1744
-
剖析材料性质之间的相互作用对电池性能的影响2021-06-02 5579
-
磁铁相互作用的基本原理2021-05-26 5333
-
什么是电磁相互作用2020-01-31 6359
-
病毒传播与级联故障相互作用过程的研究2018-01-30 1028
-
弹性轮与地面相互作用建模及仿真研究2009-12-02 1827
-
大气中固体燃烧等离子体与微波相互作用的实验研究2009-10-26 664
全部0条评论

快来发表一下你的评论吧 !

