

基于结构微流体创新的谱系细胞单克隆自动化获取策略
描述
近期,中国科学院广州健康院张骁研究员团队提出一种基于结构微流体创新的谱系细胞单克隆自动化获取策略,以无标记、无酶活反应参与、非侵入式的方式,在体细胞重编程过程出现的复杂谱系中实现了对特定谱系的单克隆性细胞的自动化获取,并研发出基于结构微流体的细胞单克隆获取整机技术(图1)。
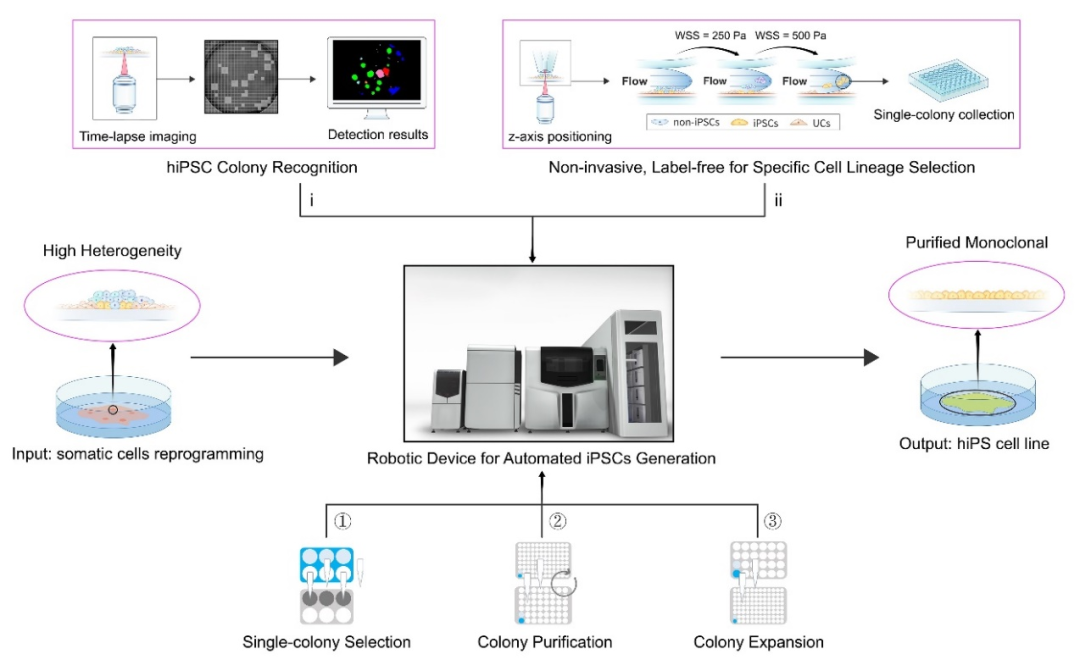
图1 自动化谱系细胞培养/及单克隆获取整机技术概要
该原创性策略被部署于广州健康院前期自主研发的自动化干细胞诱导培养装备,提高了人诱导多能干细胞(hiPSCs)单克隆的获取效率与纯度,提升了系统鲁棒性(robustness)及缩短了体细胞重编程后持续纯化hiPSCs(sub-cloning)的建系周期。相关研究成果以“Selecting Monoclonal Cell Lineages from Somatic Reprogramming Using Robotic-Based Spatial-Restricting Structured Flow”为题发表在Research期刊上。
尽管谱系节点细胞在再生医学中的应用前景广阔,但基于传统人为操作获取谱系细胞单克隆的方法需要消耗大量时间和劳动力,获取效率通常比较低,且无法以无标记、无酶活反应参与、非侵入式的方式获取谱系细胞单克隆。此外,利用微流控技术虽然可以提高谱系细胞收获效率,但这种方法无法获得基于谱系特异性的细胞单克隆。因此,发展能够高效富集谱系细胞单克隆的自动化整机技术显得尤为重要。
细胞-细胞/细胞-基质之间的粘附力变化是谱系细胞命运变化中的一个关键环节,通过调节流体剪切力大小可以实现以无标记、无酶活反应参与、非侵入式的方式分离/选择具有不同粘附特性的谱系细胞单克隆,这种策略可以应用于基于细胞类型特异性的单克隆工程化获取。张骁研究员团队前期研究中利用AI算法实现了对重编程细胞单克隆的识别和预测,并将AI技术应用于生命科学仪器整机技术研究。该团队在前期依托中国科学院广州健康院研发出了具有自主知识产权的自动化干细胞诱导培养设备,凭借这些研究背景,结合整机技术和分子组织生物学认知以及空间结构微流体操控技术,该团队研发了自动化整机,通过以编程的方式精确操控结构微流体,并产生具有空间定位的流体剪切力,实现在复杂高异质性的细胞环境中通过流体变化选择特定的细胞类型,并实现谱系细胞单克隆的特异性获取。
通过分析不同体细胞重编程过程中细胞粘附分子的表达水平变化情况,研究人员发现细胞多能性基因的表达水平与Integrin家族基因的表达量呈负相关性,而与Cadherin家族基因的表达量呈正相关性。由于Integrins是细胞与细胞外基质(ECM)相互作用的关键粘附分子,而Cadherins是细胞与细胞之间相互连接的重要分子,这意味着体细胞重编程转变成多能干细胞这一谱系命运变化过程中,细胞与ECM的连接可能会减弱,而细胞与细胞之间的连接可能会增强。为了证明这个假设,张骁研究员提出进一步通过设计平行平板流动腔实验和免疫荧光实验来进行验证。实验结果与预期假设相一致,并且平行平板流动腔实验初步证明了流体剪切力有望成为分离/选择特定类型粘附细胞的好技术路径(图2)。
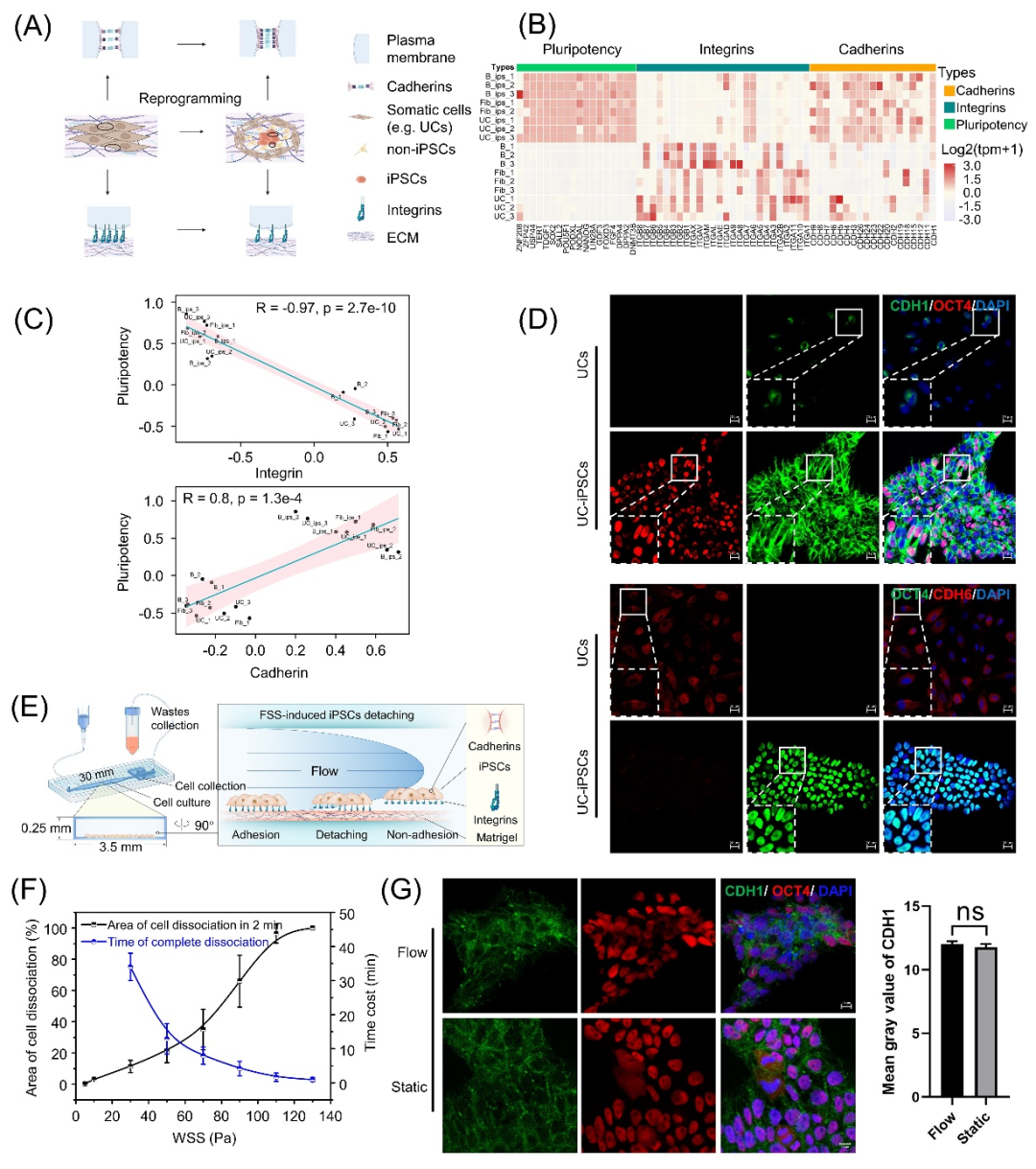
图2 体细胞重编程中细胞谱系命运变化伴随着粘附分子表达的改变,流体剪应力可用于分离粘附细胞
随后,论文第一作者陈学平博士基于流体动力学原理设计了可以产生局部结构微流体的细胞获取微型挑针结构(PTMS),团队克服了流场效果与多曲面加工实现的难题,反复校验加工结构,最终基于PTMS产生的结构微流体(PTMS-FLOW)实现了对基于空间限位谱系细胞的特异性挑取。此外,研究证明了PTMS-FLOW可根据流速变化在Z轴-h0的为常量的条件下,应对不同细胞类型的粘附力差异,实现以无标记、无酶活反应参与、非侵入式、和非接触的方式对不同谱系细胞进行特异性的选择。该研究证明了结构微流体是作为分离/选择特定谱系类型粘附细胞的可自动化的技术路径,为后续进一步研究谱系细胞单克隆的自动化获取提供了理论基础(图3)。
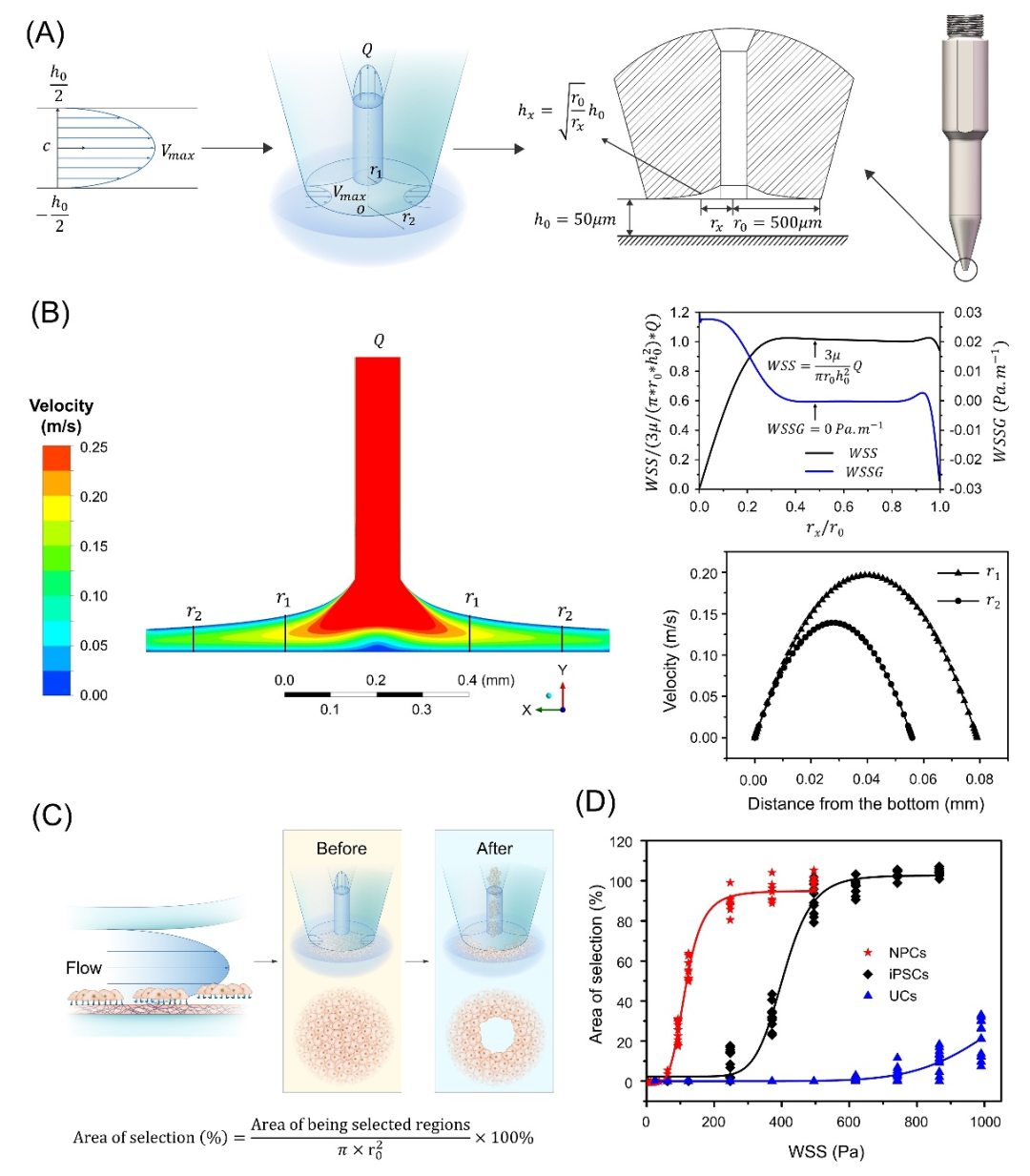
图3 基于空间定位的结构微流体研究不同谱系细胞的粘附分离作用
为了将上述策略应用于对体细胞重编程过程中特定谱系的细胞的自动化获取,研究团队通过克服机械模块控制和精准调度的难题,结合细胞光学成像和自适应算法,实现精准操控微结构的功能底部与细胞单克隆之间的Z轴间距和水平位移,从而确保精准操控PTMS-FLOW作用于单克隆性的谱系细胞上,以此实现在体细胞重编程过程出现的复杂谱系中快速获取hiPSCs细胞单克隆的目标(图4)。

图4 研发自动化谱系细胞培养/及单克隆获取整机技术
此外,研究团队借助自动化整机技术的精确的流体操控能力,设计了一种双挑模式(Dual Run Selection),通过使用两次不同强度的剪切流体分别获取不同类型粘附特性的谱系细胞,实现了对特定空间位置的hiPSCs谱系细胞单克隆的特异性选择(图5),并能为下游hiPSCs实现特异性扩增提供纯化(sub-cloning)能力。
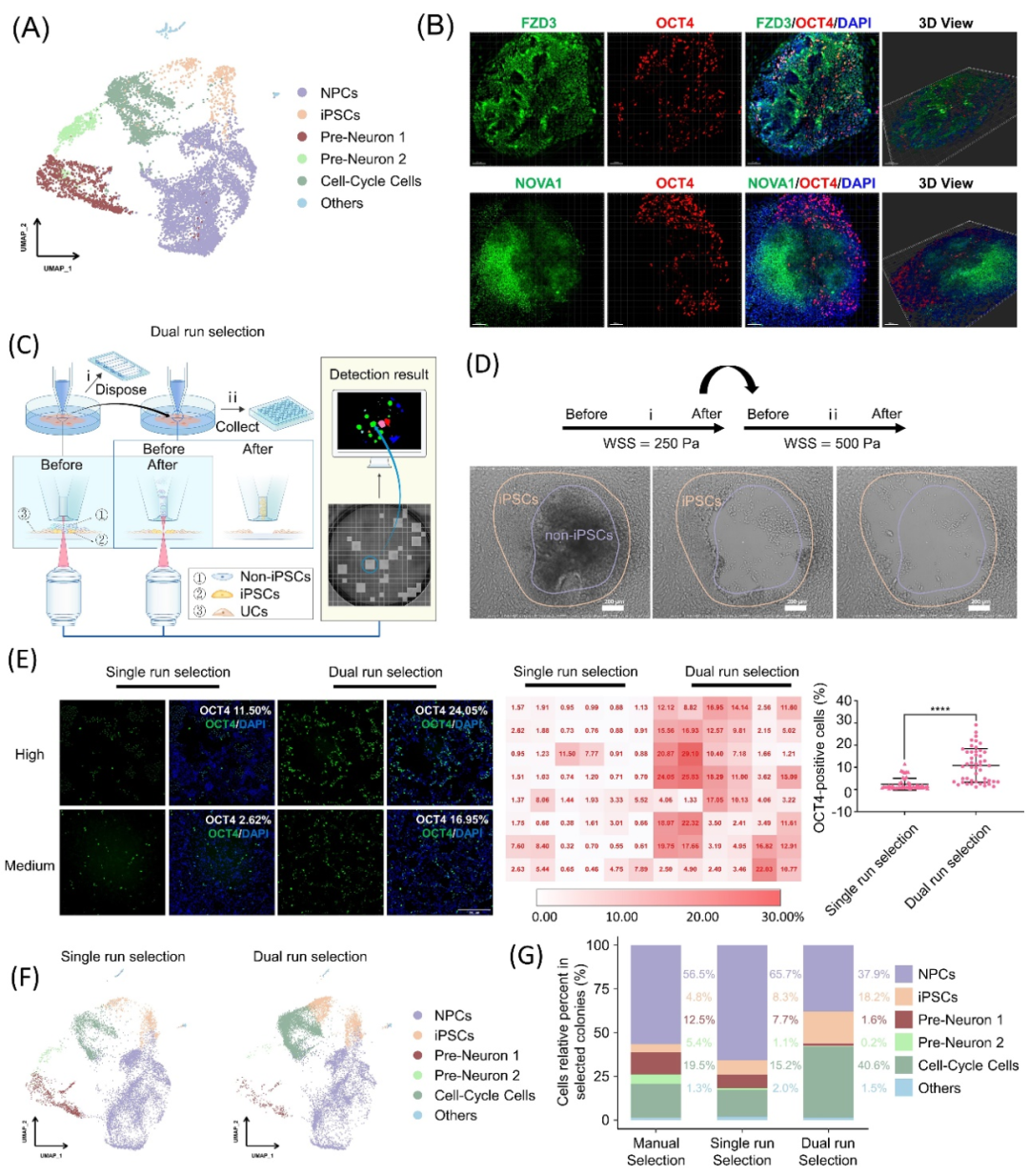
图5 基于谱系细胞粘附力的差异,应用PTMS-FLOW实现了对重编程多能干细胞单克隆的选择
综上所述,研究团队提出一种基于微型挑针结构介导的PTMS-FLOW实现了以无标记、无酶活反应参与、和非侵入式的方式快速获取谱系细胞单克隆的目标,并研发出具有自主知识产权的谱系细胞单克隆自动化获取的整机技术。该整机技术通过大幅减少谱系细胞生成过程中的时间成本,以及人工操作量,使得谱系细胞获取和培养起来更简单。该研究为自动化生产特定谱系细胞用于临床干预提供了新的技术方案,并为再生医学基础研究提供更多自动化获取谱系细胞的工具,从而从技术手段和方法学方面促进再生医学领域的基础研究和应用落地。
论文链接:
https://doi.org/10.34133/research.0338
- 相关推荐
- 热点推荐
- ai技术
-
物联网怎么普及工业自动化2016-03-16 5064
-
配电自动化系统主要由什么组成?有哪些特点?2023-04-10 2029
-
细胞融合与单克隆抗体2009-02-17 752
-
基于硅结构的微流体控制系统2009-07-11 478
-
基于免疫单克隆算法的RBF神经网络优化2009-12-29 846
-
基于软件代码演化信息的克隆谱系提取方法2017-12-08 1409
-
基于版本间克隆映射的演化模式识别及谱系构建2017-12-15 700
-
软件多版本中自动提取克隆谱系2018-01-13 834
-
微流体重编程以实现人诱导多能干细胞的多能性2019-03-25 3653
-
国卫院研发新微流体技术,抓取细胞速度快4倍2019-06-18 3967
-
单克隆抗体是否能转化应用于临床?2020-06-05 3477
-
工厂自动化结构及系统介绍2023-07-31 715
-
用于单细胞谱系追踪图像引导的微流控系统2023-08-18 2251
-
电磁阀:现代工业自动化与流体控制的精密执行者2025-09-25 1773
全部0条评论

快来发表一下你的评论吧 !

