

两只克隆猴诞生:癌症有望治愈,世界生命科学的重大突破
医疗电子
描述
两只克隆猴诞生!邂逅中中和华华,这是世界上第一批利用克隆羊多利技术成功克隆的猴子。两只猕猴出生不到10周,目前非常健康。这也是世界生命科学的重大突破。
它们的“故事”登上国际权威学术期刊《细胞》封面,这意味着中国科学家成功突破了现有技术无法克隆灵长类动物的世界难题。
雌性长尾猕猴代表着一个技术上的里程碑。它代表着能够创造出可定制和基因一致的猴子种群,从而加速治疗帕金森、阿尔茨海默病和癌症等疾病。但这一突破将不可避免地引发人们的担忧:克隆人类比以往任何时候都更加接近。
克隆猴子的中国团队说,这些猴子拥有如此巨大的潜力,因为它们都遗传了完全相同的遗传物质。
这将使科学家能够调整猴子与人类疾病相关的基因,然后监测这些变化如何改变动物的生物学特性,将其与除了改变之外基因相同的动物进行比较。研究小组称,这可以加速寻找这些疾病中出现错误的基因和过程,以及纠正它们的方法。
虽然已经有23种哺乳动物被克隆出来,包括猪,猫,狗,老鼠和牛等,但一直没有克服与人类最相近的非人灵长类动物克隆的难题。科学家曾普遍认为现有技术无法克隆灵长类动物。
2000年,研究人员首次克隆了猴子,但是通过在受精后分裂胚胎,基本上只产生了一个基因相同的双胞胎。此方法只能用于创造最多4种相同的动物。
现在,上海中国科学院神经科学研究所的孙强和他同事调整了用于克隆多利羊的技术,创造了一个理论上无限的克隆数量。
癌症有望治愈?两只克隆猴诞生
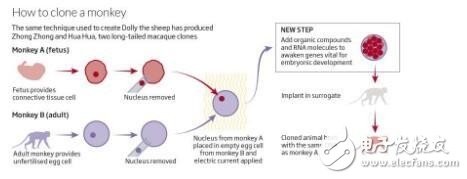
称之为体细胞核移植,该方法涉及从供体卵细胞中去除细胞核,并将其替换为从另一个动物的细胞中取出的细胞核。
电流被用来欺骗卵子,认为它已经受精,并开始发育成早期胚胎。当植入到替代母亲的子宫中时,胚胎将生长为捐献细胞核的动物副本(见图)。
以前在猴子中这样做的尝试从未突破被称为囊胚的早期胚胎阶段。
孙强和他的同事们进一步研究了两种新的营养成分和生长因子,这些因素帮助克隆胚胎在被植入替代品之前生长。这些成分——信使RNA和一种叫曲古抑菌素A的化合物——唤醒了至少2000个基因,这些基因对胚胎发育的各个阶段至关重要,使发育得以继续。
研究小组还发现,如果使用来自胎儿猕猴而不是成年猕猴的细胞,克隆猕猴更容易。中中和华华都是用注定要形成结缔组织的细胞创造出来的,这些细胞是从流产的雌性胎儿中提取出来的。
共有79个胚胎被植入到21个替代品中。这对猴子是六次怀孕中唯一存活下来的。多利是277个植入胚胎里唯一成功的。
克隆人
虽然试图从成年猕猴提取细胞进行这项技术,也产生了两只活体动物,但都在出生后不久就死亡了,而且一只身体发育异常。
2014年,马萨诸塞州安斯泰来再生医学研究所的首席科学家罗伯特·兰扎(Robert Lanza)说:“对于许多细胞类型,重编程对于成体细胞来说比对胎儿细胞更困难。”该研究小组首次克隆了人类成人皮肤细胞。这出现了这种情况。
这一技术障碍可能会平息人们在克隆成功后经常表达的恐惧:它可能会让人设想电影《逃出克隆岛》的情节——科幻小说里的克隆人是为了多余器官而创造的。
克隆羊多利之后,加利福尼亚州的雷尔运动(无神论组织)声称它已经克隆人类的婴儿。它成立了一家名为Clonaid的公司,但被认为是个骗局。
英国谢菲尔德大学的彼得·安德鲁斯(Peter Andrews)说:“这可能是克隆人的一步,但你为什么要这么做呢? “就人类生物学而言,在英国和其他许多国家克隆人是非法的,我不认为有人会理性地这样做。”
中国研究小组表示,重点是利用克隆猴子创造更好的疾病动物模型,以加速医学治疗。
安德鲁斯说,这个概念有其价值,尤其是考虑到在老鼠身上模拟像老年痴呆症和帕金森病这样复杂疾病面临长期困难。
到目前为止,所有治疗小鼠阿尔茨海默病样症状的疗法在人体试验时都失败了。反复失败的一个潜在原因是阿尔茨海默氏症的小鼠模型还不够接近人类版本疾病。
现在有可能通过敲除在猴子和人类中具有相似作用的基因(例如触发产生阻塞阿尔茨海默氏脑的β-淀粉样蛋白斑块的基因)来更好地模拟克隆猴身上的阿尔茨海默病。
中国计划通过研究克隆和基因改造的猴子来加速医学治疗的发展。
在2016年5月的一次会议上,上海神经科学研究所的蒲慕明发表了世界上第一个患有帕金森病的转基因猴,并提出了扩大猴子使用来研究神经退行性疾病的雄心勃勃的计划。
不久之后,他在《新科学家》中也提出了相同的观点,认为由于猴子与我们的关系如此密切,思想先进,社交网络复杂,所以比起小鼠,它们会告诉我们更多关于大脑疾病的信息。
“这是世界生命科学领域近年来的重大突破。”中科院神经所所长蒲慕明院士说,克隆猴的成功,将为阿尔茨海默症、自闭症等脑疾病以及免疫缺陷、肿瘤、代谢性疾病的机理研究、干预、诊治带来前所未有的光明前景。
-
据新华社等多家媒体报道!畅能达科技实现散热技术重大突破!2024-05-29 9142
-
AI for Science:人工智能驱动科学创新》第4章-AI与生命科学读后感2024-10-14 2380
-
物联网与生命科学:追踪那些小药丸2018-11-20 6184
-
在实现CAN收发器EMC优化方面有哪些重大突破?2021-05-10 2423
-
生命科学对计算机行业的影响 精选资料分享2021-07-26 1325
-
云计算和生命科学有什么关系?2021-08-30 2377
-
两只灯泡连接的并联电路(电路教学视频)2010-08-10 2289
-
两只单连开关控制两盏灯2007-09-08 2497
-
生命科学已成为科学主流,与大数据、人工智能等学科的交叉2018-11-02 9251
-
陈天桥雒芊芊研究院在脑电波研究上获得重大突破2021-04-18 3296
-
高性能计算对生命科学研究有什么作用2021-06-25 1460
-
生命科学领域新工具:北鲲云超算平台2021-07-09 1469
-
高性能计算在生命科学领域的应用2021-08-09 2414
-
生命科学领域所需要的哪些软件是北鲲云超算平台所提供的2021-10-18 832
-
光学设计在生命科学中有哪些常见的应用呢?2023-08-23 1988
全部0条评论

快来发表一下你的评论吧 !

