

全面了解荧光光谱_荧光发射光谱图分析
电子常识
描述
1. 荧光的定义
对于荧光有这样一些文字的定义和解释:a. “荧光是物质或分子发出的冷光(luminescence)”。所谓冷光,是指光并非由热产生,可以是光致、电致、化学反应所致等等(反正就不能是热致)。b. “当某种常温物质经某种波长的入射光(通常是紫外线或X射线)照射,吸收光能后进入激发态,立即退激发并发出比入射光波长长的出射光(通常波长在可见光波段);而且一旦停止入射光,发光现象也随之立即消失。具有这种性质的出射光就被称之为荧光。”
这些文字的解释都难以理解和形象化。其实对于荧光最好的解释来自于对光子与物质分子作用过程(分子的激发和驰豫)的理解。
2. 荧光从何而来 —— 分子的激发和驰豫 ?
图 1

PS:图1摘自Principles of fluorescence Spectroscopy, Joseph R. Lakowicz
图1为一种Jablonski diagram(就简单的理解为能级图吧)。图中S0,S1,S2分别表示分子中的电子基态,第一、第二电子激发态。当分子吸收光子,电子则可能从基态(S0)跃迁到激发态(S1,S2)。激发态电子不稳定,会从激发态(S1,S2)回到基态(S0),并发出荧光(这就是荧光的源头)。当然并不一定要发出荧光,可以产生热或者其他形式能量。如果电子从激发态(S1)通过系间窜越转化为电子T1激发态,然后再从激发态T1回到S0,则发出磷光。(磷光与荧光的根本区别在此)。至于S1激发态和T1激发态的区别主要在于电子自旋的方向(单线态和三线态)。
分子吸收光后其中电子的激发和驰豫分别需要满足两大规律。激发过程满足Franck – Condon规则;退激发满足Kasha规则。Franck– Condon规则(图2A)的大意为:电子的跃迁过程很快,这一过程中原子核的相对位置来不及发生变化,可以简单理解为垂直跃迁。而Kasha规则(图2B)规定在电子驰豫复合的过程中,首先电子要驰豫到电子激发态的最低能级,然后再回到基态。如图2所示:
图 2
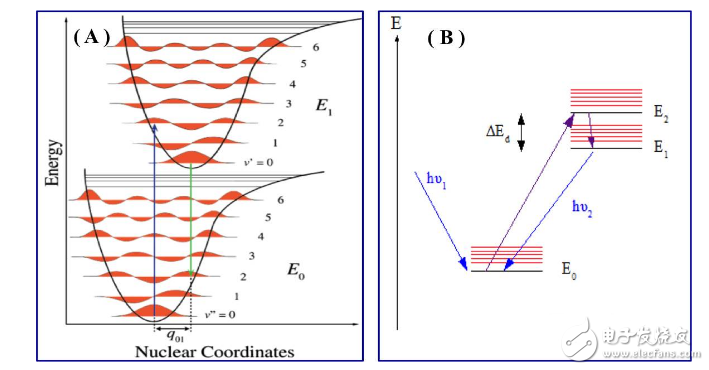
PS:图2摘自维基百科相关词条
3. 如何解读荧光光谱(稳态)
3a :荧光光谱分为:激发光谱(PLE)和发射光谱(PL)。
激发光谱:固定发射光的波长,改变激发光的波长,记录荧光强度随激发波长的变化。
发射光谱:固定激发光的波长,记录不同发射波长处荧光强度随发射波长的变化。
无论是激发还是发射荧光光谱图,其都是记录发射荧光强度随波长的变化。所以荧光光谱中纵坐标为强度,横坐标为波长。首先从图中能获取峰位和半峰宽。峰位的直观体现是荧光的颜色;半峰宽则表示荧光的纯度。
图 3
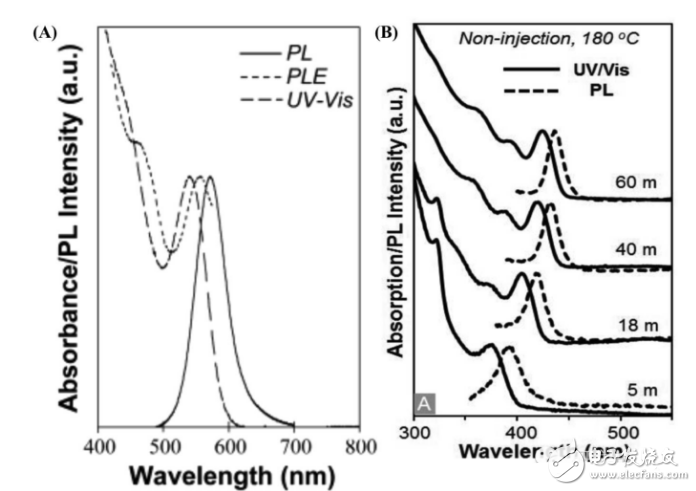
PS:图3摘自Nano Letters,2,1027
荧光光谱常与吸收光谱同时出现。所以可以与分子的吸收光谱相比较。图3A为同一物质的吸收光谱(UV - Vis)、荧光激发光谱(PLE)和荧光发射光谱图(PL)。从图中不难发现激发光谱与吸收光谱非常相似。但是两者有着本质的不同,吸收光谱的纵坐标是吸光度(Absorbance),反应物质吸收光的情况;荧光光谱的纵坐标是分子发出的荧光强度(Intensity),其不仅与物质吸光能力有关还和量子效率有关。在很多研究体系中,常常结合两者分析问题(我会在后期内容举例分析)。
3b:斯托克斯位移与发射光谱形状。
通常所说的荧光光谱指的是荧光发射光谱。大多数物质的荧光发射光谱与图3A, 3B类似,会发生红移,这一现象称为斯托克斯位移。
为什么会发生斯托克斯位移:如图1所示,处于激发态(如S1)的电子并不是直接辐射跃迁到基态(S0),而是先要经历振动松弛、内转化等方式。这些过程都会消耗一部分能量。同时跃迁到基态的电子也要一系列的振动驰豫。这些原因导致能量损失,反映在光谱图中为光谱的红移。
图 4
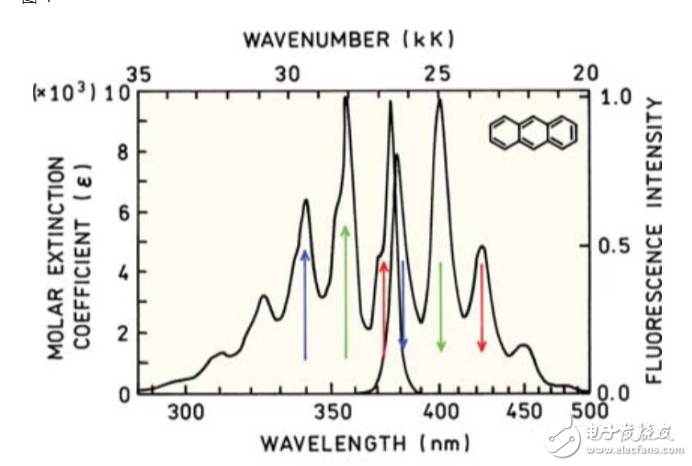
PS:图4摘自Principles of fluorescence Spectroscopy, Joseph R. Lakowicz
研究发现,荧光发射光谱的形状与激发波长无关,但是与吸收光谱保持一定的镜面对称,如图4。前者是因为Kasha规则所致,无论电子被激发到那个激发态都会先驰豫到S1,然后再辐射跃迁到基态发出荧光,所以发射光谱与激发波长无关。后者是因为电子基态和电子第一激发单重态的振动能级相似,且振动跃迁概率相似,所以成对称关系。见下图5。
图 5
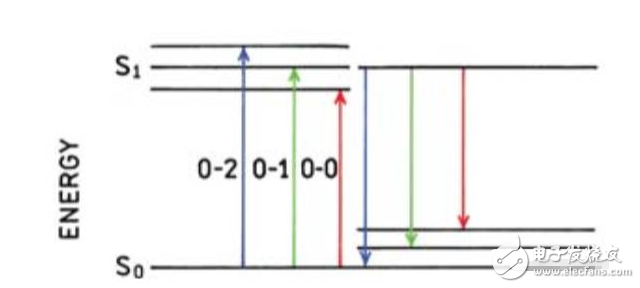
PS:图5摘自Principles of fluorescence Spectroscopy, Joseph R. Lakowicz
仔细观察则会发现图4中横坐标的刻度并不均一,这是因为分子的吸光度和相对光子通量与波长的比例不同(具体请参考《荧光分析法》)。
4. 量子效率
量子效率和荧光寿命是荧光光谱中非常重要的信息。量子效率的定义是:荧光物质发出的光子数与所吸收光子数的比值。注意区分量子效率与荧光强度的区别。某一物质的量子产率很高并不意味其荧光强度就一定大。荧光强度不仅与量子效率有关,还和物质的吸光度相关。量子效率的测量有两种方法:绝对法和相对法。
绝对法:
绝对量子效率不需用标准物来作为参比, 它的测量误差相对较小。如图6所示。首先选择合适波长、稳定、单色LED为光源(一般发射波长为400—450 nm)作为激发光源。用溶剂将某一待测样品逐级稀释成不同浓度的一系列溶液。待稀释的溶液达到平衡稳定后再开始进行绝对荧光效率的测量。打开激发光源, 将装在小瓶子里的空白溶液和配制好的一系列待测溶液分别放入光学积分球内,此时吸收后的激发光子和发射的荧光光子在光学积分球内经一系列的反射和吸收,最终通过光纤传入QE65000光谱仪系统,记录吸收后的激发光子数和发射的荧光光子数,根据定义即能计算出绝对量子效率。
图 6
PS:图6和绝对法描述摘自浙江大学博士论文《核壳量子点激子态的合成控制》。
相对法:
通过在相同激发条件下 ,比较待测物质与已知量子效率物质的积分荧光强度来计算待测物的量子效率。计算公式如下:
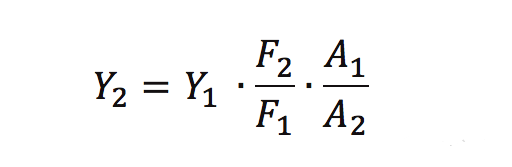
PS:公式来源于《荧光分析法》
其中:Y1, Y2分别表示参比物和待测物的量子产率;F1, F2为参比物和待测物的积分荧光强度;A1, A2为参比物和待测物的吸光度。
- 相关推荐
- 热点推荐
-
荧光激发光谱和发射光谱如何测得2023-12-19 8180
-
东方闪光|荧光光谱仪一些不常见的细节要素2023-05-19 1505
-
常规的荧光光谱仪能检测什么2023-04-11 3186
-
荧光光谱仪的原理及应用2023-03-29 2331
-
直读光谱仪和荧光光谱仪的区别2021-06-11 3904
-
三维荧光光谱在水质分析行业的应用2020-12-26 2050
-
三维荧光光谱原理_三维荧光光谱能测什么2020-12-10 23405
-
三维荧光光谱的简介2020-03-22 27062
-
基于LabVIEW软件的显微荧光光谱成像系统设计2019-06-04 4458
-
拉曼/荧光光谱知识科普2018-09-21 10314
-
什么是荧光激发光谱_荧光发射光谱的概念_发射光谱与激发光谱的关系2018-01-27 146482
-
光致发光材料荧光光谱分析2017-04-24 2719
-
荧光光谱分析(源代码)2016-11-05 1085
全部0条评论

快来发表一下你的评论吧 !

