

军用热电池国外的发展
电池
描述
军用热电池又叫热激活电池是一次性电池,用于作为炮弹的引爆电源或者导弹、核武器的工作电源,工作时间几秒~60min,炮弹引爆完,电池也灰飞烟灭。燃料电池不是一次性电池,加了氢就像汽车,加了汽油就能源源不断提供电力。
发展历程
第二次世界大战末期,德国Erb博士首先发明了热电池,战后热电池技术传到美国,引起美国国家标准局和武器发展部的重视。1948年乌利切(Wurlitzer)公司开始生产第一个热电池并实际应用在迫击炮弹中;1955年美国SAND实验室研制成功使用寿命为5min左右的热电池,并应用在核武器上。
20世纪50年代中期,美国海军武器实验室(NOL)和尤拉卡-威廉斯(Eurelca-Williams)公司首先研究成功Mg/V2O5片型热电池,从而使热电池的制造工艺从陈旧的杯型工艺向新颖的片型工艺过渡,使热电池的性能上了一个新台阶,这是热电池发展史上一个重要里程碑。
1961年SAND实验室利用上述成果开始研制片型的Ca/CaCrO4体系的热电池。1966年第一个完整的片型热电池投产,从而片型Ca/CaCrO4热电池成为美国使用在核武器上的主要能源,使它的比能量、比功率得到很大提高,特别是大大延长了电池的使用寿命(从5min延长到60min),总之,20世纪60年代和70年代初期是热电池,特别是Ca/CaCrO4热电池大发展的时期。
钙系热电池具有放电时间长、工作电压高、激活可靠、使用安全、能耐苛刻环境条件的特点,片型工艺的出现及一些高效绝热材料的应用,使热电池的比能量、比功率得到很大提高,特别是大大延长了热电池的工作寿命,使其工作寿命达到1h左右。但Ca/CaCrO4体系热电池还存在一些致命缺点。
首先该电池易形成Li-Ca合金。该合金在电池工作温度下是可流动的液体,因而容易引起电池短路和产生电噪声;其次钙阳极与CaCrO4往往发生难以预测的放热反应,从而引起电池热失控导致电池寿命提前结束;再次是电池在放电过程中,钙阳极表面产生一层惰性复盐膜(KCa-Cl3),引起电极严重极化。
为了克服这些缺点,1970年英国海军部海上技术研究中心研究锂作阳极,硫作阴极的热电池,但由于硫在高温时易挥发,后来改用FeS2和熔点高的锂合金作为阴阳极材料。
20世纪70年代中期SAND实验室利用美国海军材料实验对锂合金阳极的研究成果和阿贡实验室对二次LiMx/FeS2蓄电池研究成果,研制成片型化的小型长寿命LiMx/FeS2热电池,各项技术指标大大超过过去任何一个电化学体系的热电池,这是热电池发展史上又一重大技术突破
由于热电池具有突出的优良性能,在现代武器上得到广泛的应用,从而促进了现代武器性能的提高。现代武器的快速发展又对热电池提出了更新、更高的要求。快激活、长寿命、大功率热电池必将成为下一步热电池研究的热点。
热电池的研究方向
快激活热电池
热电池的激活时间是指从热电池激活信号到热电池达到所规定的工作电压下限所需时间。激活过程是当电点火头或火帽接到激活信号后燃烧点燃引燃条,引燃条再引燃加热片,加热片加热使电池堆处于工作温度范围之内,使电解质熔融后,热电池开始工作。激活时间一般为0.5~2S。为缩短热电池的激活时间,一方面必须提高引燃条和加热片的燃烧速度,另一方面则需提高热电池的电解质的热传导速率,电解质熔融的速度对缩短热电池的激活时间也有相当重要的影响。通过以上改进措施,热电池的激活时间可达到0.2S,甚至可达到0.1S内。
长寿命热电池
热电池中,工作寿命为60rrdn左右的电池称之为长寿命热电池。随着武器系统发展的需要,长寿命热电池的研究也日益重要。要使热电池达到长寿命技术要求,必须解决以下几个问题:
(1) 阴极材料的热分解。目前大多数热电池均采用FcS:作为阴极材料,二硫化铁作为短寿命热电池的阴极材料比较理想,但作为长寿命热电池的阴极材料,二硫化铁在热电池的工作温度450~550℃范围内存在比较严重的热分解,影响热电池放电容量和放电时间。具有放电电压平台多、成型好、化学性能稳定等优良的电化学性能特点的复合阴极材料,是今后作为长寿命热电池阴极理想的材料。CoS:也是长寿命热电池阴极材料的不错的选择。
(2) 热电池电解质在放电过程中熔点升高。LiC1.KC1电解质在放电过程中Lr离子通过电解质从阳极向阴极迁移,在电解质中形成浓度,同时阴极从电解质中吸取离子形成复盐。当Li+/K+的比例发生变化时导致电解质熔点升高,提早凝固,电池寿命终止。可采用Li+/K+的比例发生对最低共熔点变化不敏感的电解质如:KC1.LiBr—KBr三元电解质来作为长寿命热电池的电解质。
(3) 延长热电池的热寿命。热电池的内部温度必须维持在一定范围内才能使热电池正常工作,这种维持在一定温度范围内的时间称之为热寿命。采用轻质、多孔、高效的Min.K型保温材料可提高热电池的热寿命。
大功率热电池
要实现高比功率特性,除要求材料本身电化学极化要小外,还要求材料本身的电导率较高,以降低欧姆极化。CoS的电阻率为0.002Q·cm,远低于FeS2的17.71-/·cm,更有利于降低电极的欧姆极化;通过扫描电镜(SEM)分析表明人工合成CoS:为近球形多孔网络状结构,增加了CoS的比表面积,有利于降低电化学极化。CoS:大电流负载下阴极极化小,高温放电活性物质利用率高,CoS:实际高低温的平均容量比FeS高44%,这些特点很适合于高比功率、长寿命热电池设计,是进一步提高热电池性能的首选材料。
锂系热电池主要技术方向
目前,锂系热电池是热电池的主导产品并将逐步替代老式热电池。研究者们对锂系热电池的研究主要集中在电极材料和电解质上。
热电池阳极电极材料
在热电池中,阳极不仅参加电化学反应,而且还起到导电作用。热电池的阳极材料一般采用电极电位较负的金属材料,如钙箔、镁粉、锂合金等。从Et前热电池的发展来看,采用锂阳极日益增多,锂阳极可以避免钙阳极的一些缺点。但锂直接作为热电池的阳极,其熔点较低,在热电池的工作温度下呈液态,易从多孔集流器中溢出。为使锂阳极不为液态,一般采用锂合金作为阳极,其熔点高又基本保持了锂的电化学特性。在锂系热电池发展初期,Li—A1代替锂电极作为热电池阳极材料。相对于Li—Al阳极而言,Li.si阳极具有更好的性能,因而在热电池发展中,Li.A1在应用一段时间后,就很快被Li—Si所取代。目前在军事科学领域应用中,热电池主导产品为Li—Si/FeS电池。Li.si合金电极材料的制备工艺比较简单,主结构为LiI,si4(化学计量成分)。Li.si合金电极在放电过程中,随锂含量的降低,电极电压出现5个平台,各平台间有一个平滑过渡区,通常只利用第一个平台。Li—B合金是继金属锂、Li.A1、Li—si合金之后又一重要的新型热电池阳极材料。Li.B合金的性能较Li—si合金又有很大提高,其电化学性能与纯锂十分接近。锂硼合金中活性锂利用率达70%时,电位仍然很稳定,而锂硅合金不仅活性锂含量低,利用率只有20%。Li—B合金是现今比功率、比容量最大的热电池阳极材料。
热电池阴极电极材料
在锂系热电池中,优良的阴极活性物质一般需要具有以下特点:电极电位高,相对于锂电位最好大于3V;具有高的热稳定性;与电解质不发生反应;具有电子导电性,能够大电流放电;生成的反应产物能够导电或能溶人电解质,减小内阻。锂系热电池的阴极材料通常采用电位较正的金属硫化物、氧化物以及氯化物。
(1) 硫化物阴极材料
过渡族金属硫化物是一类很好的热电池阴极材料,通常采用电位较正的金属硫化物或盐类。用它取代硫做阴极材料,可解决高温下硫蒸汽的逸散问题,大大降低可溶于电解质的多硫化物的形成。FeS是目前应用最广泛的与锂合金阳极匹配的热电池阴极材料。二硫化铁有人工合成的,也有从天然矿石中提取的,锂系热电池使用的二硫化铁主要来源于天然产出的二硫化铁。研究表明,FeS阴极材料可直接从黄铁矿中加工得到,价格便宜,电性能稳定。但是FeS,在高于550℃时发生热分解,生成硫蒸汽与阳极锂合金直接化学反应产生大量的热量,使热电池热失控直至完全失效。另外,在电池激活瞬间,单体电池会产生0.2V或更高的电压脉冲即瞬间电压尖峰,使电压平稳性下降,缩短电池的工作寿命。为消除电压尖峰,解决FeS:的热稳定性问题,广大学者做了很多方面的工作。目前最有效的常规方法是采用Li:O等锂化剂对FeS:进行锂化处理,从而大大消除电池的初始电压尖峰并提高电池寿命终结时的脉冲性能。此外,采用合成纳米结构的FeS:作为阴极也为FeS,的应用指出了新的发展方向。相较于资源丰富的FeS,CoS粉末只能采用人工合成的方法。人工合成CoS粉末的方法有:晶种诱导水热合成CoS粉体、溶剂热法合成CoS纳米粉体、水热法制备CoS:空心微球以及高温硫化法。人工合成CoS,粉末大部分的颗粒都成近球形,颗粒表面比较疏松成发达的多孔状结构。与表面光滑平坦的FeS晶体相比,CoS的结构大大提高了正极材料的比表面积,从而可提高正极工作电流密度、正极材料的利用率。因此多孔网状的CoS正极材料更适合于发展高比功率和比能量的热电池,是能代替二硫化铁的理想阴极材料。
(2) 氧化物阴极材料
由于存在严重的热分解,二硫化铁是比较理想的短寿命阴极材料。Clark用溴化锂对VO、VO进行锂化处理制得锂化的氧化钒(LVO),作为热电池的阴极材料,与二硫化铁相比具有较高的电压和更好的热稳定性。LVO优点如下:混合物的热稳定性较好;电极电位很正,相对锂为2.8V;化学稳定性好,若把它与一定比例的FeS混合作为阴极,则除保持原有的优点外,还可显著提高热电池的后期放电效果。
(3) 氯化物阴极材料
金属氯化物(特别是氯化镍)是可替代二硫化铁的较为理想的阴极材料之一,具有理论容量高、放电电流密度大、电极电位正等特点。以高温处理氯化镍为正极材料的热电池,氯化镍热电池在放电后期,由于氯化镍与全锂电解质在高温时发生相互熔浸,电池的电解质材料流溢出电堆现象严重。研究表明,在氯化镍热电池中,电解质不宜选用二元电解质,锂硅合金不适合做负极。以氯化镍为正极,Li.B合金为负极,电解质选用全锂j元电解质制备电池进行放电试验,研究表明样品电池放电电压曲线平滑、无极化现象、无微短路现象;电池激活时间1.6S,样品电池的比能量达到84Wh/kg(这是热电池中较高的水平)。电池正、负极利用率都达到较高的水平,在进一步改进电池粉量配比后,电池的比能量仍有提高的可能,而且激活时间也有望缩短。
熔融硝酸盐电解质
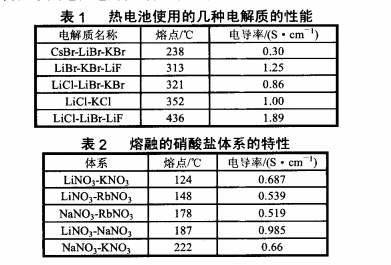
近年来,国外的一些热电池实验室(SNL、SAFTAmerica公司)采用熔融的硝酸盐应用于锂体系热电池电解质。由于该体系的低温工作区间、单体电压高、比能量高等优点,作为热电池电解质其应用备受关注。热电池的熔融盐电解质具有水溶液电解质所无法比拟的优越性:非流动性;高电导率及离子迁移速度大,允许大功率大电流放电;分解电压高,可以使用与水反应的超低电位金属及其合金作阳极,从而使电池电压高,比能量大;活性物质利用率高,电化学极化和浓差极化都很小。传统热电池电解质可选用碱金属和碱土金属的氟化物、氯化物、溴化物以及它们的低共熔点混合物。但这些电解质的熔点相对较高,电池的工作温度基本都在300~500℃。据国外的文献报道,国外的一些热电池实验室采用熔融的硝酸盐作为锂体系热电池电解质,电池工作温度范围低(150~300℃ );锂体系阳极能够与之兼容;组合电池采用高电压阴极与锂合金配对,电池的单体电压和比能量较传统热电池明显提高。表1是传统锂系热电池电解质体系特性,表2是常用的熔融硝酸盐体系一些特性。可见硝酸盐体系的熔点均小于300℃,且有较好的电导率,因此该体系应用于热电池中,体系温度较传统锂系热电池降低至少100℃,该体系与传统锂系热电池电解质都具有良好的导电性。
保温材料
要使热电池正常工作,必须维持在一定的温度范围内。通常在电池堆体的周围使用一定的保温材料来达到在较长时间内维持一定的温度的目的。保温材料性能好坏对热电池的性能(特别是工作时间)会产生很大的影响。
Min-k保温材料主要以气相SiO或SiO气凝胶粉末为主体,添加TiO2等作为遮光剂,加入一定量的纤维作为增强剂,经过混合后压制而成。气凝胶是一种新型的轻质纳米多孔性非晶固态材料,其比表面高达1000m2/g、孔率达80%~99.8%,孔洞的典型尺寸为1~100hi/1。它被认为是固体中热导率很低的材料。这是因为:气凝胶的纤细纳米多孔性结构能有效地限制局域激发的传播,其固态热导率比相应的玻璃材料低2~3数量级;气凝胶的典型孔洞尺寸在几纳米到几十纳米之间,小于常压下空气分子的平均自由程,因此气体热导率很低;掺杂遮光剂的气凝胶能使辐射热传导在一定厚度内被有效地吸收,即辐射热导率也很低。在常温常压下,气凝胶的导热系数可达O.015W/(m·K)。即使在527℃的温度下,其导热系数也只有0.038W/(m-K)。气凝胶虽然有较好的保温性能,但机械强度较差。为了提高强度,可以在制备的过程中加入纤维进行增强。真空绝热体采用不锈钢制成的双层夹套壳体,夹套内抽真空,其保温原理和热水瓶相同。若在真空室放人填充材料,如铝箔、玻璃纤维等,保温性能将大大提高。
热电池发展展望
自20世纪70年代锂合金/二硫化铁电池问世以来,世界上几个主要军事强国对该种热电池的兴趣倍增,80年代得到非常迅速的发展。可以预见,
锂合金/二硫化铁热电池将全面替代目前还在使用的几个比较落后的热电池体系。21世纪是锂合金/二硫化铁电池的全盛时期,随着材料特别是新型保温材料的发展,到那时长寿命热电池组的寿命将超过2h,功率为几千瓦级热电池组可能问世。稳态放电电流密度可能达到8~10A/cm2,脉冲放电电流密度可能超过50A/cm2,电池组的性能得到进一步提高,比功率大大超过目前水平。
随着热电池研究的不断深化,热电池必将在武器应用方面不断发展,在军事上占有越来越重要的地位
- 相关推荐
- 热点推荐
- 热电池
-
模拟导弹热电池指示信号的电路设计与实现2025-06-20 24168
-
虚拟仪器对军用测试技术有什么影响?2021-05-07 1749
-
军用宽带移动通信行业的未来发展2020-05-13 1593
-
军用连接器正朝什么方向发展?2019-08-19 2003
-
国外电磁兼容仿真软件发展到了哪一步?有什么相关应用呢?2019-07-31 3548
-
国外军用电子元器件质量等级与国内对应情况一览表2018-11-27 5917
-
一文带你走进热电池的世界2018-10-04 28785
-
国外军用可穿戴设备的现状及发展2018-04-16 9800
-
热电池是什么电池_热电池的工作原理2018-02-07 44302
-
军用无人机的用途及发展趋势2018-01-15 28594
-
[分享]电源分类及军用化2009-12-22 9079
-
导弹热电池温度测量系统2009-08-26 817
-
热电池参数测试与控制系统2009-07-11 533
-
导弹热电池参数自动化测控系统2008-10-19 901
全部0条评论

快来发表一下你的评论吧 !

