

功率放大器应用分享:利用微流控技术促进干细胞心肌组织成熟
描述
微流控技术是一种通过微小的通道和微型装置对流体进行精确操控和分析的技术。它是现代医学技术发展过程中的一种重要的生物医学工程技术,具有广泛的应用前景和重要性。它在高通量分析、个性化医疗、细胞筛选等方面有着巨大的潜力,Aigtek安泰电子今天就将为大家分享一篇微流控领域研究成果,一起接着往下看吧~
人诱导多能干细胞(hiPSC)来源的心肌组织(hiPSC-CM),是一种极具潜力且可减少药物研发中动物测试的体外组织模型。然而传统基于生化因子定向诱导分化所得的心肌组织,其不成熟的特性却显著影响了该类组织的实际应用。来自加州大学伯克利分校的KevinE.Healy团队通过在微流控芯片内部有机结合组织工程手段和培养体系优化的方式,大大提高了hiPSC来源心肌组织的成熟度,且这些诱导细胞成熟的因素对心肌细胞动作电位和钙离子调控的影响具有表型依赖性。相关论文“Metabolicallydrivenmaturationofhuman-induced-pluripotent-stem-cell-derivedcardiacmicrotissuesonmicrofluidicchips”发表于杂志NatureBiomedicalEngineering。
基于已有的研究报道,研究者猜想将组织工程手段与可溶性因子优化进行结合,将有望提高现有hiPSC-CM的成熟度。为此,研究者首先在微流控芯片中建立了大小不同、特异性排列的微柱阵列,以作为心肌细胞的附着位点,从而促进多层组织自组装的一致性,并实现心肌组织的肌节排列和单轴跳动(图1)。随后,研究者将同源的hiPSC-CM和基质细胞(hiPSC-SC)在上述芯片微生理系统(MPS)中进行共培养,并探索了葡萄糖、油酸、棕榈酸和白蛋白(这里选用BSA)等不同碳源对心肌组织成熟度的影响。在10天的培养过程中,研究者通过对心肌组织的跳动现象和钙通量表征,最终确认同时存在油酸和棕榈酸两类脂肪酸、降低葡萄糖含量、提高BSA含量的新型成熟培养基(MM)为最佳促成熟组合。
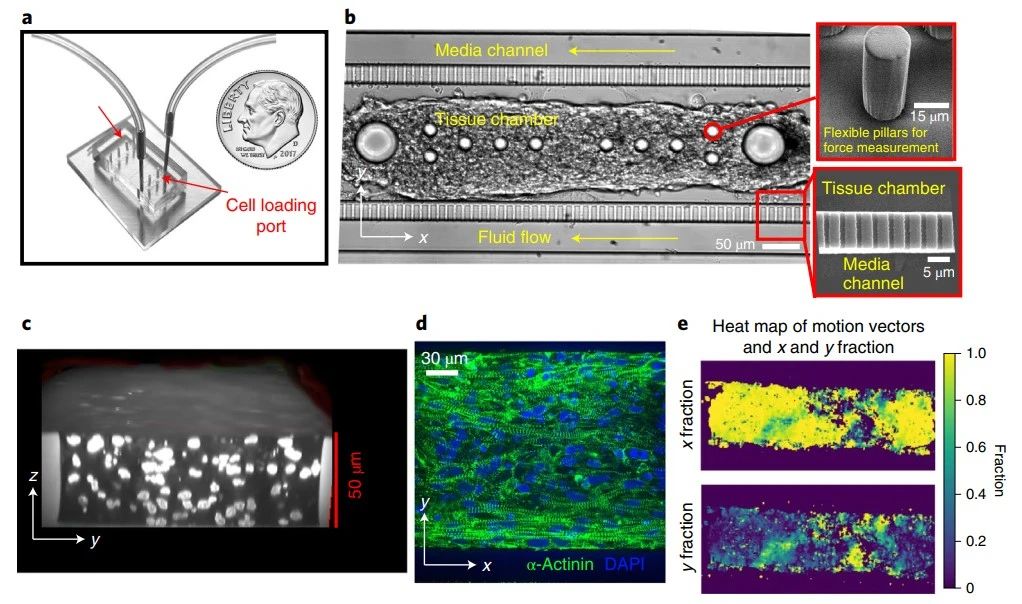
图1优化的hiPSC来源心肌微生理系统
在完成微流控芯片的构建和碳源优化后,研究者基于WTC(野生C型)hiPSC建立了心肌微生理系统,并对MM引起的心肌钙瞬变和动作电位变化进行了系统的表征。结果表明,MM有效缩短了心肌微生理系统中的心肌动作电位时程(APD),并提高了基线标准化的钙振幅;但同样的测试在2D培养的心肌组织中无明显变化。接着,研究者利用WTC和SCVI20(斯坦福大学心血管生物库细胞系20)两类hiPSC来源的心肌组织,探究了MM对不同基因型细胞作用的差异。从动作电位的角度看,SCVI20心肌组织的初始APD更短,但随着培养时间达到10天,该类组织的APD与WTC心肌和原代成人心肌逐渐趋同;从钙离子通量的角度看,SCVI20心肌组织与WTC组织具有类似的变化趋势,但其最大钙离子上升速度提升更明显(图2)。这也初步说明了微流控芯片中的3D培养环境和优化的MM对心肌组织动作电位和钙瞬变的影响具有协同效应,且这种影响具有基因型的特异性。
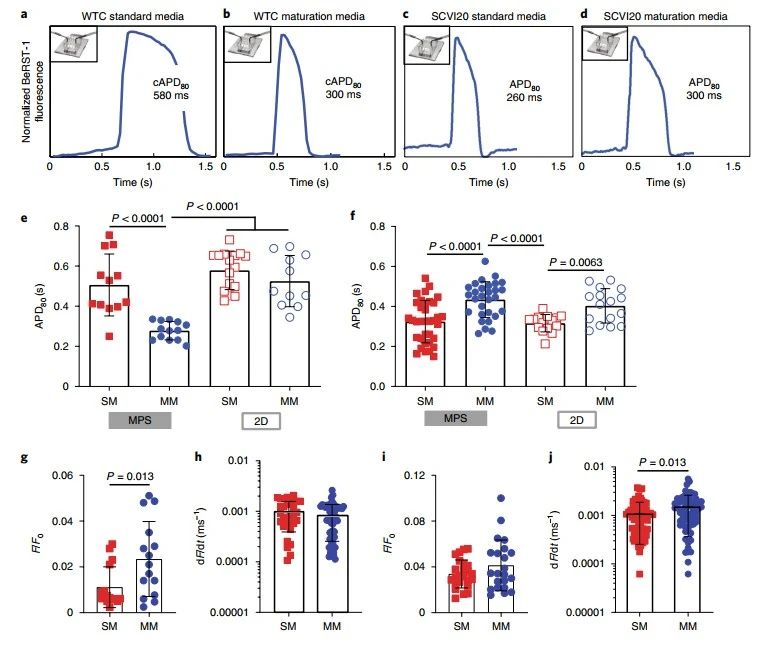
图2成熟心肌MPS的动作电位表征
随后,研究者探究了MM对心肌组织中线粒体形态结构的影响。基于荧光表征不难发现,不同hiPSC来源的心肌组织,其中线粒体内跨膜电位都有显著上调,提示MM培养基处理后的心肌MPS中氧化磷酸化现象明显增加。另外,尽管线粒体的密度没有明显变化,但MM的处理使其排布更加规则,并使线粒体延伸出更多丝状物从而形成网络。当然,在2D培养的心肌组织中,未发现上述变化(图3)。这些数据可以说明,优化后的MM培养基在心肌MPS中有效改变了细胞中线粒体的状态,使心肌组织处于更趋向于成熟态的代谢表型。
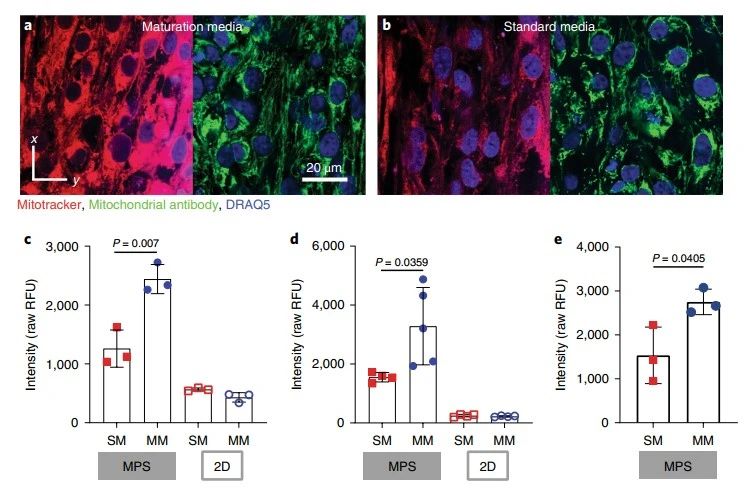
图3MM处理心肌MPS后的线粒体形态学变化
接着,研究者观测了心肌微生理系统中的力学效应。首先,仅从肌节形态和排布来看,MM的处理在WTC和SCVI20来源心肌中都不会产生显著影响。将微流控芯片中微柱的形变转化为受力的大小,可以发现:在高浓度钙离子的刺激下,MM处理组和常规培养基组的心肌组织施力效果相近。然而MM处理后的WTC心肌组织却表现出对低浓度钙刺激更敏感的效应。同时,在一定范围内MM处理的心肌MPS会对钙离子浓度变化响应更为剧烈。当在心肌MPS中施加异丙肾上腺素这一诱因时,WTC和SCVI20来源的心肌组织分别表现为轻微的响应迟钝或敏感;而时序性改变异丙肾上腺素的刺激时,两类心肌组织则都表现为响应更为迟钝(图4)。总体来看,这些数据表明MM的处理不会损害肌节或干扰兴奋-收缩耦合及受体反应性;但在细胞外钙的含量受限时,MM处理则会增强钙收缩耦合。
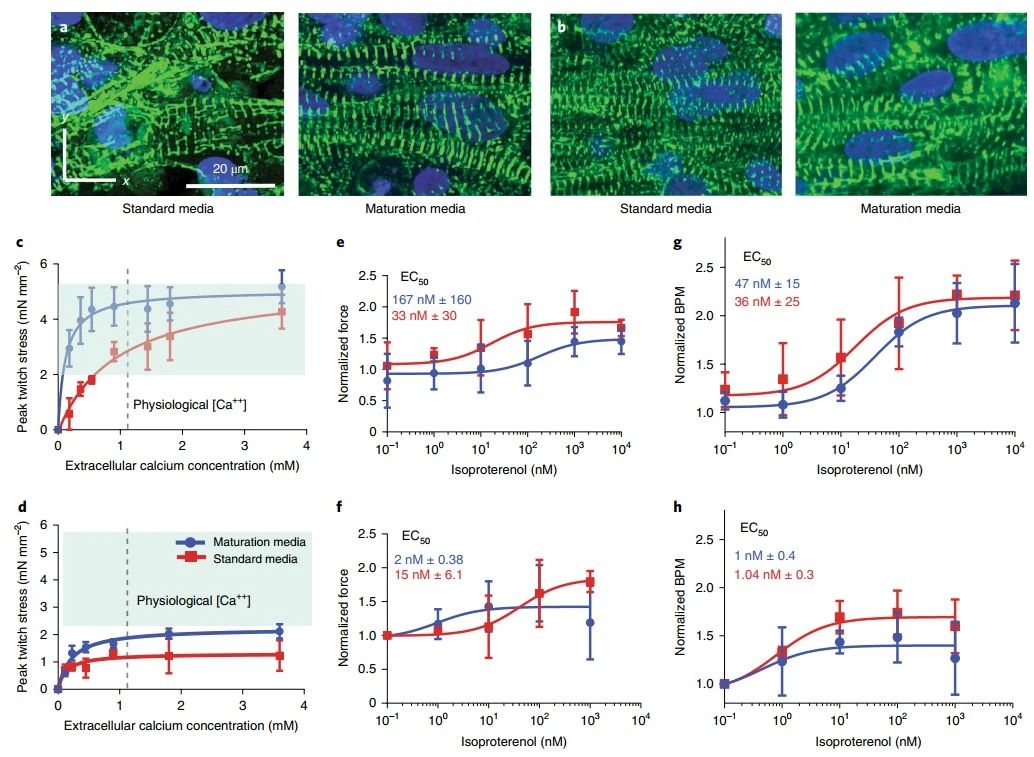
图4MM处理后心肌MPS的变力响应
在接下来的部分,研究者从基因表达的角度表征了MM处理后心肌MPS的变化。结果表明,MM的处理并不会显著改变WTC和SCVI20心肌组织中电生理学、细胞特性、收缩性和钙调控相关的基因表达。但在WTC心肌组织中,肌脂蛋白和钙离子通道相关的基因(SLN、HCN2和CACNB2)表达有上调趋势,而与钾离子通道和乙醛脱氢酶相关的基因(KCND2和ALDH1A1)表达则有下调趋势。对SCVI20心肌组织来说,与钾离子通道相关的KCNJ2和KCND2基因分别出现了显著的下调和上调;而与肌脂蛋白和钙离子通道相关的基因(SLNCACNB2)则只有轻微的上调。同样地,很难在2D培养的心肌组织中发现这些较为显著的变化(图5)。
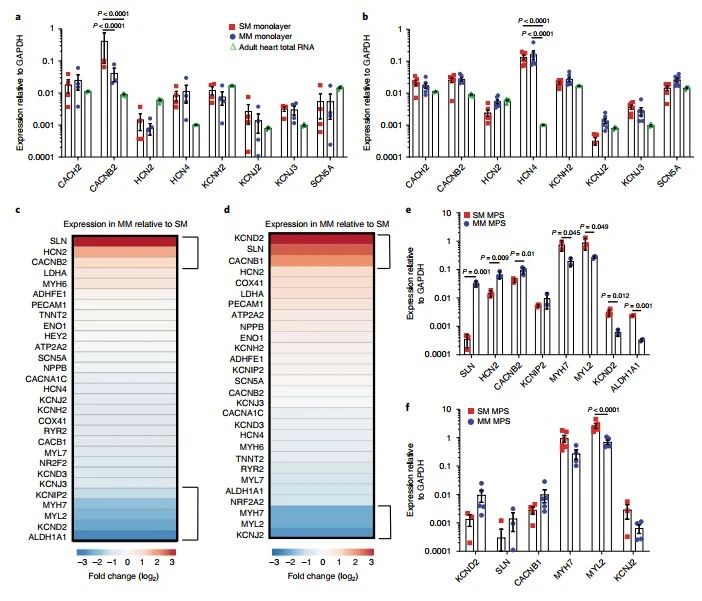
图5脂基MM处理单层心肌组织和MPS后的基因表达分析
从上述结果不难发现,MM的处理在WTC和SCVI20来源心肌MPS中产生了对APD相反的影响,但其最终结果是使两者的APD和钙调控行为都接近于原代生理组织。当然,这并不意味着两类心肌细胞内的电流值相近,而电流值又直接影响了心肌组织的药学响应等,因而对细胞内电流的测定是一个不可忽视的问题。受限于活细胞很难从心肌MPS中取出的问题,研究者创造性地采用了计算模拟的方式:由APD和钙离子变化的数据来推算细胞内的电流值。模拟预测的结果表明,MM的处理对WTC和SCVI20心肌组织中动作电位的改变和钙调控影响的数值不同,但两种来源细胞的成熟表型却非常相似。
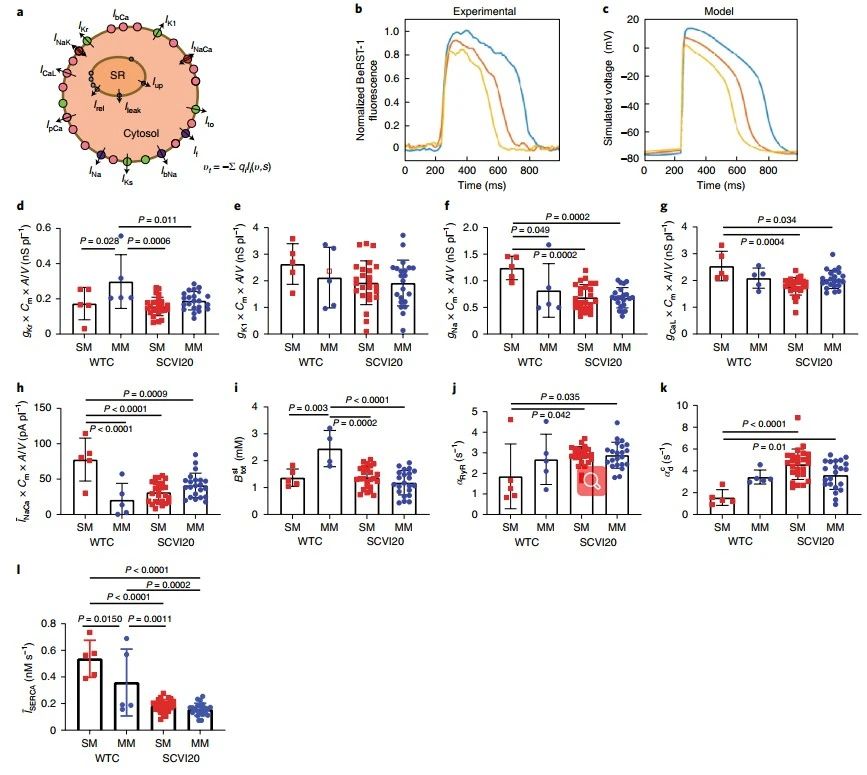
图6单一电流和钙离子调控对单层心肌组织和MPS动作电位影响的数学模型
最后,研究者将不同来源的心肌微生理系统用于药效学研究,以证明该体外模型的实用价值。文中选用了维拉帕米(Verapamil)、氟卡尼(Flecainide)和阿夫唑嗪(Alfuzosin)等几类可改善心律不齐的临床药物进行测试。结果表明,尽管WTC和SCVI20心肌组织对不同药物的具体反应不同,但总体上,在心肌MPS中使用MM培养的组织,能有效减少假阳性(维拉帕米)和假阴性(阿夫唑嗪)药物反应的预估(图7)。这进一步证明了该成熟化的微生理系统在药物评价和预测方面的优势。
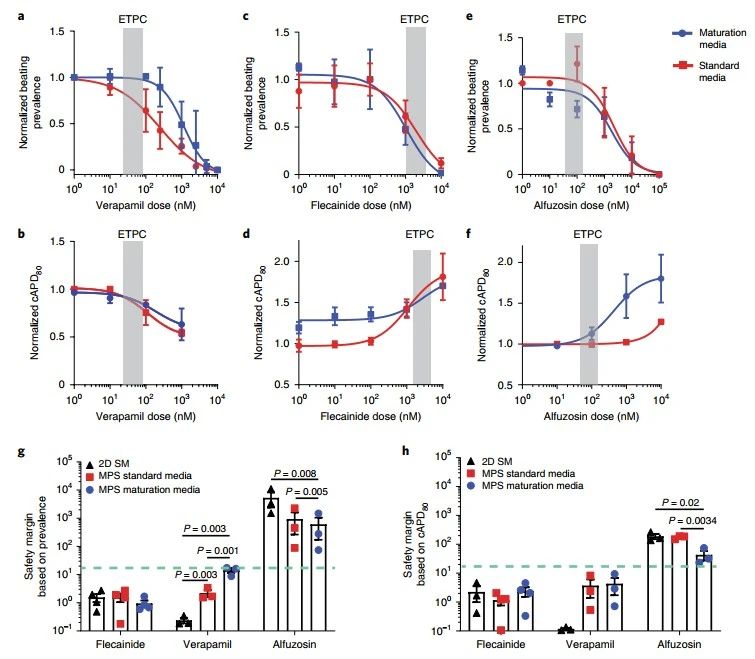
图7成熟的WTC心肌MPS中抗心律失常药的药理学研究
总而言之,本文证明了在MPS中使用基于脂肪酸的培养基进行干细胞来源心肌组织的3D培养,可以有效促进hiPSC-CM动作电位的成熟。且所得心肌组织的APD和钙瞬变行为会更接近于原代生理组织。同时,这种变化是可以经过一定的理论模拟来进行判定和预测。而这种较为成熟的心肌组织也有望为相关治疗药物的研发和药物安全性测试提供更好的先决条件。
ATA-2082高压放大器

西安安泰电子是专业从事功率放大器、高压放大器、功率信号源、前置微小信号放大器、高精度电压源、高精度电流源等电子测量仪器研发、生产和销售的高科技企业,为用户提供具有竞争力的测试方案。Aigtek已经成为在业界拥有广泛产品线,且具有相当规模的仪器设备供应商,样机都支持免费试用。功率放大器www.aigtek.com
审核编辑 黄宇
-
功率放大器在声空化微流控器件中的应用2025-11-11 178
-
创新应用:安泰功率放大器赋能声空化微流控器件2025-08-07 388
-
功率放大器在液滴微流控细胞分选中的应用2025-04-03 645
-
Aigtek功率放大器在微流控医学领域研究中有哪些应用2025-04-01 640
-
功率放大器在磁场促心肌组织成熟化的实现中的应用2023-04-10 913
-
一文解读功率放大器(功率放大器如何选型)2022-11-15 3855
-
高压功率放大器磁场促心肌组织成熟化的实现中的应用2022-10-26 825
-
剖析功率放大器在微流控技术液滴微颗粒分选中的应用2022-01-14 565
-
RF功率放大器的设计2021-12-22 12556
-
功率放大器,超声功率放大器定义分类和应用2017-12-15 5729
-
功率放大器类型有哪些?功率放大器如何选择厂家2017-10-17 4184
-
AGITEK功率放大器---在生物工程学院典型案例2017-08-03 1928
-
基于CPLD的数字功率放大器的研究与实现2015-07-01 3245
-
线性功率放大器设计和乙类和丙类功率放大器设计2008-08-17 9178
全部0条评论

快来发表一下你的评论吧 !

