

里程碑式进展!新型光电多模态传感器诞生,糖尿病监测迎来革命性突破!暨南大学、东莞理工学院
电子说
描述
近日,来自暨南大学和东莞理工学院的科研团队取得重要突破,成功研发出一种柔性光电混合微光纤长周期光栅多模态传感器,相关成果“Flexible Optoelectronic Hybrid Microfiber Long-period Grating Multimodal Sensor”发表于国际知名期刊《Advanced Science》。该研究的通信作者为暨南大学的 Li-Peng Sun、Jie Li、Yi Zhang以及 Bai-Ou Guan 。文章介绍了一种新型的柔性光电混合微光纤长周期光栅多模态传感器,该传感器集成了光学和电学两种传感机制,可同时监测生物力学信息和葡萄糖,为可穿戴传感器的设计提供了新的思路,在糖尿病管理等领域具有潜在的应用价值。
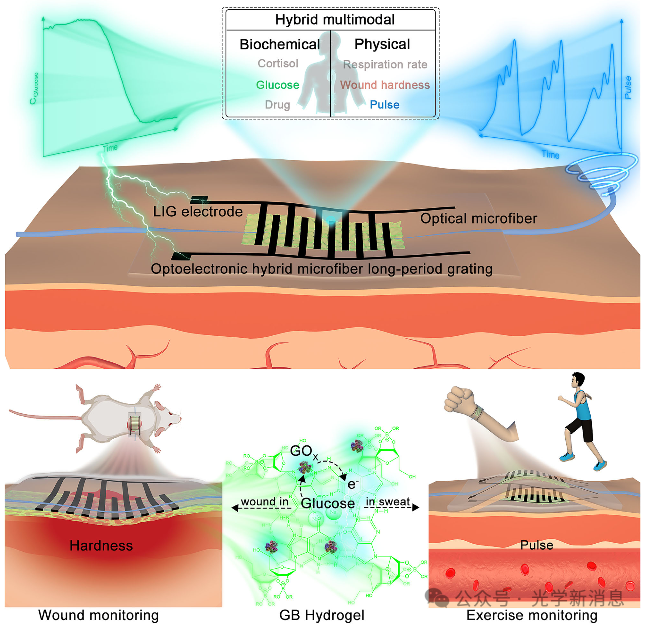
图1. LIG-mLPG柔性光电混合多模态传感器示意图。插图:功能化LIG-mLPG用于监测动物和人体模型中汗液葡萄糖和物理量的示意图。
1.研究背景:全球范围内,高血糖已成为威胁人类生命健康的重要因素,它是导致死亡和残疾的高危因素之一。随着全球糖尿病患者数量呈上升趋势,深入探究人体健康状况,准确预测葡萄糖代谢紊乱并诊断糖尿病,已成为关乎人类健康的紧迫任务。糖尿病患者因胰岛素失衡导致血糖浓度异常,这会引发一系列严重并发症,如足部感染,严重时甚至可能导致截肢,还会对眼睛、肾脏、血管、心脏等重要器官造成损害。传统的葡萄糖测量方法主要依赖侵入性的针刺采血检测,这种方法不仅在检测和评估之间存在时间延迟,给患者带来心理负担,而且难以在生理状况突然变化时快速监测动态血糖水平。可穿戴生物传感器的出现,为糖尿病的持续无创管理带来了新的希望。这类传感器利用间质液、汗液、唾液和眼泪等替代体液进行葡萄糖监测,通过对人体汗液、脉搏、运动行为等生化或物理变化进行现场样本分析,能够高效、便捷地监测慢性疾病,有助于评估佩戴者日常活动中的病理生理异常情况。近年来,可穿戴生物传感器平台不断发展,功能逐渐向测量多种生化和物理健康参数转变,以避免单一参数分析可能导致的误诊。然而,目前大多数生物标志物检测研究存在问题,要么基于冗余的传感阵列,不利于传感器的集成和小型化;要么基于单一组分的多模态传感器,由于单一机制下的信号相关性,往往需要复杂的算法进行解耦,以确保每个检测量都能输出可靠的数据。此外,在日常活动中同时监测心率、血压等重要生物力学参数以及伤口愈合状态,能够全面评估人体健康状况,为医疗决策提供有力支持。这促使了具有不同自解耦机制的混合多模态生物传感器的发展,以优化对生化和物理参数的同时感知能力,有效减少信号干扰。但将多种传感模式集成到一个可穿戴平台,在传感器集成以及不同制造技术的兼容性方面面临挑战,尤其是在处理复杂融合和跨模态精度的多元输出数据时,增加了电子设备小型化的复杂性。因此,开发能够构建高度集成的异构生物传感设备的新方法,以实现准确的生化和物理监测至关重要。
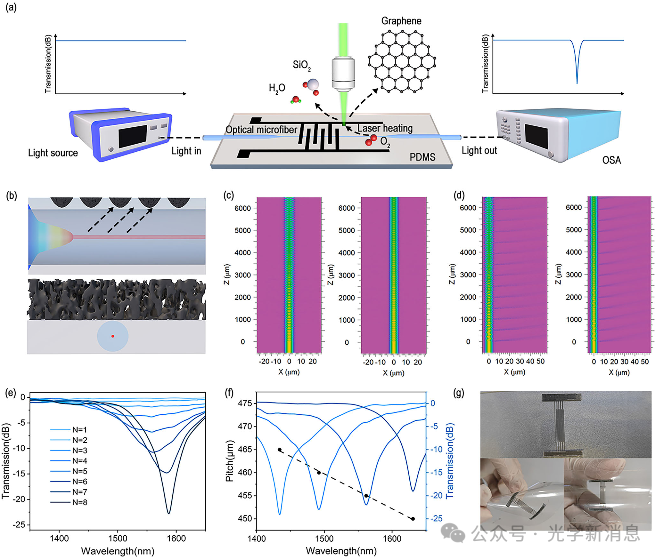
图2. a) 基于激光诱导石墨烯调制的微光纤长周期光栅(mLPG)概念图;b) 顶部:LIG-mLPG的轴向结构图;底部:LIG-mLPG的横截面图;c) 当光以谐振(相位匹配,左图)和非谐振(非匹配,右图)波长入射时,通过光栅区域传播的光的模拟振幅分布的俯视图;d) 当光以谐振(相位匹配,左图)和非谐振(非匹配,右图)波长入射时,通过光栅区域传播的光的模拟振幅分布的侧视图;e) 在LIG-mLPG调制过程中,透射光谱随调制周期数的变化;f) 光栅周期与谐振波长之间的关系;g) LIG-mLPG的实物图。
2.LIG-mLPG的设计与制备:通过火焰刷技术拉制微光纤,将其封装在PDMS中,再利用激光诱导PDMS形成LIG,LIG的图案化结构对微光纤的消逝场进行周期性调制,从而制备出LIG-mLPG。这种方法避免了激光或电弧脉冲对微光纤的损伤,且LIG的调制效果受激光功率和扫描速度影响。
3.LIG-mLPG的表征:利用SEM、XPS、Raman光谱和FTIR光谱等对LIG进行表征,结果表明激光照射使PDMS的化学键断裂重组形成石墨烯。Raman光谱显示,激光功率影响石墨烯的质量,适当的激光功率和扫描速度有助于制备高质量的石墨烯。
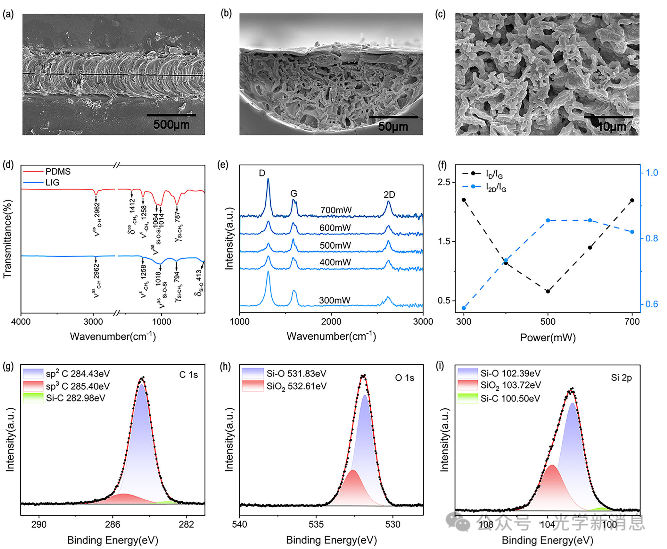
图3. a) 激光诱导石墨烯(LIG)的俯视图扫描电子显微镜(SEM)图像;b) LIG的横截面SEM图像;c) LIG横截面的放大SEM图像;d) 聚二甲基硅氧烷(PDMS,红色曲线)和LIG(蓝色曲线)的傅里叶变换红外光谱(FTIR);e) 不同调制功率下LIG的拉曼光谱;f) 拉曼光谱中(I_D/I_G)(黑色)和(I_{2D}/I_G)(蓝色)随激光调制功率的变化情况;g) LIG的碳(C 1s)X射线光电子能谱(XPS);h) LIG的氧(O 1s)XPS;i) LIG的硅(Si 2p)XPS。
4.传感器性能
压力传感性能:LIG-mLPG通过光学信号实现生物力学传感,对压力敏感,灵敏度为(2.06nm/kPa),检测限为(0.008kPa),响应时间和恢复时间分别约为(2.8ms)和(15.5ms),稳定性良好。其对折射率的响应可通过界面修饰调节,未修饰时对生物标志物不敏感,适合作为生物力学敏感元件。
石墨烯电极的电学响应:LIG叉指电极通过电学信号实现生化传感,结合GB水凝胶可构建应变不敏感的葡萄糖传感器。GB水凝胶具有良好的导电性、生物相容性、粘弹性和自愈合性。该传感器对葡萄糖检测具有特异性,检测限为(0.0246mM) ,且光栅光学信号对葡萄糖变化不敏感。
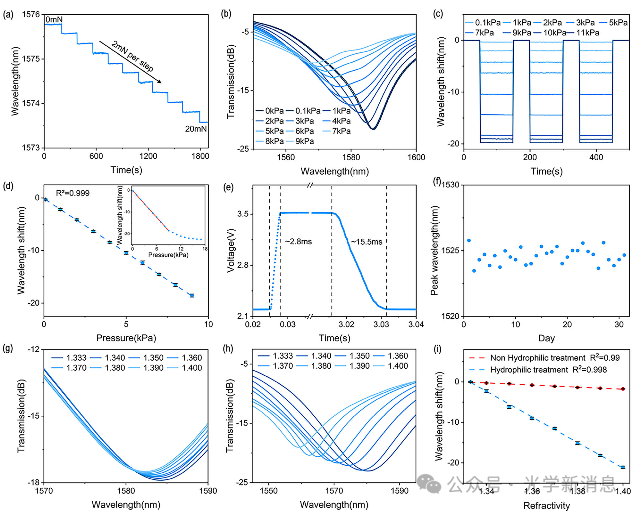 图4. a) 施加2 mN应力阶跃时,测量得到的微光纤长周期光栅(mLPG)的凹陷波长位移;b) 不同压力水平下单个凹陷的透射光谱记录;c) LIG - mLPG在不同压力水平下波长位移的重复性;d) 测量得到的凹陷波长位移随施加压力的变化;e) LIG - mLPG在1 kPa压力下的响应时间和恢复时间;f) LIG - mLPG在一个月内的稳定性;g) 亲水处理前和h) 亲水处理后,不同折射率下单个凹陷的透射光谱记录;i) 亲水处理前后,测量得到的凹陷波长位移随折射率的变化。
图4. a) 施加2 mN应力阶跃时,测量得到的微光纤长周期光栅(mLPG)的凹陷波长位移;b) 不同压力水平下单个凹陷的透射光谱记录;c) LIG - mLPG在不同压力水平下波长位移的重复性;d) 测量得到的凹陷波长位移随施加压力的变化;e) LIG - mLPG在1 kPa压力下的响应时间和恢复时间;f) LIG - mLPG在一个月内的稳定性;g) 亲水处理前和h) 亲水处理后,不同折射率下单个凹陷的透射光谱记录;i) 亲水处理前后,测量得到的凹陷波长位移随折射率的变化。
5.LIG-mLPG传感器在糖尿病伤口愈合检测中的应用:将LIG-mLPG传感器贴在糖尿病大鼠伤口处,可监测伤口硬度和葡萄糖水平变化。伤口硬度随时间增加,传感器光学信号变化与之相符;注射胰岛素后,伤口渗出液中葡萄糖浓度下降,传感器电学信号变化与血糖仪测量结果一致,同时还能捕获呼吸信号。
6.人体健康实时多参数监测:将LIG-mLPG传感器贴在人体不同部位,可分别监测脉搏和汗液葡萄糖信号,且两种信号相互独立。对不同志愿者的运动实验表明,传感器能有效监测运动过程中脉搏波和汗液葡萄糖水平的变化,为糖尿病患者的日常监测提供了重要依据。
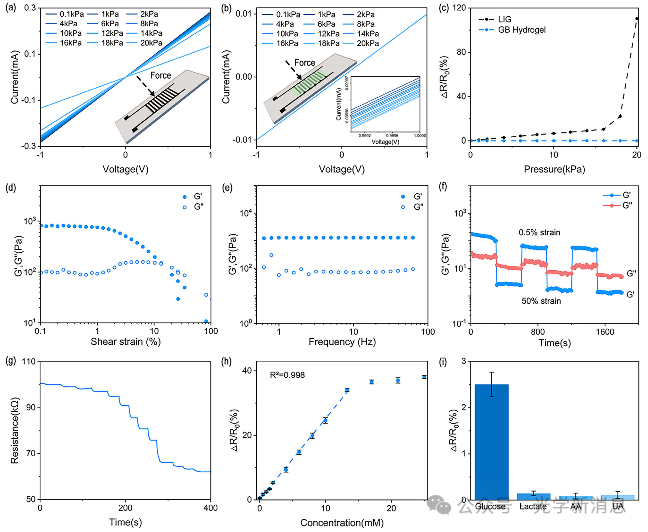 图5. a) 在20 kPa压力范围内,LIG电极(正负电极相连)的电流-电压(I-V)特性;b) 在20 kPa压力范围内,GB水凝胶/LIG(叉指电极结构)的I-V特性;c) LIG正负连接模式与GB水凝胶/LIG在不同压力下电阻变化的对比;d) GB水凝胶在不同剪切应变下储能模量G′和损耗模量G″的变化;e) GB水凝胶在不同频率下储能模量G′和损耗模量G″的变化;f) 在大应变(50%)和小应变(0.5%)之间交替切换剪切应变进行的流变恢复测试;g) 掺杂葡萄糖氧化酶(GOx)的GB水凝胶在不同葡萄糖浓度(0 - 25 mM)下的电阻变化;h) 电阻随不同葡萄糖浓度的变化;i) 对葡萄糖的特异性。
图5. a) 在20 kPa压力范围内,LIG电极(正负电极相连)的电流-电压(I-V)特性;b) 在20 kPa压力范围内,GB水凝胶/LIG(叉指电极结构)的I-V特性;c) LIG正负连接模式与GB水凝胶/LIG在不同压力下电阻变化的对比;d) GB水凝胶在不同剪切应变下储能模量G′和损耗模量G″的变化;e) GB水凝胶在不同频率下储能模量G′和损耗模量G″的变化;f) 在大应变(50%)和小应变(0.5%)之间交替切换剪切应变进行的流变恢复测试;g) 掺杂葡萄糖氧化酶(GOx)的GB水凝胶在不同葡萄糖浓度(0 - 25 mM)下的电阻变化;h) 电阻随不同葡萄糖浓度的变化;i) 对葡萄糖的特异性。
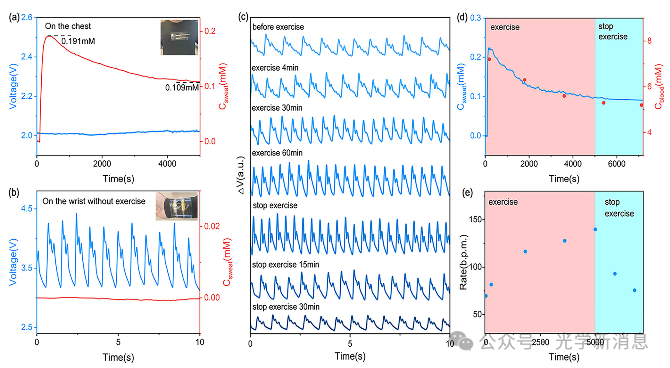
图7. a) 运动时在胸部进行监测(无变形,仅有汗液);b) 静止时在手腕处进行监测(无汗液,脉搏引起变形);c) 运动时手腕处脉搏波的变化;d) 运动过程中汗液中葡萄糖浓度的变化(蓝色)以及使用商用血糖仪测量的血糖变化(红色);e) 脉搏率随时间的变化。
7. 研究结论:成功制备了一种可同时监测生物力学和葡萄糖的光电混合多模态可穿戴光纤传感器。该传感器集成度高、响应快、灵敏度高且稳定性好。未来可通过集成光学和电学信号读出系统、优化LIG电学性能和开发更好的水凝胶等方式进一步改进。
该研究得到了国家自然科学基金、广东省基础与应用基础研究基金等多个项目的支持。科研团队表示,未来将进一步优化传感器,通过集成光学和电学信号读出系统、优化 LIG 的电学性能、开发更好的水凝胶等,提升传感器的性能,为糖尿病管理和可穿戴医疗设备发展提供新的解决方案。
原文链接:https://advanced.onlinelibrary.wiley.com/doi/epdf/10.1002/advs.202501352
审核编辑 黄宇
-
常熟理工学院计算机科学与技术嵌入式培养2021-07-16 1631
-
泰克MTM400和MTS4SA助力新加坡南洋理工学院学生学习2008-11-10 704
-
准确预测儿童是否有患1型糖尿病的检测新技术2018-07-24 3743
-
伍斯特理工学院研发最新生物传感器2018-12-24 4842
-
谷歌联手麻省理工学院研究冷聚变 进展才得以发布2019-05-29 4575
-
麻省理工学院开发低成本传感器手套 成本仅为10美元2019-06-03 4626
-
爱立信5G商用迎来里程碑式突破,已获100个5G商用合同2020-08-13 825
-
麻省理工学院关于电磁脉冲的新实验2021-04-19 984
-
美国麻省理工学院和加州理工学院:研发可吞咽传感器助力监测胃肠道健康2023-02-21 1819
-
瑞士洛桑联邦理工学院(EPFL):研发新型传感器可诊断神经退行性疾病2023-07-27 2186
-
力促人才培养,东莞理工学院携手泰克共建微电子创新实验室!2023-10-13 1694
-
感谢东莞理工学院对我司导热系数测试仪的认可2024-06-25 861
-
美国佐治亚理工学院一行莅临达实智能调研2024-09-26 1375
-
美国加州理工学院:研究量子传感技术可实现粒子时空高精度探测2025-05-11 919
-
Wolfspeed与纽约州立大学理工学院加强教育研究合作2025-07-04 1101
全部0条评论

快来发表一下你的评论吧 !

