

ph电极的工作原理(PH电极的特点和分类及用途)
电子常识
描述
一、PH电极的概念
pH电极又称pH探头、pH传感器,英文名称pHelectrode或pHsensor,是PH计上与被测物质接触的部分,用来测电极电位的装置。
二、PH电极的特点
1、采用先进的固体电介质和大面积聚四氟乙烯液接界。不易阻塞,维护方便。
2、长距离的参比扩散途径,极大的延长了电极在恶劣环境中的使用寿命。
3、新型设计的玻璃球泡,增加了球泡面积,可防止内缓冲液中干扰气泡的生成使测量更加可靠。
4、电极采用优质低噪音电缆线,可使信号输出长度大于20米以上无干扰。
三、PH电极分类
1、液体pH电极
液体电极例如InPro2000系列,是一种可填充式液体电极,这种电极是pH电极发明历史上设计最经典、品质最出众、适用范围最广的一款电极,适用于多种工业过程的测量。
2、凝胶pH电极
凝胶电极是升级改良版的液体电极,譬如InPro3250系列,这种电极维护量低,而且适合在要求严格的应用中进行在线测量,它可以在经历数次CIP(原位清洗)和SIP(蒸汽消毒)后仍能长久使用。
3、固体pH电极
固体电极例如InPro4260系列,DXK系列电极、InPro4010、InPro4501和InPro4550,这类电极较普遍用于化工行业,采用了新式固体聚合物参比电解质,进行准确pH测量的同时使用寿命长,即使在最恶劣的工业环境下也可保持良好性能。
四、pH电极的工作原理
PH测量属于原电池系统,它的作用是使化学能转换成电能,此电池的端电压被称为电极电位;此电位由两个半电池构成,其中一个称为测量电极,另一个称为参比电极;此电位遵循能斯特方程:
对于氧化还原体系:
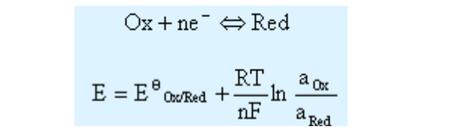
对于金属电极,还原态是纯金属,其活度是常数,定为1,则上式可写作:
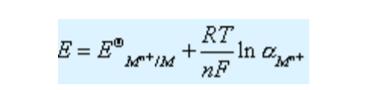
式中:E—电极电位
E0—电极的标准电压
R—气体常数(8.31439焦耳/摩尔和℃)
T—开氏绝对温度(例:20℃=273+293开尔文)
F—法拉弟常数(96493库化/当量)
n—被测离子的化合价(银=1,氢=1)
aMe—离子的活度
对于PH电极。它是一支端部吹成泡状的对于pH敏感的玻璃膜的玻璃管。管内充填有含饱和AgCl的3mol/lkcl缓冲溶液,pH值为7。存在于玻璃膜二面的反映PH值的电位差用Ag/AgCl传导系统,如第二电极,导出。PH复合电极如图
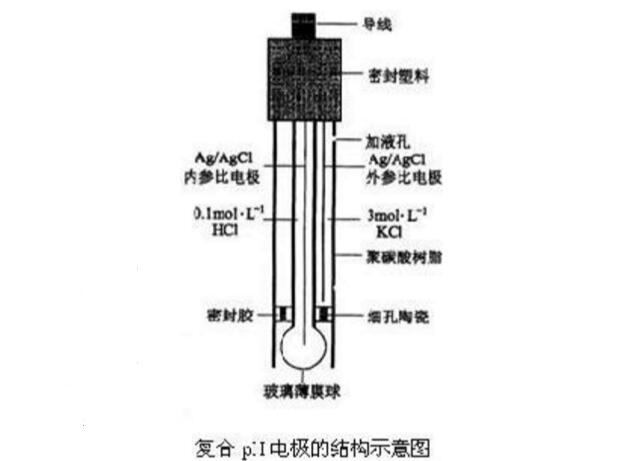
此电位差遵循能斯特公式:
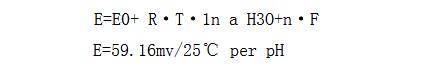
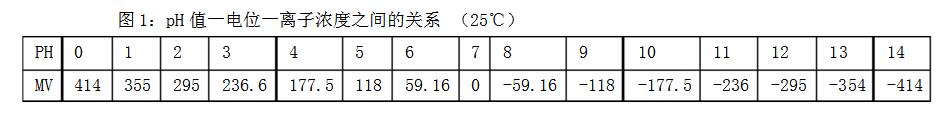
式中R和F为常数,n为化合价,每种离子都有其固定的值。对于氢离子来讲,n=1。温度“T”做为变量,在能斯特公式中起很大作用。随着温度的上升,电位值将随之增大。对于每1℃的温度变大,将引起电位0.2mv/perpH变化。用pH值来表示,则每1℃第1pH变0.0033pH值。这也就是说:对于20~30℃之间和7pH左右的测量来讲,不需要对温度变化进行补偿;而对于温度>30℃或<20℃和pH值>8pH或6pH的应用场合则必须对温度变化进行补偿。
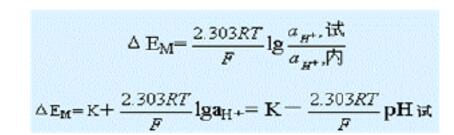
内参比电极的电位是恒定不变的,它与待测试液中的H+活度(pH)无关,pH玻璃电极之所以能作为H+的指示电极,其主要作用体现在玻璃膜上。当玻璃电极浸入被测溶液时,玻璃膜处于内部溶液(αH+,内)和待测溶液(αH+,试)之间,这时跨越玻璃膜产生一电位差ΔEM(这种电位差称为膜电位,下节讨论),它与氢离子活度之间的关系符合能斯特公式:
当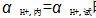 时,
时,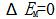 。但实际上
。但实际上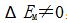 ,跨越玻璃膜仍有一定的电位差,这种电位差称为不对称电位(ΔE不对称),它是由玻璃膜内外表面情况不完全相同而产生的。此式表明玻璃电极ΔEM与pH成正比。因此,可作为测量pH的指示电极。
,跨越玻璃膜仍有一定的电位差,这种电位差称为不对称电位(ΔE不对称),它是由玻璃膜内外表面情况不完全相同而产生的。此式表明玻璃电极ΔEM与pH成正比。因此,可作为测量pH的指示电极。
膜电位理论:
用离子选择性电极测定有关离子,一般都是基于内部溶液与外部溶液之间产生的电位差,即所谓膜电位。膜电位的产生是由于溶液中的离子与电极膜上的离子发生了交换作用的结果。以玻璃电极为例来说明。其要点如下:
玻璃电极在使用前要在纯水中浸泡,离子交换理论认为,当玻璃电极浸入水溶液中时,玻璃表面会吸水而使玻璃溶胀,在它的表面形成溶胀的硅酸层(水化层),这种水化层的是逐渐形成的,只有当玻璃膜浸泡24小时以上后,才能完全形成并趋于稳定。其厚度很薄(约为玻璃膜厚度的1/1000)。同样,膜内表面与内参比溶液接触,亦已形成水化层。在水化层形成的过程中,伴随着水溶液中H+与玻璃种Na+的交换作用(Ca2+结合牢固不易交换),此交换反应可表示如下:
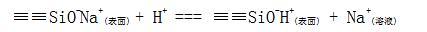
浸泡好的玻璃膜在膜与溶液的界面上存在如下离解平衡:
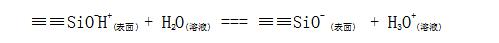
若内部溶液和外部溶液的pH不同,则膜内、外固液界面上电荷分布不同,这样跨越膜的两侧界面就有一个电势差,即膜电位。
当浸泡好的玻璃膜进入待测试液时,膜外层的水化层与试液接触,由于H+活度变化,将使上式离解平衡发生移动,此时,就可能有额外的H+由溶液进入水化层,或有水化层转入溶液,因而膜外层的固液界面上电荷分布不同,跨越膜的两侧界面的电势差发生改变,这个改变与试液中的[H+]有关。
玻璃电极的构造如下图
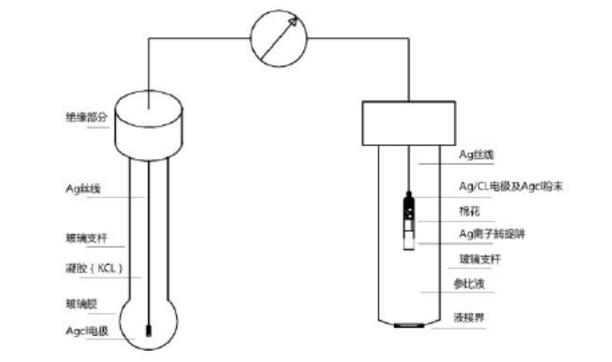
五、PH电极的用途
最初人们对酸碱的意识是入口食物的味道,譬如醋是酸的,柠檬也是酸的,尝起来涩涩的碱面是碱性的,这是pH值或酸碱度最初的由来,简单直观。
以摩尔值表示水相溶液中的氢离子浓度,浓度从100(1)到10-14,再以10为底的负对数换算,pH范围即为0-14。pH是拉丁文pondushydrogenii的缩写,pondus=压强,hydrogenii=氢。因此,更精准的pH值定义应是水相溶液中氢离子活度的负对数值,理解这一点非常重要。您可以因此了解到第一:相对而言,液体更容易实现精确的pH值测量,第二:水相溶液环境里更容易实现精确的pH值测量。
而且,日常生活工作和生产中大部分的pH[1]值测量都是围绕液体工作的。例如人类摄入的食物药物以及液体居多,即使终产品不是液体其来源环境也是液体,譬如人类的液体食物有很多:白酒、啤酒、碳酸饮料、果汁、咖啡和茶叶,pH值影响着食物的风味和品质,pH值是药物生产中的重要指标。而pH值检测并不简单,工业制药生产液态物质比固态物质多得多(由此不难理解工业上水的重要性了),常见工业用水有冷却水、清洗用水、加热水、蒸汽和溶剂用水等,除此之外,还包括需要进一步做环保处理的污水。那么,工业生产中,物质经历着各种变化,相当一部分反应又伴随着氢离子浓度的变化,因此检测水相溶液中氢离子浓度的大小即pH值尤为重要。
精确的pH测量可以帮助实现:
1、生产出我们预期想要的产品
2、尽可能的以最低成本生产
3、防止物料损坏、人员伤亡和环境污染
4、满足法规要求
5、研发工作顺利进行

六、pH电极的保养与维护
1、PH电极平时不使用,可以浸泡在3mol/l的kcl溶液或饱和kcl溶液中,严格禁止将电极浸泡在蒸馏水,去离水或自来水等离子含量极少的液体中。
2、如果PH电极长期干放而暴露在空气中,在重新使用之前,请先将电极浸泡在3mol/l的kcl溶液或饱和kcl溶液中2~3天,使电极恢复活性,如果有条件,请先将电极浸泡在9895电极再生液中1分钟左右,然后再用蒸馏水洗干净,浸泡在3mol/l的kcl或饱和kcl溶液中至少1天才能使用。
3、如果电极敏感膜或白色陶瓷隔膜孔受到蛋白质污染而发黄,可以购买9891电极清洗液,将电极浸泡在其中数小时,然后再用蒸馏水洗干净,最后浸泡在3mol/l的kcl或饱和kcl溶液中至少1天才能使用。
4、如果电极白色陶瓷隔膜孔受到Aq2S污染而变黑,可以购买9892隔膜清洗液,将电极浸泡在其中数小时直至隔膜孔再变白,然后再用蒸馏水洗干净,最后浸泡在3mol/l的kcl或饱和的kcl溶液中至少1天才能使用。
5、如果电极使用时间过长而造成敏感膜老化,可以购买9895电极再生液,将电极浸泡在其中1~10分钟(根据敏感膜老化的程度及斜率决定浸泡时间长短),然后再用蒸馏水洗干净,最后浸泡在3mol/l的kcl和饱和kcl溶液至少1天才能使用,严格禁止将斜率在56mv/ph以上的PH电极用9895处理,因为9895电极再生液中含有HF溶液,9895的原理就是用HF将表面的敏感膜老化层腐蚀掉,如果新电极浸泡在9895的电极再生液中或旧电极浸泡在其中时间过长,HF会将好的敏感膜部分也腐蚀掉。
6、如果PH电极被无机物质污染可以用0.1mol/l的Hcl或NaOH溶液清洗数分钟,然后再用蒸馏水洗干净。
7、如果PH电极被有机物质污染,可以用酒精或丙酮清洗,然后再用蒸馏水洗干净。
8、如果你知道用何种物质可以将污染电极的物质溶解,你就用何种物质清洗。
9、请切记,用9891、9892或9895处理过的PH电极,请勿马上校准或测量,因为那时电极无法进行测量,必须将电极浸泡在3mol/l或饱和kcl溶液中至少1天才能使用。
10、PH电极上端和电缆线相连接处的接头是高阻抗部件,禁止用水等液体浸泡或蒸气等潮湿空气侵蚀,可以用新电极所带的红色小螺帽盖住,电极电缆的接头也属于高阻抗部件,严禁用水等液体浸泡或蒸气等潮湿空气侵蚀,一定要存放在干燥处。
- 相关推荐
-
按照OPA129U的PH电极信号的放大的参考设计做了一个电路,结果接上PH电极后,电压输出不稳定,为什么?2024-09-23 0
-
[转帖]PH和ORP电极2010-05-13 0
-
PH电极信号放大问题2013-10-22 0
-
罗斯蒙特PH计 396P-02-12-55 pH电极2019-07-22 0
-
ph电极问题,新探头校准液正确2022-06-25 0
-
PH计特点及型号2017-10-26 1624
-
ph计电极保护液是什么_ph计电极保护液怎么配_酸度计电极保护液配置2017-12-26 111303
-
ph计复合电极构造_ph计复合电极的使用方法_ph计复合电极怎么维护2017-12-28 19409
-
PH传感器的工作原理_PH传感器的使用方法2018-03-20 55215
-
PH电极电路原理图免费下载2019-03-19 2764
-
PH电极的浸泡方法/检查/使用寿命2021-03-14 22817
-
PH电极电路原理图2021-06-15 1698
-
ph电极的维护与保养是怎样的2022-01-11 2121
-
在线PH计电极寿命有多久受什么影响2022-11-23 3132
-
ph传感器的工作原理 ph传感器的使用方法2024-02-03 5581
全部0条评论

快来发表一下你的评论吧 !

