

国科大在光功能材料研究中取得进展
描述
近日,中国科学院大学化学科学学院教授田志远课题组在近红外(near-infrared,NIR)光学活性材料的设计构建及生物应用研究中取得进展,设计构建了具有双光子激发、近红外发射特性的仿生荧光探针并成功将其应用于活体肿瘤的高清晰度荧光成像。
由于具有高灵敏度、优良的时-空分辨率、相对于其它技术而言的良好生物兼容性等特性,基于光学活性材料的荧光探测及诊疗技术已在生命科学及生物医学领域发挥日益重要的作用。生物荧光成像需要由外源性荧光团提供读出信号或增强成像的对比度,这使得荧光探测手段的功效在很大程度上取决于荧光探针的性能。传统生物荧光成像所使用的荧光探针多以可见光作为激发源、而且信标光位于可见光区;而对于以深源的细胞或组织为探测目标的应用而言,这类激发光和信标光都位于可见光区的荧光成像会在穿透深度上受到很大限制。
针对以上问题,田志远带领的低维光学活性材料与生物探测实验室近年来在新型荧光探针的设计构建及其生物探测方面开展了系统研究:设计构建了用NIR光通过双光子吸收过程进行激发、发射NIR荧光的复合型聚合物荧光探针,其荧光成像穿透深度可高达1.2毫米、对深置目标及具有一定厚度的生物样品进行成像具有实用意义(ACS Applied Mater. Interfaces,2015,7,20640-20648);设计合成了一类可用NIR光触发、具有良好的生物兼容性及隐身能力、优越的氧气通透性及对活性单重态氧的递送能力、可进行程序化递送的光动力学治疗(PDT)纳米载体,实现了对模型小动物肿瘤极为有效的光动力学治疗效果(Nanoscale,2015,7,9806-9815);构建了具有超常斯托克斯位移(大于200nm)的NIR荧光开关探针,基于超常的斯托克斯位移、NIR荧光信号、及动态比照荧光开关转换三重机制的共同作用,成功克服背景噪音的干扰、将细胞内荧光成像的灵敏度提高两个数量级(ACS Appl. Mater. Interfaces,2016,8,4399-4406)。
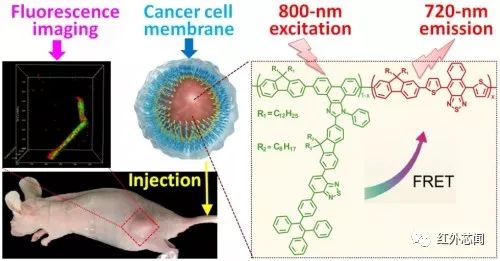
在前期工作的基础上,田志远课题组在近日设计并合成了将具有双光子激发特性的能量捕获单元和能发射NIR荧光的能量受体单元集成到了聚合物分子链中的新型嵌段共聚共轭聚合物,并基于这种光学活性聚合物构建了肿瘤细胞膜包覆的、可实现NIR光激发、NIR荧光发射的“NIR input-NIR outgoing”的仿生荧光探针。这种荧光探针以波长在具有最大光通透性的生物窗口范围的光(700-1000nm)为激发源且具有双光子激发荧光(two-photon excited fluorescence,TPEF)特性,无需将能量给体与受体进行掺杂,在确保探针结构稳定性的前提下实现高的荧光成像穿透深度。该探针所具有的高度特异性靶向能力及对活体肿瘤的高清晰度荧光成像能力在模型荷瘤小鼠实验中得到了充分验证。
国科大在光功能材料研究中取得系列进展 相关研究成果发表在ACS Nano上,第一作者为博士研究生吕岩霖。该研究得到了国家自然科学基金委、中科院率先行动“百人计划”、国科大的资助,以及中科院过程工程研究所生化工程国家重点实验室研究员马光辉、魏炜课题组,哈尔滨工业大学材料科学与工程学院教授张勇课题组的合作。
-
本源量子和中科大团队合作在非绝热几何量子计算领域取得重要进展2023-05-08 1229
-
本源量子参与的可滑动纳米机电谐振器研究取得重要进展2022-11-03 1245
-
本源量子联合中科大研究团队在二维材料栅控量子点器件研究方向取得新进展2022-05-21 1661
-
中国科大在多参数量子精密测量研究中获得重大发现2021-02-24 1836
-
利用六光子系统实验在高维量子通信中取得重要进展2020-12-21 2025
-
我国在新型高性能钾离子电池的负极材料研究方面取得新进展2020-03-23 1739
-
中科大在人工智能领域取得了最新的技术性突破2019-11-11 5824
-
中科院科学家在实现高效圆偏振发光材料方面获得进展2019-06-06 9784
-
中国科学院在薄膜太阳能电池材料的研究方面取得新进展2018-05-30 3821
-
中科大量子存储研究再获新进展2016-12-07 1155
-
光互连技术的研究进展2016-01-29 2551
-
微电子所在阻变存储器微观机制研究中取得系列进展2012-04-13 1480
-
微电子所在阻变存储器研究中取得新进展2010-12-29 2190
-
锂离子电池合金负极材料的研究进展2009-10-28 4778
全部0条评论

快来发表一下你的评论吧 !

