

经颅电刺激适应症系列之tDCS对抗疲劳
描述
关键脑区与疲劳调控
前额叶皮层是疲劳调控的核心区域。通过孟德尔随机化分析发现,右侧外侧眶额叶、左/右尾中额叶和右侧吻侧中额叶的灰质体积与疲劳风险显著负相关。体积较大的个体在警觉性任务中表现更优,表明这些区域通过调节注意力和情绪降低疲劳感。
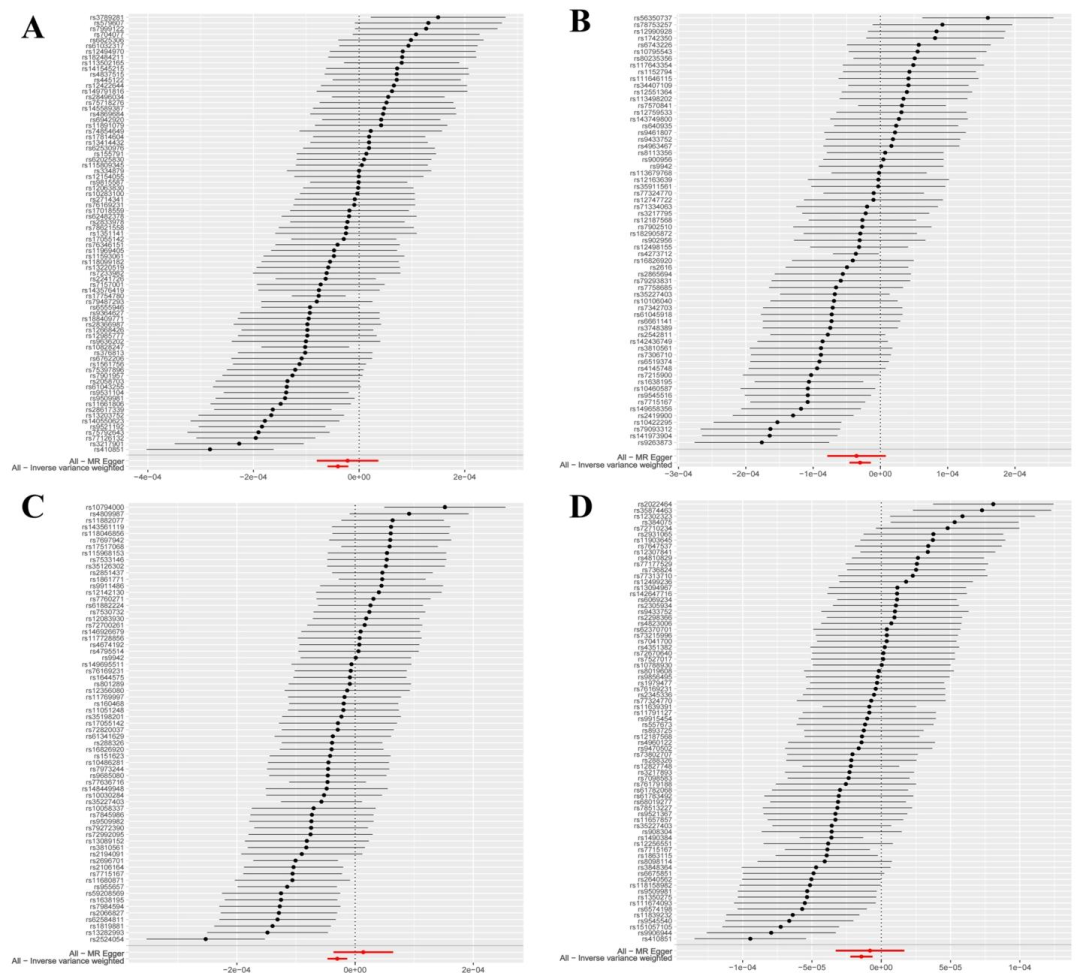
四个脑区与发生疲劳的风险显著呈负相关
此外,前扣带回皮层(ACC)整合奖励价值与能量消耗信息,决定是否继续任务,当能量成本超过预期奖励时,ACC活动减弱,触发疲劳信号。
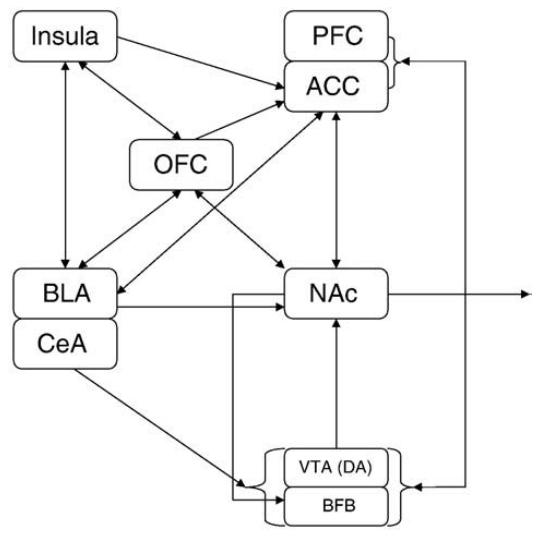
奖赏价值和厌恶价值进行编码后传递到前扣带回皮质(ACC)
伏隔核(NAc)和眶额叶皮层(OFC)也参与疲劳机制。伏隔核通过多巴胺信号调节动机强度,而OFC评估任务奖励与风险。动物实验显示,NAc多巴胺耗竭会减少高努力选项的选择,说明其直接关联努力决策。
基因调控与氧化应激
通过基因共定位分析,发现ECE2、GPX1和SNF8在额叶皮层中与疲劳显著相关。大鼠实验显示,中枢疲劳大鼠模型行为测试表现出学习记忆下降等症状,以及中枢疲劳大鼠模型额叶皮质中这些基因的mRNA水平显著升高。
ECE2:与神经退行性疾病相关,可能通过调节β-淀粉样蛋白代谢影响疲劳。
GPX1:作为抗氧化酶,在氧化应激状态下表达增加,清除自由基以维持神经元功能。
SNF8:参与自噬功能,突变可能导致能量代谢异常。
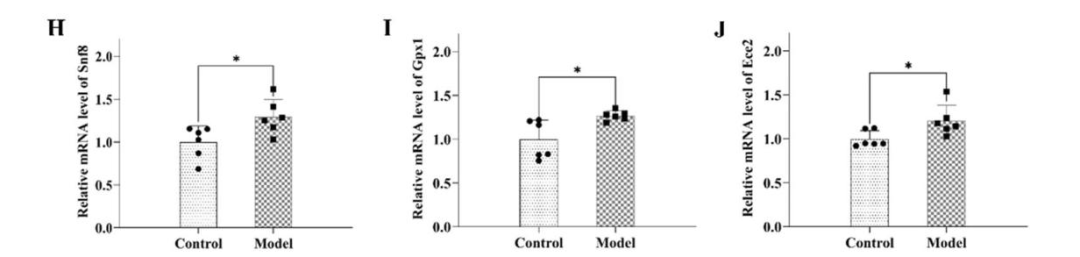
中枢疲劳大鼠模型额叶皮质中Snf8、Gpx1 和 Ece2 相对表达水平显著升高
能量成本与奖励评估系统
疲劳源于能量消耗与奖励的失衡。脑岛监测生理状态(如血糖水平),ACC整合脑岛、OFC和杏仁核的信息,判断是否继续投入能量。当能量成本超过奖励时,多巴胺活性下降,动机减弱,引发主观疲劳感。例如,长时间工作后,OFC对奖励的估值降低,而脑岛信号增强,最终ACC判定“不值得努力”,则产生疲劳感。
HUIYING
tDCS缓解疲劳的神经机制
靶向调节前额叶皮层
tDCS通过阳极刺激背外侧前额叶(DLPFC,F3区域),增强神经元兴奋性。2 mA电流持续30分钟可提升警觉性任务表现,效果持续6小时以上。其原理包括:
抑制腺苷积累:疲劳时脑内腺苷水平升高,阻断多巴胺释放。tDCS可能通过调节腺苷A1受体,减少其抑制作用。
增强多巴胺传递:刺激DLPFC间接激活中脑多巴胺通路,提升伏隔核和ACC的多巴胺水平,增强动机。
神经可塑性与持续效应
tDCS的长期效果(>6小时)源于突触可塑性变化,类似长时程增强(LTP)。30分钟刺激可诱导胶质细胞释放神经递质,维持神经元兴奋性。此外,tDCS改善资源理论相关的认知资源损耗,而非仅提升觉醒水平,因此对抗疲劳效果更显著。
HUIYING
临床研究验证:tDCS vs咖啡因
研究方法
实验研究对象为30名军人,分为三组:
tDCS组:30分钟2 mA阳极刺激+安慰剂口香糖。
咖啡因组:200 mg咖啡因口香糖+假刺激。
对照组:假刺激+安慰剂。
实验在30小时持续清醒后进行,在 04:00 接受不同处理(tDCS + 安慰剂口香糖、假 tDCS + 安慰剂口香糖、咖啡因口香糖 + 假 tDCS),期间定时进行任务和问卷评估(评估警觉性、工作记忆和主观疲劳)。
研究结果
警觉性任务(Mackworth 时钟测试):tDCS 组准确性显著高于假刺激组和咖啡因组,且在 04:00、08:00 表现更优。
工作记忆任务(DMS):咖啡因组和 tDCS 组反应时均优于假刺激组,但组间差异不显著,且对分数 / 准确性无明显影响。
心理运动任务(PVT):咖啡因组和 tDCS 组平均反应时均优于假刺激组,组间无显著差异,对其他心理运动指标无影响。
主观疲劳问卷:tDCS 组在困倦、精力等方面主观感受优于假刺激组,在疲劳、综合情绪等方面也有优势,且 tDCS 组准确性变化与主观情绪无关,而咖啡因组和假刺激组相关。
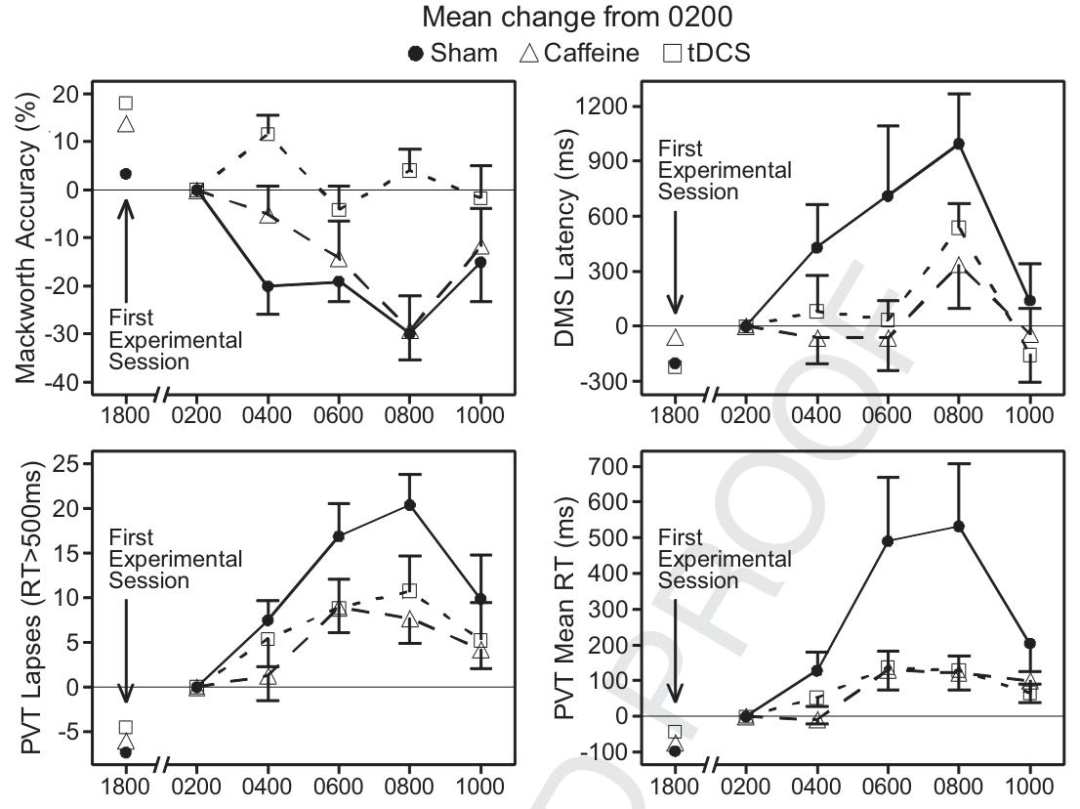
各性能任务相对于凌晨 2 点(基线)的平均变化情况
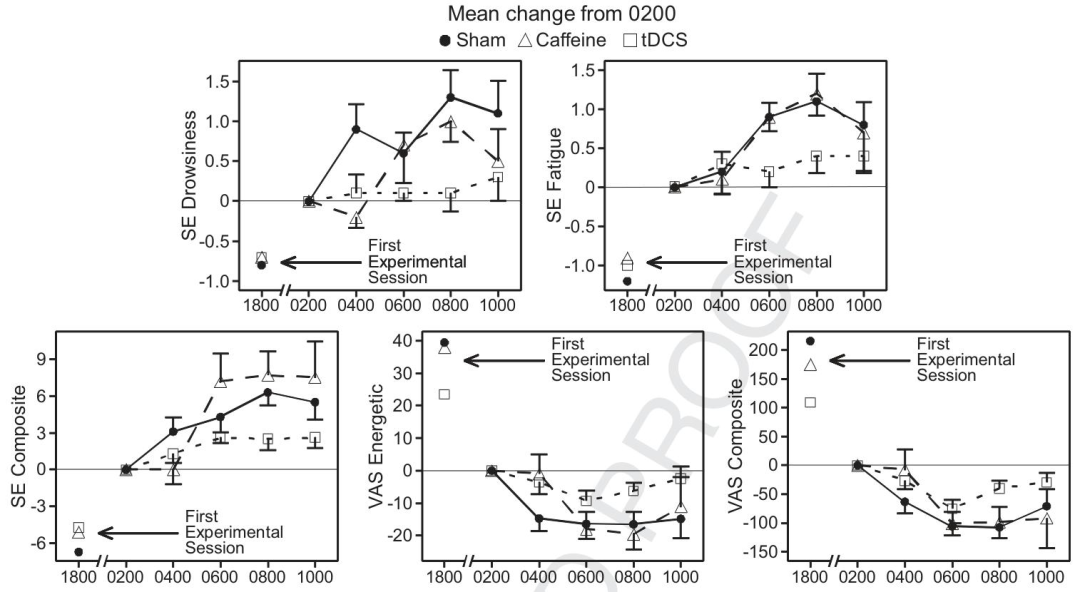
疲劳主观测量值相对于凌晨 2 点(基线)的平均变化情况
副作用与适用性
tDCS组仅报告轻微头皮刺痛,而咖啡因可能引发焦虑和心率升高。长期使用咖啡因效果递减,而tDCS无耐受性报告。
研究结论
tDCS 在提高警觉性方面比咖啡因更有效,效果持续至少 6 小时,且能改善情绪,减少疲劳和困倦感。两者对工作记忆和心理运动表现的影响相似。tDCS 或可作为抗疲劳的有效替代方法,但长期使用效果和更高剂量的影响有待进一步研究。
HUIYING
tDCS治疗参数
参数类别
| 设置详情
|
阳极
| F3(10-20 EEG系统定位)
|
阴极
| 对侧右三角肌(减少皮层外效应)
|
电极阵列
| 5个银/氯化银EEG电极
|
成人tDCS
| 电流:1-2 mA,时间:20分钟,频率:每日按需
|
青少年tDCS
| 电流:0.5-1 mA,时间:20分钟,频率:每日按需
|
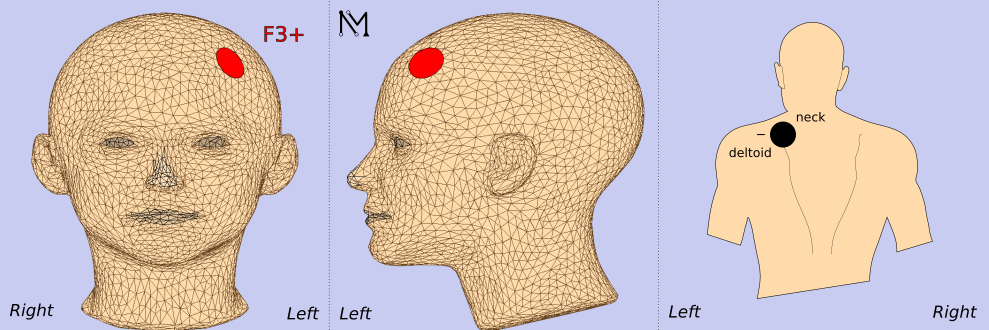
电极位置示意图
安全性与禁忌症:癫痫史、颅内金属植入物、皮肤损伤。
总结
tDCS通过靶向前额叶皮层,调节多巴胺和腺苷系统,显著改善警觉性和主观疲劳感,且效果持久。结合基因研究发现,未来可针对ECE2、GPX1等靶点开发个性化干预方案。这一方案为军事、医疗等高疲劳风险职业提供了新的应对策略。
HUIYING
回映产品
1.便携式HD-tES
回映便携式高精度经颅电刺激仪(HD-tES)创新地采用type-C转生物电极的设计使得产品能够非常便捷地被使用。回映便携式高精度经颅电刺激仪(HD-tES)通过多电极配置(1个中心电极和4个返回电极)实现高精度电流聚焦,精准刺激目标脑区。其核心优势在于通过缩小电极尺寸(直径12mm的环形电极)和增加电极数量,显著提升刺激的聚焦性和精准性。
HD-tDCS模式:调节皮层兴奋性,适用于中风康复、抑郁症干预等。
HD-tACS模式:精准锁定脑电频段(如β-γ频段改善强迫症,4Hz增强工作记忆)适配认知障碍治疗等。
HD-tRNS模式:HD-tRNS 对显式和隐式计时任务的影响不同,用于研究大脑的计时机制和时间处理能力等。
适用范围:神经系统疾病治疗,意识障碍和认知功能调节,康复治疗,运动和认知功能恢复。

回映自研type-C转生物电极示意图
基本参数
刺激强度:-2mA~2mA 连续可调,调节分辨率0.01mA,输出电流误差 <=±10%;
刺激时间:0~60min 可调;
刺激频率:针对于 tPCS/tACS 模式,1Hz ~ 99Hz范围内可调,频率步进1Hz, 输出频率误差<=±5%;
淡入淡出时间:0~120s 可调,确保刺激的安全性;
脱落检测:通过实时阻抗检测分析电极脱落状态确保刺激有效性;
相位同步:<=±2.5us; <=0.09°;
2.手持式tES
经颅电刺激调控设备采用低强度的电流(±2mA以内)对大脑皮层的靶区域进行刺激,进而达到调节大脑皮层神经元兴奋性、调节脑电波节律、促进神经重塑和修复、改善脑部供血等。
经颅直流电刺激(tDCS):治疗精神分裂症、抑郁症、物质成瘾、阿尔茨海默病、脑卒中后的运动功能障碍、语言障碍、认知障碍等
经颅交流电刺激(tACS ):治疗视功能障碍、认知障碍,提高学习能力、工作记忆等
经颅脉冲电刺激(tPCS):增强运动技能,缓解疲劳,促进知觉学习任务、算术任务,调节注意力切换任务的准确性,改善帕金森病患者的步态平衡等
经颅随机噪声刺激(tRNS):治疗耳鸣,提高工作记忆、认知能力等
适应症:焦虑、抑郁、失眠、癫痫、强迫症、注意缺陷多动障碍、巩固记忆、运动控制等。

回映便携式tES设备示意图
基本参数
刺激强度:10mA~30mA 连续可调,调节分辨率0.01mA,输出电流误差<=±10%
刺激频率: 1Hz~99Hz 范围内可调,频率步进为 1Hz,输出频率误差 <=±5%
载波频率: 2KHz~100KHz 范围内可调,频率步进为 1KHz,输出频率误差 <=±1%
刺激时间:0~60min可调
淡入淡出时间:0~120s 可调,确保刺激的安全性
脱落检测: 通过实时阻抗检测分析电极脱落状态确保刺激有效性
参考文献
1.Mapping fatigue: discovering brain regions and genes linked to fatigue susceptibility(作者Yifei Zhang, Zehan Zhang, Qingqian Yu, Yutong Jiang, Chenyu Fei, Fengzhi Wu and Feng Li)
2.Mental fatigue: Costs and benefits(Maarten A.S. Boksem,b,d,, Mattie Topse)
3.A Comparison of the Effects of Transcranial Direct Current Stimulation and Caffeine on Vigilance and Cognitive Performance During Extended Wakefulness(Lindsey K. McIntire a, R. Andy McKinley b, Chuck Goodyear a, Justin Nelson a)
-
经颅超声脉冲刺激(TPS)适合干预哪些适应症?2026-02-28 322
-
闭眼是tDCS经颅电刺激的最佳状态?2026-02-04 405
-
时间干涉经颅磁刺激TI-TMS是经颅磁的未来吗2025-09-17 2360
-
经颅电刺激系列之时域相干电刺激tTIS2025-08-25 8571
-
经颅电刺激系列之交叉短脉冲刺激 ISP2025-06-21 4189
-
经颅电刺激系列之调幅经颅电刺激AM-tACS2025-06-18 1467
-
经颅电刺激系列之otDCS 振荡经颅直流电刺激2025-06-09 2498
-
经颅电刺激适应症系列之tDCS提高数学能力2025-04-30 1632
-
经颅电刺激适应症之tDCS治疗注意力缺陷ADHD2025-04-22 143
-
经颅电刺激适应症系列之改善抑郁情绪2025-04-15 1779
-
经颅电刺激系列之高精度经颅电刺激HD-TES2025-02-15 4343
-
经颅电刺激系列之高强度经颅交流电刺激Hi-tACS2025-02-10 3679
-
经颅直流电刺激对孤独症谱系障碍儿童脑电的研究2022-02-21 808
-
经颅直流电刺激技术介绍2021-09-15 760
全部0条评论

快来发表一下你的评论吧 !

