迷走神经电刺激适应症之taVNS缓解认知障碍
描述
轻度认知障碍(MCI)是痴呆前期的关键阶段,抑郁症状作为MCI常见共病,可使痴呆转化风险增加2.3倍。全球约15.5%的老年人患有轻度认知障碍(MCI),其中23.8%将进展为阿尔茨海默病(AD)。目前胆碱酯酶抑制剂等药物治疗存在疗效有限、副作用明显等问题,而单克隆抗体类药物成本高昂(年治疗费用约5.6万美元),临床亟需安全有效的替代疗法。经皮耳迷走神经刺激(taVNS)融合中医耳穴理论与现代神经调控技术,通过耳甲部迷走神经分支刺激实现无创干预。
HUIYING
认知障碍的神经生理基础
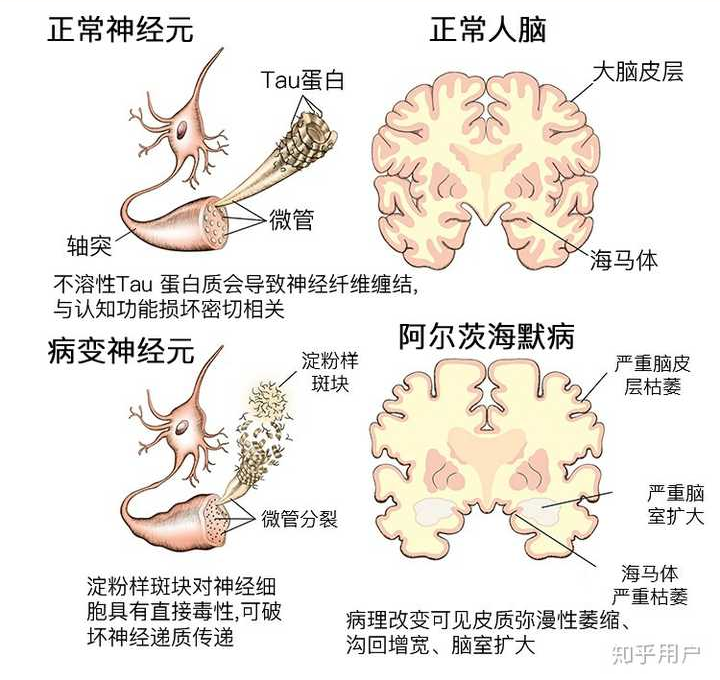
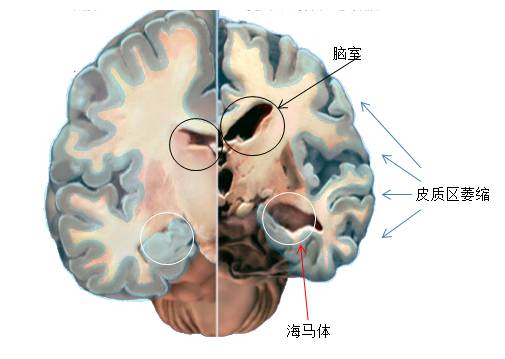
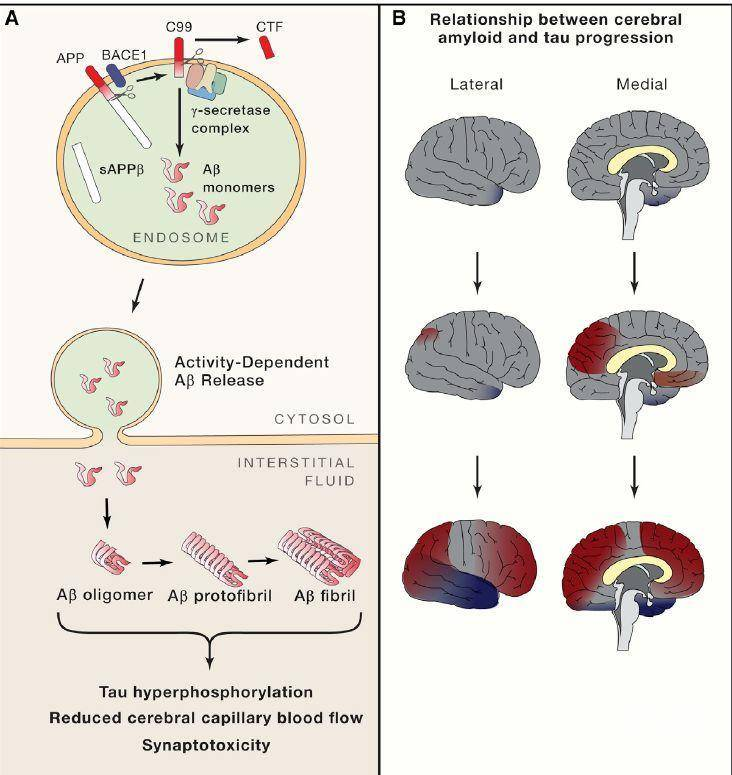
认知障碍的典型分子病理解释就是:Aβ形成斑块,tau蛋白形成神经纤维缠结,共同危害神经元健康。
神经递质系统失调
认知障碍的核心神经生理机制涉及多种神经递质系统的失衡:
去甲肾上腺素(NE)系统:蓝斑核(LC)是NE的主要合成来源,其退化与阿尔茨海默病(AD)早期病理密切相关。LC神经元减少导致NE释放不足,影响记忆巩固、注意力调控和突触可塑性。在AD患者中,LC的tau蛋白沉积早于其他脑区,加速认知衰退。
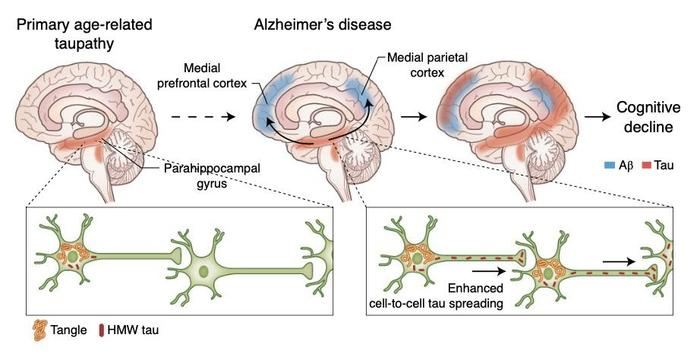
tau 蛋白病变的脑区扩散及神经元间传播过程图
乙酰胆碱(ACh)系统:基底前脑的基底核(nbM)是胆碱能神经元的主要集群,其退化导致海马体和皮层ACh水平下降,直接损害记忆编码和执行功能。AD患者的胆碱乙酰转移酶(ChAT)活性降低。
GABA能系统:抑制性神经递质GABA的失衡可能导致神经网络过度兴奋或抑制不足。老年人群中,前额叶GABA水平下降与工作记忆衰退相关。
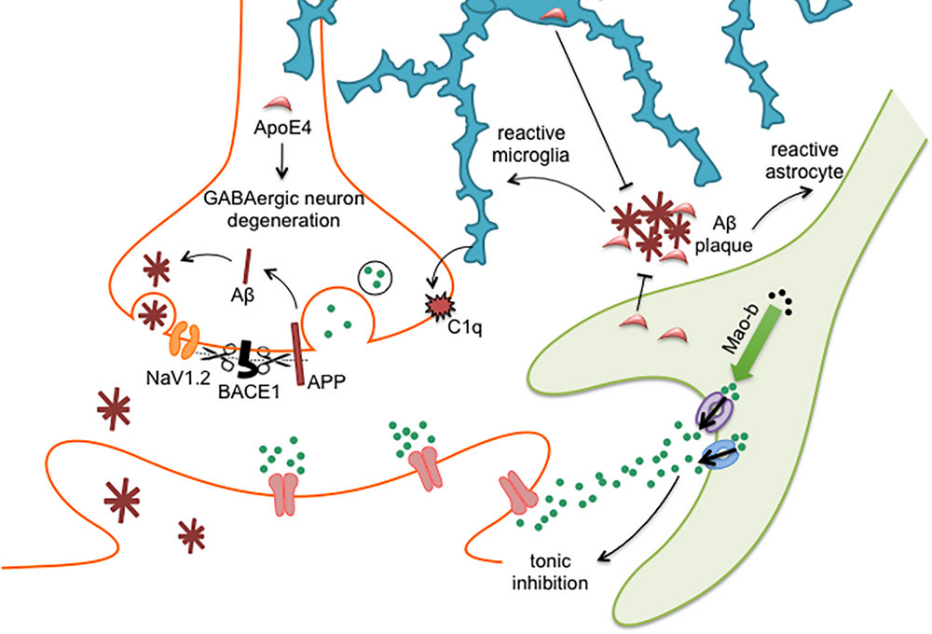
大脑中导致GABA能系统功能异常的机制
神经炎症与免疫机制
慢性神经炎症是认知障碍的重要驱动因素:
小胶质细胞激活:在AD和血管性痴呆(VD)中,小胶质细胞过度激活释放促炎因子(如TNF-α、IL-1β),导致神经元损伤和突触丢失。动物模型中,脂多糖(LPS)诱导的炎症可显著损害海马依赖性记忆。
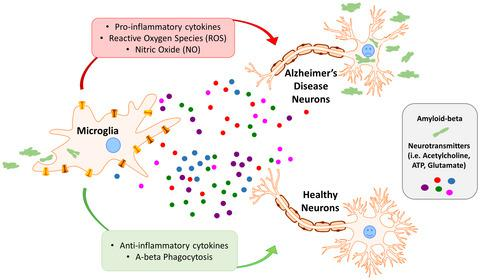
AD中神经元和小胶质细胞的交流
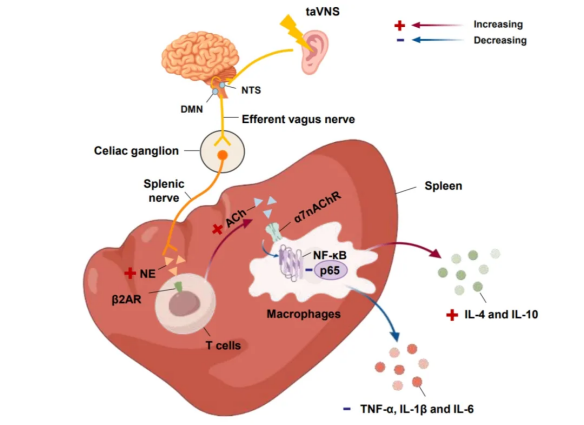
胆碱能抗炎通路(CAIP):迷走神经通过激活α7烟碱型乙酰胆碱受体(α7nAChR)抑制外周和中枢炎症反应。AD模型大鼠中,tVNS上调α7nAChR表达,减少海马IL-1β水平。
脑区功能连接异常
海马体萎缩:AD患者海马体积减少与情景记忆衰退直接相关。MRI研究显示,早期AD患者的海马激活减弱。
默认模式网络(DMN)失调:DMN(包括内侧前额叶、后扣带回)在静息态下活性异常升高或降低,与AD和轻度认知障碍(MCI)的病理进展相关。
颞极与内侧眶额回:颞极负责语义记忆和社会情感整合,其功能异常常见于MCI伴抑郁患者。
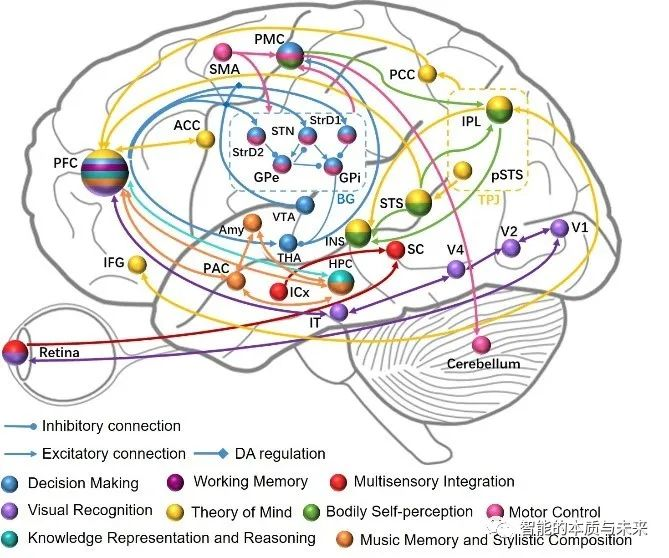
整合的多项认知功能以及对应的脑区和神经环路
HUIYING
taVNS缓解认知障碍的机制
神经递质调节
taVNS通过迷走神经-脑干-皮层通路调控神经递质释放:
NE释放增强:刺激耳甲艇激活孤束核(NTS)和LC,提升NE水平。fMRI研究显示,taVNS后LC的信号显著增强。NE通过β-肾上腺素受体增强前额叶突触可塑性。
ACh通路激活:taVNS通过NTS间接刺激的胆碱能神经元,提高海马ChAT活性。AD模型大鼠中,taVNS减少β-淀粉样蛋白沉积,改善空间记忆。
GABA能平衡:taVNS增强脊髓三叉神经核的GABA释放,抑制杏仁核过度反应,缓解焦虑相关认知障碍。
抗炎与神经保护
抑制促炎因子:taVNS通过迷走神经-脾脏轴减少外周TNF-α和IL-6水平。在LPS诱导的炎症模型中,taVNS显著降低海马TNF-α浓度。
调节小胶质细胞表型:taVNS促进小胶质细胞从促炎表型(M1)向抗炎表型(M2)转化。AD小鼠模型中,taVNS减少CD68(M1标志物)表达,延长神经元存活。
taVNS 调节免疫系统
脑网络功能重塑
增强DMN连接:taVNS干预后,MCI患者内侧前额叶与后扣带回的功能连接增强,静息态网络协调性改善。
颞极与内侧眶额回激活:个案fMRI显示,taVNS治疗后右侧颞极的ALFF(低频振幅)和ReHo(局部一致性)值升高。
HUIYING
临床实验研究验证
随机双盲对照试验
Wang等(2022)对52例MCI患者进行24周随机双盲试验:
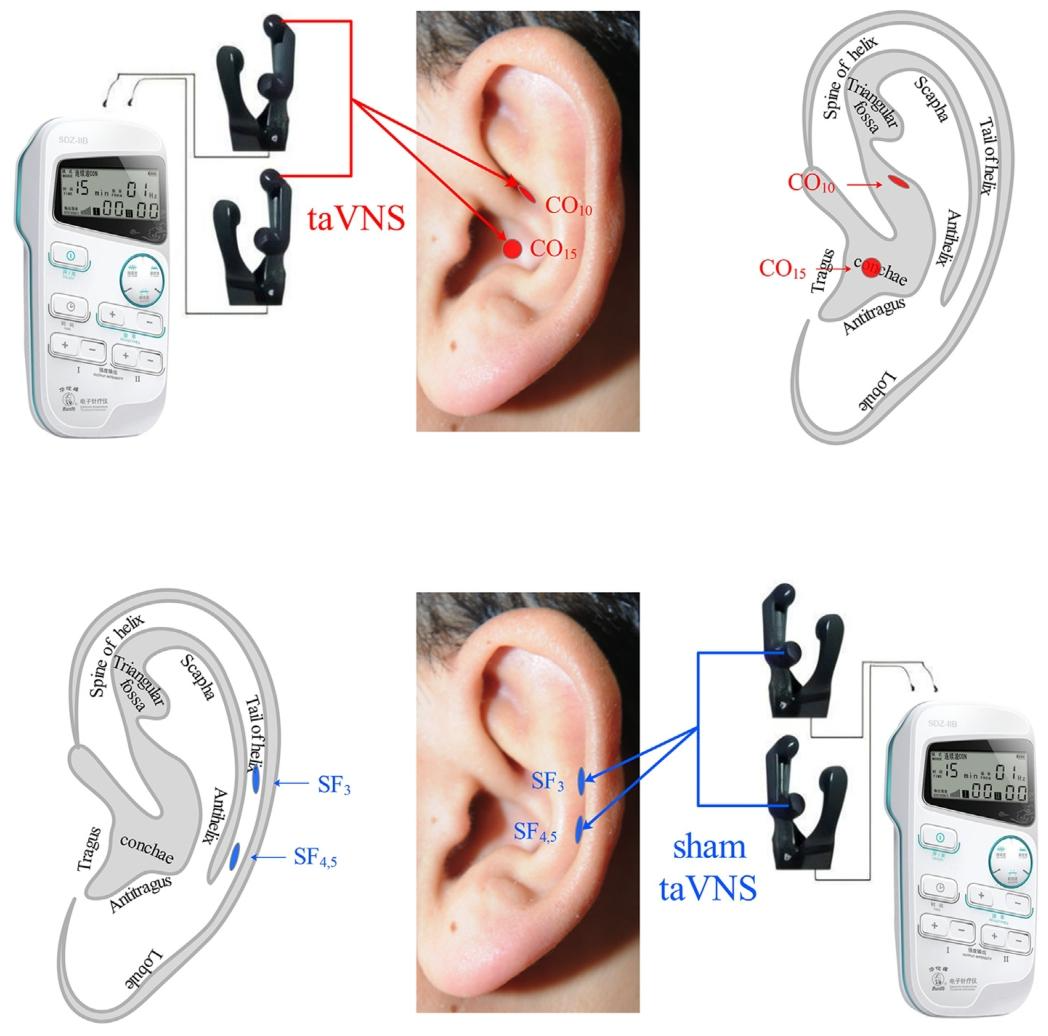
干预组(taVNS):刺激耳甲区心(CO15)、肾(CO10)穴,使用20/100 Hz疏密波,强度0.6–1.0 mA,每日2次,每次30分钟。
对照组(假刺激):刺激耳舟区肘(SF3)、肩(SF4.5)穴,参数相同。
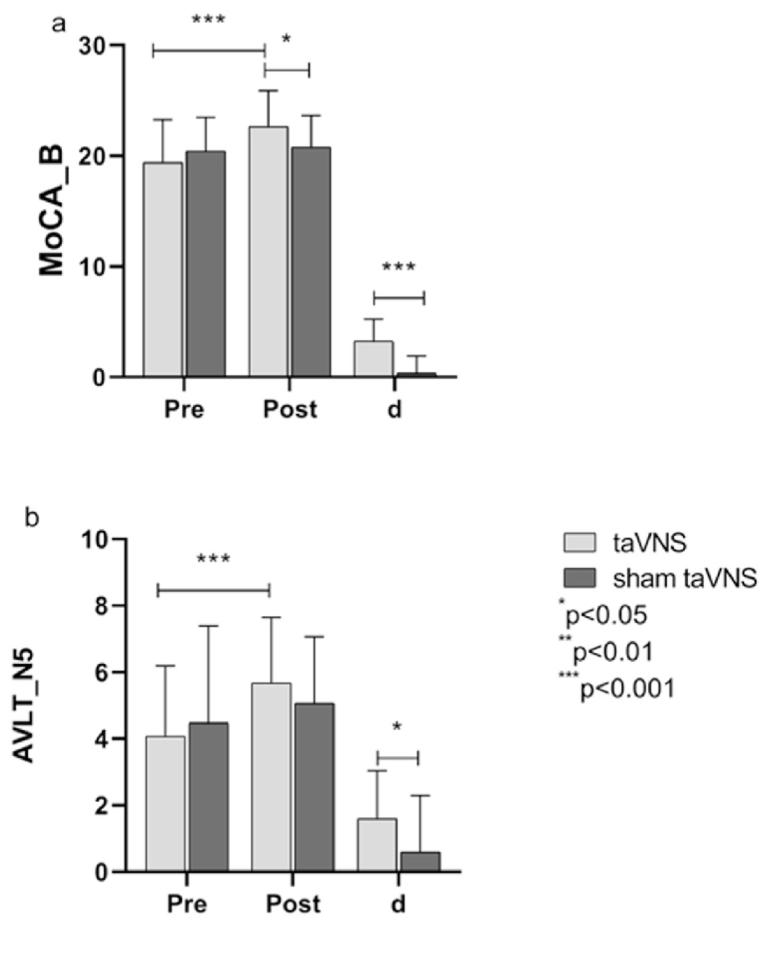
结果:taVNS组MoCA-B总分显著提高(p=0.033),AVLT-H的NS(即时回忆)和N7(延迟回忆)评分均显著增加(p<0.001)。
蒙特利尔认知评估(MoCA-B)(a)、听觉言语学习测验(AVLT)(b)测验评分
taVNS 组在多个认知和睡眠相关指标上有显著改善,如听觉言语学习测验部分指标、波士顿命名测试、睡眠质量相关指标、功能活动问卷等。taVNS 组 1 例鼓膜穿孔史患者出现轻微不良反应,停药 1 周后恢复,两组均未出现严重不良反应。
多模态脑成像研究
通过fMRI发现:
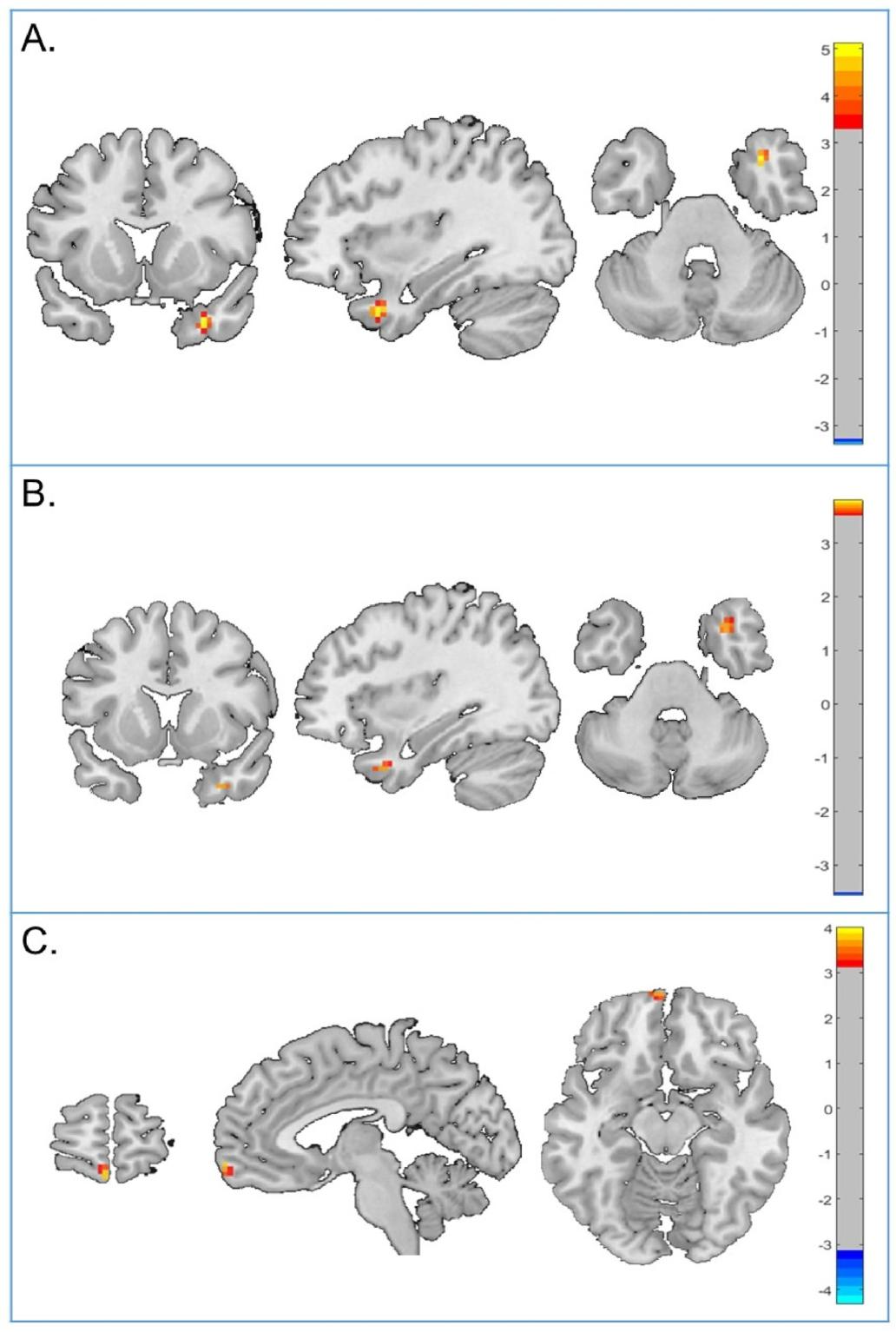
taVNS治疗后,MCI患者左侧前扣带-右侧扣带功能连接(FC)增强(p<0.05)。
颞极与内侧眶额回的ALFF值升高,与执行功能改善相关(p=0.016)。
taVNS治疗前后的脑功能活动变化
治疗后患者认知功能和情绪显著改善,右侧颞极上部、左侧额叶眶内侧脑功能活动增强,这些脑区与认知和情绪相关。
HUIYING
具体治疗参数
刺激部位:耳甲区心(CO15)、肾(CO10),位于迷走神经耳支分布区。
刺激参数:
频率:20 Hz(10 s)与100 Hz(50 s)交替的疏密波。
强度:0.6–1.0 mA,根据个体耐受性调整。
时长:每日2次,每次30分钟,每周5天,持续24周。
HUIYING
回映产品
经皮耳迷走神经刺激(taVNS)
本产品采用经皮耳迷走神经刺激(taVNS)技术,通过非侵入性电刺激耳甲腔及耳甲艇的迷走神经分支,精准调控耳部迷走神经分支(耳甲腔CO10、耳甲艇CO15等穴位);具有多种刺激模式、信号调节范围大,直接作用于神经生理机制,可适用于睡眠障碍、焦虑症状、认知障碍、乏力、食欲减退、偏头痛、以及癫痫等多种疾病的辅助治疗。
经皮耳迷走神经刺激(taVNS)
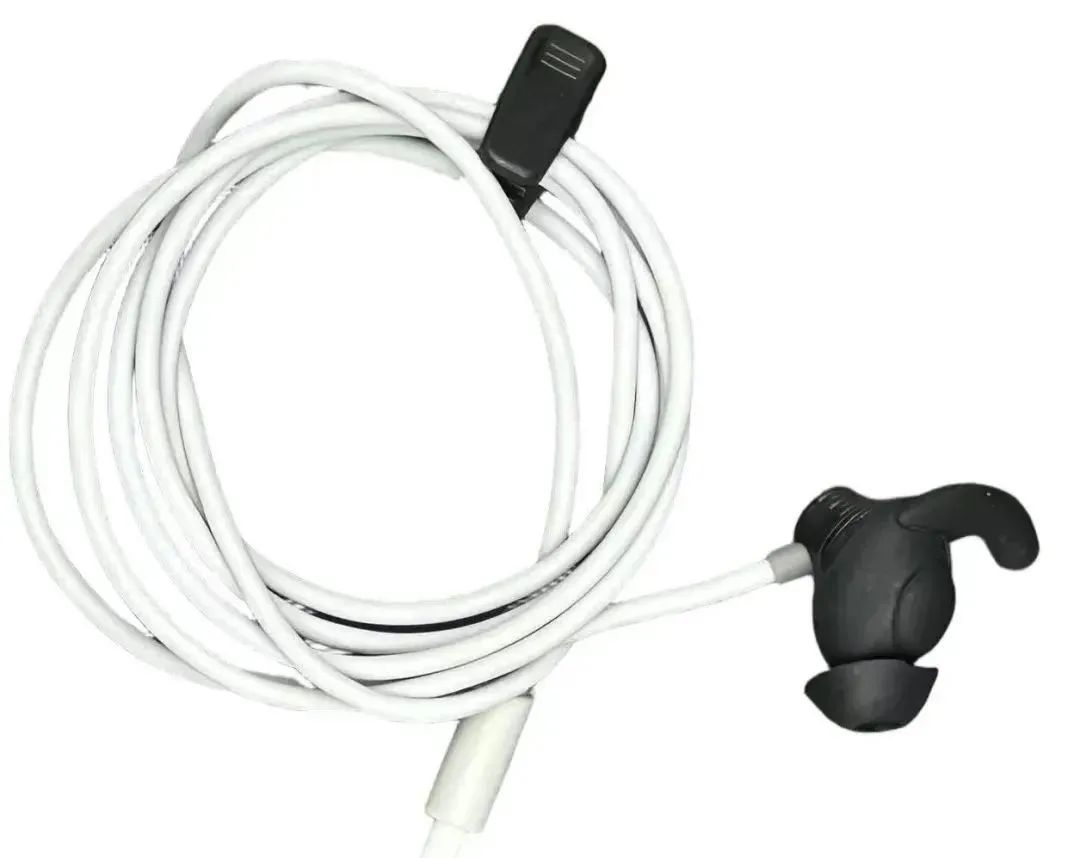
回映自研经耳迷走神经电刺激耳甲电极
基本参数
刺激强度:0 - 30mA;
刺激频率:1 - 200Hz;
刺激脉宽:100 - 1000us;
刺激维持ON状态:1 - 500s;
刺激间歇OFF状态:1 - 500s;
淡入淡出时间:0 - 10s.
声明:本文内容及配图由入驻作者撰写或者入驻合作网站授权转载。文章观点仅代表作者本人,不代表电子发烧友网立场。文章及其配图仅供工程师学习之用,如有内容侵权或者其他违规问题,请联系本站处理。
举报投诉
-
超微型化闭环迷走神经刺激系统(CLV)如何实现(中风)2025-10-29 505
-
呼吸门控闭环经皮迷走神经刺激(taVNS)系统2025-09-27 900
-
Aigtek宽带功率放大器赋能无创迷走神经无线电刺激新策略2025-09-10 491
-
呼吸门控闭环经耳迷走神经电刺激taVNS如何缓解抑郁2025-08-22 1654
-
经皮耳迷走神经刺激(taVNS)与心脑轴交互2025-08-06 2230
-
闭环经皮耳廓迷走神经刺激(taVNS)与 EEG、HRV 的技术融合2025-07-14 2652
-
闭环 taVNS 刺激对中风后上肢运动功能的改善治疗2025-07-07 734
-
taVNS经耳迷走神经电刺激适应症之缓解偏头痛2025-05-21 2279
-
taVNS经耳迷走神经电刺激适应症之改善功能性消化不良2025-05-13 1826
-
迷走神经电刺激适应症之taVNS改善功能性消化不良2025-05-12 1288
-
taVNS经耳迷走神经电刺激适应症之改善慢性/原发性失眠2025-05-07 1906
-
经颅电刺激适应症之tDCS治疗注意力缺陷ADHD2025-04-22 143
-
经颅电刺激适应症系列之改善抑郁情绪2025-04-15 1285
-
经颅电刺激系列之迷走神经刺激(VNS)2025-03-07 2995
全部0条评论

快来发表一下你的评论吧 !