

时域干涉电刺激tTIS可持续增强运动皮层活动?
描述
定义:
初级运动皮层(图1)自发神经活动指的是在没有外部任务或刺激的情况下,大脑神经元的自发性、内在性电活动,通常通过 resting-state fMRI 中的低频波动(如 fALFF)和区域一致性(ReHo)等指标来量化。这些活动反映了大脑的基础功能状态和神经网络的自我组织能力。
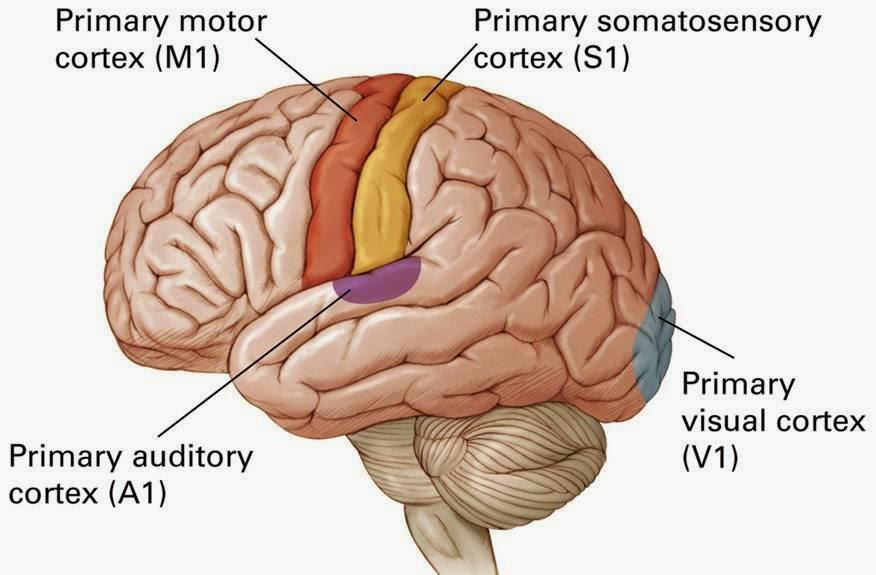
图1 大脑皮层的功能组织
刺激目的:
使用 tTIS(Temporal Interference Stimulation)和 HD-tDCS 对 M1 进行刺激,旨在调制其自发神经活动,从而:
增强神经可塑性;
改善运动功能;
为神经系统疾病(如中风、帕金森病)提供非侵入性治疗策略。
HUIYING
HD-tDCS 对 M1 自发神经活动的调控
核心过程(图2):
HD-tDCS 使用多电极(4×1环形配置)在C3(M1区)施加微弱直流电(2mA),通过阳极增强神经元兴奋性,阴极抑制,从而调节局部神经活动。
它通过改变神经元膜电位,影响GABA能神经传递,调节局部脑血流和代谢,进而影响自发神经活动。
目的:
增强M1区的局部神经同步性和低频率波动振幅(fALFF),促进运动皮层的功能连接和神经可塑性。
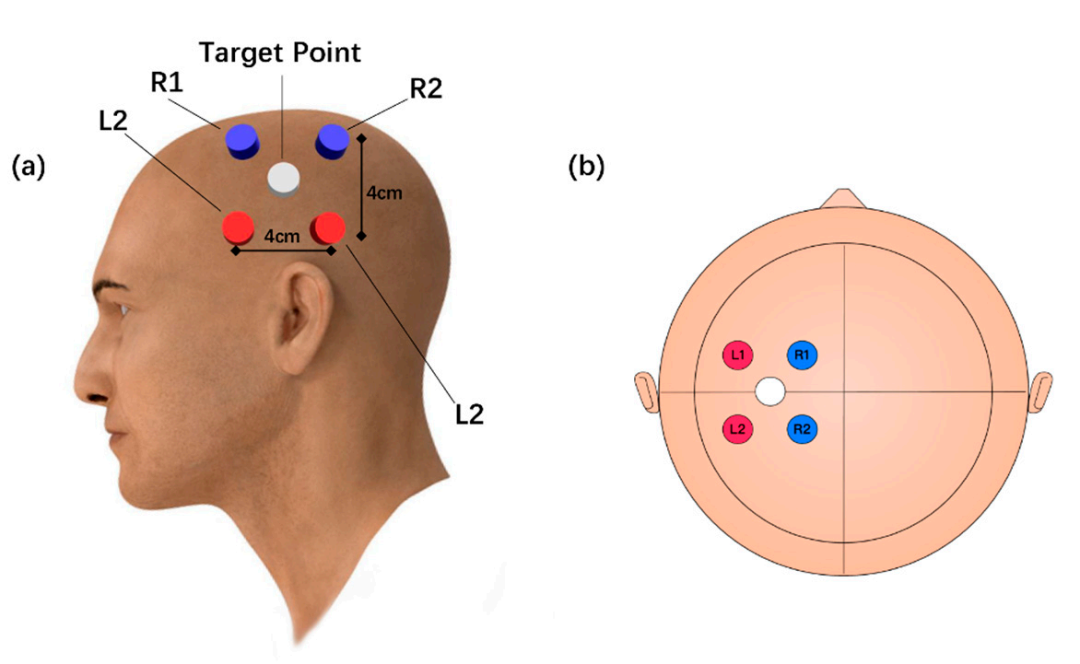
图2 HD-tDCS的模拟模型、电极放置和电场分布
HUIYING
TI 对 M1 自发神经活动的的调控
核心过程:
TI 使用两路高频交流电(2000Hz vs 2020Hz),通过干涉产生低频包络(20Hz),穿透颅骨并精准刺激深部脑区(如M1),同时减少对表浅组织的影响。
该技术通过调节神经振荡(尤其是γ波段),增强局部神经同步性和功能连接。
目的:
实现更深、更聚焦的神经调制,增强M1区的ReHo和fALFF,并产生更持久的后效应。
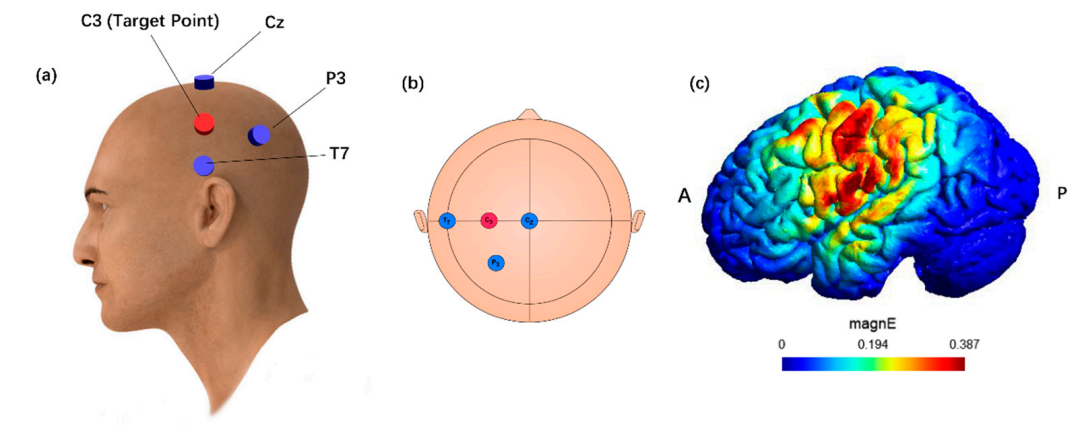
图3 TI刺激的模拟模型和电极放置
HUIYING
临床研究
研究方法(图4):
随机交叉设计,40名右利手健康成人;
每人接受20分钟TI或HD-tDCS刺激,fMRI在四个时间点(S1–S4)采集数据;
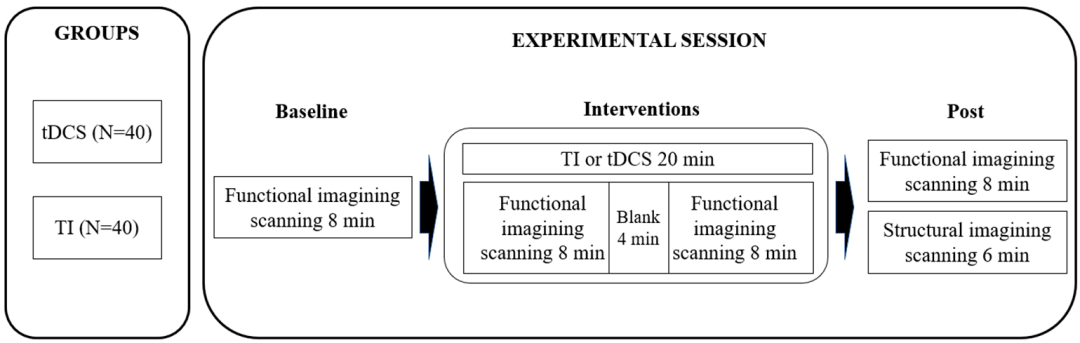
图4 实验设计流程图
分析指标:
ReHo (Regional Homogeneity,区域一致性):衡量大脑局部神经元活动的同步性。
dReHo(Dynamic Regional Homogeneity,动态区域一致性):衡量上述局部同步性随时间波动的动态稳定性。
fALFF(Fractional Amplitude of Low-Frequency Fluctuations,低频波动振幅分数):衡量大脑自发神经活动的信号强度。
dfALFF(dynamic fractional Amplitude of Low-Frequency Fluctuations,动态低频波动振幅分数):衡量上述自发活动强度随时间波动的动态变异性。
统计方法:
双因素重复测量ANOVA:用于分析刺激类型(TI/HD-tDCS)和时间(S1-S4)两个因素对脑活动指标的交互作用和主效应。
FDR校正:一种多重比较校正方法,用于控制统计检验中错误发现的比例,确保结果的可靠性。
研究结果
结果1:
TI对局部神经同步性(ReHo)的调制更强、更持久。
发现: 在刺激后半段(S3),TI组比HD-tDCS组在左侧颞上回和左侧中央后回(感觉运动网络的关键区域)引发了更显著的ReHo升高。

图5 TI与HD-tDCS在S3时期ReHo的组间差异脑图
图5 直接展示了TI减HD-tDCS在S3时的脑区差异,彩色区域明确指出了TI优势脑区的具体位置。
发现: TI的效应在刺激结束后(S4)依然存在(与基线S1相比仍有差异),而HD-tDCS的效应则很快消失。
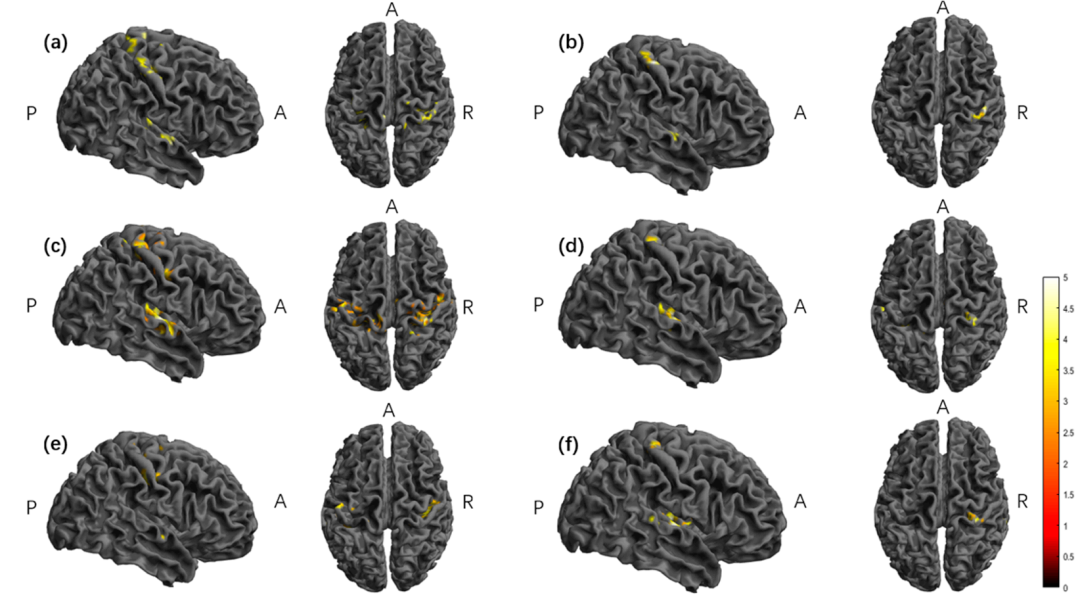
图6 ReHo指标在不同时间点对比下的组内差异脑图
图6e 显示TI-S4 vs TI-S1的比较中,右侧中央前回仍有显著激活(彩色区域),证明了TI效应的持续性,这是其相对于HD-tDCS的一个巨大临床优势。
结果2:
两种刺激均能增强神经活动的时间稳定性(dReHo)。
发现: 在刺激后期(S3),两种刺激都使得感觉运动皮层的dReHo值显著降低。
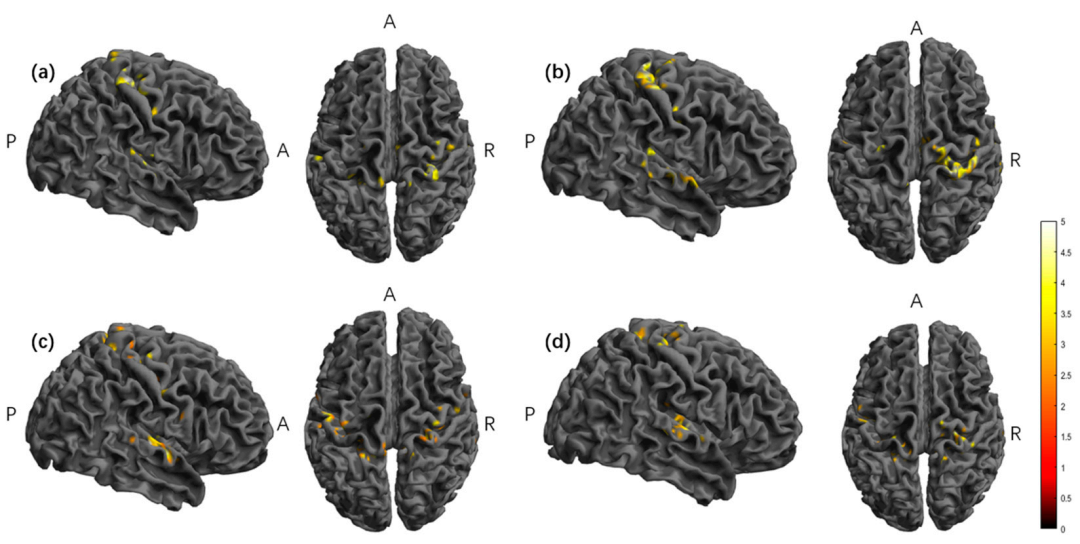
图7 dReHo指标在不同时间点对比下的组内差异脑图
图7a &7c 中,彩色区域表示S1减S3有显著差异的脑区,即S3时期的dReHo值显著低于基线期。这意味着刺激使大脑局部神经活动的同步性变得更加稳定,波动减小。这种“稳化”效应可能为异常的、不稳定的大脑网络(如癫痫、帕金森震颤)提供治疗思路。
结果3:
TI能特异性增强自发神经活动的强度(fALFF)。
发现: 只有TI刺激显著提高了fALFF值,即在刺激中后期(S3)和刺激后(S4),大脑感觉运动区的低频活动强度显著增强。
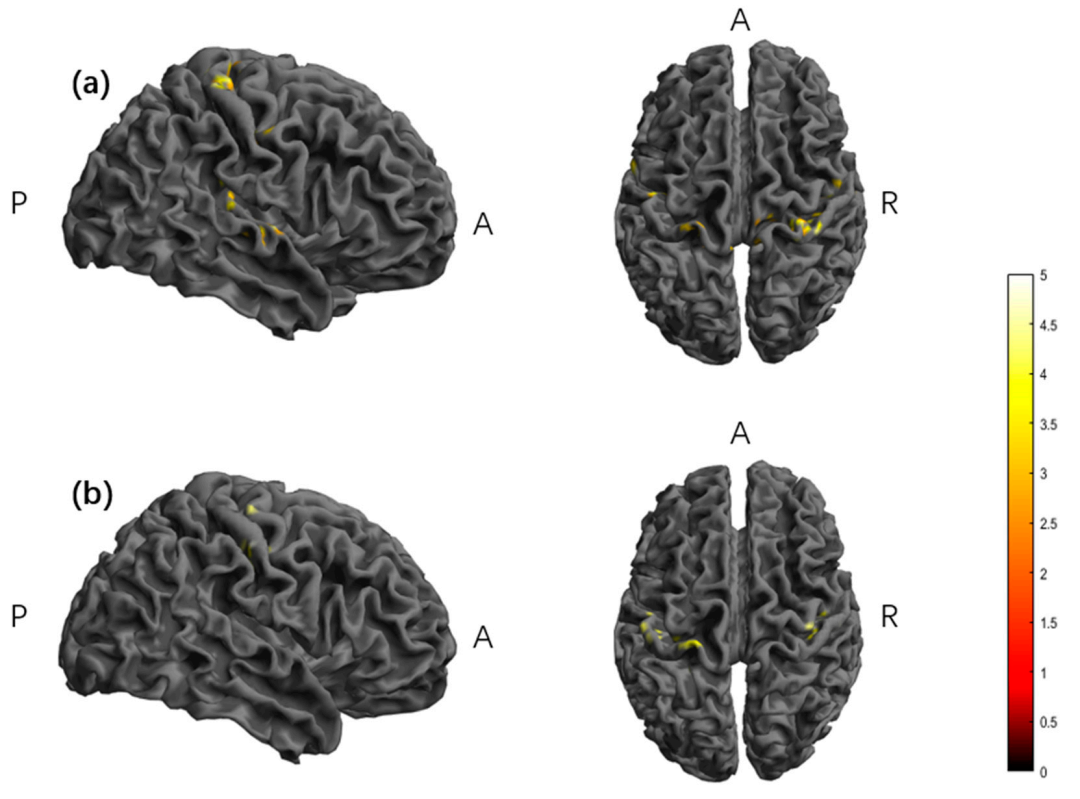
图8 fALFF指标在TI组内不同时间点对比下的差异脑图
图8a & 8b 独家展示了TI组内部的fALFF变化。图8a显示S3时期右侧中央后回、颞横回活动增强,图8b显示S4时期双侧中央前/后回活动依然高于基线。这表明TI在增强神经活动“能量”方面具有独特优势,而HD-tDCS未引起此效应。
结果4:
动态活动强度(dfALFF)未受调节。
发现: 两种刺激对dfALFF均无显著影响。说明它们改变了活动的强度和同步性的稳定性,但并未改变强度本身的波动模式。
HUIYING
总结
本研究系统比较了TI和HD-tDCS对M1自发神经活动的调制效果,发现:
TI 具有更强、更持久的调制能力,尤其在对深部脑区的精准刺激方面表现优越;
HD-tDCS 虽也能调制M1活动,但效应较弱且不持久;
TI在增强局部神经同步性和低频波动方面更具潜力,适用于需要持续神经调节的临床场景(如中风康复、帕金森病);
研究为个性化非侵入性脑刺激方案的优化提供了重要依据。
HUIYING
回映产品
产品1:手持式经皮脊髓神经电刺激(tSCS)
本设备采用经皮脊髓电刺激(transcutaneous Spinal Cord Stimulation, tSCS)技术,是一种基于生物电调控原理的非侵入性神经调控系统。其核心技术特征为:通过高频载波信号的低频脉冲幅度调制(Pulse Amplitude Modulation, PAM),在保证刺激深度的同时显著降低皮肤阻抗带来的不适感。刺激电流经体表电极耦合至目标脊髓节段,可选择性激活脊髓后柱神经通路及中间神经元网络。
从临床应用维度,本系统具有多节段调控能力:颈段tSCS通过调节颈膨大(C5-T1)神经环路,可有效改善中枢性上肢运动功能障碍;腰骶段tSCS作用于腰膨大(L1-S2)神经中枢,能促进下肢运动功能重建(包括直立位平衡及步态训练),同时通过门控机制实现疼痛调控。现有循证医学证据支持其在慢性脊髓损伤康复、神经源性膀胱管理及急性痛症干预等领域的辅助治疗价值。
产品2:48通道8脑区同步高精度经颅电刺激设备
回映电子科技院线级多脑区高精度经颅电刺激设备(MXN-48)是一款可8脑区/8人同步干预的高精度经颅电刺激实验平台。其已突破了Soterix对该技术的垄断(Soterix产品Soterix MXN-33 高精度经颅电刺激系统其之前是市面上唯一款可对不同脑区进行同步精确干预的设备)回映高精度经颅电刺激产品M×N-48其具有48个独立输出通道,每个通道的波形,强度等参数都可以独立设置,可以实现对8个不同脑区的同步干预,不同脑区的相位同步性<0.1°,大大增强了tES的神经调控效果。回映高精度经颅电刺激设备提供了两种不同的操作模式以供研究者选择——基础模式和自由模式。基础模式使用更加方便,设定简单;自由模式则允许导入自定义电流波形,功能更加强大。
适用范围:康复医学:运动功能障碍、语言障碍、认知障碍、吞咽障碍、意识障碍、上肢肌张力障碍、卒中后抑郁、卒中后疼痛等精神病学:抑郁症、焦虑症、强迫症、物质成瘾、创伤后应激障碍﹑精神分裂症等儿童康复:脑瘫、运动功能障碍、注意缺陷多动障碍、孤独症、阅读障碍、语言发育迟缓等神经病学:睡眠障碍、耳鸣、慢性疼痛、帕金森病、纤维肌痛、慢性疼痛(脊髓损伤下肢)、阿尔茨海默病、单侧忽略﹑偏头痛、神经性疼痛等脑科学研究:记忆、学习、言语等
产品3:手持式高精度经颅电刺激HD-tES设备
回映便携式高精度经颅电刺激仪(HD-tES)创新地采用type-C转生物电极的设计使得产品能够非常便捷地被使用。回映便携式高精度经颅电刺激仪(HD-tES)通过多电极配置(1个中心电极和4个返回电极)实现高精度电流聚焦,精准刺激目标脑区。其核心优势在于通过缩小电极尺寸(直径12mm的环形电极)和增加电极数量,显著提升刺激的聚焦性和精准性。
回映HD-tES支持多模式刺激,覆盖多场景需求:HD-tDCS模式:调节皮层兴奋性,适用于中风康复、抑郁症干预等。HD-tACS模式:精准锁定脑电频段(如β-γ频段改善强迫症,4Hz增强工作记忆)适配认知障碍治疗等。HD-tRNS模式:HD-tRNS 对显式和隐式计时任务的影响不同,用于研究大脑的计时机制和时间处理能力等。
回映便携式HD-TES设备示意图

回映自研type-C转生物电极示意图
适用范围:神经系统疾病治疗,意识障碍和认知功能调节,康复治疗,运动和认知功能恢复。产品4:便携式经颅强交流电刺激仪(Hi-tACS)
该设备采用非侵入性的10-30mA刺激电流直接刺激大脑区域,进而刺激大脑深部的神经核团、改变神经递质水平,影响脑电节律、改善脑区间的联络,从而增强脑功能,治愈疾病。
-
基于双光束干涉的相位敏感光时域反射计2016-05-27 972
-
经颅电刺激系列之高强度经颅交流电刺激Hi-tACS2025-02-10 3514
-
经颅电刺激系列之高精度经颅电刺激HD-TES2025-02-15 4198
-
经颅电刺激系列之相移经颅交流电刺激Phase-shifted tACS2025-06-09 1513
-
经颅电刺激系列之时域相干电刺激tTIS2025-08-25 8331
-
PWM-TI是时域干涉电刺激tTIS新的未来吗2025-09-08 1976
-
Theta-TI比传统经颅时域干涉电刺激tTIS更有效吗2025-09-10 5405
-
多点时域干涉电刺激MTI如何用2对电极对实现多脑区的同步调控2025-09-15 5199
-
多极性时域干涉电刺激mTI比传统TI更聚焦?2025-10-09 1082
-
时域干涉电刺激tTIS真正有效的适应症是哪些?(PD震颤)2025-11-12 1211
-
闭眼是tDCS经颅电刺激的最佳状态?2026-02-04 332
-
Burst-iTBS-tTIS比传统时域干涉电刺激调控PD是否更有效?2026-03-15 2274
-
tFUS+HD-tDCS如何实现毫米级皮层精准调控?2026-03-21 2472
-
tTIS阈上刺激可工程化吗?2026-04-09 98
-
MEP如何可量化的评估tTIS的刺激干预效果?2026-04-20 74
全部0条评论

快来发表一下你的评论吧 !

