

皮肤电活动测量系统的设计、开发与评估
电子说
描述
近年来,活跃跟踪器和其它可穿戴电子设备越来越受欢迎,因为用户希望实时监控、测量和跟踪与其健康相关的各种实时指标,包括步数、心率、心率变异指数(HRV)、用户体温、活动水平和/或压力水平等。现有一种已知的压力水平测定技术涉及监控、测量和/或跟踪皮肤电活动(EDA),是通过测量皮肤阻抗或皮肤电导率来实现的。研究显示,为响应环境、心理和/或生理反应,皮肤电导率会上升。通过测量皮肤阻抗或皮肤电导率在时间上的变化,可以获得与用户活动水平、压力水平、疼痛水平和/或与用户当前心理和/或生理状况相关的其他因素,使用户或医师能根据取得的指标采取适当的措施,处理出现的状况。
本文的最终目的是提供一个有用的实体系统,用于研究并最终评估/量化人的压力水平。
简介
压力是导致身体或精神紧张的生理、心理或情绪因素。压力分为外部压力(环境压力、心理压力或社会因素所致压力)和内部压力(疾病或医疗程序导致的压力)。压力可能引发“战或逃”的反应,后者是神经系统和内分泌系统的一种复杂反应。
“战或逃”反应(在创伤后压力症中也称为战斗、逃跑、僵死或服从反应,反应过度,或急性应激反应)是对感知到的有害事件、攻击或生存威胁作出的一种生理反应。
该反应始于杏仁核,结果在下丘脑中触发神经反应。初始反应后,脑下垂体被激活并分泌促肾上腺皮质激素。肾上腺被同时激活并释放肾上腺激素。
释放化学信使后会产生皮质醇激素,导致血压和血糖升高,对免疫系统形成抑制作用。触发初始反应和后续反应是为了增加能量。肾上腺素与肝细胞结合后产生血糖,实现能量的提升。另外,皮质醇循环是为了把脂肪酸转换成可用的能量,结果促使人体肌肉做好反应准备。儿茶酚胺类激素(如肾上腺素或去甲肾上腺素)会促进即时身体反应,为激烈的肌肉反应做好准备。
然而,在持续需求下,压力系统长期处于活跃状态,可能损害人体健康。
压力会导致多种疾病,对人的身心造成影响。1 我们会在本文后面部分讨论这些。
方法
有不同的方法可以用来检测和确定压力水平。最重要的方法是:测量皮质醇水平,取得心率变异指数,或者获得皮肤电活动数据。
测量皮质醇水平
皮质醇是糖皮质类激素中的一种甾类激素,是人体肾上腺中的肾上腺皮质产生的。人体释放皮质醇是对压力的回应。因此,测量皮质醇水平被认为是量化压力水平的黄金标准方法。2 然而,该技术存在两个重要问题。第一个问题是从威胁出现到皮质醇水平发生变化这一过程的延迟问题,延迟可能长达15分钟。第二个也是最重要的问题是要检测用户日常生活中的威胁和压力状况,就需要持续取得压力水平数据。因此,无论对谁来说,这种方法都太复杂、太昂贵、太不友好;可见,皮质醇测量并不适合普通用途。
获取HRV
HRV是两次心跳间时间间隔发生变化的这种生理现象。其测定标准是心跳间时间间隔的变化。3
目前,市场上有多种设备都能测量心率。这些设备的分辨率最高为每分钟一次(心跳/分钟)。该分辨率足以满足多种应用的需求。然而,针对压力评估的HRV分辨率要高10或100倍。这意味着采样频率和算法复杂程度一定非常高,所以,系统功耗也是个大问题,无法满足可穿戴式产品或24/7全天候应用的需求。
获取EDA
EDA是衡量汗腺渗透率神经介导性效应的一项间接指标,为小电流下皮肤电阻的变化或者皮肤不同部分的电位差。4
EDA在功耗、人体工程设计和电路尺寸方面比其他技术更有优势。
系统描述
本研究旨在开发一种用于研究和估测人的压力水平的有用工具。人的压力水平不是恒定不变的,而是取决于人感知到的威胁。每个人对这些威胁的感知是不同的,有许多因素会使一个人眼中的简单事件变成另一个人眼中的巨大威胁。在医院里进行压力测试以确定人的压力水平是没用的,因为这些威胁出现在患者的正常生活当中。可见,有必要开发一种系统,使我们能在人的正常生活中估测其压力水平。因此,该系统必须具有非介入性、用户友好和可穿戴的特点。最后,该系统还必须能工作数天而无需充电或更换。
针对最终设备的这些要求意味着系统必须符合下列特点:
u 电池供电,因为必须可穿戴
u 低功耗,因为必须对患者监控数天时间
u 小尺寸,因为必须可穿戴且用户友好
u 低成本,因为如果太贵,解决方案就无法被运用到任何消费级设备当中
u 符合安全法规
为了确保系统的非介入性,必须考虑数据记录部位。电极的最佳安放部位是手腕上部,因为这种设计可以确保设备的下列特点:非介入性;用户友好性;机械设计的简单性。然而,在该部位获取的信号在质量上不如从身体其他部位获取的EDA信号,比如食指与中指的中节指骨。5
一旦确定了EDA信号获取电极的安放部位,我们就知道,最终(目标)系统要采用智能手表或类似设备的形式。这里要确定的下一个指标是EDA电路可以使用的面积。为了确定这个参数,我们分析了多款智能手表,并就这个话题咨询了多家供应商。结论是,EDA电路的最大面积要小于5 mm × 5 mm。
EDA电路的功耗是要明确的第三个参数。该参数是确保系统能持续数天记录EDA信号而无需充电或更换设备的关键。我们取得了不同智能手表的电池容量数据和部分可能商用系统的功率预算数据。经过研究,确定了功耗目标,要求平均功耗不得超过200 μA。
最后,要明确的最后一项指标是成本。然而,目前还无法确定该指标,因为有多种因素可能会影响到设备的最终成本。精心选择电路拓扑结构和器件,确保最终解决方案的成本处于合理水平。
硬件设计
本节描述电路拓扑结构、测量范围和分辨率的确定方式。
其中一个关键决定是确定电路的拓扑结构。基本而言,测量阻抗的方法有两种。系统可以施加电流并测量阻抗范围内的电压,也可以施加电压并测量阻抗范围内的电流。另外,这些施加信号既可以是直流信号,也可以是交流信号。6 重要的是要分析每种方法的优势和不足。
有多种电路可以测量交流信号,每种都有自己的优势和劣势。然而,为了达到性能、成本和面积方面的限制要求,我们认为最佳选择是以下解决方案。
我们最后决定,用一个交流电压源作为激励源,测量通过患者身体的电流,由此确定皮肤电导率。该解决方案可以避免在单个汗腺上施加高压,从而避免了汗腺受损的危险,并且符合IEC6060-1标准的要求。交流信号消除了电极极化问题。7
我们需要数字化、存储和分析要测量的电流。意味着电路需要一个模数转换器(ADC)。由于多数ADC转换的是电压而不是电流,所以,我们需要先把通过患者身体的电流转换成电压。这可以通过一个跨阻放大器(TIA)来实现的。在选择最佳运算放大器时,要考虑的三个关键指标是噪声规格、尺寸和功耗;在实现TIA时要用到这些指标。
一旦确定的系统的拓扑结构,下一步就是确定要开发的系统的测量范围和分辨率。
EDA信号放大方面的问题主要源于其宽范围和高分辨率要求。一般地,皮肤电导设备必须覆盖的范围为0 μS至100 μS,还要能检测0.05 μS的波动。分辨率可以通过12位分辨率以上的ADC实现。对于分辨率,本项目的目标是0.01μS,因此需要采用14位或16位分辨率的ADC。8
为了在100 μS的范围内获得0.05 μS的分辨率并达到安全法规的要求,需要采用下列模块。
u 一个交流电压源
u 确保符合IEC6060-1规范的保护元件
u 用于测量通过患者身体的电流的电路
环境温度和皮肤温度的变化会导致EDA信号变化。9 因此,也有必要取得环境温度和皮肤温度。这可以通过一个简单的热敏电阻和几个分立元件以及一个ADC来实现。
最后,功耗是该电路中的一个关键参数。为了降低功耗,确保仅在需要进行新的测量时激活系统,必须同时集成一个电源管理单元。该模块必须能由主微控制器轻松控制,并且必须为整个EDA测量电路供电。图1所示为完整的功能框图。
图1.系统框图。
在以下各节中,我们将明确本应用的最佳组件。
电源管理单元
我们决定用ADP151系列实现电源管理单元,因为该系列具有多个不错的特性,其封装和噪声水平也非常适合本应用的需要。10
电平转换器
有多种方式和广泛的集成电路可以用来形成电平转换器。然而,这些集成电路的面积和价格却无法满足本项目的限制要求。因此,本电路中的电平转换器是用分立元件实现的。基本地,电平转换器由一个晶体管DMN2990UFZ,11和一个电阻构成。
低通滤波器和TIA
为了实现低通滤波器和TIA,我们选用了ADA4505-2ACBZ,因为它具有优秀低功耗水平、小尺寸和输入偏置电流超低等特点。12
ADC
符合所有系统要求的ADC是AD7689BCBZ。这款强大的ADC集成了可以在不使用时关闭的基准电压源,因而可以降低功耗。13
最后,为了确保达到面积限制要求,我们将使用的组件和功能数量降至最低,并且为所有组件选择了最小的封装。图2所示为该系统的布局和尺寸。
图2.EDA分立式电路布局。
软件设计
如前所述,系统需要生成一个激励信号,用于测量皮肤的电导率。该激励信号是一个交流信号,从交流测量值抽取的两个参数是信号幅度和激励信号与获取的信号之间的相位延迟。最重要的参数是幅度,可以通过多种方式从交流信号中获取该参数。然而,在本系统中,获取幅度的最佳方法是实现离散傅里叶变换(DFT)。14
也可以将DFT视为滤波器组,其衰减水平与样本数成正比,最大值的位置取决于激励信号。
在这里,有理由采用较大的样本数(N)来实现DFT,因为这样做可以改善SNR。然而,DFT的功耗(如果直接实现)与样本数成比例,采集的样本越多,功耗越大。这意味着在样本数与功耗之间存在一个重要的折衷点。
另一个重要参数是采样频率与激励频率之比。如果采样频率为激励频率的4倍,则用于实现DFT的等式会非常简单。这种情况下,涉及浮点乘法的复杂等式会成为加法。如果可用处理器为DSP或Cortex®-M4,则乘法也是可行的。然而,如果必须在Cortex-M0中进行计算,则这可能会成为一个重要问题。不妨比较等式1和100 Hz频率窗口(FCENTER)的单点DFT计算滤波器表达式,其中,采样频率(FS)为400 Hz和500 Hz。
明确要采用的技术以及激励频率与采样频率之比之后,下一步就是确定激励频率。
激励频率必须尽可能低,以确保电流会流过患者的皮肤,但不会渗入身体。15 因此,激励频率必须小于1 kHz。同时需要指出的是,本应用的主要噪声源是市电产生的50 Hz/60 Hz噪声。
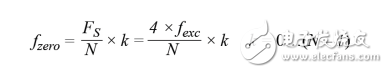
如等式2所示,DFT的各个组分X(k)抵消了n × FS/N形式的频谱组分的贡献,其中,n = 0, 1, 2.。.N – 1,N = k时除外。通过正确定义激励频率,我们可以抵消50 Hz噪声源的贡献。然而,不能使用高频率的原因如前所述。所以,不错的折衷点是100 Hz,虽然我们可能会捕捉到市电干扰源的谐波。
如果激励信号为100 Hz,采样频率为400 Hz,则在50 Hz下,当N等于8、16和32时,会出现零。我们同时要记住的是,样本数必须尽可能小,以尽量降低功耗。因此,一种不错的折衷选项是用16个样本实现DFT。必要时,为了改善SNR,可以增加样本数。当然,如果噪声为60 Hz而非50 Hz,则采样频率应为480 Hz,激励频率应为120 Hz。频率响应如图3所示,只涉及加法的数学公式如等式3所示。
图3.可以把DFT视为滤波器组。这是16个样本条件下的DFT频率响应,其中,采样频率为400 Hz,中心频率为100 Hz,频率窗口为矩形。
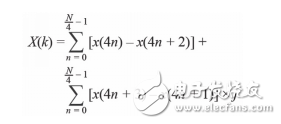
机械设计
我们开发了一个评估系统,用于测试和证明以上提出的解决方案。该平台由EDA测量需要的主传感器以及其它必要特性构成。移动和温度可能会影响皮肤阻抗测量结果。9, 16 因此,同时我们也测量了含有移动和温度的信号。
系统还包括一个电池充电器,用于对平台中使用的LIPO电池充电。该设备需要采用高容量电池,因为我们希望能实现24小时信号采集。阻抗、温度和加速度测量值被保存到存储于微型SD卡上的文件中,也可以通过低功耗的蓝牙®把数据发送到平板电脑或个人电脑上。图4所示为评估平台。
图4.EDA评估平台。ADI watch GEN II。
结果
SNR研究
我们进行了数学分析,确保能在所选组件的噪声水平以及系统带宽条件下,实现要求的分辨率。然而,该特性需要用实际测量值检验。为此,我们用原型系统测量了多个电阻网络,以便检验功能。研究涉及对同一电阻网络进行多次测量,以检查可重复性,从而获得系统的精度数据。在这项测试中,我们对每个网络进行了100次测量,通过从取得的结果中的最大值减去最小值,取得了最大误差。误差值始终等于或小于0.01 μS。
在验证系统精度以后,下一步是检查系统的线性度。为了进行此项实验,我们将原型接入可编程电阻替代器,以1 kΩ的步进对10 kΩ-500 kΩ的范围进行了评估。系统的R2为0.9999992。
功耗研究
EDA系统由一个有不同状态的状态机构成,用于获取患者皮肤电导率,确保使功耗维持于最低水平。开始时,在状态1(S1)下,我们关闭了EDA的AFE,只有微控制器和加速度计处于开启状态。平均功耗为139 μA。大约150 ms后,我们打开EDA AFE,由MCU生成方波信号,然后交由LPF滤波。在该阶段(S2),我们关闭了ADC基准电压源,因为信号还不稳定。确保信号稳定需要6个周期,在最差情况下,S2下的平均功耗为230 μA。我们在S3下打开了ADC基准电压源,系统等待10 ms,确保基准电压源稳定下来——本阶段的平均功耗为730 μA。系统在四个周期中获取4个样本,以取得用于在S4中实现DFT的16个样本点。本阶段的功耗为880 μA。DFT在阶段S5中实现的。同时在该状态下取得了加速度计数据,本阶段的功耗为8 mA左右。图5所示为系统功耗。本研究证明,EDA AFE的平均功耗要低于170 μA。
图5.功耗分析。
实验检验
现在,我们已经对系统进行过电子验证——因此,下一步是比较EDA电路与基准系统的性能。在本例中,我们以Empatica的E4平台作为基准系统,因为它具有良好的性能。
确定基准以后,我们要确定能看到EDA信号的变化的测试。选择的是“放松-压力”测试。该测试分为两步:第一步是放松练习,第二步是压力练习。
放松练习由10分钟的控制呼吸组成,目的是达到放松状态。压力状态是通过“颜色-词语-声音”游戏实现的。在该应用中,用户会听到一种颜色,看到一种颜色的文字,该文字是用一种颜色展示出来的。听到的颜色、用文字描述的颜色和展示的颜色可能相同,也可能不同。正如读者在图6中观察到的那样,可能有一个下面这样的句子:
u 选择颜色
u 选择声音
u 选择词语
根据句子传递的信息和声音、文字或颜色,受试者需要按下正确的按钮。用户必须在进度条走完之前做出反应。
如果在这段时间内用户没有反应,或者如果反应是错误的,则会减去相应的分值。如果正确,则会增加相应的分值。最后,交换按钮位置。
在该应用中,有多种设置可以修改,以改变实验等级(压力水平)。
图6.“颜色-词语-声音”测试应用。
理论上,在放松任务中,皮肤电导率应该会下降,在压力活动中,应该增加。在压力活动中,应该能观察到峰值或尖峰。直流电平的变化对应于压力源的强直性反应。在压力活动中观察到的峰值被认定为形势反应,在放松任务中不会出现。
在明确用于取得EDA信号显著变化和预期响应的程序之后,下一步是进行实验,对我们的EDA解决方案与Empatica E4平台进行性能比较。为了进行比较,受试在进行测试时同时戴上两款设备。Empatica解决方案戴在右手上,测试系统则戴在左手上。这意味着预期信号必须相似,但不完全相同,因为设备是戴在不同的手臂上,测量部位不完全相同;Empatica从腕关节底部获取EDA信号,我们的解决方案则从腕关节顶部获取信号。两台设备获取的信号非常相似,如图7所示。在不同患者身上重复了多次本实验,以便验证系统。
图7.“放松-压力”测试(左侧为测试系统,右侧为基准设备)。
结论
本EDA电路是一种巧妙的皮肤电导率获取方案。得益于平均功耗和尺寸优势,可以将其集成到任何智能手表或类似平台中。设备取得了预期性能效果,可以在较宽的范围内,以高分辨率测量皮肤电导率。EDA电路采用特殊设计,避免了极化和半电池电位效应,可以兼容任何类型的电极。另外,还达到了IEC6060-1的要求。
为了评估和测试电路的特性,我们设计了一个原型。系统设计用以可以在不充电的情况下,24小时持续获取EDA信号以及皮肤温度、环境温度和移动数据,并把信息存储起来或者以无线方式实时发射出去。因此,可以用该平台从处于不同状况的不同人身上采集EDA数据,不受时间限制。最后,可以利用这些信息开发算法,以便检测、估测或预测人的压力水平。
参考文献
1 Melissa Conrad Stöppler,“压力,”MedicineNet.com,2016.
2 Danmin Miao、Li Luo、Lijun Xioa和Xiaomin Luo,“从波形量化分析角度看心理压力所致皮质醇水平变化与血管反应之间的关系:血管变化压力相干指数研究”,Biomedical Engineering and Biotechnology,2012年7月。
3 Chu Kiong Loo、Einly Lim、Manjeevan Seera、Naoyuki Kubota和Wei Shiung Liew,“以Salivary Biomarkers为基准条件下基于心率变异指数的压力分类研究”,IEEE Transactions on Neural Networks and Learning Systems,2016年10月。
4 Wolfram Boucsein,“皮肤电现象原理”,Electrodermal Activity,第1-86页,Springer U.S.,2012。
5 Wolfram Boucsein,“记录压力”,Electrodermal Activity,第104-109页,Springer U.S.,2012。
6 Wolfram Bouscein,“皮肤电测量简介”,Electrodermal Activity,第88-103页,Springer U.S.,2012。
7 Banu Onaral、Herman P. Schwan、Banu Onaral,“生物电极的电气属性”,IEEE Transactions on Biomedical Engineering,1984年12月。
8 Wolfram Boucsein,“皮肤电测量的具体问题”,Electrodermal Activity,第96-98页,Springer U.S.,2012。
9 Wolfram Boucsein,“气候条件”,Electrodermal Activity,第189-192页,Springer U.S.,2012。
10 ADP151数据手册,ADI公司,2017。
11 DMN2990UFZ数据手册,Diodes公司,2015。
12 ADA4505-2数据手册,ADI公司,2017。
13 AD7689数据手册,ADI公司,2017。
14 Julius O. Smith III,“离散傅里叶变换(DFT)的数学原理:以音频应用为例”,斯坦福大学,2002。
15 Wolfram Boucsein,“用交流电实现体外记录,”,Electrodermal Activity,第126-129页,Springer U.S.,2012。
16 Wolfram Boucsein. “Physiologically Based Artifacts.” Electrodermal Activity, pp 141-143, Springer U.S., 2012.
16 Wolfram Boucsein,“生理伪像”,Electrodermal Activity,第141-143页,Springer U.S.,2012。
作者简介
Javier Calpe 毕业于西班牙瓦伦西亚大学,于1989年和1993年分别获得理学学士学位和物理学博士学位。Javier现为ADI公司西班牙瓦伦西亚开发中心负责人。
Jose Carlos Conchell现为ADI公司西班牙瓦伦西亚工业与医疗健康事业部的一名产品应用工程师。他专注于生物阻抗应用的研发。José Carlos Conchell于2011年加盟ADI。他毕业于西班牙瓦伦西亚大学,于2007年、2010年和2016年分别获得理学学士学位、电气工程硕士学位和生物医学工程硕士学位。
-
求助:请问一下皮肤黑色素怎么测量啊?2012-11-17 2979
-
zz:集成在你的皮肤上的电子电路2012-11-28 22335
-
一种巧妙的皮肤电导率软硬件设计方案2018-06-13 6202
-
一文读懂皮肤电活动测量系统的设计、开发与评估2018-10-23 2789
-
基于DSP的人体皮肤测量仪的设计2010-12-08 1088
-
无线电测向活动,无线电测向活动是什么意思2010-03-29 3697
-
业内首款皮肤电反射测量参考设计,加速可穿戴设备开发2015-05-20 2571
-
ADI开发了一个称为AD594x系列的新型阻抗测量芯片2019-03-26 16794
-
通过数据采集平台进行皮肤电活动的测量2019-07-17 4100
-
设计、开发和评估获得皮肤电活性的系统2023-01-03 2151
-
AN-1557: AD5940和AD8233在完整生物电系统中的实现2023-06-16 6875
-
步态分析足弓测量智能评估系统2021-11-17 3560
-
皮肤电信号(GSR)及其原理简析2023-10-08 8390
-
一文了解皮肤电活动测量系统的设计、开发与评估2023-11-24 1011
全部0条评论

快来发表一下你的评论吧 !

